Similar presentations:
Кристаллические решётки
1. Кристаллические решётки
2. Основные понятия:
• Основные понятия:• Аморфные и кристаллические вещества.
• Кристаллические решётки:
• атомные, молекулярные, ионные.
• Вещества молекулярного и
немолекулярного строения.
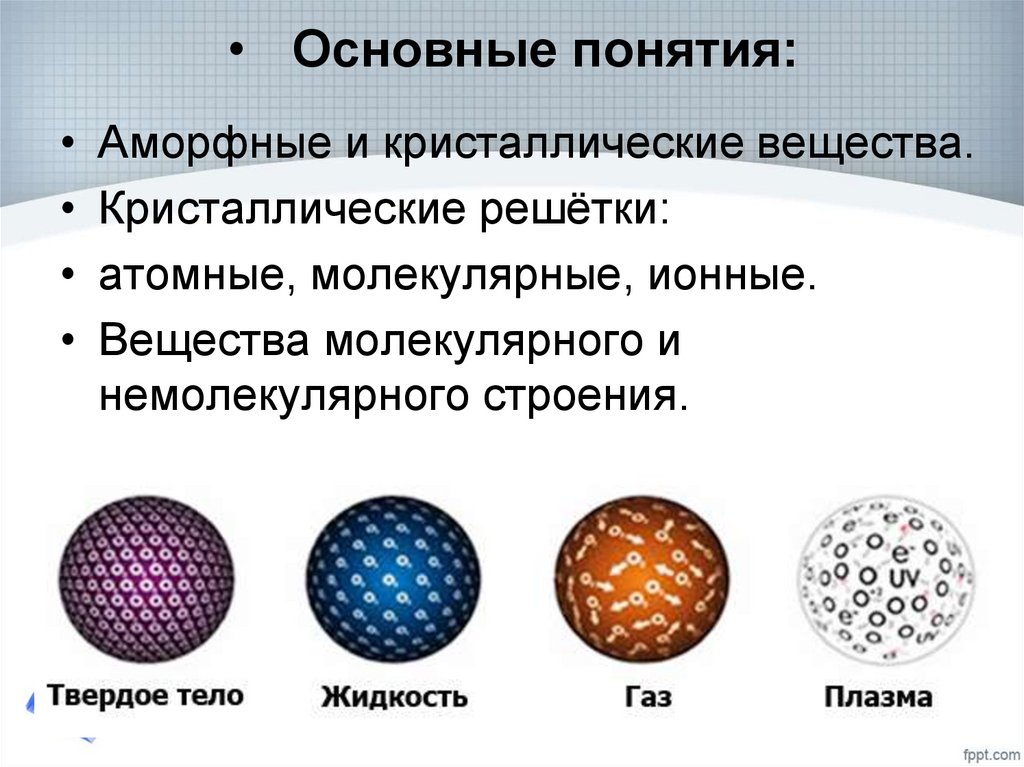
3. В природе вещества встречаются в 3-х состояниях:
Твёрдом;Жидком;
Газообразном
4.
Твёрдое тело имеетсобственную форму и объём.
• Жидкости легко меняют свою
форму, но сохраняют объём.
• Вещество в газообразном состоянии
• не имеет собственной формы и объёма.
• Газы принимают форму сосуда и занимают
предоставленный объём.
5.
Твёрдые телаКристаллические
Аморфные
6. Свойства кристаллических тел
•Каждое вещество имеетсвою
•кристаллическую решетку.
•Совокупность точек
пространства, в которых
располагаются частицы,
образующие кристалл, называют
КРИСТАЛЛИЧЕСКОЙ РЕШЁТКОЙ.
•Механическая прочность;
•Температура плавления
постоянная;
•Оптические,
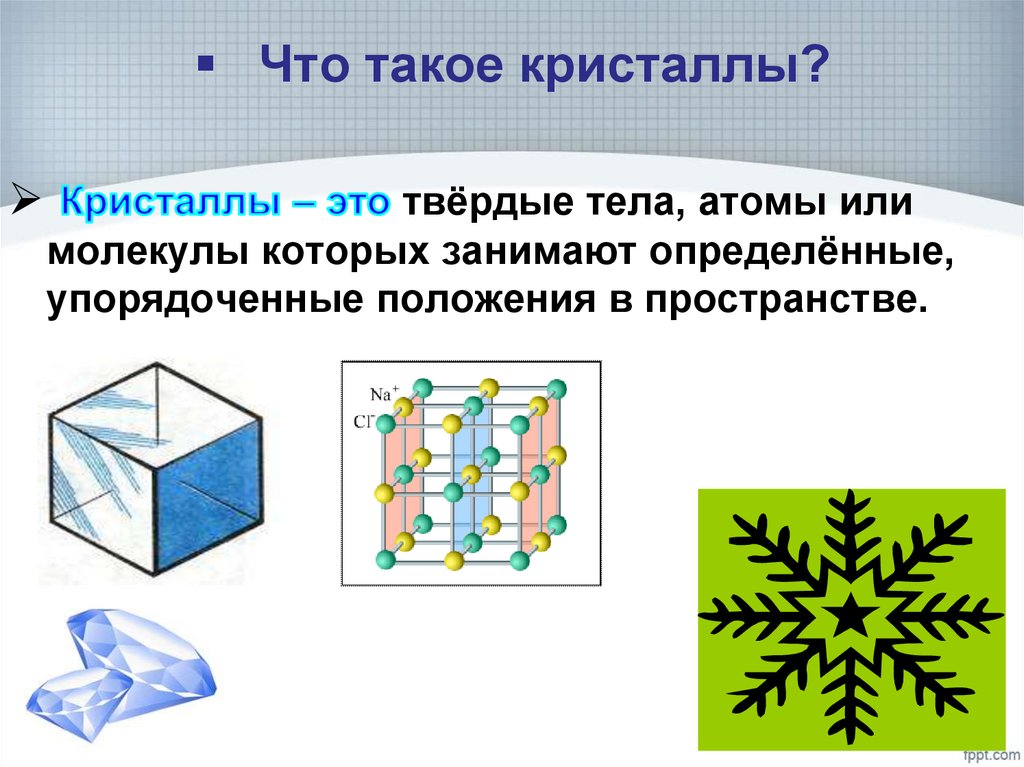
7. Что такое кристаллы?
твёрдые тела, атомы илимолекулы которых занимают определённые,
упорядоченные положения в пространстве.
8. Кристаллические тела
• Кристаллические тела- этотела определённой
геометрической формы,
ограниченные
естественными плоскими
гранями
9. Кристаллические тела
10. Кристаллические решетки
Криста́ллы (от греч. κρύσταλλος, — лёд,горный хрусталь, кристалл) — твёрдые
тела, в которых атомы расположены в
строго определенных точках пространства,
образуя каркас, называемый
кристаллической решёткой
11. Кристаллические решетки
Кристаллы – твердые вещества, частицыкоторых образуют периодически
повторяющуюся в пространстве структуру –
кристаллическую решетку.
Кристаллические решётки веществ упорядоченное расположение частиц
(атомов, молекул, ионов) в строго
определённых точках пространства.
Точки размещения частиц называют узлами
кристаллической решётки.
В узлах кристаллической решетки могут быть
молекулы, атомы или ионы.
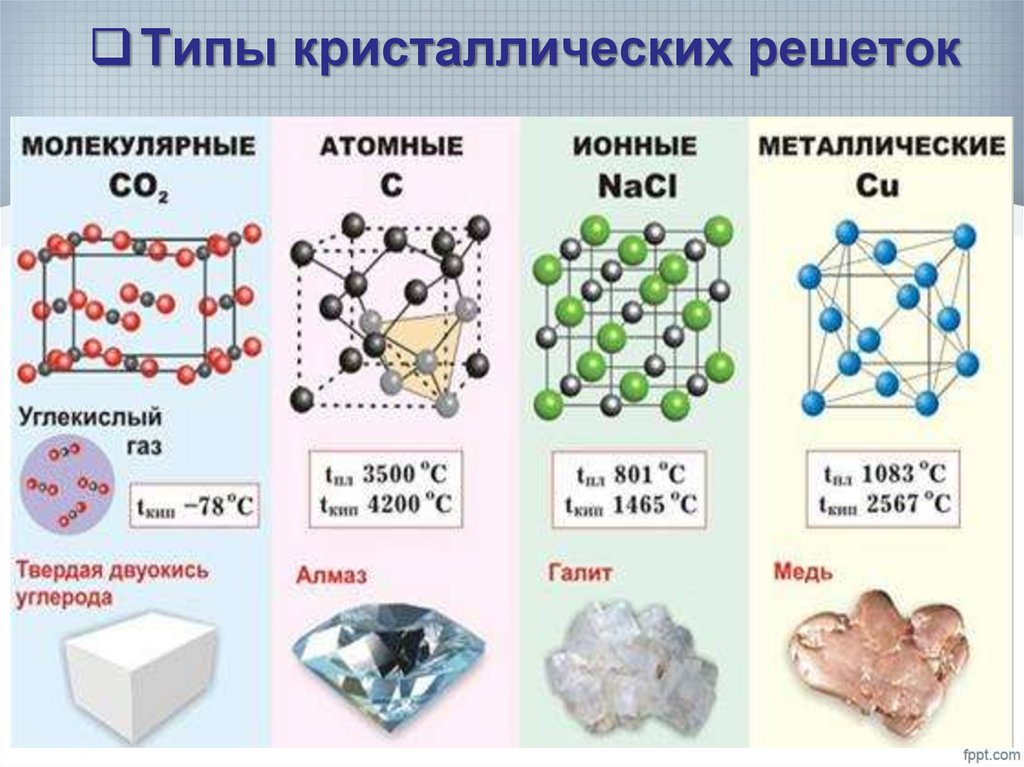
12. Типы кристаллических решеток
Атомные кристаллическиерешетки
Молекулярные
кристаллические решетки
Металлические
кристаллические решетки
Ионные кристаллические
решетки
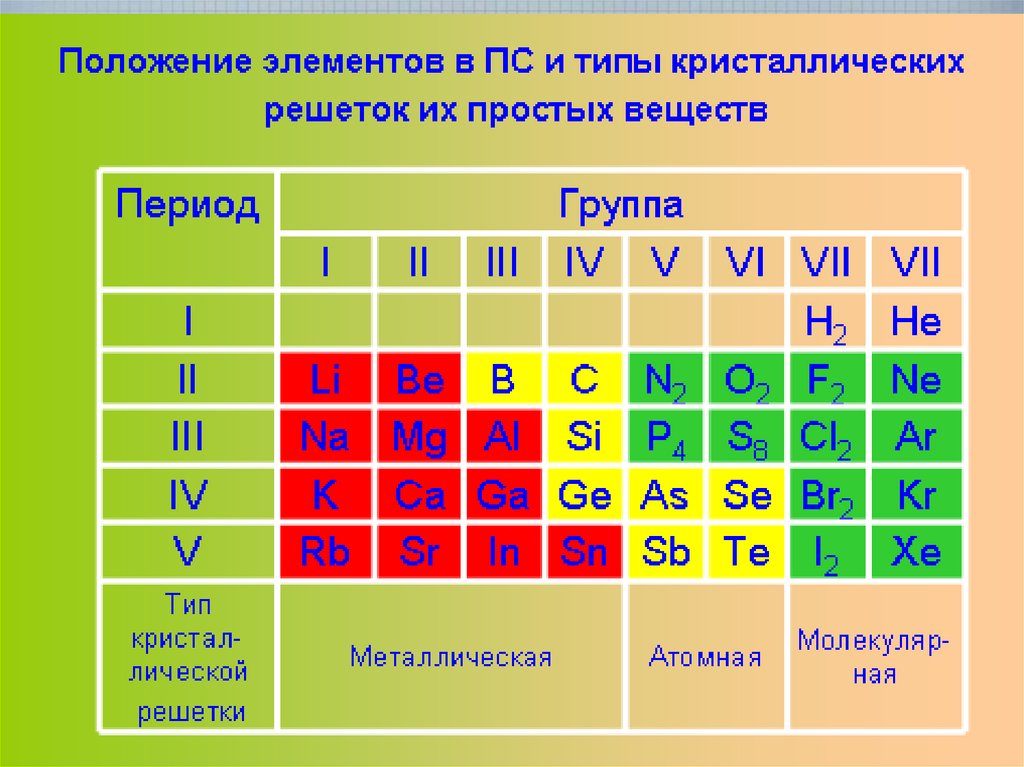
13. Типы кристаллических решеток
14.
15. АТОМНЫЕ КРИСТАЛЛИЧЕСКИЕ РЕШЕТКИ
• В узлах атомных кристаллических решеток находятсяотдельные атомы.
• Связи между атомами веществ, находящихся в узлах
кристаллической решетки прочные, с трудом
разрушаются.
• Вещества с атомной кристаллической решеткой имеют
высокие температуры плавления, обладают
повышенной твердостью.
• Алмаз – самый твердый природный материал
Кристаллическая решетка алмаза
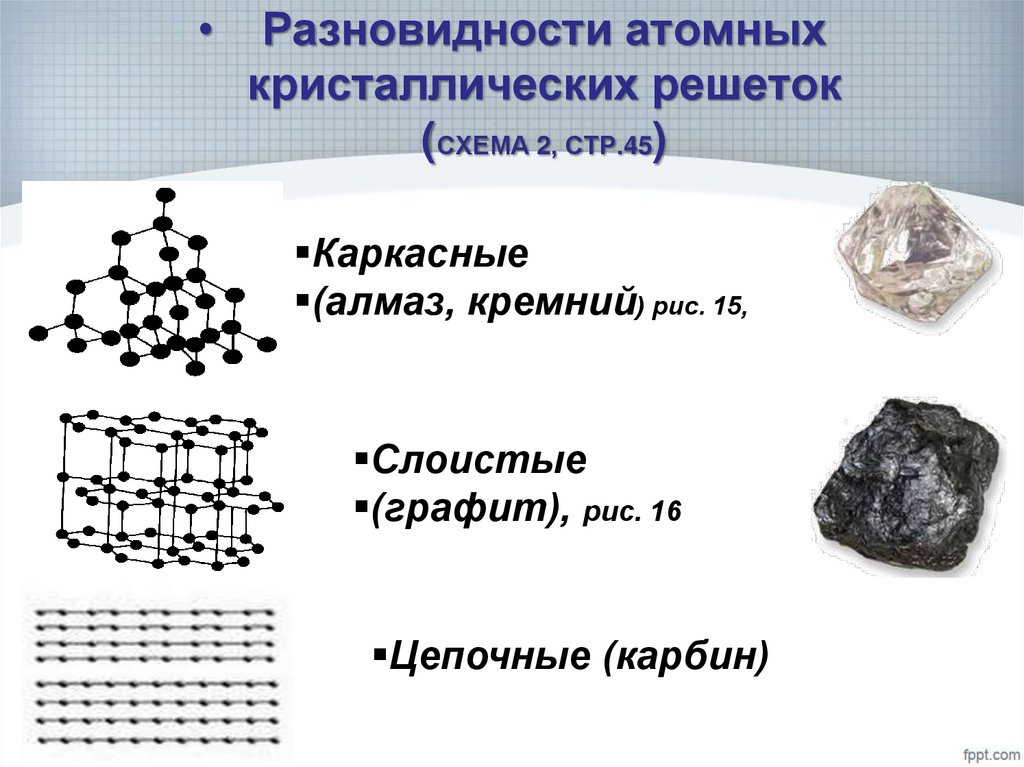
16. Разновидности атомных кристаллических решеток (СХЕМА 2, СТР.45)
Разновидности атомных
кристаллических решеток
(СХЕМА 2, СТР.45)
Каркасные
(алмаз, кремний) рис. 15,
Слоистые
(графит), рис. 16
Цепочные (карбин)
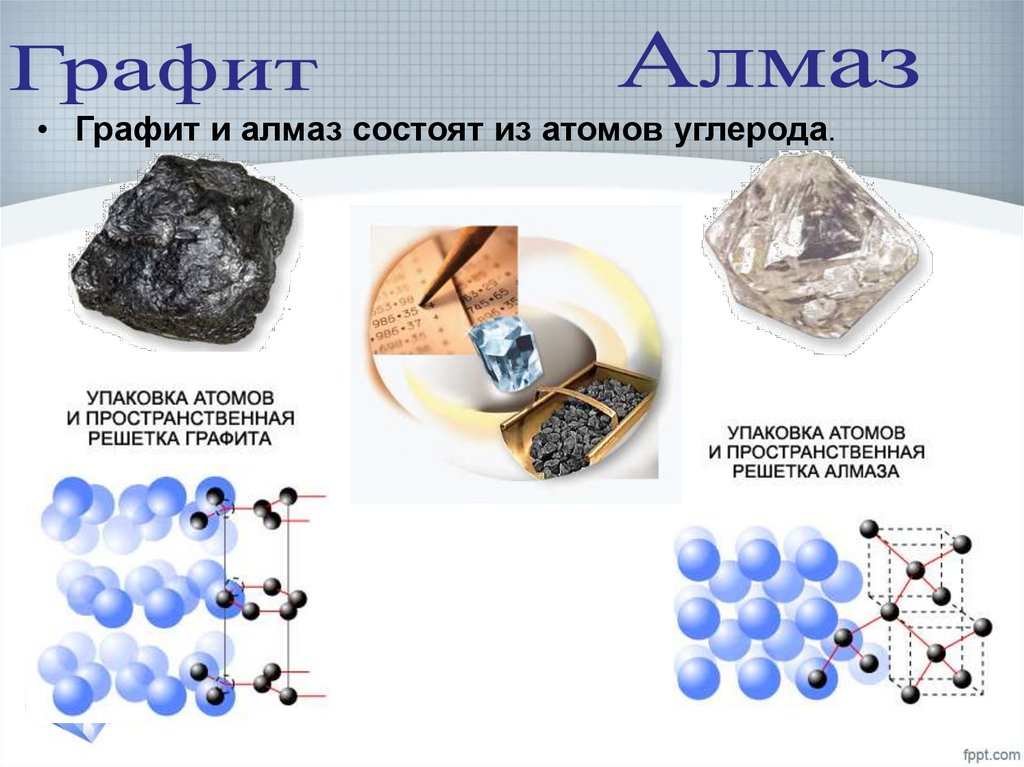
17.
• Графит и алмаз состоят из атомов углерода.18. МОЛЕКУЛЯРНЫЕ КРИСТАЛЛИЧЕСКИЕ РЕШЕТКИ Свойства веществ:
• В узлах располагаются молекулы веществ.• Связи между молекулами веществ слабые, легко
разрушаются
• Вещества с молекулярной кристаллической решеткой
имеют:
• малую твёрдость,
• плавятся при низкой температуре,
• летучие,
• при обычных условиях находятся в газообразном,
жидком (О2, N2, СО2, Н2О) твердом состоянии.
Кристаллическая решетка йода
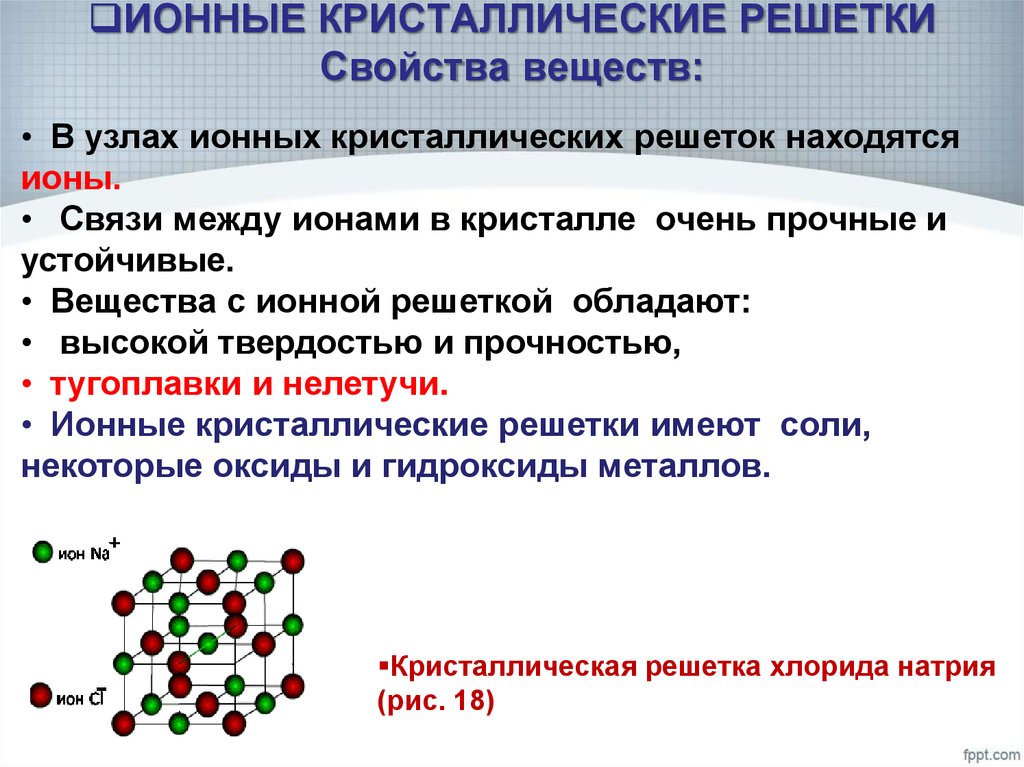
19. ИОННЫЕ КРИСТАЛЛИЧЕСКИЕ РЕШЕТКИ Свойства веществ:
• В узлах ионных кристаллических решеток находятсяионы.
• Связи между ионами в кристалле очень прочные и
устойчивые.
• Вещества с ионной решеткой обладают:
• высокой твердостью и прочностью,
• тугоплавки и нелетучи.
• Ионные кристаллические решетки имеют соли,
некоторые оксиды и гидроксиды металлов.
Кристаллическая решетка хлорида натрия
(рис. 18)
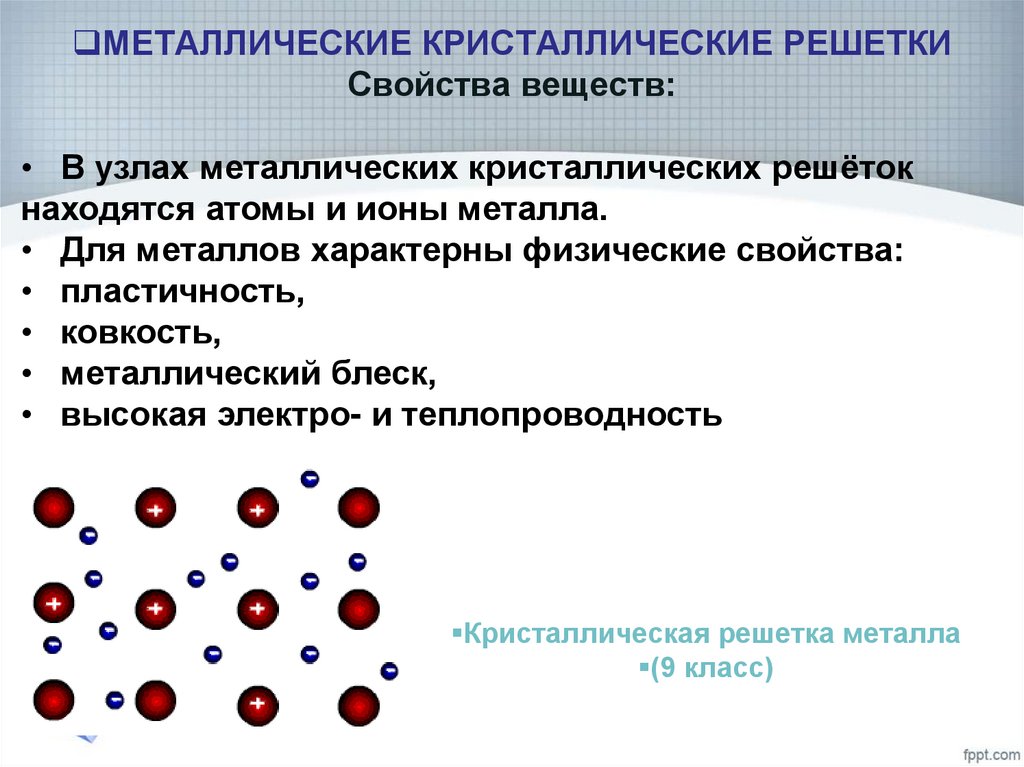
20. МЕТАЛЛИЧЕСКИЕ КРИСТАЛЛИЧЕСКИЕ РЕШЕТКИ Свойства веществ:
• В узлах металлических кристаллических решётокнаходятся атомы и ионы металла.
• Для металлов характерны физические свойства:
• пластичность,
• ковкость,
• металлический блеск,
• высокая электро- и теплопроводность
Кристаллическая решетка металла
(9 класс)
21. Кристаллические решетки
Амо́рфные вещества́ (тела́)(от греческого ἀ «не- отрицание» и морфе - «вид,
форма»)
Амо́рфные вещества́ не имеют четкой
(постоянной) температуры плавления – при
нагревании они постепенно размягчаются и
переходят в текучее состояние
Способны переходить в кристаллическое и
жидкое состояние.
22. Аморфные вещества
Это твёрдые тела, у которых нет строгого порядка врасположении атомов,
Не имеют кристаллического строения,
Обладают текучестью
при низких температурах они ведут себя подобно
кристаллическим телам, а при высокой подобны
жидкостям.
кремнезём, смола,
стекло, канифоль,
сахарный леденец
• янтарь
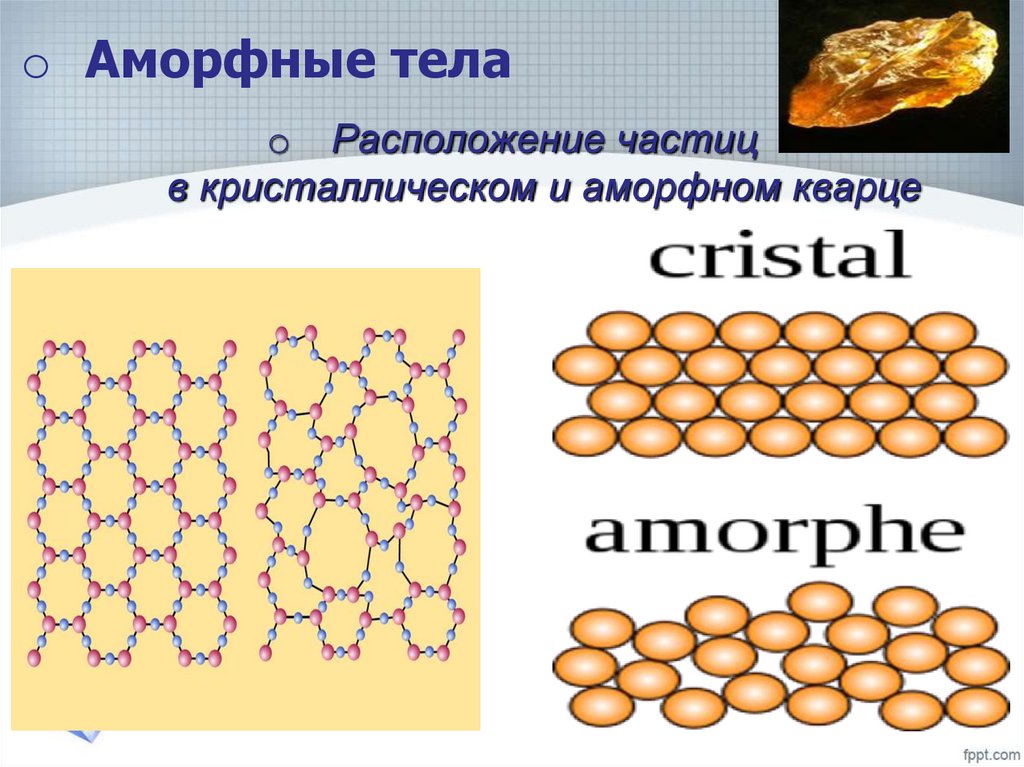
23. Расположение частиц в кристаллическом и аморфном кварце
o Аморфные телаo Расположение частиц
в кристаллическом и аморфном кварце
24.
25. Применение кристаллических и аморфных тел
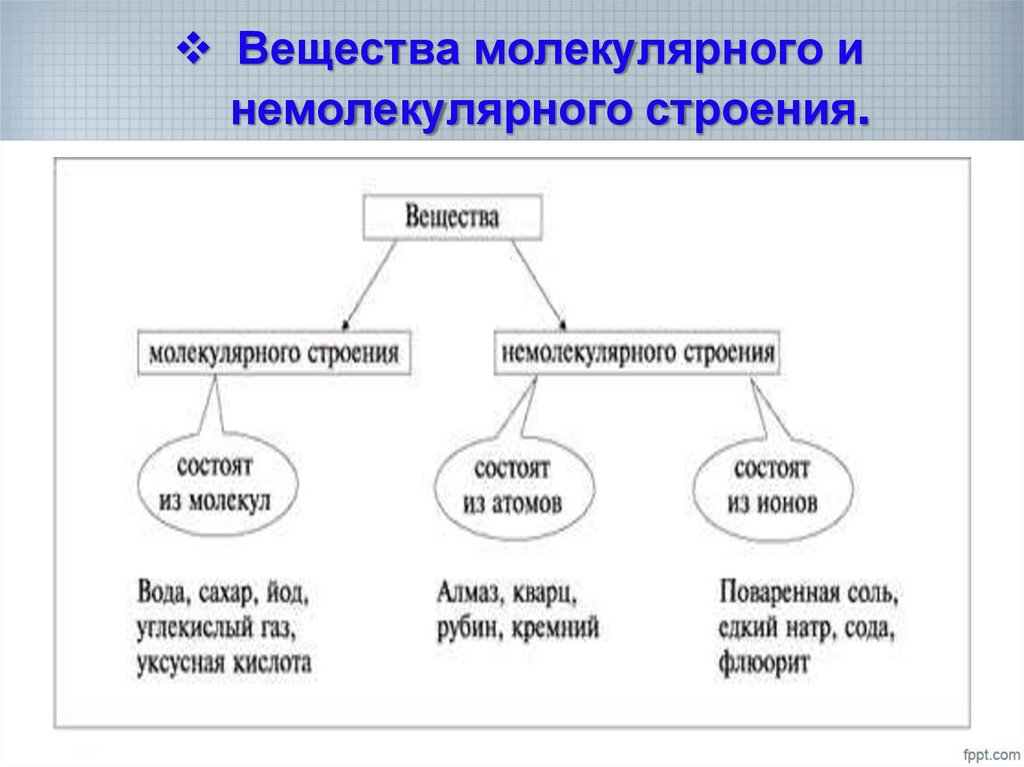
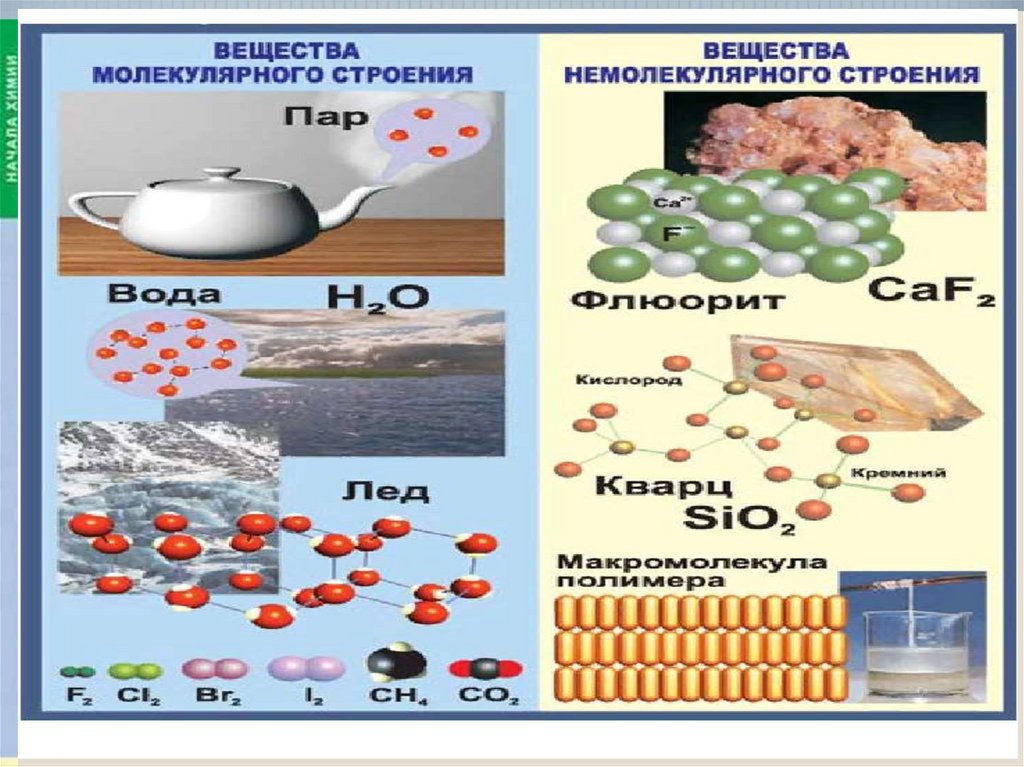
26. Вещества молекулярного и немолекулярного строения.
27.
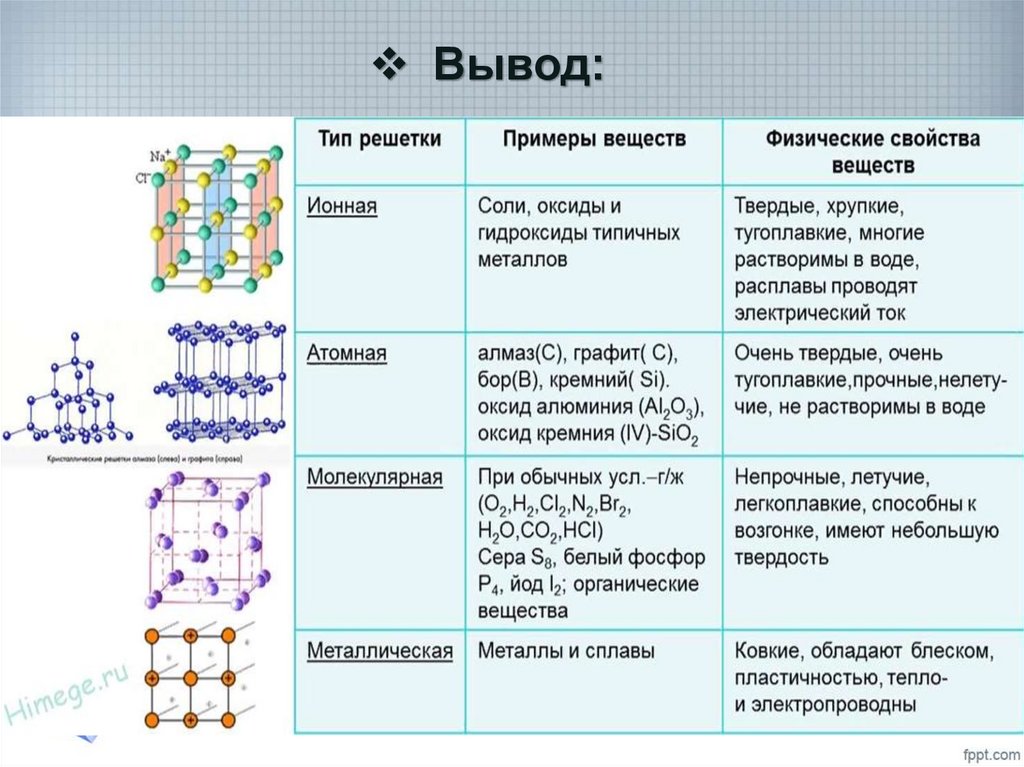
28. Вывод:
• Вещества молекулярного и немолекулярногостроения отличаются по своим свойствам.
• Физические свойства веществ зависят от
строения кристаллической решетки.














 chemistry
chemistry








