Similar presentations:
Коллоидная химия. Коллоидные ПАВ (лекция 9)
1.
Коллоидная химияИТХТ им. М.В. Ломоносова
кафедра НС и ПЯ
группы ХХБО-01-03-2022
ХТБО-01-2022
ЛЕКЦИЯ 9
Шубенкова Екатерина Гаррьевна
2.
Коллоидная химияЛЕКЦИЯ 9
КОЛЛОИДНЫЕ ПАВ.
2023
Шубенкова Е.Г.
3.
План лекции:1. Классификация ПАВ по химическому строению.
Понятие о гидрофильно-липофильном балансе (ГЛБ).
2. Количественные характеристики свойств ПАВ. Числа
ГЛБ. Расчет чисел ГЛБ по методу Дэвиса.
3. Мицеллообразование, строение мицелл в водной и
углеводородной среде. Термодинамика образования
прямых и обратных мицелл.
4. Солюбилизация в водных мицеллярных растворах ПАВ.
Микроэмульсии.
5. Критическая концентрация мицеллообразования (ККМ).
Методы определения ККМ. Влияние различных факторов
на величину ККМ в полярных и неполярных средах.
6. Влияние температуры на растворимость ионогенных
ПАВ. Диаграмма состояния системы. Точка Крафта.
7. Влияние температуры на растворимость неионогенных
ПАВ. Точка помутнения и точка высаливания.
4.
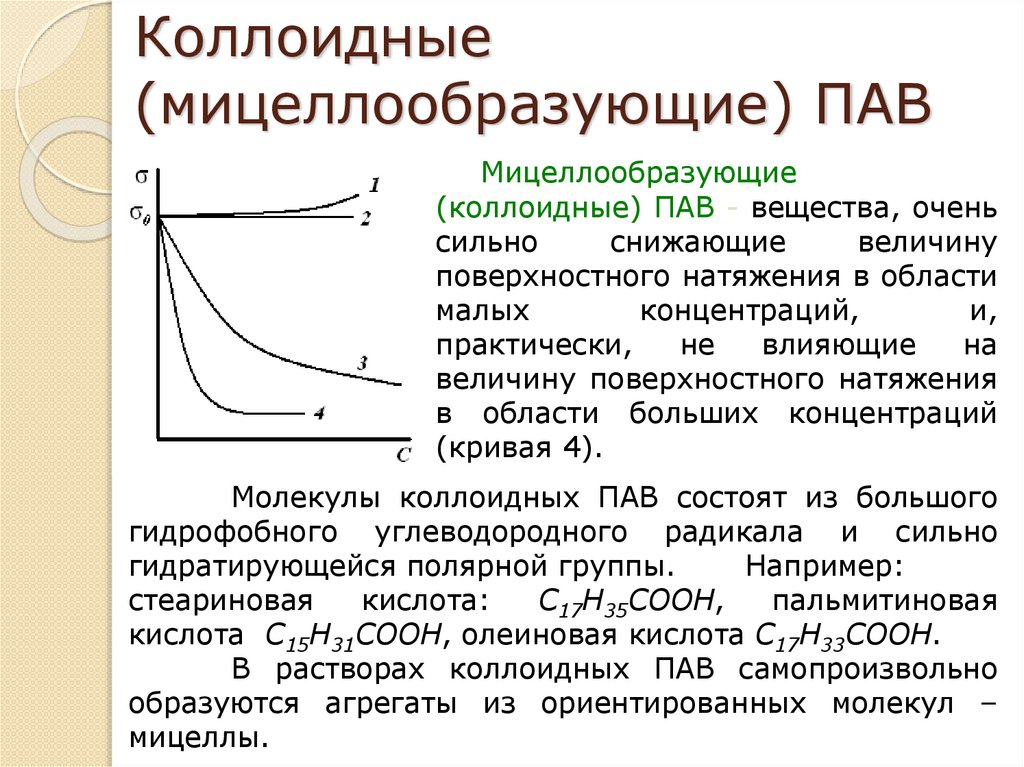
Коллоидные(мицеллообразующие) ПАВ
Мицеллообразующие
(коллоидные) ПАВ - вещества, очень
сильно
снижающие
величину
поверхностного натяжения в области
малых
концентраций,
и,
практически,
не
влияющие
на
величину поверхностного натяжения
в области больших концентраций
(кривая 4).
Молекулы коллоидных ПАВ состоят из большого
гидрофобного углеводородного радикала и сильно
гидратирующейся полярной группы.
Например:
стеариновая
кислота:
С17Н35СООН,
пальмитиновая
кислота С15Н31СООН, олеиновая кислота С17Н33СООН.
В растворах коллоидных ПАВ самопроизвольно
образуются агрегаты из ориентированных молекул –
мицеллы.
5.
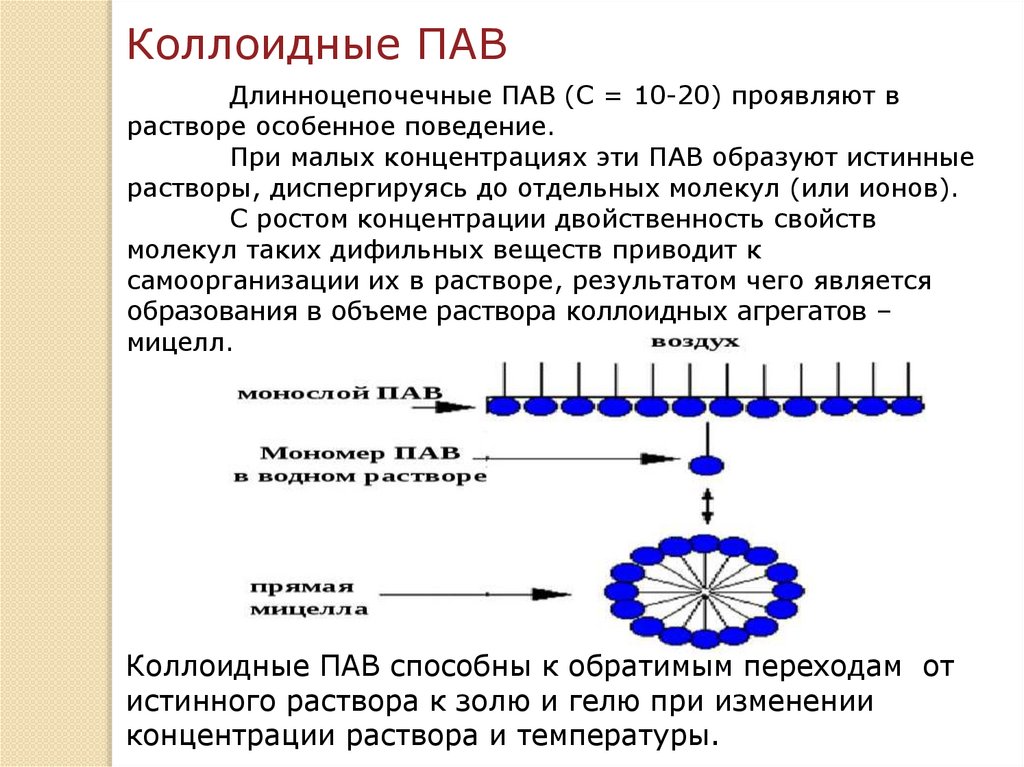
Коллоидные ПАВДлинноцепочечные ПАВ (С = 10-20) проявляют в
растворе особенное поведение.
При малых концентрациях эти ПАВ образуют истинные
растворы, диспергируясь до отдельных молекул (или ионов).
С ростом концентрации двойственность свойств
молекул таких дифильных веществ приводит к
самоорганизации их в растворе, результатом чего является
образования в объеме раствора коллоидных агрегатов –
мицелл.
Коллоидные ПАВ способны к обратимым переходам от
истинного раствора к золю и гелю при изменении
концентрации раствора и температуры.
6.
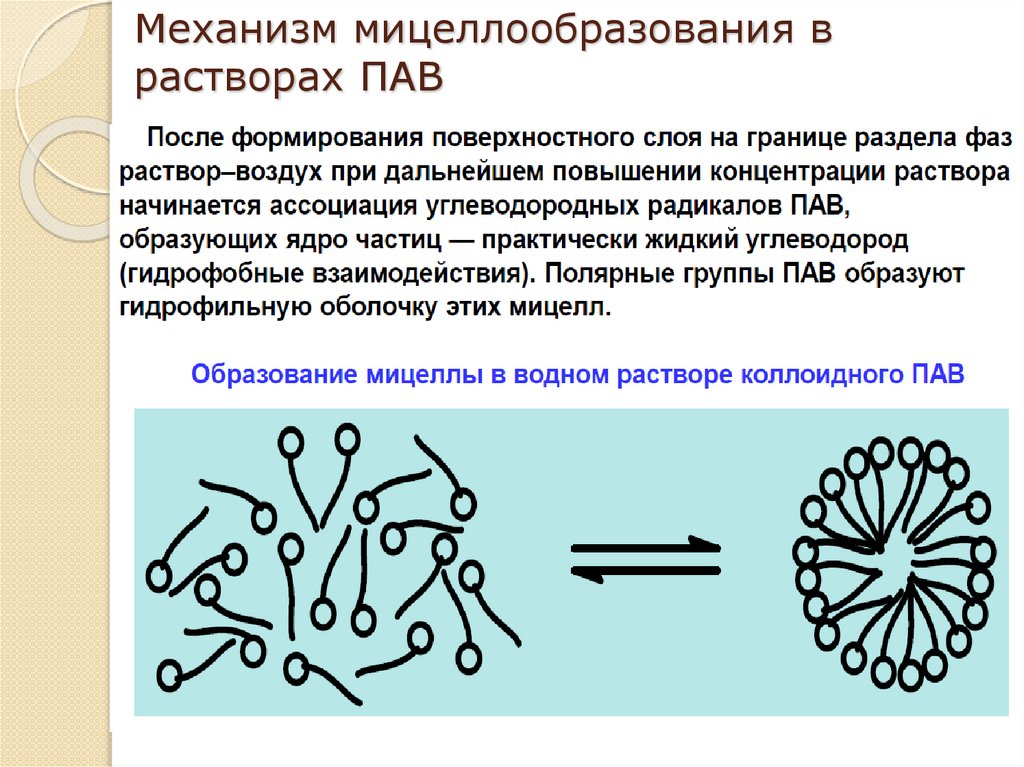
Механизм мицеллообразования врастворах ПАВ
7.
Мицеллообразование врастворах ПАВ
Мицелла - ассоциат дифильных молекул, лиофильные
группы которых обращены к растворителю, а лиофобные
группы собираются вместе, образуя ядро мицеллы.
Прямые мицеллы - мицеллы
ПАВ, образующиеся в водной среде
(гидрофильные
полярные
группы
снаружи,
а
гидрофобные
углеводородные радикалы – внутри).
Обратные мицеллы - мицеллы
ПАВ, образующиеся в неполярной
жидкости
(гидрофильные
полярные
группы
внутри,
а
гидрофобные
углеводородные радикалы – снаружи).
8.
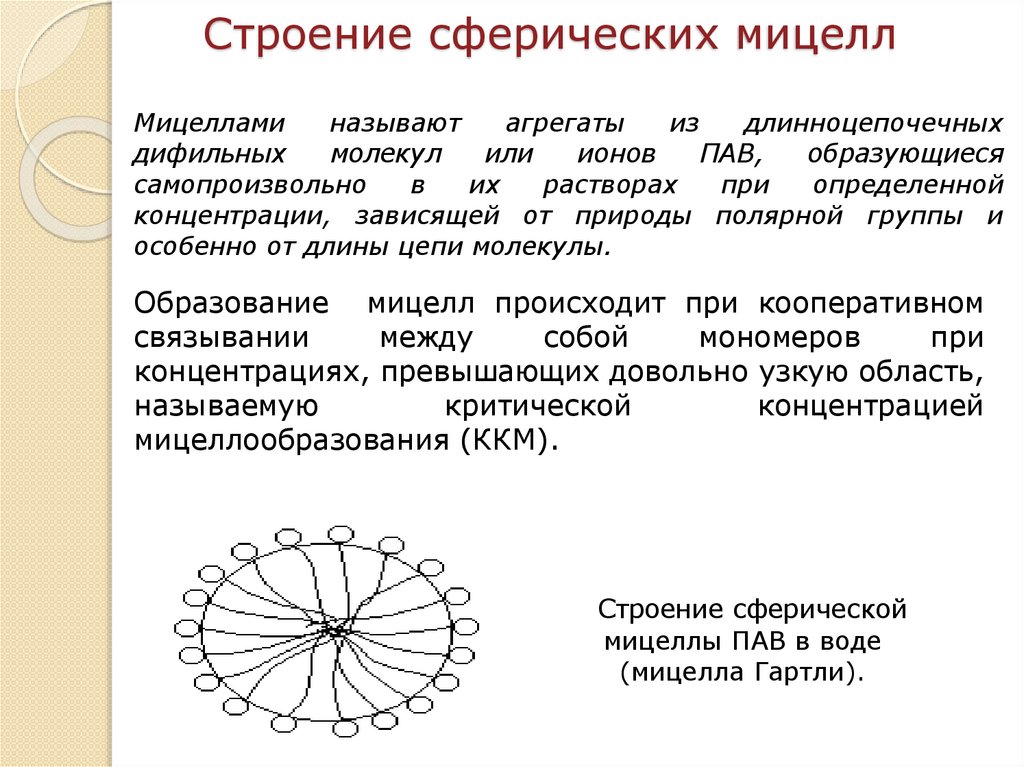
Строение сферических мицеллМицеллами
называют
агрегаты
из
длинноцепочечных
дифильных
молекул
или
ионов
ПАВ,
образующиеся
самопроизвольно
в
их
растворах
при
определенной
концентрации, зависящей от природы полярной группы и
особенно от длины цепи молекулы.
Образование мицелл происходит при кооперативном
связывании
между
собой
мономеров
при
концентрациях, превышающих довольно узкую область,
называемую
критической
концентрацией
мицеллообразования (ККМ).
Строение сферической
мицеллы ПАВ в воде
(мицелла Гартли).
9.
Критическая концентрациямицеллообразования
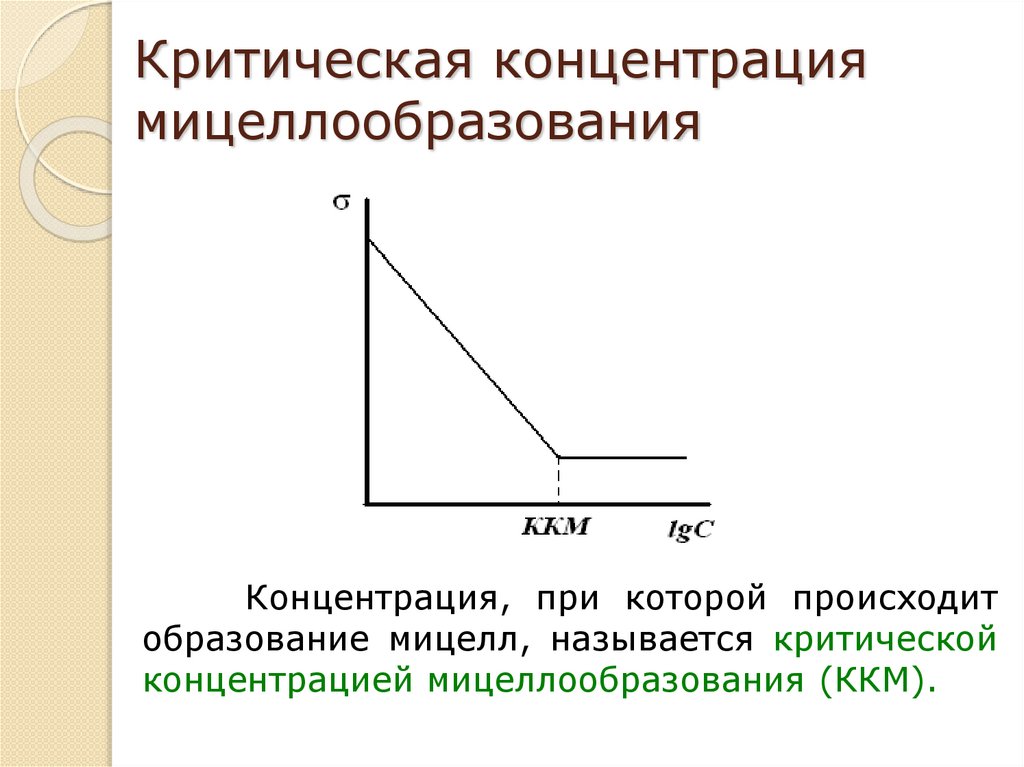
Концентрация, при которой происходит
образование мицелл, называется критической
концентрацией мицеллообразования (ККМ).
10.
Критическая концентрациямицеллообразования
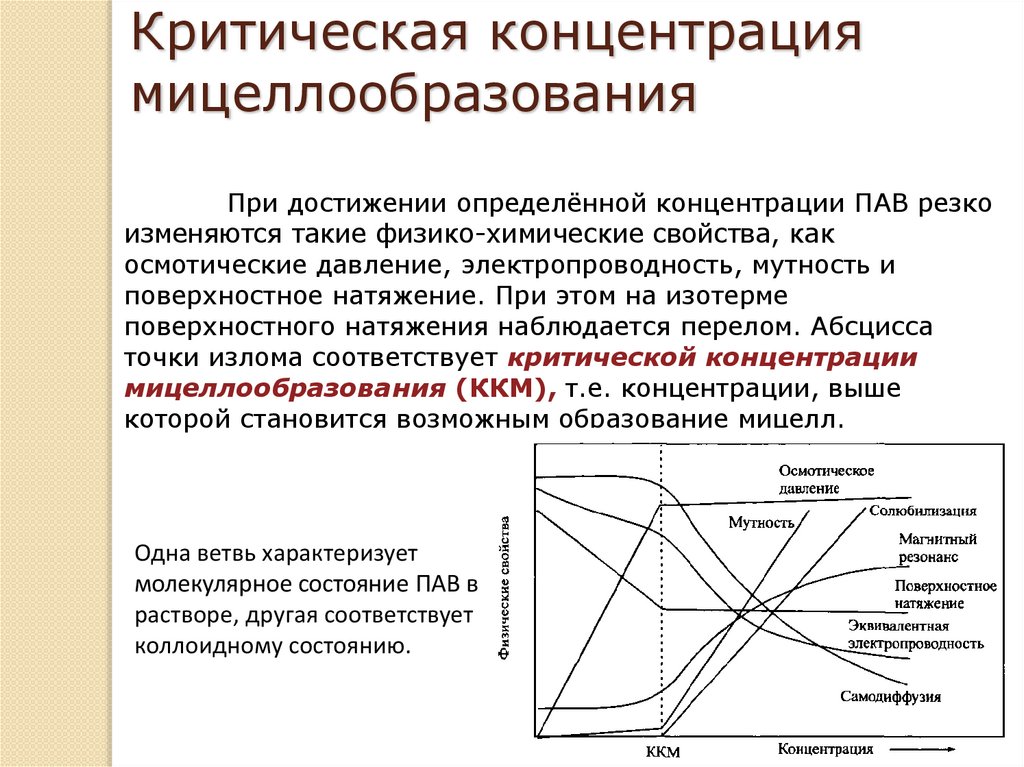
При достижении определённой концентрации ПАВ резко
изменяются такие физико-химические свойства, как
осмотические давление, электропроводность, мутность и
поверхностное натяжение. При этом на изотерме
поверхностного натяжения наблюдается перелом. Абсцисса
точки излома соответствует критической концентрации
мицеллообразования (ККМ), т.е. концентрации, выше
которой становится возможным образование мицелл.
Одна ветвь характеризует
молекулярное состояние ПАВ в
растворе, другая соответствует
коллоидному состоянию.
11.
Мицеллы образуют только ПАВ, обладающиеоптимальным соотношением между гидрофобной и
гидрофильной частями, т.е. величиной гидрофильнолипофильного баланса (ГЛБ). Истинная растворимость
таких ПАВ невелика ~10-3 моль/л.
ККМ – наиболее важная характеристика ПАВ, связанная
с гидрофильно-липофильным балансом молекул ПАВ и
использующаяся при рассмотрении всех вопросов
практического использования ПАВ.
Величина ККМ зависит от:
• строения молекулярного ПАВ;
• присутствия в растворе различных
веществ;
• температуры.
12.
При равном количестве углеродных атомовкооперативность уменьшается, ККМ растет:
При циклизации цепи:
для n-тетрадецилсульфонат натрия С14Н29SО3Na ККМ=2,5ммоль/л,
для n-октибензолсульфонат натрия C8H17C6H4SO3Na ККМ=11 ммоль/л.
При введении в углеводородный радикал двойных связей,
полярных групп:
(стеарат натрия C17H35COONa – 0,18 моль/м3;
олеат натрия С8Н17СН=СН(СН2)7СООNa – 1,1 моль/л.
Увеличение ККМ связано с тем, что введение ароматических
циклов, кратных связей, полярных групп, гетероатомов приводит к
уменьшению гидрофобности радикала.
При переходе к перфторуглеродной цепи наблюдается
резкое снижение ККМ:
Величина ККМ октилсульфоната натрия С8Н17SО3Na составляет
177 моль/ м3, а для перфтороктилсульфоната С8F17SО3Na ККМ 8,5 моль/ м3.
Это связано с тем, что фторированные ПАВ значительно более
гидрофобны и обладают высокой поверхностной активностью, чем
углеводородные аналоги.
13.
Введение электролитов в раствор ПАВ всегда снижаетвеличину ККМ
• электролит частично дегидратирует полярные группы ионов
ПАВ, т. к. связывает воду за счет гидратации своих ионов.
Понижение гидратации ионов ПАВ повышает их склонность к
ассоциации.
• добавленный электролит понижает эффективную степень
диссоциации
поверхностно-активного
вещества,
как
в
истинном растворе, так и в мицеллярном состоянии.
Характер влияния зависит от размера углеводородного
радикала органического вещества.
Длинноцепочечные спирты понижают ККМ, причем
степень
снижения
увеличивается
при
увеличении
молекулярной массы спирта. Увеличенный размер мицелл и
вязкость растворов ПАВ объясняются образованием смешанных
мицелл ПАВ + спирт.
Низкомолекулярные добавки (метанол, ацетон, диоксан)
повышают ККМ и понижают мицеллярную массу коллоидных
ПАВ.
14.
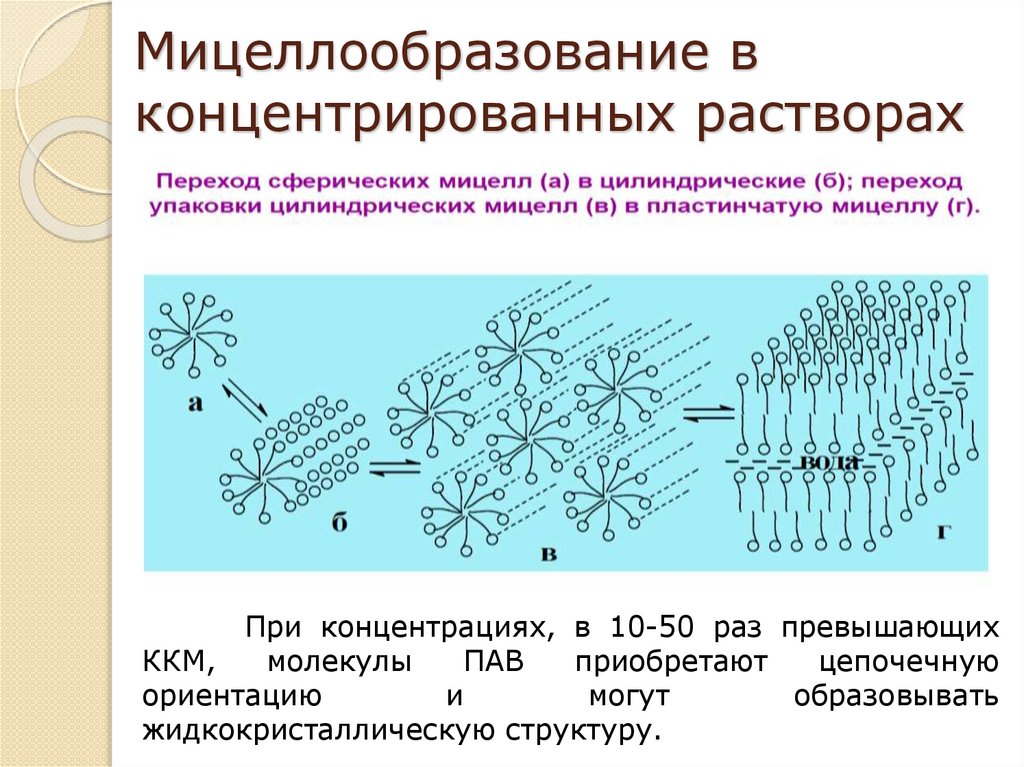
Мицеллообразование вконцентрированных растворах
При концентрациях, в 10-50 раз превышающих
ККМ,
молекулы
ПАВ
приобретают
цепочечную
ориентацию
и
могут
образовывать
жидкокристаллическую структуру.
15.
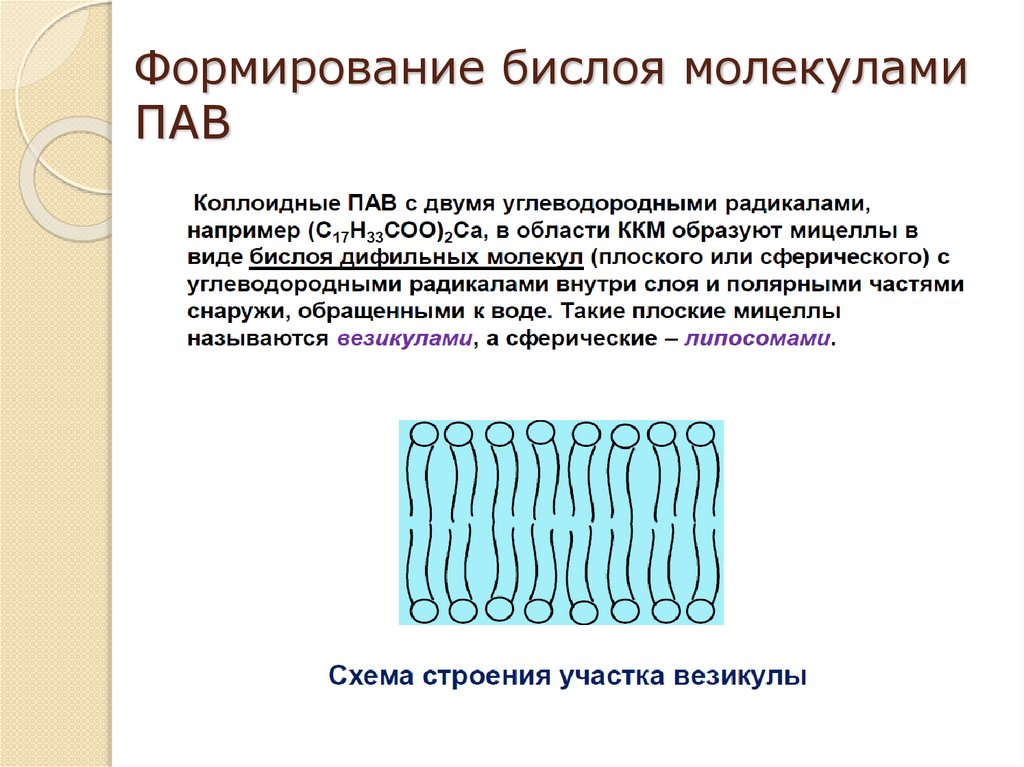
Формирование бислоя молекуламиПАВ
16.
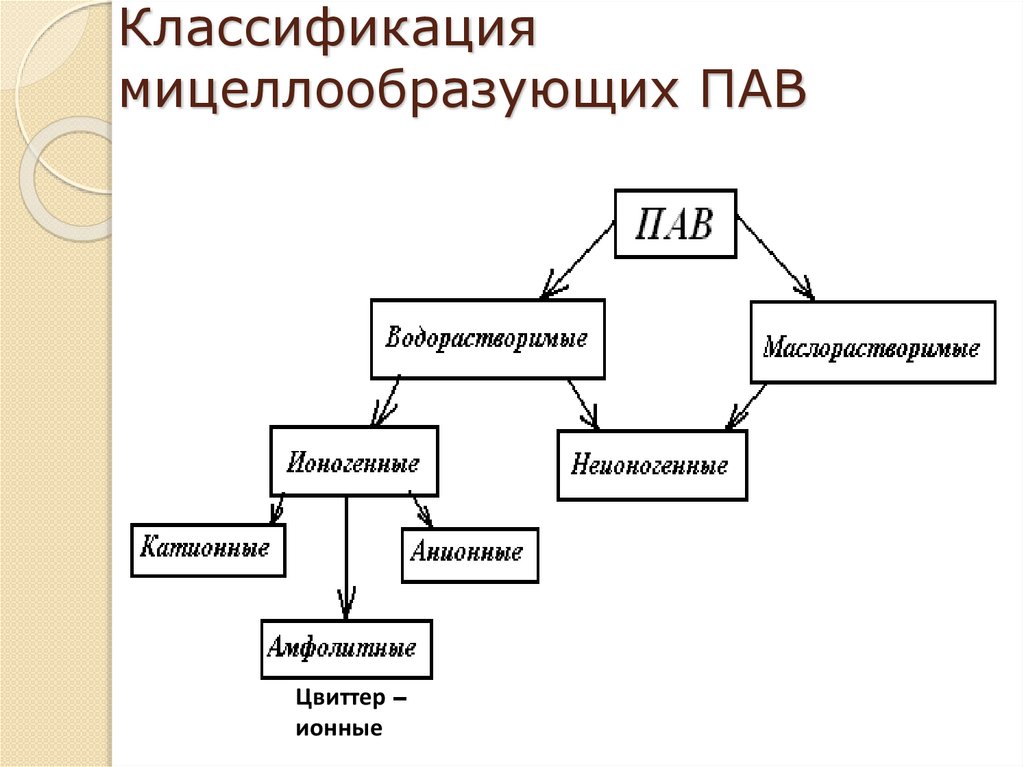
Классификациямицеллообразующих ПАВ
Цвиттер –
ионные
17.
Классификация мицеллообразующих ПАВКоллоидные поверхностно-активные вещества (ПАВ)
состоят из ассиметричных молекул с одной или несколькими
гидрофильными группами и гидрофобным радикалом.
Неионогенные
Анионные
Катионные
Амфолитные
18.
Классификация мицеллообразующих ПАВАнионные, диссоциируя в воде, образуют анион с крупным углеводородным
радикалом, обладающим поверхностной активностью, при этом катион не
является поверхностно-активным на границе вода-воздух.
Анионные ПАВ содержат гидрофильные функциональные группы:
-СОО-;
–SО3-;
–SО4-;
Например: RCOO- Me+;
Катионные ПАВ, наоборот, диссоциируют с образованием катиона,
обладающего поверхностной активностью.
Катионные ПАВ содержат гидрофильные функциональные группы:
-N(CH3)3+; -NH3+
Например RNH3+ Cl-
Неионогенные ПАВ не диссоциируют в воде.
Неионогенные ПАВ содержат гидрофильные функциональные группы:
-ОН; (CH2-CH2-O)H
К НПАВ относятся продукты присоединения окиси этилена к веществам с
развитыми углеводородными радикалами; оксиэтилированные спирты.
Амфолитные ПАВ содержат в молекуле кислотную (карбоксильную) и
основную (амино) группы. В зависимости от рН могут проявлять себя как
анионные и катионные ПАВ. К ним относятся аминокислоты и белки.
19.
Термодинамика мицеллообразования вводной среде
Мицеллообразование в растворах ПАВ происходит
самопроизвольно
и
сопровождается
уменьшением
свободной энергии Гиббса ∆G, которое складывается из
энтальпийного и энтропийного членов:
∆G=∆H - T∆S
Знак при ∆G будет определяться соотношением этих
членов.
Экспериментально установлено, что энтальпия
мицеллообразования ионногенных ПАВ невелика (3-4
кДж/моль) и может принимать как положительные
значения, так и в некоторых случаях (например для
алканоатов калия (с С10 – С14)) практически равна
нулю. В случае неионных ПАВ ∆H больше и всегда
положительно, т. е. мицеллообразование происходит с
поглощением тепла.
Решаюшую роль в протекании самопроизвольной
ассоциации ПАВ в мицеллы играет энтропийный вклад
в изменение энергии Гиббса.
20.
Положительный энтропийный эффект примицеллообразовании
Движущей силой мицеллобразования является
увеличение энтропии системы.
Рассмотрим изменение энтропии всей системы (ПАВ и
воды):
∆Sсист. = ∆Sмиц. + ∆Sводы
При объединении молекул ПАВ в мицеллу энтропия
мицелообразования уменьшается, т.к. число степеней свободы
ПАВ уменьшается.
Вода является сильно ассоциированной структурированной
жидкостью с упорядоченной
тетраэдрической льдоподобной
структурой.
При растворении в воде углеводородов и углеводородных
радикалов ПАВ за счет гидрофобных взаимодействий структура
воды становится более упорядоченной. Это подтверждено
изменением диэлектрических свойств растворов, расширением
линий
ЯМР,
снижением
коэффициента
самодиффузии.
Увеличение структурированности
воды предопределяет
притяжение гидрофобных частиц.
Когда молекулы ПАВ образуют мицеллу, водородные связи
в воде разрушаются, молекулы воды приобретают больше
степеней свободы, и энтропия воды, а значит, и всей системы
увеличивается.
21.
Образование лиофильных коллоидных системОбразование лиофильных дисперсных происходит
самопроизвольно, с уменьшением свободной энергии:
ΔF= ΔU + ΔS12 σ12 - TΔS <0
При диспергировании:
•Объем системы не меняется (V=const), следовательно ΔU =0;
•Площадь границы раздела фаз возрастает - ΔS12 >0
•Энтропия системы увеличивается – ΔS>0
Таким образом, самодиспергирование будет происходить
при условии, что
ΔS12 σ12 < TΔS
•изменение площади пропорционально числу частиц n и их
размеру a: ΔS12 ~ na2
•изменение энтропии пропорционально кинетической энергии
частиц: TΔS~nγkT, γ-безразмерный коэффициент
na2 σ12 < nγkT,
Условие самопроизвольного образования дисперсных
систем:
σ 12 < σcryt , где σcryt = γkT/a2
Малое значение σ 12 возможно только при сильном
взаимодействии двух фаз, на практике такое достигается лишь
22.
Зависимость растворимости ионогенных ПАВ вводе от температуры
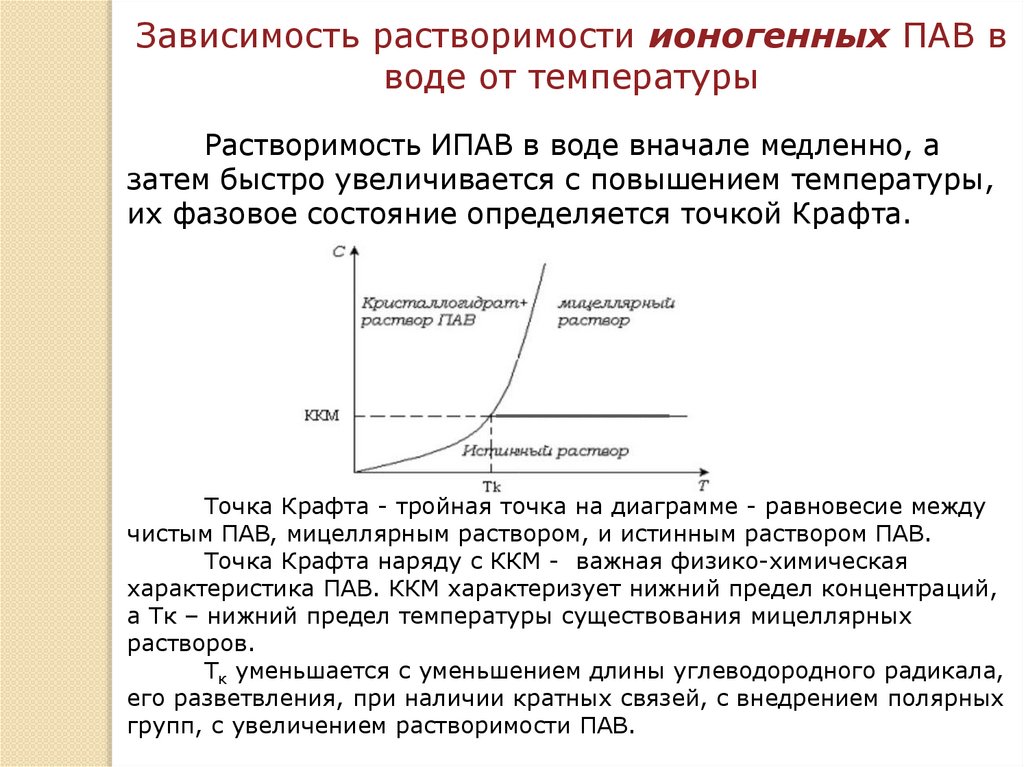
Растворимость ИПАВ в воде вначале медленно, а
затем быстро увеличивается с повышением температуры,
их фазовое состояние определяется точкой Крафта.
Точка Крафта - тройная точка на диаграмме - равновесие между
чистым ПАВ, мицеллярным раствором, и истинным раствором ПАВ.
Точка Крафта наряду с ККМ - важная физико-химическая
характеристика ПАВ. ККМ характеризует нижний предел концентраций,
а Тк – нижний предел температуры существования мицеллярных
растворов.
Тк уменьшается с уменьшением длины углеводородного радикала,
его разветвления, при наличии кратных связей, с внедрением полярных
групп, с увеличением растворимости ПАВ.
23.
Растворимость неионогенных ПАВРастворы неионогенных ПАВ
обладают специфической способностью
существенно изменять свои физикохимические свойства при нагревании.
Неионогенные ПАВ оксиэтилированные жирные спирты
общей формулы R(OCH2CH2)nOH
(например ситанол).
Растворимость
НПАВ
уменьшается
с
повышением
температуры, для них характерна точка помутнения.
Растворимость
оксиэтилированных
ПАВ
обусловлена
образованием гидратов вследствие возникновения водородных
связей. При нагревании происходит дегидратация молекул ПАВ,
т.е. уменьшение их растворимости, что приводит к агрегации
молекул и к появлению опалесценции, а затем и к помутнению
раствора.
При дальнейшем нагревании этого раствора происходит
укрупнение частиц вплоть до выделения капелек ПАВ в виде
отдельной фазы, то есть их “высаливание”.
24.
Оценка дифильных свойств ПАВОдной из характеристик дифильных свойств ПАВ является
гидрофильно-липофильный баланс (ГЛБ), характеризующий
соотношение масс гидрофильной полярной группы и
липофильного радикала.
Шкала чисел ГЛБ была предложена Гриффином в 1949 г.
ГЛБ является эмпирической величиной, для олеиновой
кислоты ГЛБ выбрано равным 1, для олеата натрия- 18, чем
выше гидрофильность, тем выше число ГЛБ, которое изменяется
от 1 до 40.
Число ГЛБ рассчитывают по формуле:
Где ГЛБ см – число ГЛБ смеси ПАВ, обеспечивающее получение
устойчивой эмульсии стандартного масла, WA – количество эмульгатора
А с известным ГЛБ, WB – количество эмульгатора с известным ГЛБ.
При значении ГЛБ от 1 до 4, ПАВ не растворяются и не диспергируются в
воде, при значении от 8 до 10 образуют в воде стабильные дисперсии
типа молока, а выше 13 – прозрачные растворы.
По значению ГЛБ можно определить область применения
ПАВ: эмульгаторы - 3÷6, смачиватели - 7÷9, моющие вещества 13 ÷15.
25.
Метод ДэвисаЧисло ГЛБ для данного ПАВ можно рассчитать по аддитивной
формуле, зная числа ГЛБ для каждой структурной единицы.
ГЛБ ПАВ=7+∑(ГЛБ)Г + ∑(ГЛБ)Л
(Метод Девиса)
Значения чисел ГЛБ для некоторых групп
Числа ГЛБ для некоторых распространенных ПАВ
26.
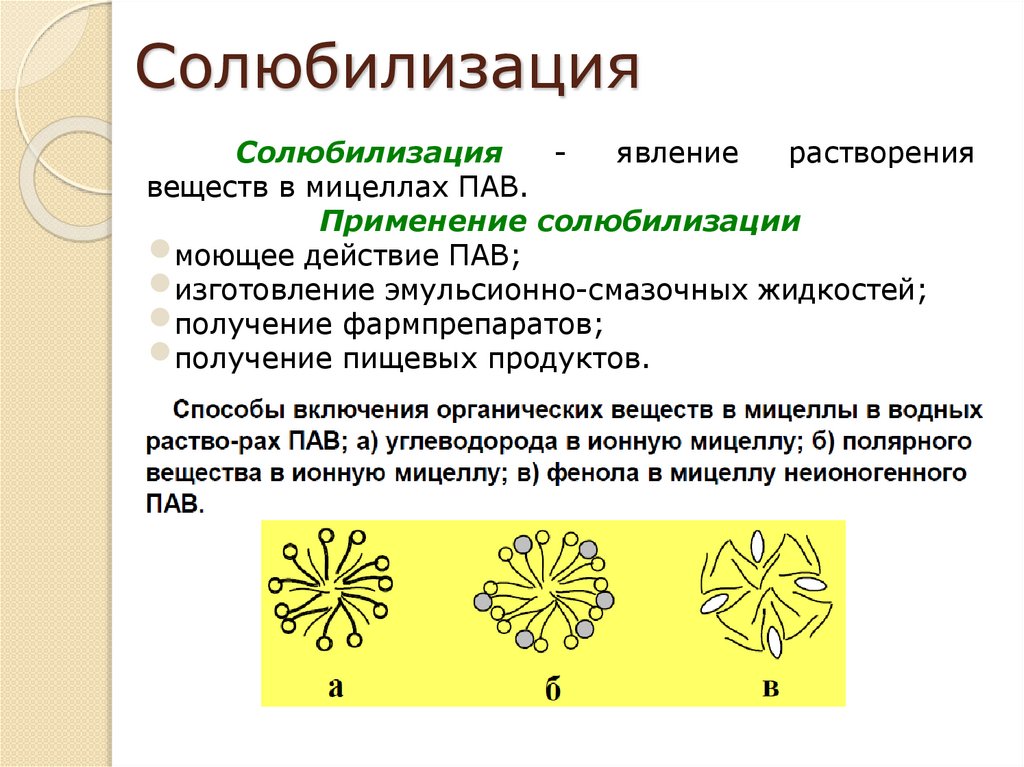
СолюбилизацияСолюбилизация
явление
растворения
веществ в мицеллах ПАВ.
Применение солюбилизации
моющее действие ПАВ;
изготовление эмульсионно-смазочных жидкостей;
получение фармпрепаратов;
получение пищевых продуктов.
27.
CолюбилизацияПод солюбилизацией понимают растворение
слабо
растворимых
в
обычных
условиях
в
дисперсионной среде веществ (жидких, твердых,
газообразных) за счет их перераспределения в мицеллы
и им подобные агрегаты ПАВ с образованием
термодинамически и агрегативно устойчивого раствора.
Вещество, солюбилизированное раствором
ПАВ, называют солюбилизатом, а ПАВ —
солюбилизатором.
Явление солюбилизации представляет как
большой теоретический интерес, так и находит широкое
практическое применение.
В прямых мицеллах ПАВ растворяются
маслорастворимые красители и углеводороды.
В обратных мицеллах растворяются
водорастворимые красители, вода, электролиты.
28.
Способы включения молекулолеофильных добавок в прямые
сферические мицеллы ПАВ
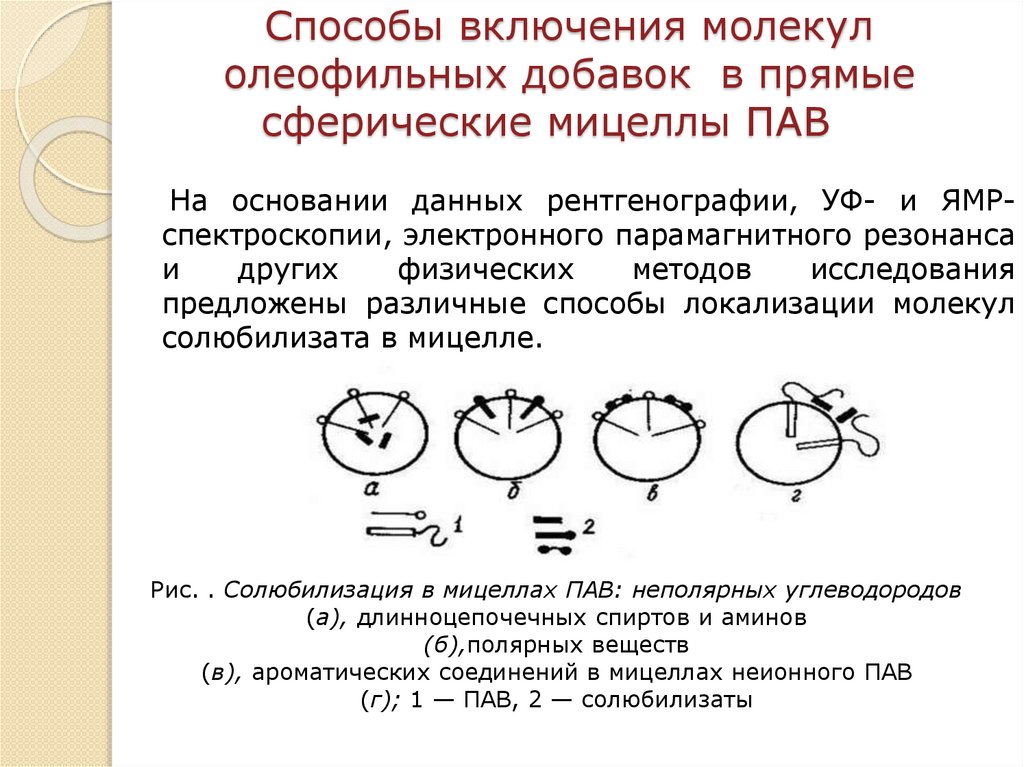
На основании данных рентгенографии, УФ- и ЯМРспектроскопии, электронного парамагнитного резонанса
и
других
физических
методов
исследования
предложены различные способы локализации молекул
солюбилизата в мицелле.
Рис. . Солюбилизация в мицеллах ПАВ: неполярных углеводородов
(а), длинноцепочечных спиртов и аминов
(б),полярных веществ
(в), ароматических соединений в мицеллах неионного ПАВ
(г); 1 — ПАВ, 2 — солюбилизаты
29.
1. Влияние длины углеводородного радикалаСолюбизирующая
способность
растворов
ПАВ
увеличивается во всех случаях, когда те или иные
изменения молекулярной структуры приводят к повышению
гидрофобных свойств их молекул.
Молярная солюбилизация растворов ПАВ возрастает при
увеличении длины углеводородного радикала.
2. Строение углеводородного радикала
Солюбилизирующая способность снижается при введении в
углеводородный радикал полярных групп, кратных связей,
гетероатомов, т. е. при снижении его гидрофобности.
3. Добавки электролитов и неэлектролитов
Влияние различных добавок на солюбилизацию обусловлено
воздействием их на свойства мицелл (размер, форму,
степень диссоциации и гидратации полярных групп).
Введение электролитов в растворы коллоидных ПАВ
вызывает понижение их эффективной степени диссоциации
и гидратации, т. е. происходит гидрофобизация мицелл.
Солюбилизация
неполярных
веществ
при
введении
электролитов обычно заметно возрастает.
30.
Природа солюбилизатаВнутримицеллярная
растворимость
органических
веществ зависит от их олеофильности, на которую
влияет длина углеводородной цепи, циклизация,
разветвление, наличие полярных групп, кратных
связей.
Солюбилизация повышается при уменьшении
олеофильности растворяемого вещества.
Внутримицеллярная растворимость углеводородов
при прочих равных условиях повышается:
при уменьшении длины цепи у нормальных
парафинов или алкильного заместителя в бензольном
кольце (н-гептан > н-октан; толуол > этилбензол);
при циклизации углеводородной цепи и с
появлением ароматического цикла (толуол > нгептан; этилбензол > н-октан).
при разветвлении углеводородного радикала.
31.
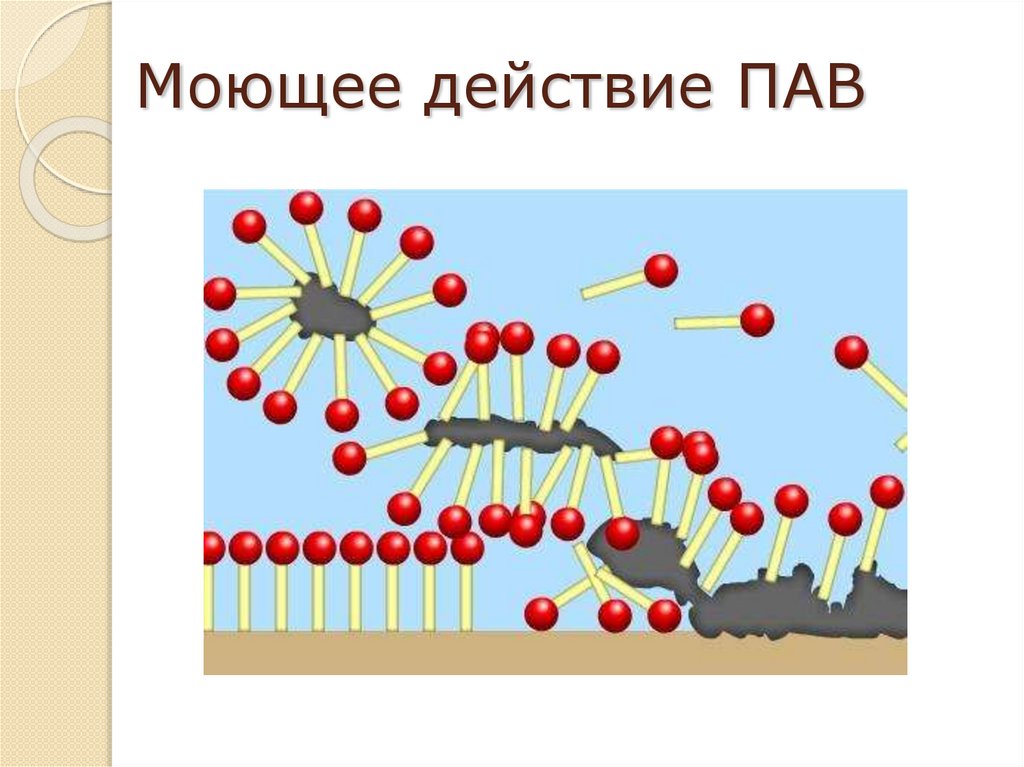
Механизм и основные стадиимоющего действия
По теории Ребиндера можно различить четыре основных
стадии в механизме моющего действия, которым
предшествует
растворение
водорастворимых
загрязнителей.
смачивание загрязненных изделий раствором моющего
вещества;
образование адсорбционных слоев на поверхности
ткани и загрязнителей и перевод последних в
активированное состояние, в результате чего
происходит измельчение частиц;
удаление
загрязнителей
с
поверхности
диспергированием (в результате эмульгирования,
суспендирования, пенообразования и солюбилизации
жидких нерастворимых в воде компонентов);
стабилизация
дисперсий
загрязнений
и
предотвращение их обратного осаждения на ткани.
32.
Моющее действие ПАВ33.
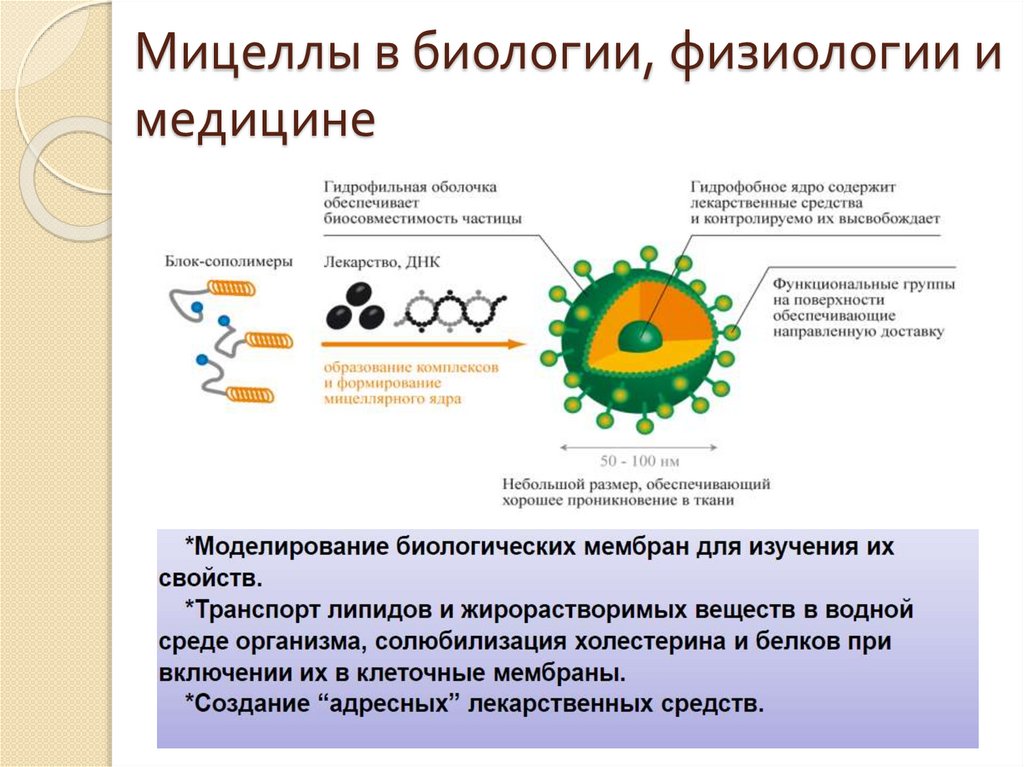
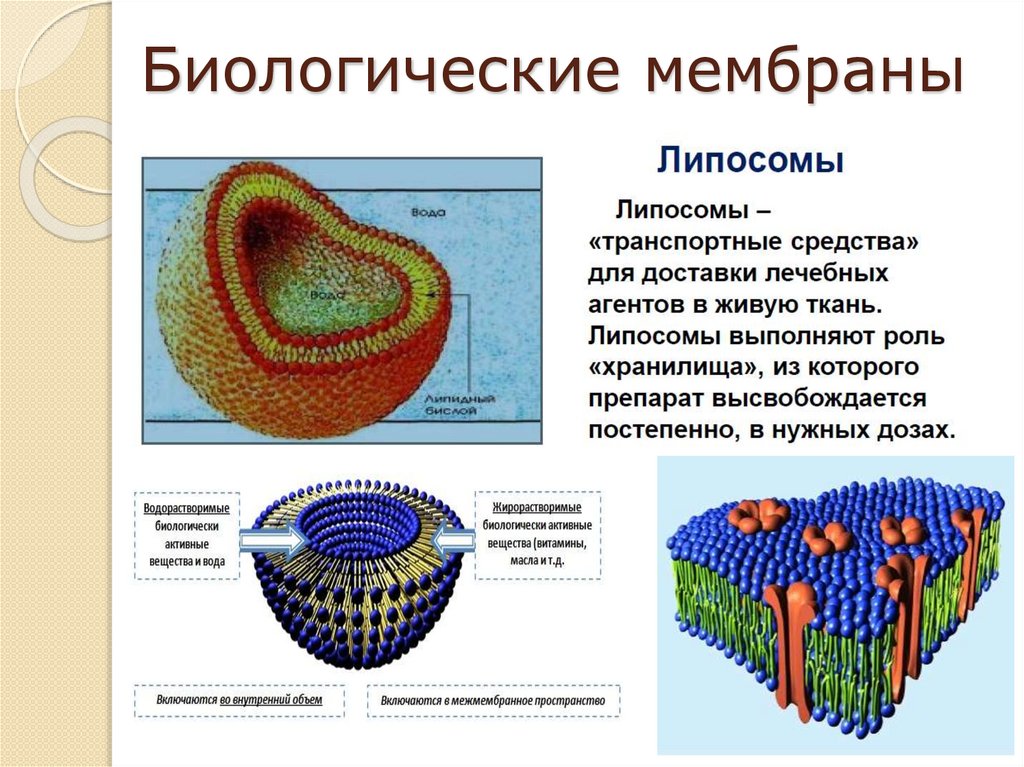
Мицеллы в биологии, физиологии имедицине



















 chemistry
chemistry








