Similar presentations:
Алкадиены. Бутадиен-1,3 и метилбутадиен-1,3. Получение синтетического каучука и резины
1.
Алкадиены. Бутадиен-1,3 иметилбутадиен-1,3. Получение
синтетического каучука и
резины
2.
1.Введение -3-
2.
Классификация алкадиенов -4-
3.
Номенклатура алкадиенов -5-
4.
Способы получения алкадиенов -6-
5.
Физические свойства -7-
6.
Химические свойства алкадиенов -8,9-
7.
Каучук и продукты его вулканизации -10,11,12,13-
8.
Применение -14-
9.
Заключение -15-
10.
Информационные источники -16-
2
3.
Алкадиены – это непредельные (ненасыщенные)углеводороды, в молекулах которых присутствует две
двойные связи между атомами углерода. Алкадиены
также называют диеновыми углеводородами. Общая
формула
гомологического
ряда
алкадиенов:
CnH2n-2
Простейшее соединение гомологического ряда
- пропадиен - CH2=C=CH2.
3
4.
В зависимости от того, как чередуются двойные связи вмолекуле алкадиена, они подразделяются на следующие
типы:
1. Кумулированные двойные связи (если две двойные
связи прилежат к одному и тому же атому углерода).
Пример: пропадиен-1,2 - CH2=C=CH2
2. Сопряженные двойные связи (если две двойные связи
разделены одной одинарной связью).
Пример: бутадиен-1,3 - CH2=CH-CH=CH2
3. Изолированные двойные св (если две двойные связи
разделены двумя и более одинязиарными связями).
Пример: пентадиен-1,4 - CH2=CH-CH2-CH=CH2
4
5.
Названия алкенов формируются путем добавлениясуффикса "диен" к названию алкана с соответствующим
числом. Например: пропадиен, бутадиен, пентадиен и т.д.
При составления названия алкадиена важно учесть, что
главная цепь атомов
углерода должна обязательно
содержать
двойные
связи.
Нумерация атомов углерода в ней начинается с того края, к
которому ближе двойная связь. В конце названия
указывают атомы углерода, у которых начинается двойная
связь.
5
6.
Для получения диеновых углеводородов в промышленности используютреакцию дегидрирования, то есть отщепления водорода. В качестве
исходного вещества берут предельный углеводород с тем же строением
углеродной цепи, что и у получаемого продукта. В результате отщепления
водорода от молекулы алкана образуются двойные связи. Дегидрирование
происходит при повышенной температуре и в присутствии катализатора:
Реакция
С.В.Лебедева
(дегидрирование
и
дегидратация):
6
7.
1. Бутадиен-1,3 (дивинил) и пропадиен – бесцветныйгаз с неприятным запахом, температурой плавления –
4,5°C. Практически нерастворим в воде.
2. 2-Метилбутадиен-1,3 (изопрен) – при обычных
условиях – жидкость с температурой кипения 34°C.
3. Алкадиены с изолированными двойными связями –
жидкости; высшие алкадиены - твердые вещества.
7
8.
1.Реакции присоединенияДля алкадиенов, как и для алкенов характерны реакции
присоединения по двойной связи С=С, при которых протекает разрыв
пи-связи в молекуле. Присоединение галогеноводородов происходит
в соответствии с правилом В.В.Марковникова.
В.В. Марковников
(1838 – 1904)
8
9.
2. Окисление алкадиеновПри горении алкадиены, как и все органические соединения,
сгорают с образованием углекислого газа и воды - полное
окисление.
3. Полимеризация
Сопряженные диеновые углеводороды способны к реакциям
полимеризации.
Полимеризация - цепная реакция синтеза полимеров, при
котором
молекула
полимера
образуется
путем
последовательного соединения молекул мономеров.
9
10.
Каучуки можно рассматривать как продукты полимеризациисопряженных диенов или их производных. Каучуки относят к
эластомерам. Такое название эти полимеры получили потому, что
обладают эластичностью, то есть способностью изменять форму
под действием внешних сил. Другие свойства каучуков –
водонепроницаемость и газонепроницаемость.
Природными источниками каучука служат растения, богатые
млечным соком: гевея, фикусы, молочаи, одуванчики.
Натуральный (природный) каучук
В промышленных масштабах природный каучук получают из сока
тропического дерева гевеи.
Рис. 1. Источник каучука – одуванчики
Рис. 2. Источник каучука – дерево гевея
10
11.
Чувствительность натурального каучука к перепадам температури потерю при этом эластичности устраният его вулканизация.
Этот процесс заключается в «сшивании» полимерных цепей
атомами серы при нагревании за счёт разрыва некоторой части
двойных связей в этих цепях. Так получают резину.
Если «сшить» полимерные цепи каучука атомами серы за счёт
разрыва подавляющего большинства двойных связей, то
образуется эбонит, который уже не обладает эластичностью и
является хорошим диэлектриком.
Рис. 1. Резина
Рис. 2. Эбонит
11
12.
Источники каучука нашей страны (одуванчики) содержат оченьмало млечного сока.
Проблему получения синтетического каучука решил коллектив
учёных под руководством академика Сергея Васильевича
Лебедева в 1931 году. Этот каучук назвали бутадиеновым
каучуком, потому что в качестве мономера для его получения был
выбран бутадиен – 1,3.
В процессе полимеризации двойные связи
алкадиена
разрываются,
за
счёт
освободившихся
валентностей
крайних
углеродных атомов растёт полимерная цепь.
Одновременно с этим между центральными
атомами углерода образуется двойная связь:
Сергей Васильевич Лебедев
(1874 – 1934)
12
13.
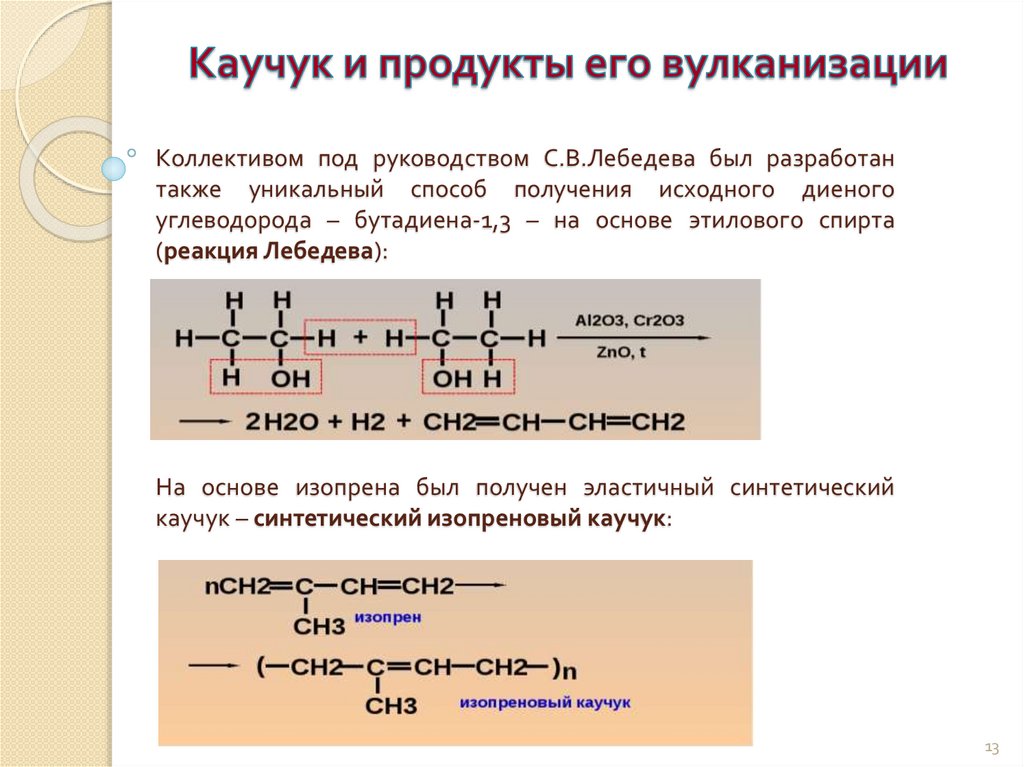
Коллективом под руководством С.В.Лебедева был разработантакже уникальный способ получения исходного диеного
углеводорода – бутадиена-1,3 – на основе этилового спирта
(реакция Лебедева):
На основе изопрена был получен эластичный синтетический
каучук – синтетический изопреновый каучук:
13
14.
Поскольку при разложении природного каучука образовывалисьдиеновые углеводороды, стало ясно и обратное: полимеризацией
диенов можно получать синтетические каучукоподобные материалы.
Диеновые углеводороды применяются в производстве синтетических
каучуков, из которых в том числе делают и резину.
Применение резины: товары народного потребления (резиновые
перчатки и сапоги, плащи, шланги), автомобильные покрышки.
Природный каучук является липким эластичным, резиноподобным
материалом,
но
по
сравнению
с
каучуком
выше.
Рис. 1. Резиновые перчатки
Рис. 2. Шланг
Рис. 3. Автомобильные покрышки
14
15.
Можно сделать вывод, что углеводороды – незаменимое сырье дляпроизводства многих необходимых веществ и материалов.
Алкадиены обладают большой химической активностью.
За счёт наличия кратной связи, они вступают в реакции
окисления,
присоединения
и
полимеризации.
Свойства алкадиенов определяются их строением и взаимных
расположением
двойных
связей
в
молекуле.
15














 chemistry
chemistry








