Similar presentations:
Основы термодинамики
1.
Основытермодинамики
2.
• На первый планвыступают тепловые
процессы и
энергетические
преобразования
3.
ИЗ ИСТОРИИ РАЗВИТИЯ ТЕРМОДИНАМИКИАВТОР
СУТЬ ВВЕДЕННЫХ ПРЕДСТАВЛЕНИЙ
Д. Фаренгейт (1685-1736)
В 1710 – 1714 годах предложил шкалу и термометр:
0° - температура смеси воды, льда и поваренной соли,
32° - температура смеси воды и льда, 212° температура кипения воды, 96° - температура тела
человека.
А. Цельсий (1701 – 1744),
В 1742 году предложил стоградусную шкалу температур:
0° - температура таяния льда, 100° - температура
кипение воды
голливудский физик, мастерстеклодув
шведский физик и астроном.
Ж. Понселе (1788 – 1867),
французский физик и инженер.
В 1826 году ввел понятие работы и единицы её
измерения.
С. Карно (1796 – 1832),
французский физик и инженер.
Ввел представление об идеальной тепловой машине, а в
1824 году фактически дал формулировку второго начала
термодинамики, связал тепло с движение частиц тела.
Б. Клапейрон (1799 –
1864), французский физик и
В 1834 году вывел уравнение состояния идеального
газа, обобщенное в дальнейшем Д. И. Менделеевым.
инженер.
4.
ИЗ ИСТОРИИ РАЗВИТИЯ ТЕРМОДИНАМИКИАВТОР
СУТЬ ВВЕДЕННЫХ ПРЕДСТАВЛЕНИЙ
Р. Майер (1818 – 1878),
В 1842 году одним из первых сформулировал закон
сохранения и превращения энергии.
Дж. Джоуль (1818 – 1889),
В 1843 году первый вычислил механический
эквивалент теплоты и пришел к закону сохранения
энергии.
немецкий врач и
естествоиспытатель.
английский физик
Г. Гельмгольц (1821 – 1894), В 1847 году дополнив идеи Майера и опыты Джоуля,
немецкий физик и
естествоиспытатель
сформулировал и математически обосновал закон
сохранения и превращения энергии.
Р. Клаузиус (1822 – 1888),
немецкий физик-теоретик.
В 1850 году сформулировал второе начало
термодинамики, а в 1854 г. дал математическую
формулировку первого начала.
У. Томсон (Кельвин) (1824 – 1907),
В 1848 году ввел понятие абсолютной температуры,
в 1851 году сформулировал второе начало
термодинамики.
английский физик.
5.
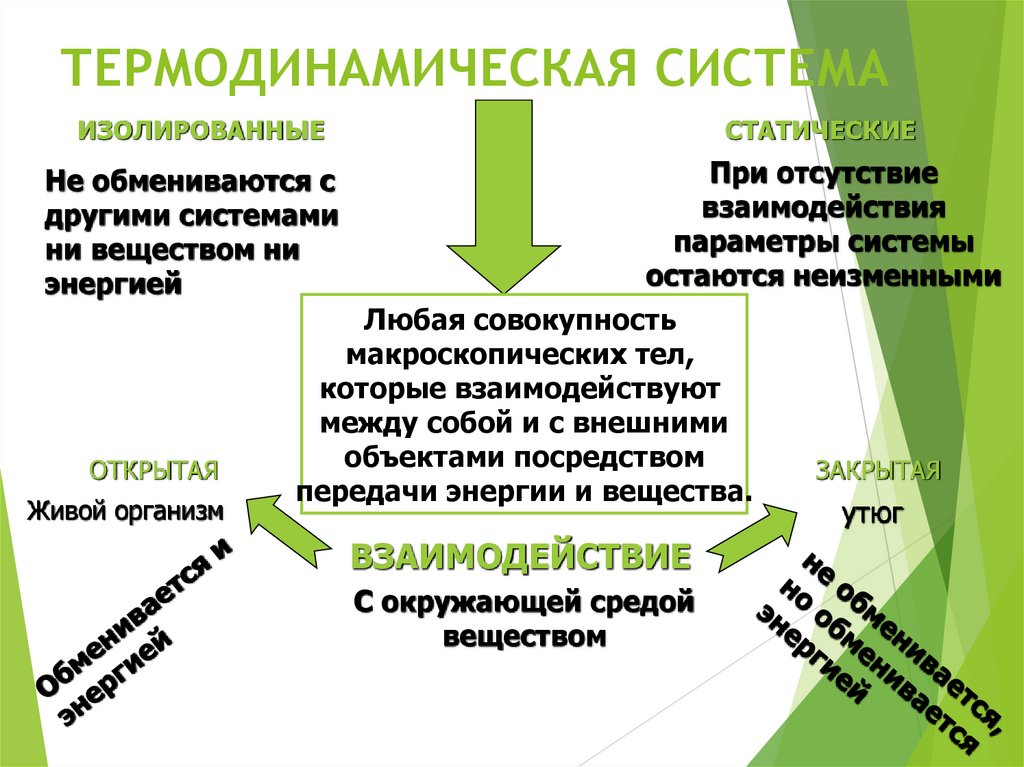
ТЕРМОДИНАМИЧЕСКАЯ СИСТЕМАИЗОЛИРОВАННЫЕ
СТАТИЧЕСКИЕ
Не обмениваются с
другими системами
ни веществом ни
энергией
При отсутствие
взаимодействия
параметры системы
остаются неизменными
ОТКРЫТАЯ
Живой организм
Любая совокупность
макроскопических тел,
которые взаимодействуют
между собой и с внешними
объектами посредством
передачи энергии и вещества.
ВЗАИМОДЕЙСТВИЕ
С окружающей средой
веществом
ЗАКРЫТАЯ
утюг
6.
ЧТО ИЗУЧАЕТ ТЕРМОДИНАМИКА?Возникла как наука тепловых процессов,
рассматриваемых с точки зрения энергетических
преобразований.
Не рассматривает явления с точки зрения движения
молекул.
Изучает наиболее общие свойства макроскопических
систем, находящихся в равновесном состоянии, и
процессы их перехода из одного состояния в другое.
Термодинамический метод широко используется в
других разделах физики, химии, биологии.
Как и любая физическая теория или раздел физики,
имеет свои границы применимости.
7.
ГРАНИЦЫ ПРИМЕНИМОСТИТЕРМОДИНАМИКИ
Неприменима к
системе из нескольких молекул.
•Не может быть применима ко
всей Вселенной, слишком
сложной и неопределенной
физической системе.
8.
ТЕРМОДИНАМИЧЕСКИЕПАРАМЕТРЫ
Совокупность физических величин, характеризующих
свойства термодинамической системы.
V - объём
Р - давление
T - температура
U - внутренняя энергия
9.
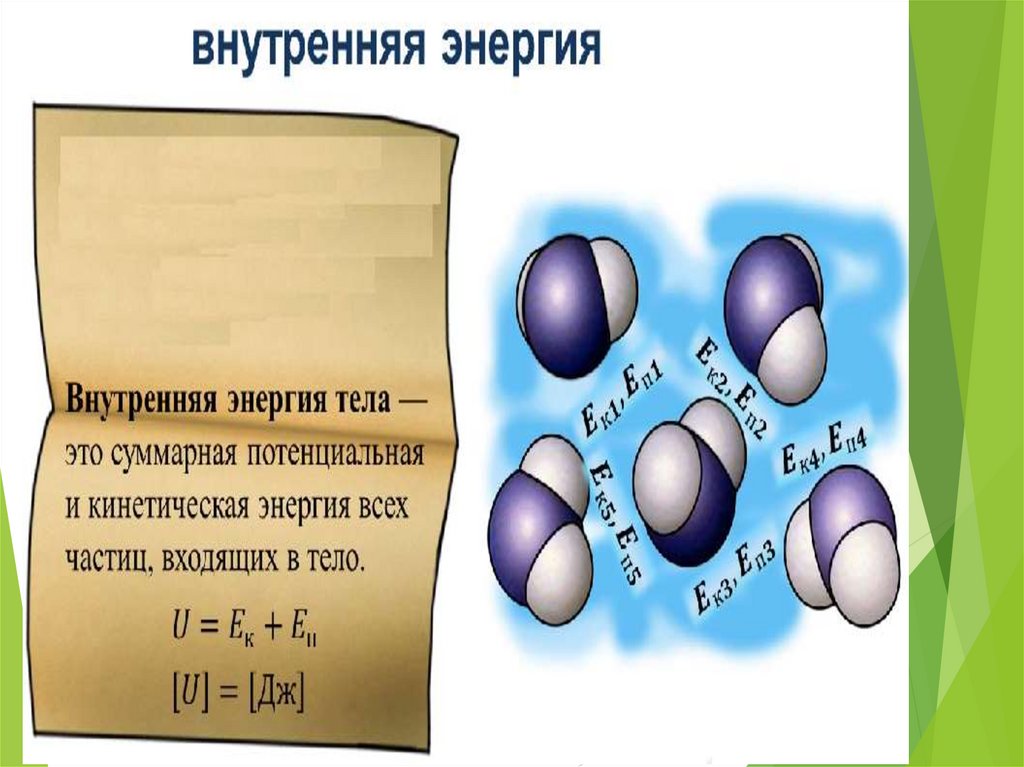
Внутренняя энергияОпределение:
Внутренняя энергия тела – это сумма
кинетической энергии хаотического
теплового движения частиц (атомов и
молекул) тела и потенциальной энергии
их взаимодействия
Обозначение:
U
Единицы измерения:
[Дж]
10.
11.
12.
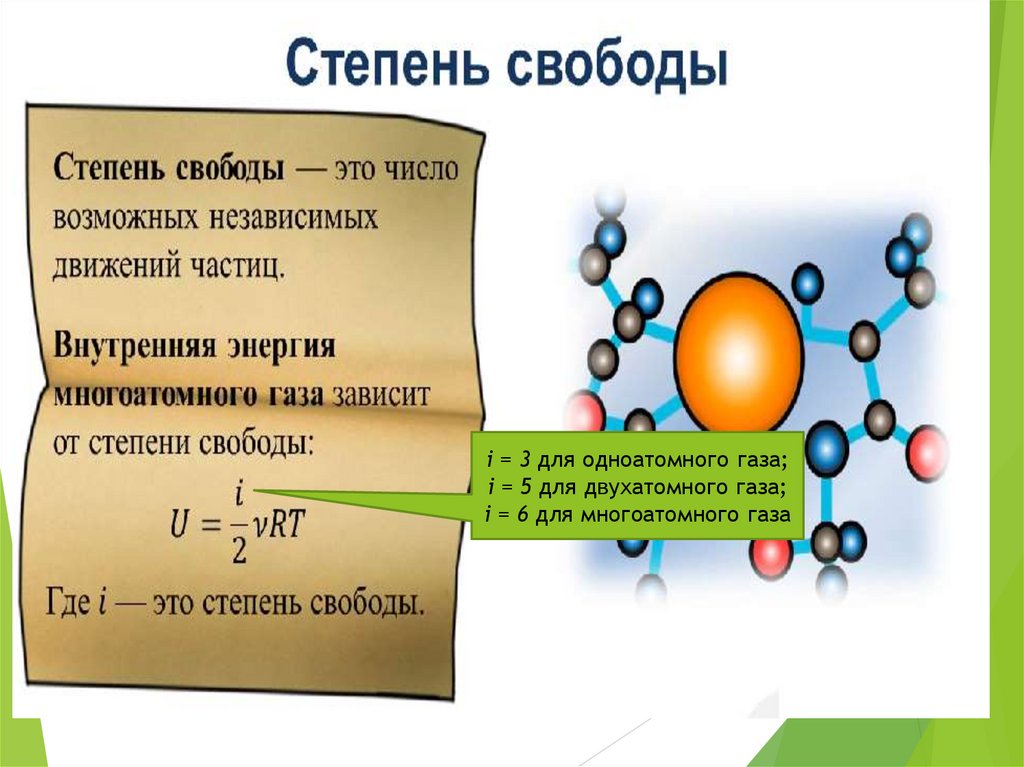
i = 3 для одноатомного газа;i = 5 для двухатомного газа;
i = 6 для многоатомного газа
13.
Внутренняя энергияидеального одноатомного газа
3m
U
RT
2M
14.
Внутренняя энергияидеального двухатомного газа
5m
U
RT
2M
15.
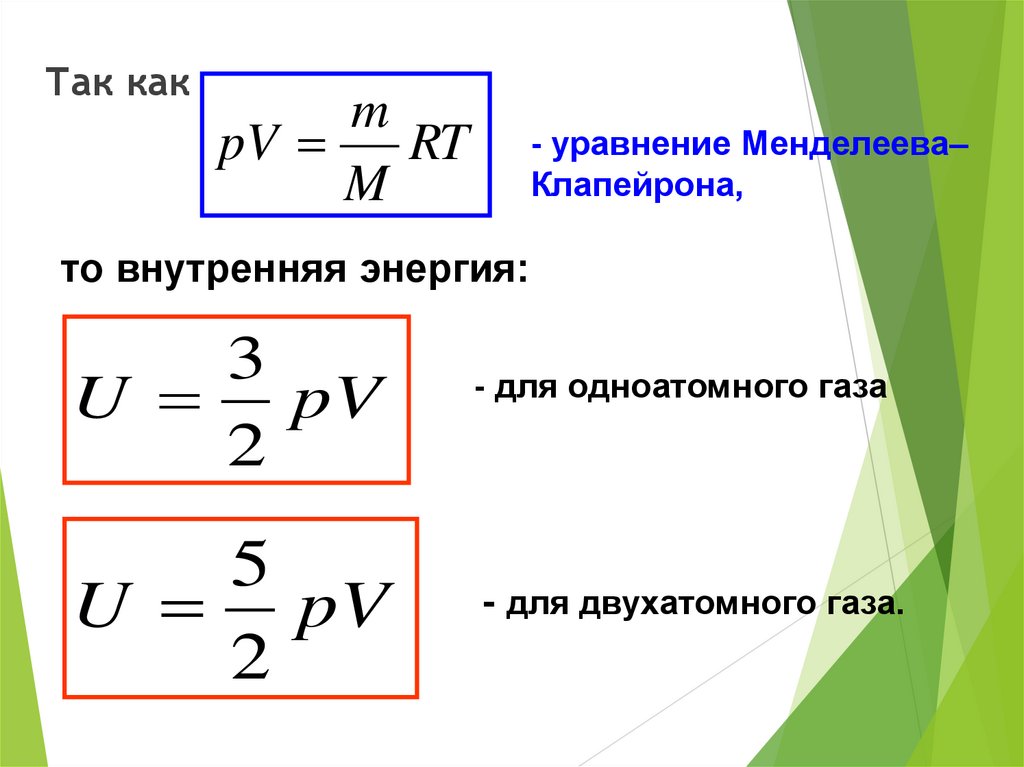
Так какm
pV
RT
M
- уравнение Менделеева–
Клапейрона,
то внутренняя энергия:
3
U pV
2
5
U pV
2
- для одноатомного газа
- для двухатомного газа.
16.
В общем виде:i m
i
U
RT pV
2M
2
где i – число степеней свободы молекул газа
(i = 3 для одноатомного газа и i = 5 для
двухатомного газа)
17.
18.
Изменение внутреннейэнергии тела ΔU
Совершение
работы А
Теплообмен Q
теплопроводность
над
самим
телом
телом
ΔU
ΔU
излучение
конвекция
19.
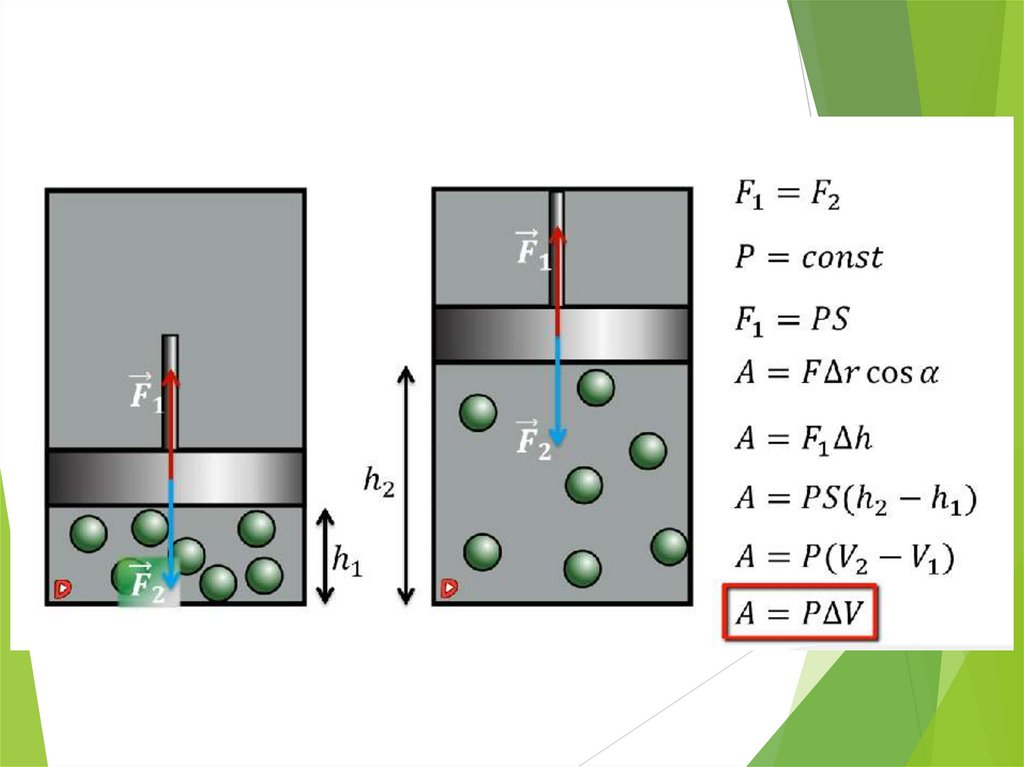
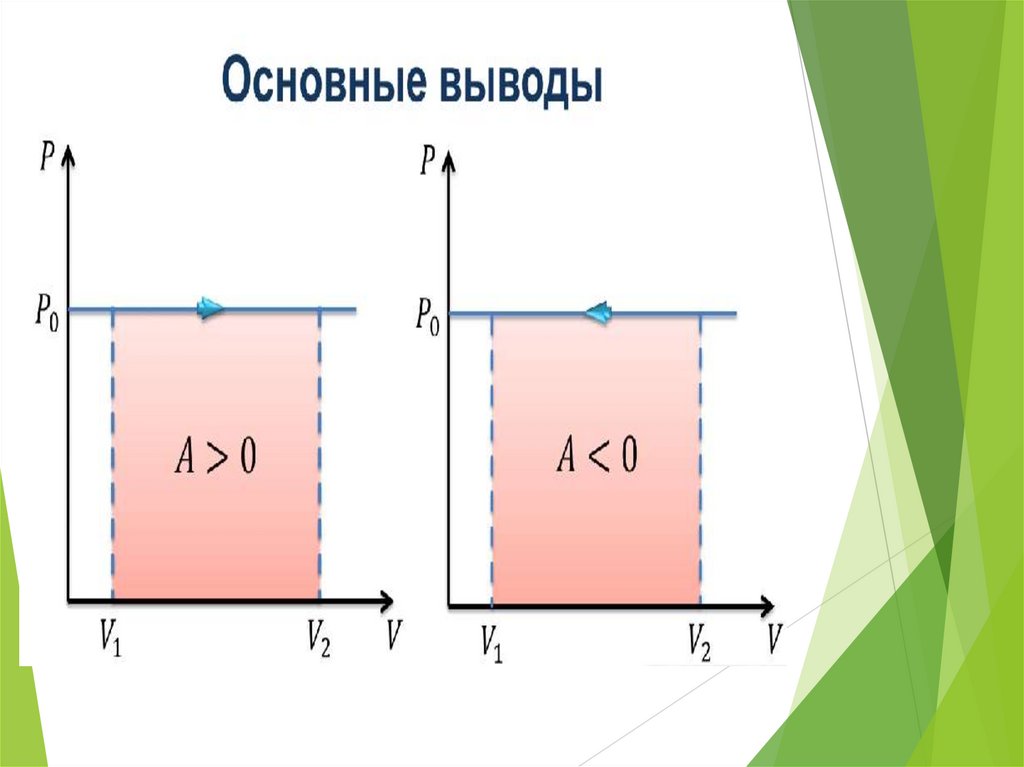
Работа в термодинамикеРабота газа:
A p(V2 V1) p V
Работа внешних сил:
A A
20.
21.
22.
23.
24.
25.
26.
27.
28.
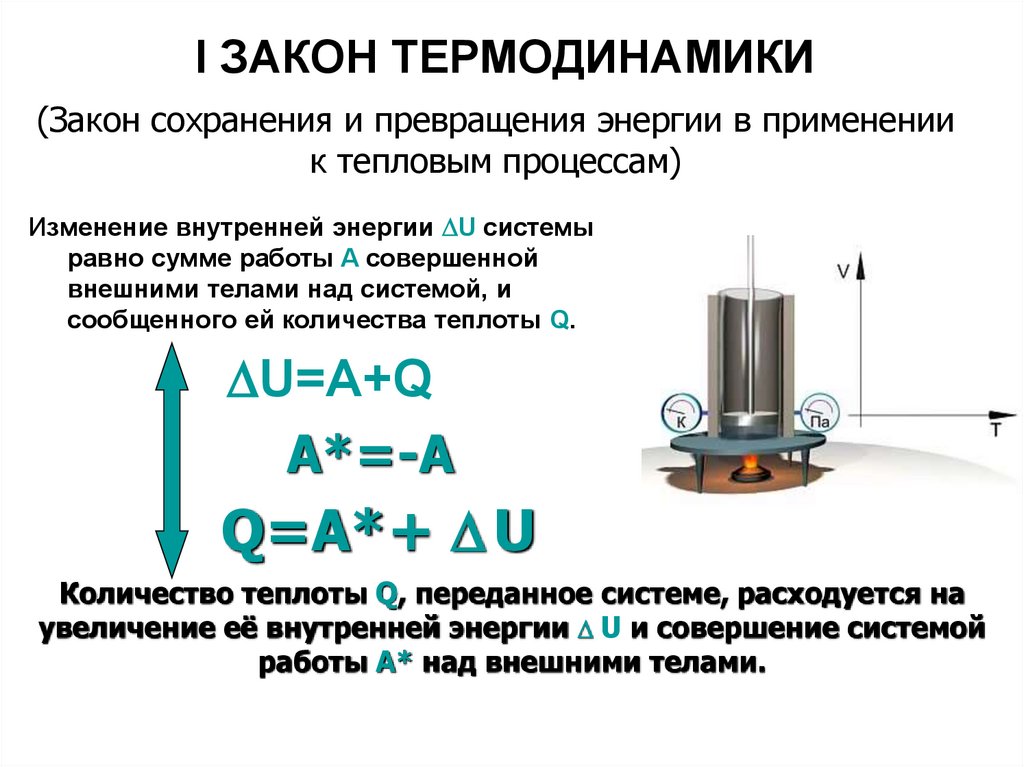
I ЗАКОН ТЕРМОДИНАМИКИ(Закон сохранения и превращения энергии в применении
к тепловым процессам)
Изменение внутренней энергии U системы
равно сумме работы A совершенной
внешними телами над системой, и
сообщенного ей количества теплоты Q.
U=A+Q
A*=-A
Q=A*+ U
Количество теплоты Q, переданное системе, расходуется на
увеличение её внутренней энергии U и совершение системой
работы A* над внешними телами.
29.
Первый закон термодинамикиИзменение внутренней
энергии системы при
переходе её из одного
состояния в другое равно
сумме работы внешних
сил и количества
теплоты, переданного
системе
Количество теплоты,
переданное системе,
идёт на изменение её
внутренней энергии и на
совершение системой
работы над внешними
телами
U A Q
Q U A
30.
ТЕРМОДИНАМИКА ИЗОПРОЦЕССОВ.Процессы, происходящие при постоянном
значении одного из параметров состояния (T,V
или P) с данной массой газа называются
изопроцессами.
ИЗОТЕРМИЧЕСКИЙ
ИЗОХОРНЫЙ
ИЗОБАРНЫЙ
АДИАБАТНЫЙ
31.
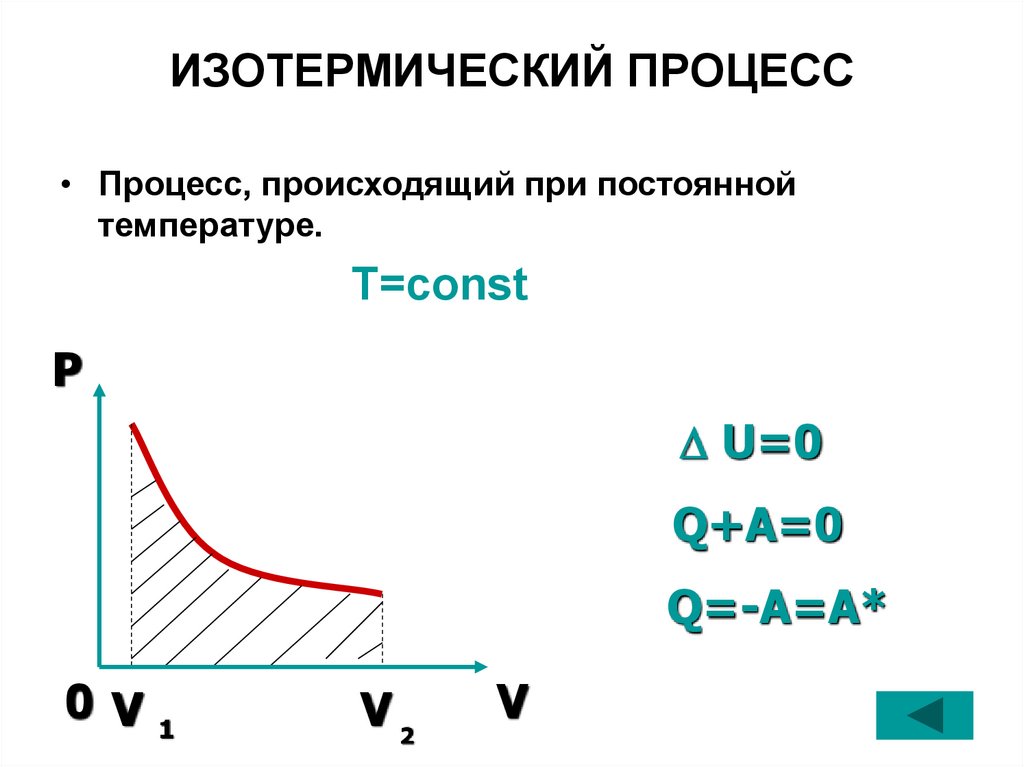
ИЗОТЕРМИЧЕСКИЙ ПРОЦЕСС• Процесс, происходящий при постоянной
температуре.
T=const
P
U=0
Q+A=0
Q=-A=A*
0 V1
V2
V
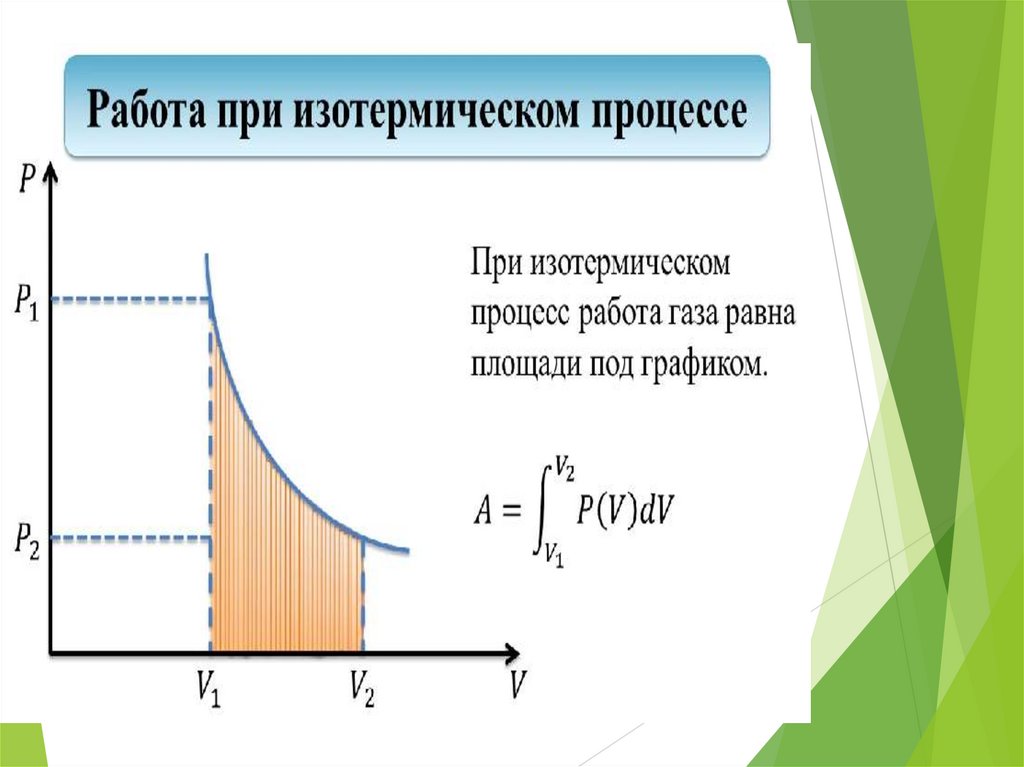
32.
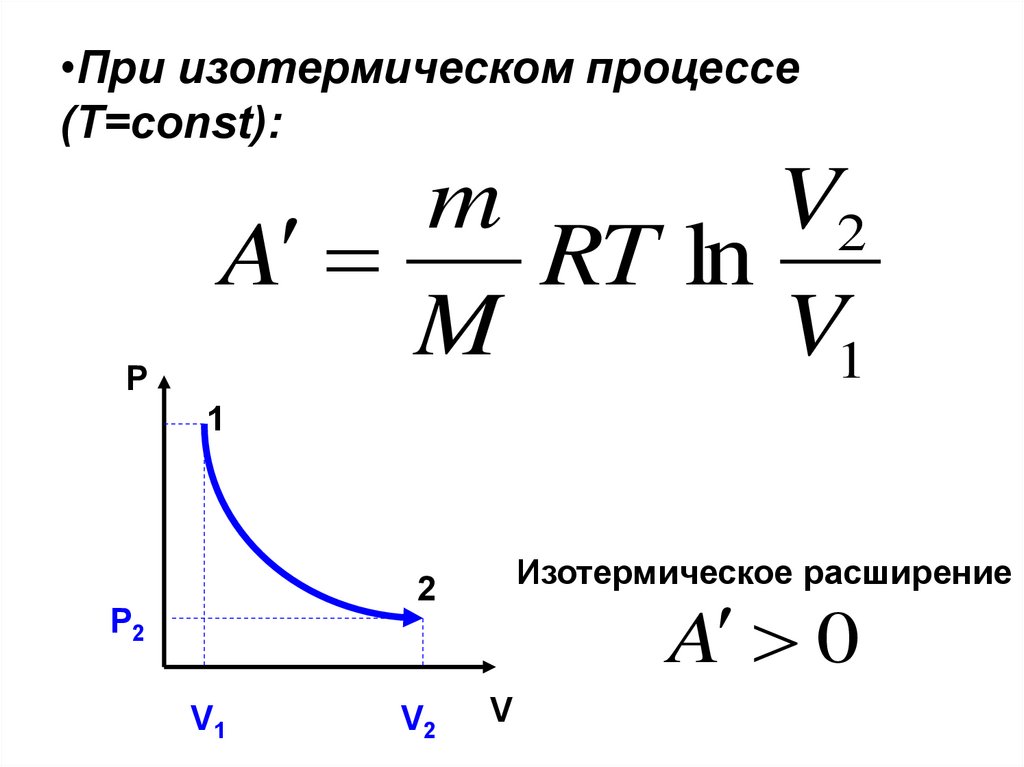
•При изотермическом процессе(Т=const):
P
m
V2
A
RT ln
M
V1
1
Изотермическое расширение
2
Р2
V1
V2
A 0
V
33.
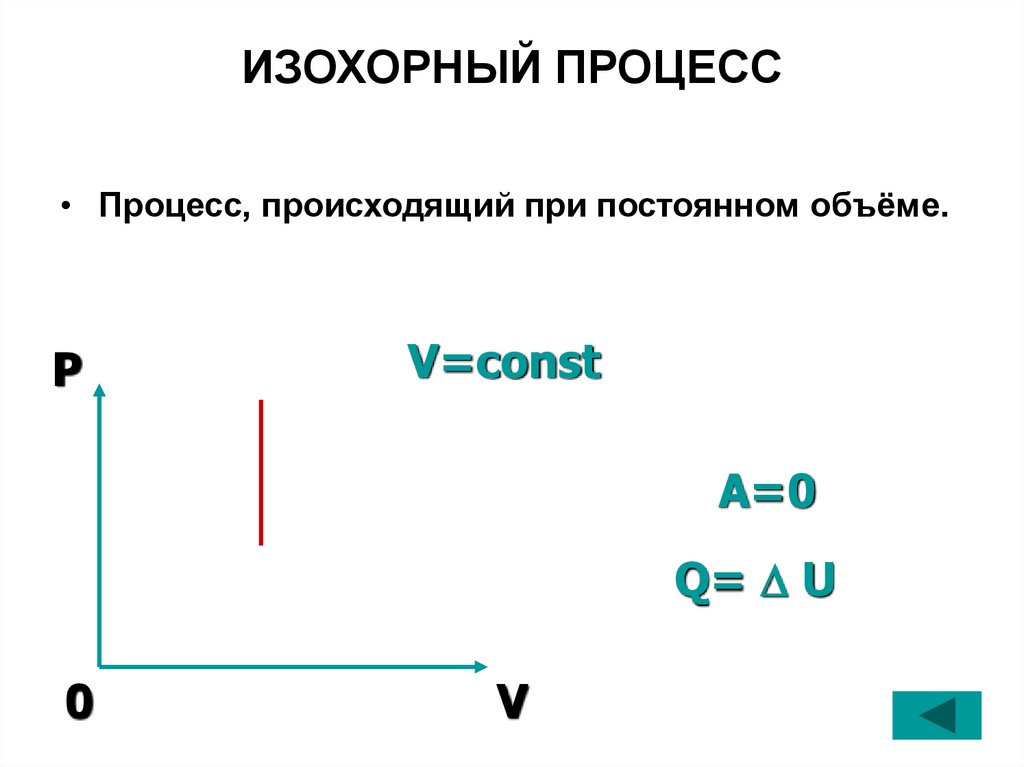
ИЗОХОРНЫЙ ПРОЦЕСС• Процесс, происходящий при постоянном объёме.
P
V=const
A=0
Q= U
0
V
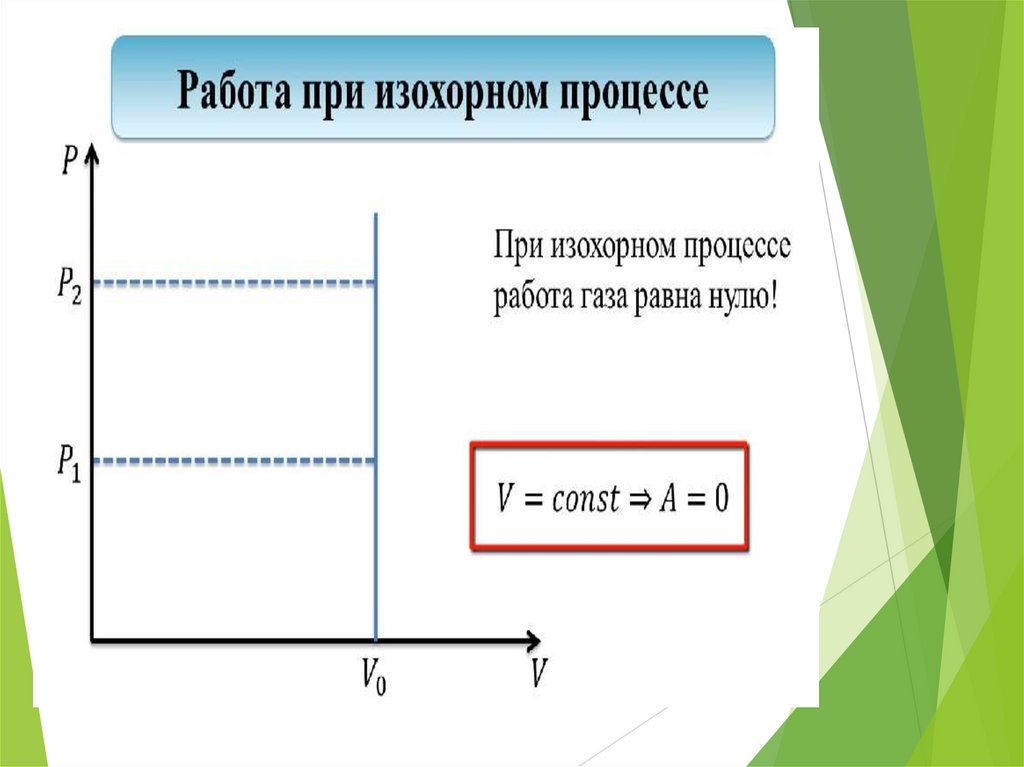
34.
Работа газа при изопроцессах• При изохорном процессе (V=const):
ΔV = 0 работа газом не совершается:
A 0
P
V
Изохорное нагревание
35.
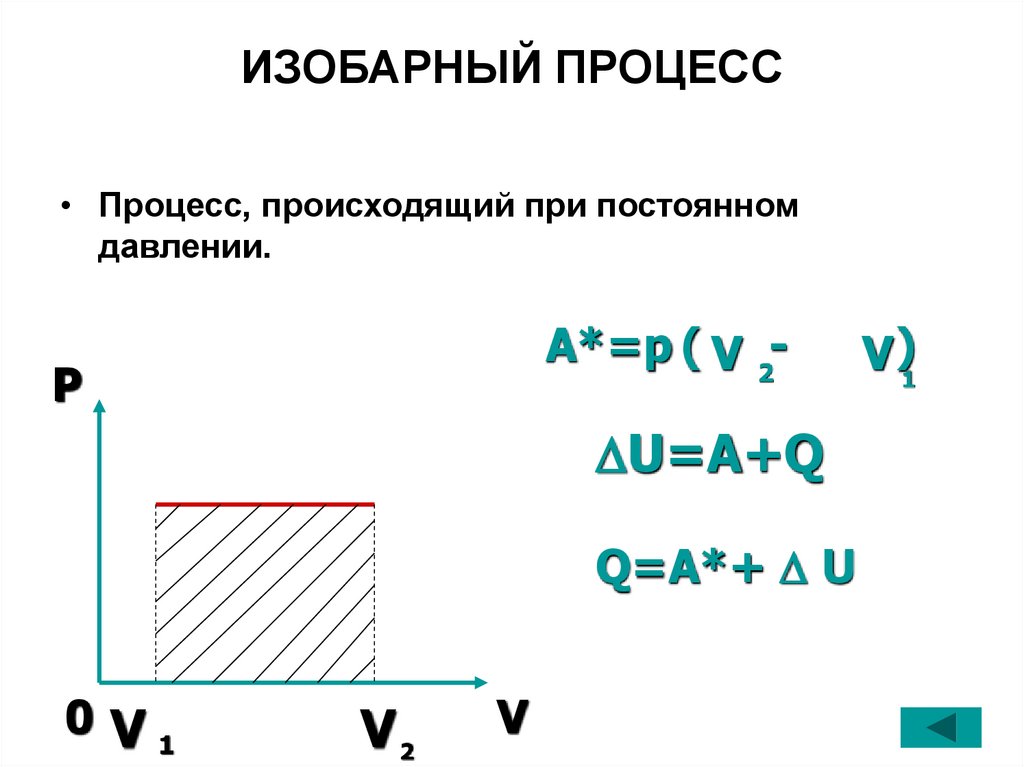
ИЗОБАРНЫЙ ПРОЦЕСС• Процесс, происходящий при постоянном
давлении.
A*=p ( V 2-
P
U=A+Q
Q=A*+ U
0V1
V2
V
V )1
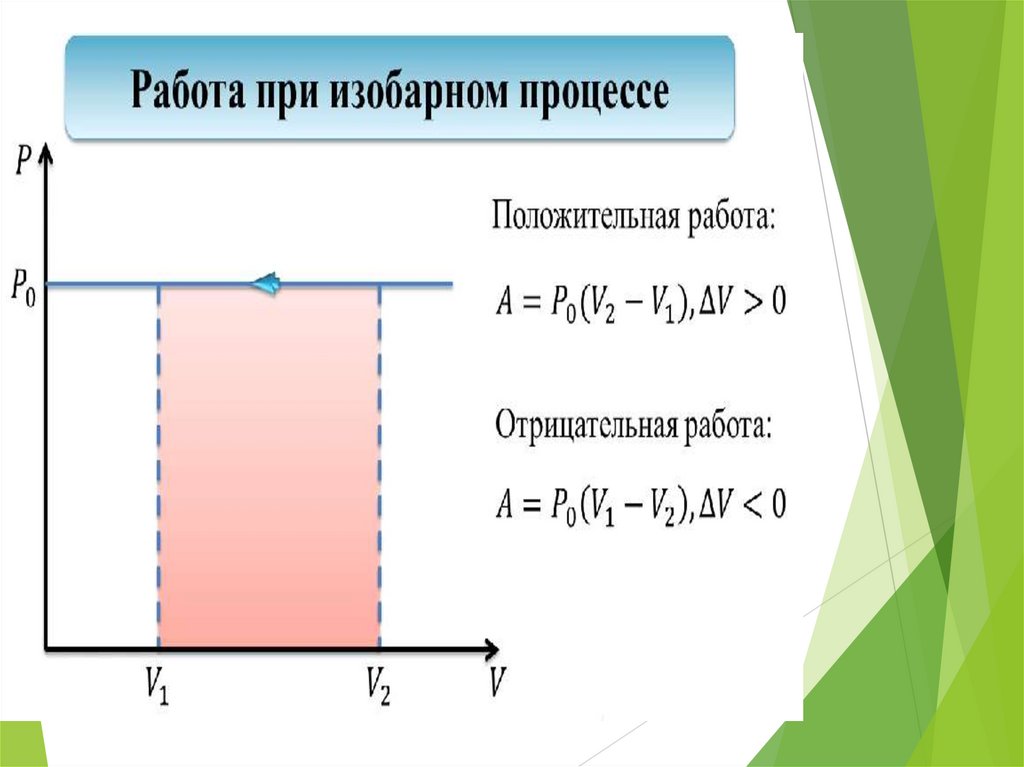
36.
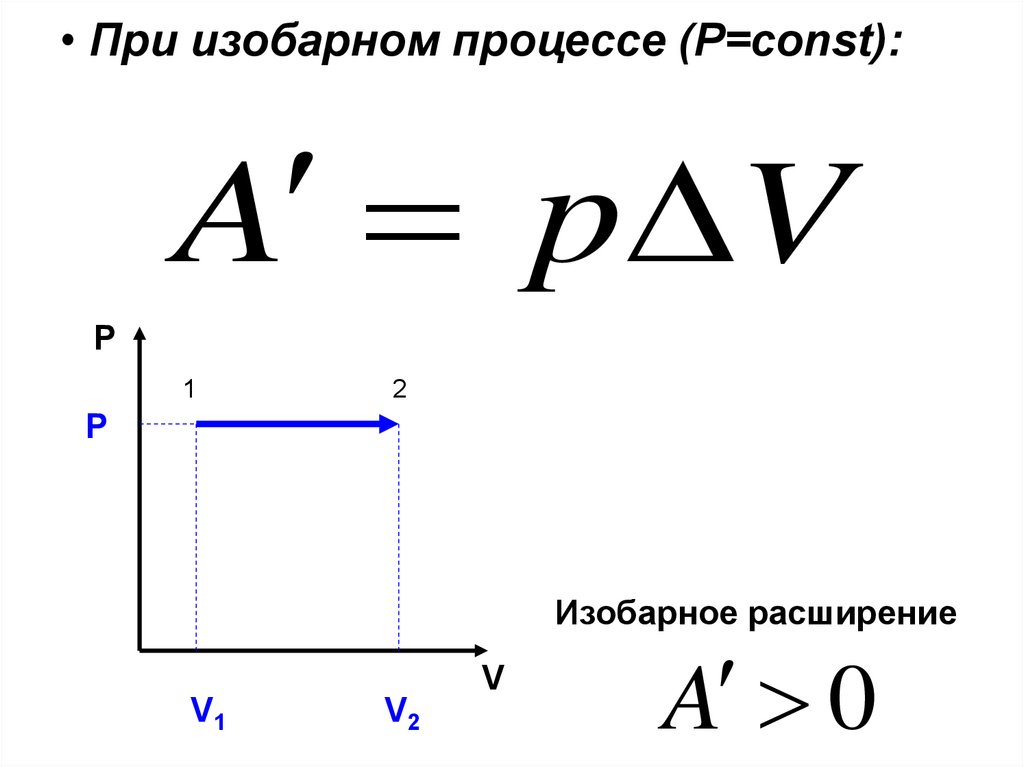
• При изобарном процессе (Р=const):A p V
P
1
2
P
Изобарное расширение
V
V1
V2
A 0
37.
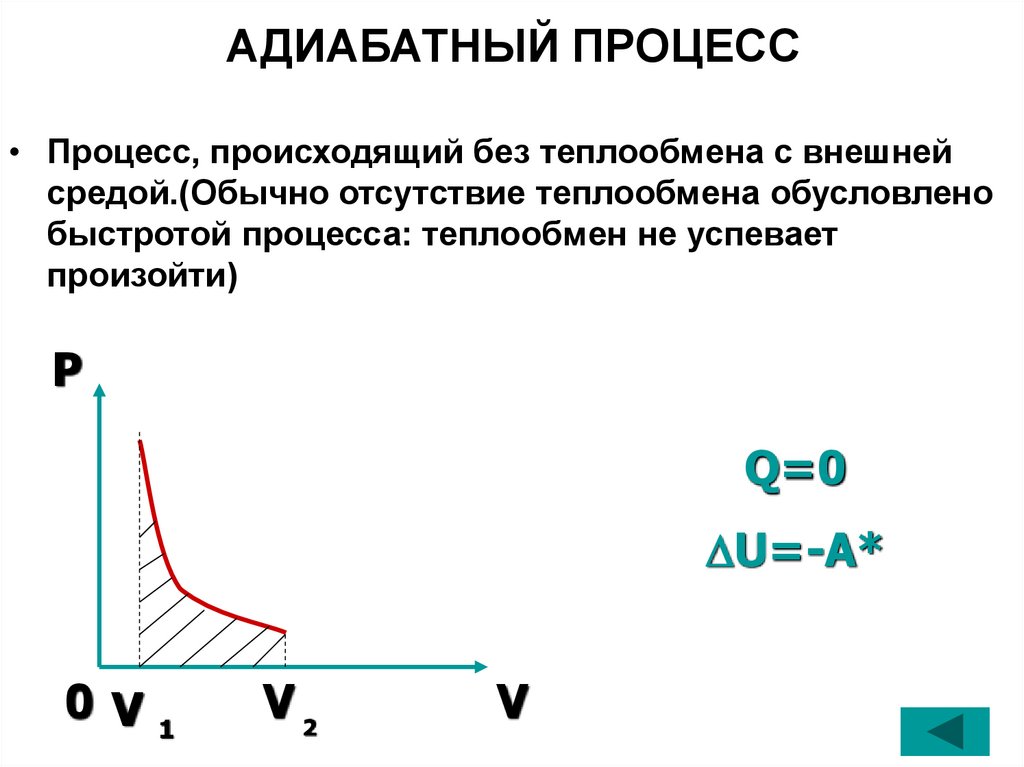
АДИАБАТНЫЙ ПРОЦЕСС• Процесс, происходящий без теплообмена с внешней
средой.(Обычно отсутствие теплообмена обусловлено
быстротой процесса: теплообмен не успевает
произойти)
P
Q=0
U=-A*
0 V1
V2
V
38.
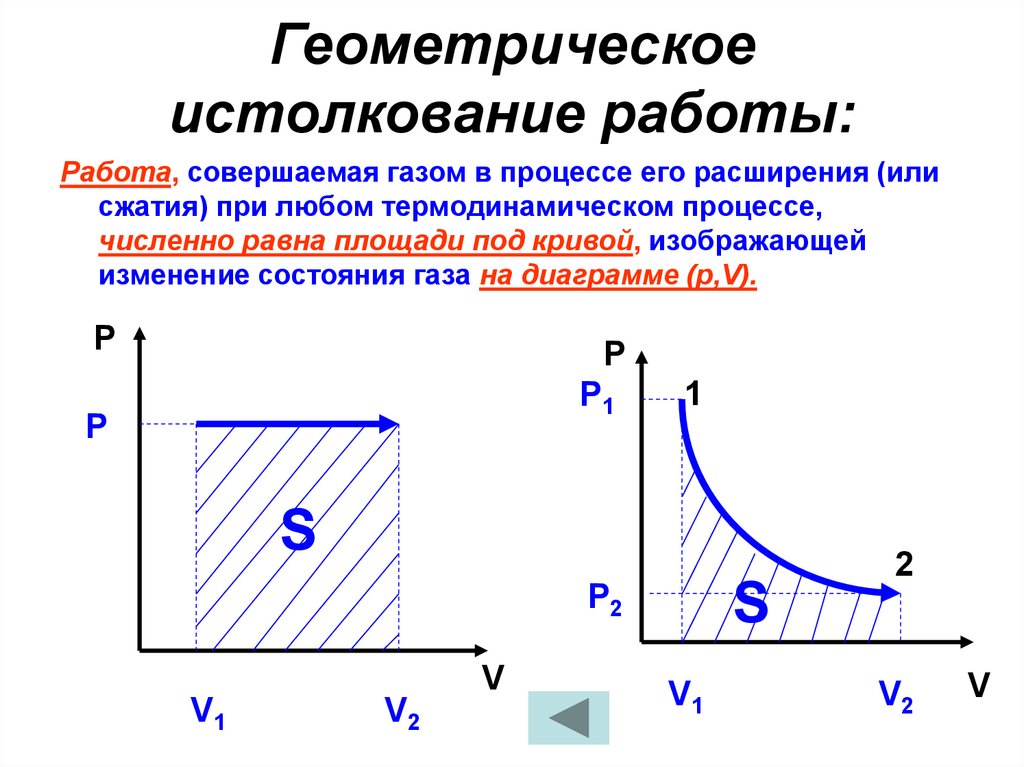
Геометрическоеистолкование работы:
Работа, совершаемая газом в процессе его расширения (или
сжатия) при любом термодинамическом процессе,
численно равна площади под кривой, изображающей
изменение состояния газа на диаграмме (р,V).
P
P
Р1
P
1
S
Р2
V
V1
V2
S
V1
2
V2
V
39.
Количество теплоты – частьвнутренней энергии, которую тело получает или
теряет при теплопередаче
Процесс
Нагревание или
охлаждение
Кипение или
конденсация
формула
Q cm T
Q rm
С – удельная теплоёмкость
вещества [ Дж/кг 0К], m –
масса [кг], ΔT – изменение
температуры [ 0K].
r – удельная теплота
парообразования [ Дж/кг ]
Плавление или
кристаллизация
Q m λ- удельная теплота плавления
Сгорание
топлива
– удельная теплота сгорания
Q qm qтоплива
[ Дж/кг ]
вещества [ Дж/кг ]
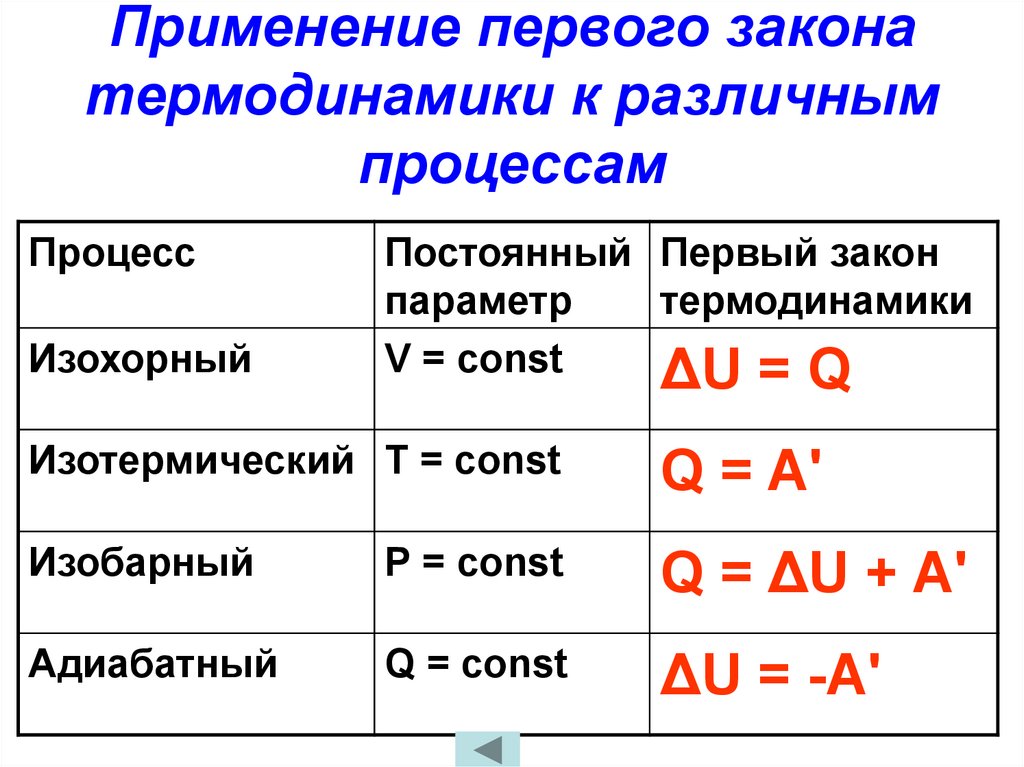
40.
Применение первого законатермодинамики к различным
процессам
Процесс
Изохорный
Постоянный Первый закон
параметр
термодинамики
V = const
ΔU = Q
Изотермический Т = const
Q = A'
Изобарный
Р = const
Q = ΔU + A'
Адиабатный
Q = const
ΔU = -A'
41.
II ЗАКОН ТЕРМОДИНАМИКИНе возможно перевести теплоту от более холодной системы
к более горячей при отсутствии других одновременных
изменений в обеих системах или окружающих телах.
Не возможен круговой процесс, единственным
результатом которого было бы производство работы за
счет охлаждения теплового резервуара.
Не возможен круговой процесс, единственным
результатом которого является передача теплоты от
менее нагретого тела более нагретому.
Тепловые процессы необратимы.
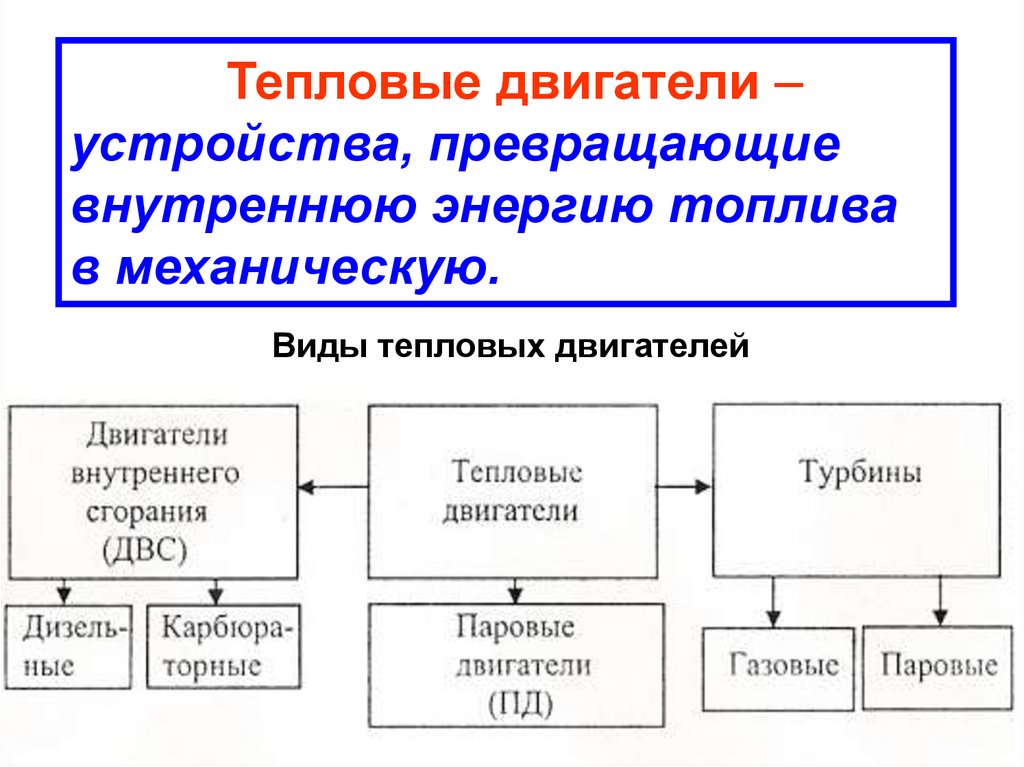
42.
Тепловые двигатели –устройства, превращающие
внутреннюю энергию топлива
в механическую.
Виды тепловых двигателей
43.
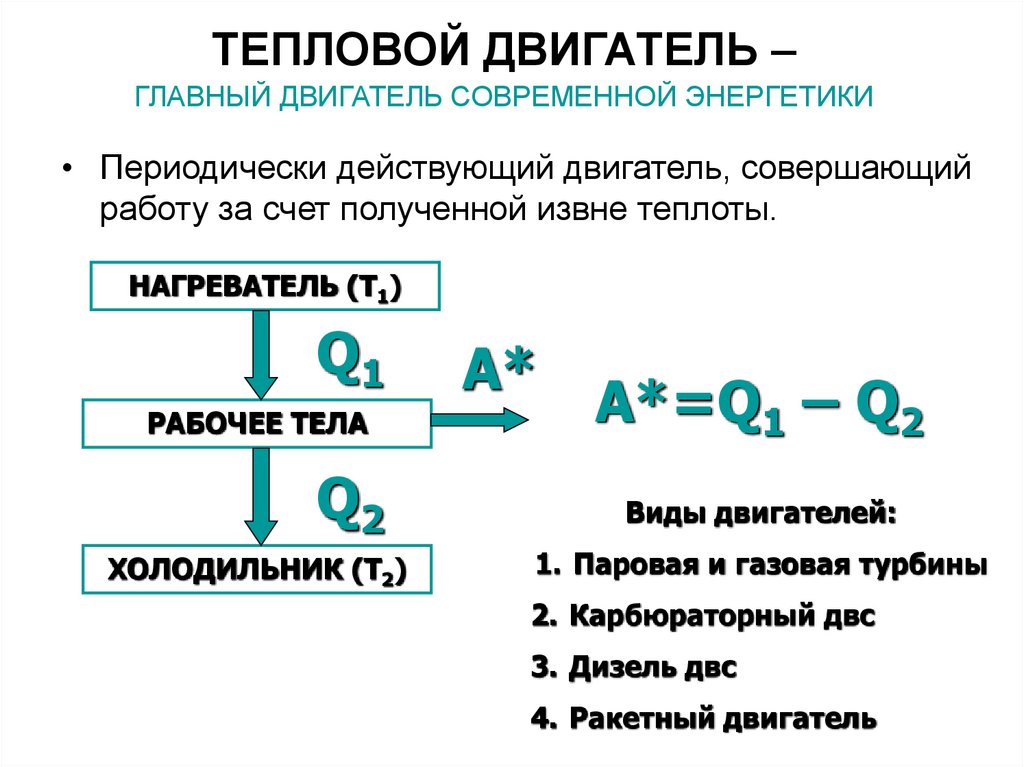
ТЕПЛОВОЙ ДВИГАТЕЛЬ –ГЛАВНЫЙ ДВИГАТЕЛЬ СОВРЕМЕННОЙ ЭНЕРГЕТИКИ
• Периодически действующий двигатель, совершающий
работу за счет полученной извне теплоты.
НАГРЕВАТЕЛЬ (Т1)
Q1
РАБОЧЕЕ ТЕЛА
Q2
ХОЛОДИЛЬНИК (Т2)
A*
A*=Q1 – Q2
Виды двигателей:
1. Паровая и газовая турбины
2. Карбюраторный двс
3. Дизель двс
4. Ракетный двигатель
44.
Принцип действия тепловых двигателейТ1 – температура
нагревателя
Т2 – температура
холодильника
Q1 – количество
теплоты,
полученное от
нагревателя
Q2 – количество
теплоты, отданное
холодильнику
45.
Коэффициент полезногодействия (КПД) теплового
двигателя –
отношение работы А’, совершаемой двигателем, к
количеству теплоты, полученному от
нагревателя:
А
Q1
46.
гдеА Q1 Q2 -работа, совершаемая
двигателем
тогда
Q1 Q2
1
При
Q1
1
Q2
Q1
КПД всегда меньше единицы, так
как у всех двигателей некоторое
количество теплоты
передаётся холодильнику
Т1 Т 2 0 двигатель не может работать
47.
Максимальное значение КПДтепловых двигателей (цикл Карно):
T1 T2
max
T1
48.
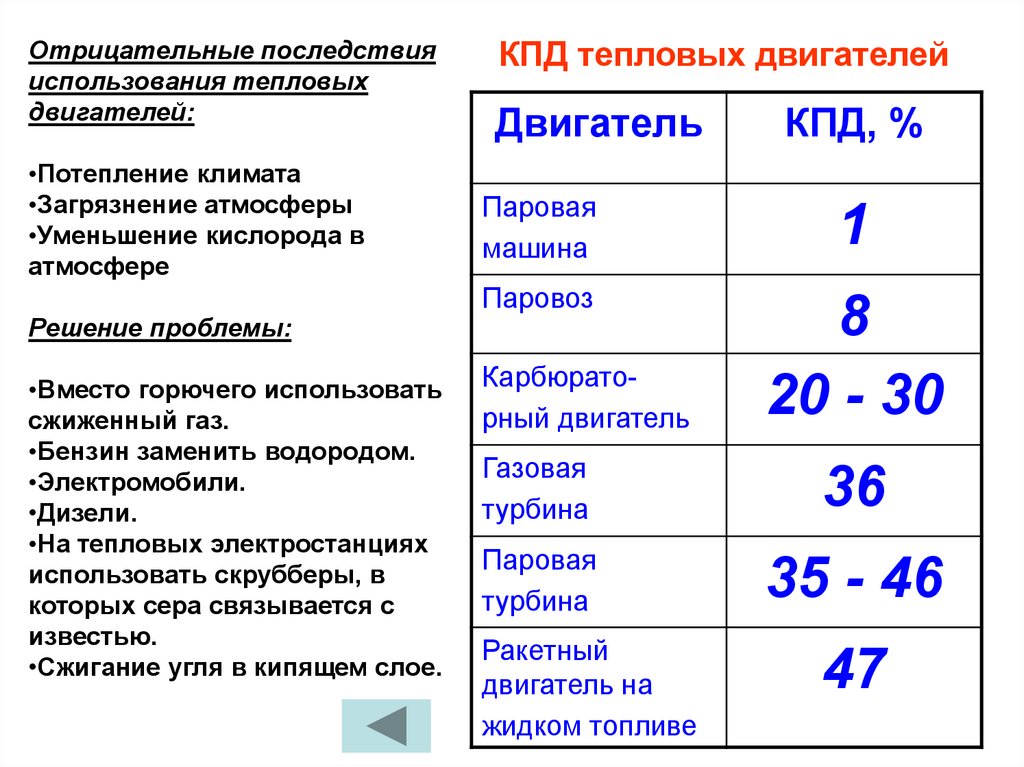
Отрицательные последствияиспользования тепловых
двигателей:
•Потепление климата
•Загрязнение атмосферы
•Уменьшение кислорода в
атмосфере
Решение проблемы:
•Вместо горючего использовать
сжиженный газ.
•Бензин заменить водородом.
•Электромобили.
•Дизели.
•На тепловых электростанциях
использовать скрубберы, в
которых сера связывается с
известью.
•Сжигание угля в кипящем слое.
КПД тепловых двигателей
Двигатель
КПД, %
Паровая
машина
1
Паровоз
8
20 - 30
Карбюраторный двигатель
Газовая
турбина
36
Паровая
турбина
35 - 46
Ракетный
двигатель на
жидком топливе
47
49.
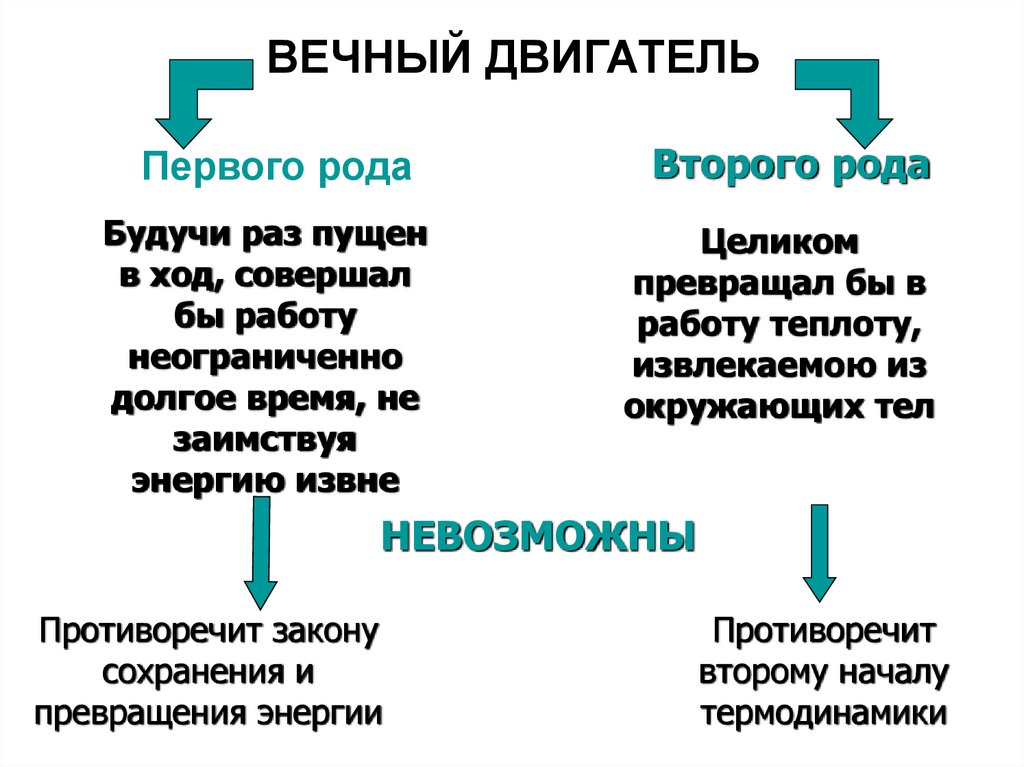
ВЕЧНЫЙ ДВИГАТЕЛЬПервого рода
Второго рода
Будучи раз пущен
в ход, совершал
бы работу
неограниченно
долгое время, не
заимствуя
энергию извне
Целиком
превращал бы в
работу теплоту,
извлекаемою из
окружающих тел
НЕВОЗМОЖНЫ
Противоречит закону
сохранения и
превращения энергии
Противоречит
второму началу
термодинамики
50.
ТЕРМОДИНАМИКА И ПРИРОДАВ окружающей нас природе термодинамически
обратимых процессов нет.
Энтропия в термодинамически не обратимых процессах,
протекающих в изолированной системе, возрастает.
По определению А. Эддингтона, возрастание энтропии,
определяющей необратимые процессы есть «стрела
времени»:чем выше энтропия системы, тем больше
временной промежуток прошла система в своей эволюции.
Возрастание энтропии вселенной должно привести к тому,
что температура всех тел сравняется т. е. наступит
тепловое равновесие и все процессы прекратятся, наступит
«тепловая смерть Вселенной». (Выводы второго закона
термодинамики не всегда имеют место в природе и его
нельзя применить ко всем существующим процессам).




























 physics
physics








