Similar presentations:
Химия полимерных материалов для буровых растворов. Лекция 3. Технологические жидкости для бурения скважин
1. Технологические жидкости для бурения скважин Лекция 3: Химия полимерных материалов для буровых растворов к.х.н., доцент кафедры БС ИПР ТПУ М
2. ПОЛИМЕРЫ
» Три основных типа полимеров˃ Природные
+ Крахмал, XC полимер
˃ Природные модифицированные
+ Карбоксиметилцеллюлоза (кмц), полианионная
целлюлоза (пац), карбокисметилированный крахмал
(кмк), гидроксиэтилцеллюлоза (гэц)
˃ Синтетические
+ Полиакрилат натрия,
+ Частично гидролизованный полиакриламид
3. ПОЛИМЕРЫ
Простейшим полимером является(C2H4)n
Молекулярная масса =28
полиэтилен:
Молекулярная масса большинства полимеров в
среднем составляет от 50 000 до 200 000
Наибольшая
молекулярная
масса
у
биополимеров (Ксантанова смола), от 2 000 000
до 5 000 000
4. ПОЛИМЕРЫ
Область применения:˃ Контроль фильтрации
˃ Регулирование вязкости
˃ Обеспечение устойчивости ствола скважины
˃ Полная флокуляция
˃ Селективная флокуляция
˃ Структурирование (Сшивание)
5. ПОЛИМЕРЫ
Применение:» Контроль фильтрации
˃ Стабилизация- КМЦ (низкой вязкости) , ПАЦ низкой вязкости,
крахмалы.
˃ Загущение жидкой фазы(воды) – КМЦ (высокой вязкости),
ПАЦ высокой вязкости, ксантан
˃ Закупоривание пор в фильтрационной корке
» Регулирование вязкости
˃ Загущение жидкой фазы
˃ Флокулянты с высокой молекулярной массой/адсорбируются
на глине функциональными группами
Разжижители с малой молекулярной массой
6. ПОЛИМЕРЫ
СТРУКТУРА ПОЛИМЕРОВ:˃ ЛИНЕЙНАЯ - КМЦ, ГЭЦ, ПОЛИАКРИЛАТ, ЧАСТИЧНО
ГИДРОЛИЗОВАННЫЙ ПОЛИАКРИЛАМИД
˃ РАЗВЕТВЛЕННАЯ – КРАХМАЛ, КМК, БИОПОЛИМЕРЫ
˃ СШИТАЯ – структурированные биополимеры
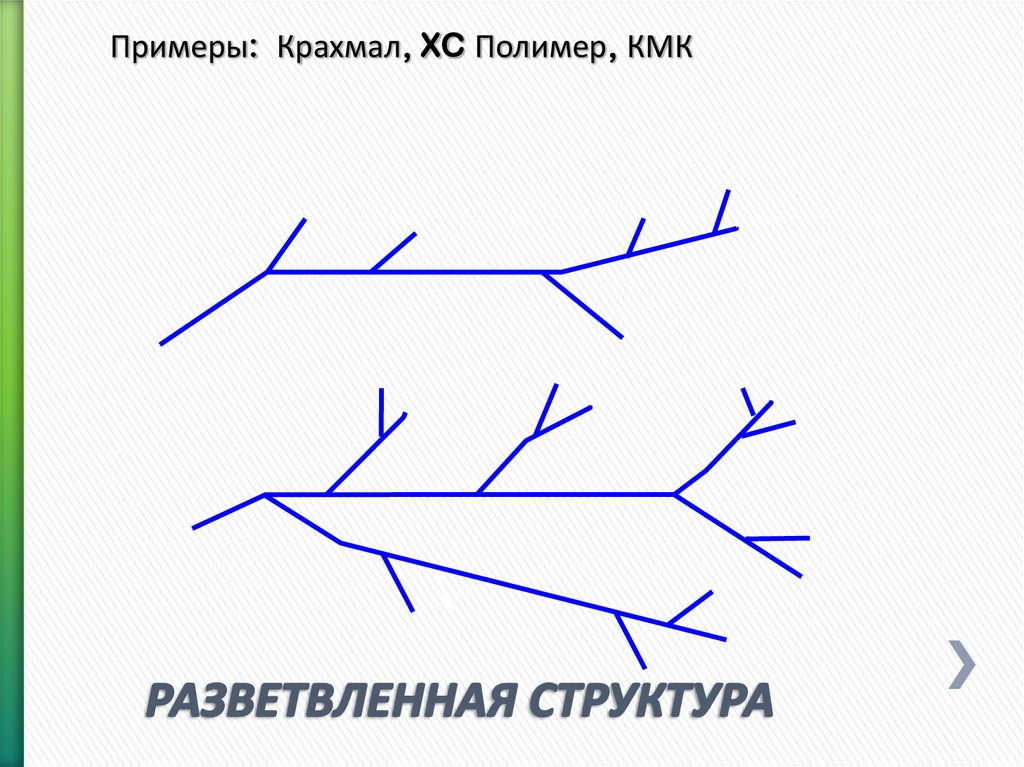
7. ЛИНЕЙНАЯ СТРУКТУРА
Примеры: КМЦ, ГЭЦ, Полиакрилат, PHPA8. РАЗВЕТВЛЕННАЯ СТРУКТУРА
Примеры: Крахмал, XC Полимер, КМК9. СШИТАЯ СТРУКТУРА
Пример: Сшитый XC Полимер10. ПОЛИМЕРЫ
СТЕПЕНЬ ПОЛИМЕРИЗАЦИИ:Длина
полимера,
определяемая
числом
повторяющихся звеньев в цепи.
Степень
полимеризации
большинства
используемых полимеров от 500 до 5000.
Определяет функцию полимера:
˃
˃
˃
˃
˃
Разжижитель
Понизитель фильтрации
Загуститель
Ингибитор глин
Селективный флокулянт
Низкая молекулярная масса
Средняя мол. масса
Высокая мол. масса
Высокая мол. масса
Высокая мол. масса
11. ПОЛИМЕРЫ
Длина цепи - Определяет функцию полимераКороткая:
Полимеры-разжижители - (мм ≈ 10,000)
Средняя:
˃ Понизители фильтрации - (мм ≈ 100 000 - 200 000)
˃ Загустители - (мм ≈ 200 000 – 300 000)
Длинная:
˃ Загустители - (мм ≈ 300 000 – 800 000)
˃ Ингибиторы глин - (мм ≈ 800 000 – 2 000 000)
˃ Флокулянты - (мм ≈ 2 000 000 – 50 000 000)
12. ПОЛИМЕРЫ
СТЕПЕНЬ ЗАМЕЩЕНИЯ:Доля
замещенных групп на 100 повторяющихся звеньев
полимера
Способствует тому, что полимер становится:
Устойчивым к бактериальному воздействию
Более устойчивым к воздействию кальция, магния и хлоридов
Водорастворимым
Максимальная степень замещения молекулы глюкозы – 3,0, т.к. в
молекуле содержится три гидроксильные группы, могущие
вступать в реакцию. Если степень замещения достигает значения
0,45 и выше, полимер становится водорастворимым. Чем выше
данное значение, тем более устойчив полимер к воздействию
жесткости и соли.
13.
ЦЕЛЛЮЛОЗАCH 2 OH
H H
OH
H
O
O
OH
H
H
H
H
O
H
OH
H
O
CH 2OH
n
OH
H
O
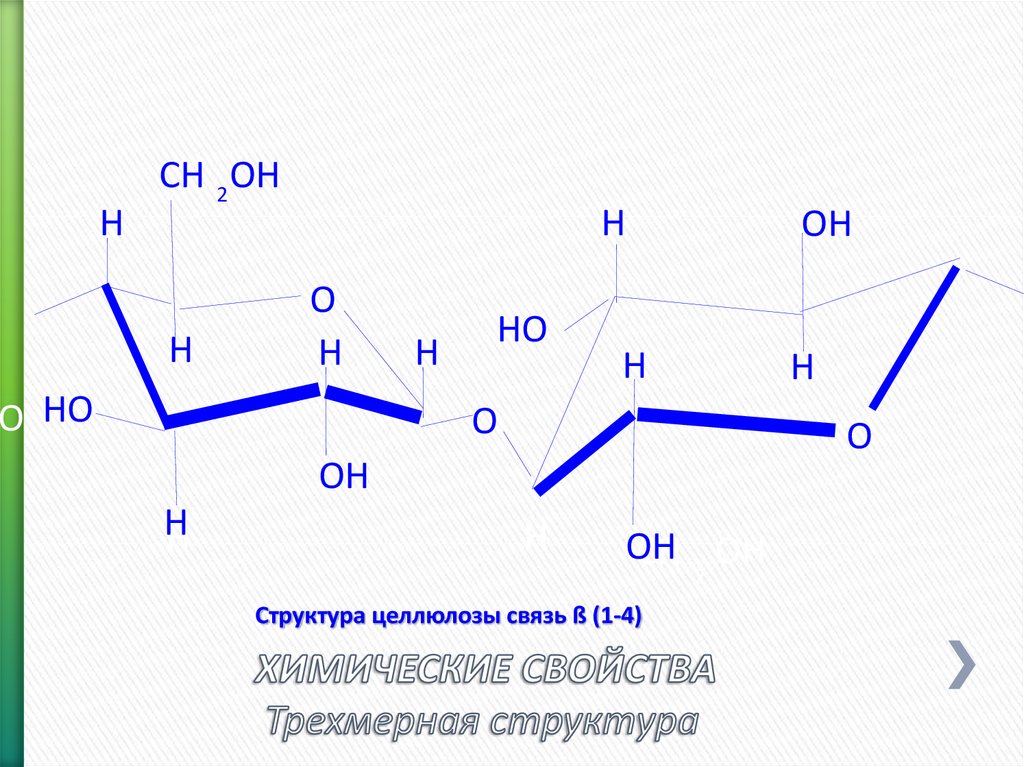
14. ХИМИЧЕСКИЕ СВОЙСТВА Трехмерная структура
HCH 2 OH
H
H
O
H
O НO
H
НO
H
O
H
O
OH
H
H
OH
H
OH
CH 2 OH
Структура целлюлозы связь ß (1-4)
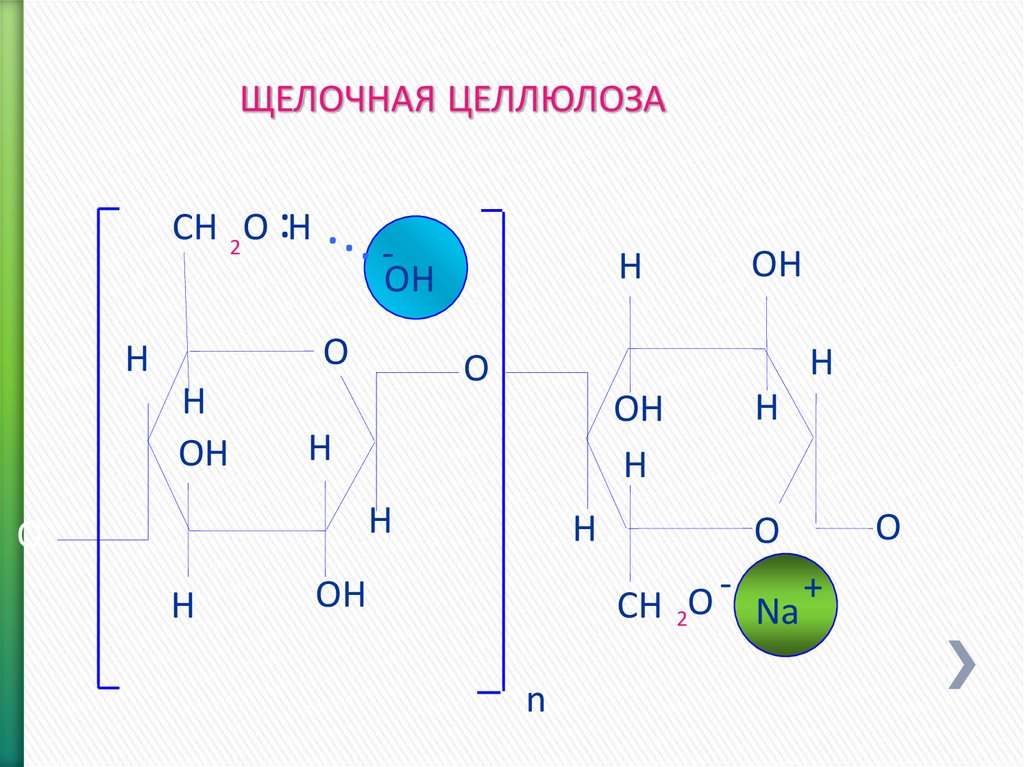
15.
ЩЕЛОЧНАЯ ЦЕЛЛЮЛОЗАCH 2 O :H
... -
H
ОН
O
H
H
OH
H
O
OH
H
H
H
O
H
OH
H
H
O
+
O
CH 2
Na
OH
n
O
16. Модифицирующие агенты
» Монохлорацетат натрияCl CH2 COO Na
» Монохлоуксусная кислота
ClCH2COO H
17. Реакция замещения (первый способ)
» Щелочная целлюлоза + М. А.--- CH2 O Na + CH2 CL COO Na =
--- CH2 О CH2 COO Na + Na CL
18. Реакция замещения (второй способ)
» Щелочная целлюлоза + МХУК--- CH2 O Н + CH2 CL COO Н =
--- CH2 О CH2 COO Н + Н CL
Н CL + Na ОН = Na CL + Н ОН
19. ХИМИЧЕСКИЕ СВОЙСТВА - СТЕПЕНЬ ЗАМЕЩЕНИЯ
КАРБОКСИМЕТИЛЦЕЛЛЮЛОЗА.
CH 2OCH 2COO ..
Na +
H H
OH
O
O
OH
O
OH
H
H
H
H
H
H
OH
n
H
H
O
O
CH 2OCH 2 COO .-..
Na +
20. ХИМИЧЕСКИЕ СВОЙСТВА ФУНКЦИОНАЛЬНАЯ ГРУППА
Функциональные группы разделяютсяна:
Неионогенные
Анионные
Катионные
В молекуле может присутствовать более, чем один
тип групп. Природа заряда некоторых групп зависит
от рН среды и меняется с неионной на катионную или
анионную.
21. ХИМИЧЕСКИЕ СВОЙСТВА ФУНКЦИОНАЛЬНАЯ ГРУППА
» Гидроксильная (--ОН)» Гидроксиэтильная (--OСН2СН2ОH)
» Карбоксильная (--СОО- )
» Карбоксиметильная (--СН2СОО- )
» Сульфогруппа (--SO3-)
» Фосфатная (-- PO3-)
» Аминная (--NH2+ )
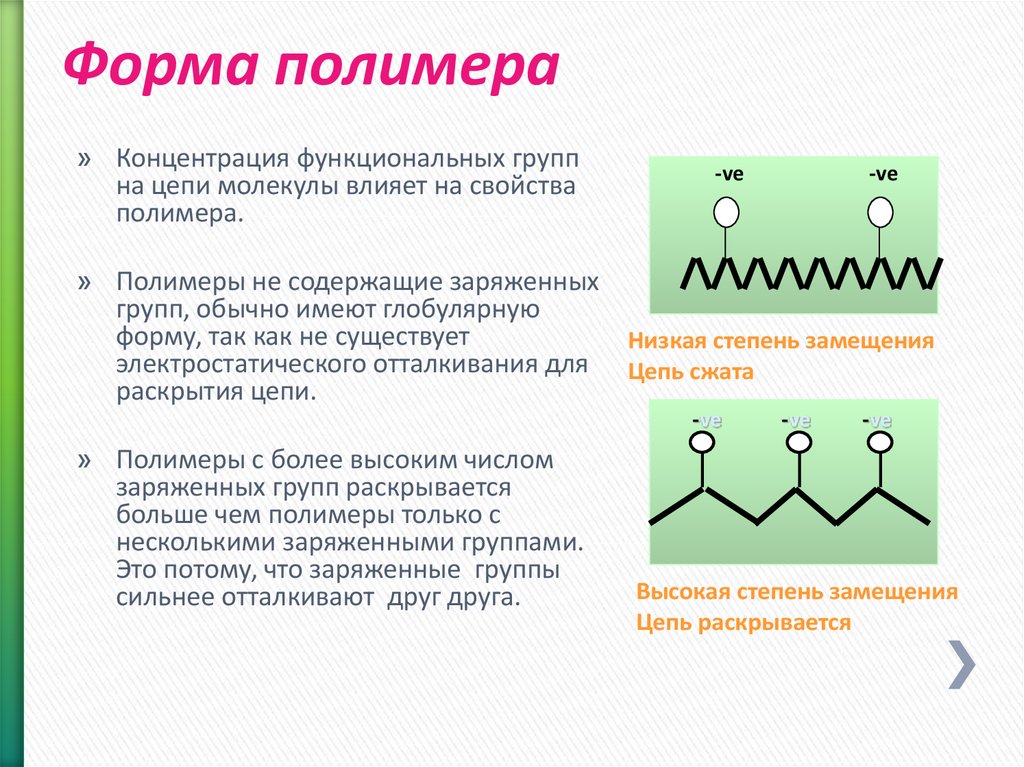
22.
Форма полимера» Концентрация функциональных групп
на цепи молекулы влияет на свойства
полимера.
-ve
-ve
» Полимеры не содержащие заряженных
групп, обычно имеют глобулярную
форму, так как не существует
Низкая степень замещения
электростатического отталкивания для Цепь сжата
раскрытия цепи.
-ve
» Полимеры с более высоким числом
заряженных групп раскрывается
больше чем полимеры только с
несколькими заряженными группами.
Это потому, что заряженные группы
сильнее отталкивают друг друга.
-ve
-ve
Высокая степень замещения
Цепь раскрывается
23. Форма полимера
» Форма полимера зависит и отионной силы раствора.
Электролиты уменьшают
электростатическое отталкивание
между фукциональными группами.
-
-
-
Пресная вода
» Вязкость раствора увеличивается,
когда цепь полимера развернута ( в
пресной воде) и наоборот,
уменьшается в соленной воде
-
-
-
Соленная вода
24. Форма полимера
Поливалентные катионы будутреагировать с несколькими
анионными функциональными
группами на цепи полимера. Это
уменьшает общий размер и
эффективность полимера.
Жесткость воды ограничивает
способность полимеров
гидратироваться.
_
Са+2
-
-
-
25. Форма полимера
------
Са+2
-
Са+2
--
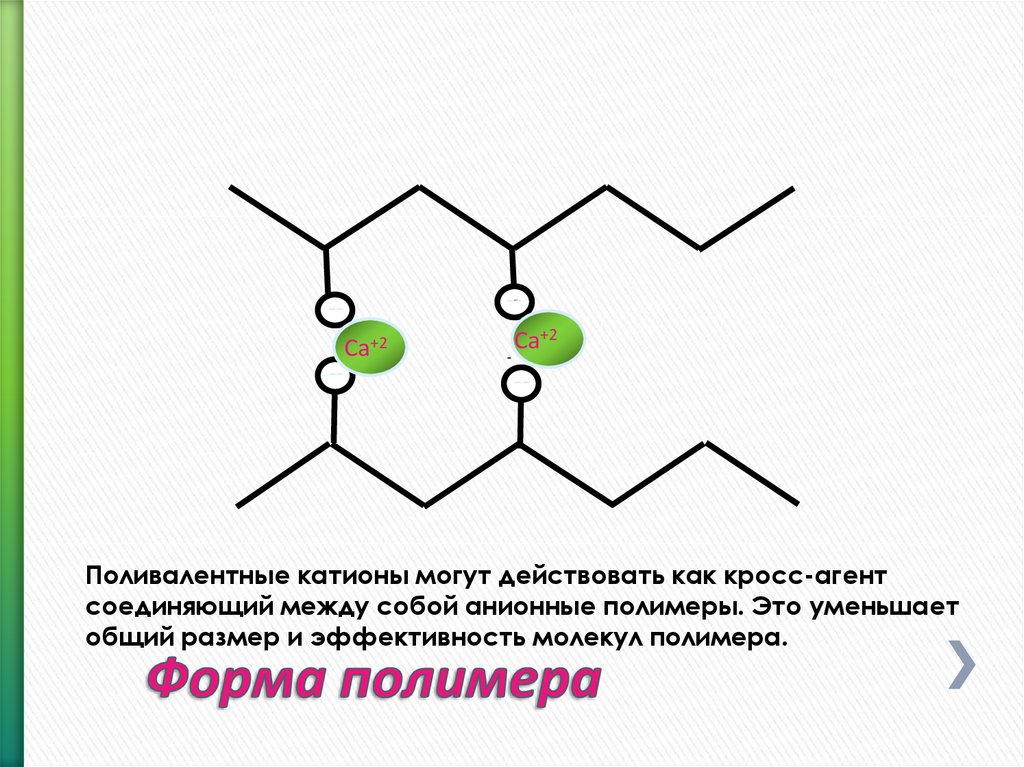
Поливалентные катионы могут действовать как кросс-агент
соединяющий между собой анионные полимеры. Это уменьшает
общий размер и эффективность молекул полимера.
26.
Форма полимера» Форма большинства полимеров будет зависеть от pH среды.
Например, полимеры, содержащие карбоксильную кислоту
станут ионизированными в щелочном pH и раскрываясь в
длинные цепи лучше растворяются в воде
-ve
neutral
-ve
neutral
кислота
щелочь
» Оптимальная растворимость анионных полимеров обычно
находится в диапазоне pH 8 и 9.5. Выше pH может разрушить
некоторые полимеры или привести к частичной дегидратации
27. ФАКТОРЫ ВОЗДЕЙСТВУЮЩИЕ НА ЭФФЕКТИВНОСТЬ ПОЛИМЕРА
» Концентрация полимера» Химия воды
˃ Минерализация
˃ Жесткость
˃ pH
» Содержание твердых частиц
» Температура
» Бактерии
28.
Природные полимеры29. ПРИРОДНЫЕ ПОЛИМЕРЫ
» К природным полимерам относятся˃ кукурузный крахмал
˃ картофельный крахмал
˃ Биополимеры
+ Бактерии Xanthamonas Campestri выделяют полимер в
виде оболочки вокруг тела клеток
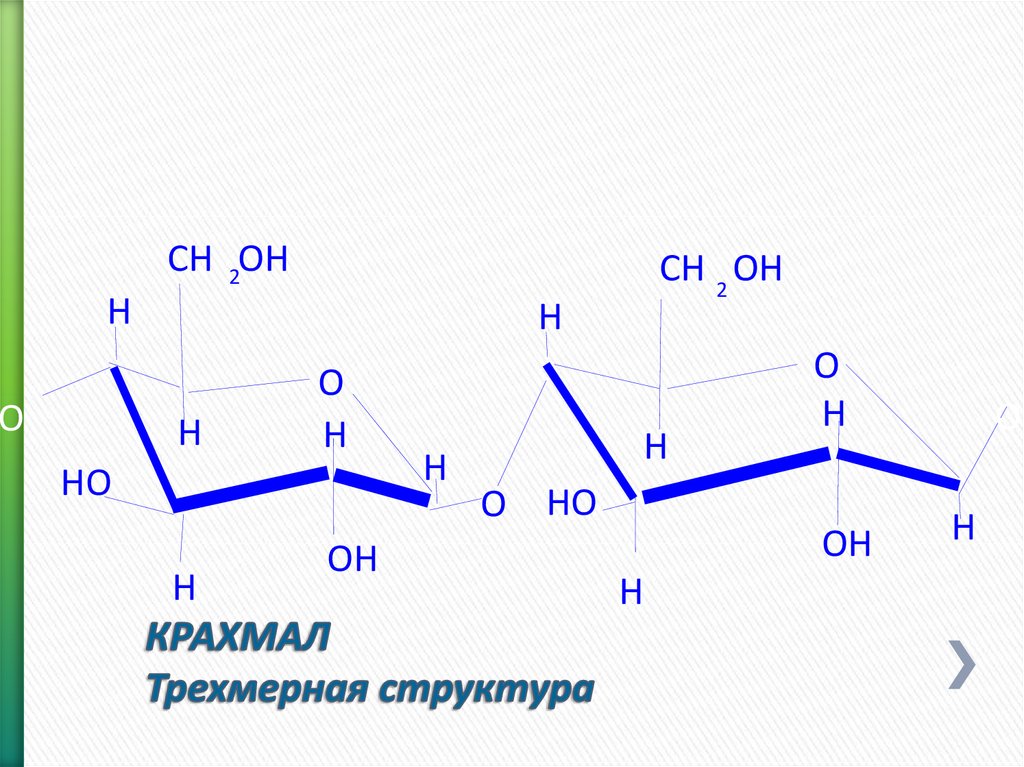
30. КРАХМАЛ Трехмерная структура
CH 2OHH
O
CH 2 OH
H
H
O
H
НO
H
OH
H
H
O НO
O
H
OH
H
O
H
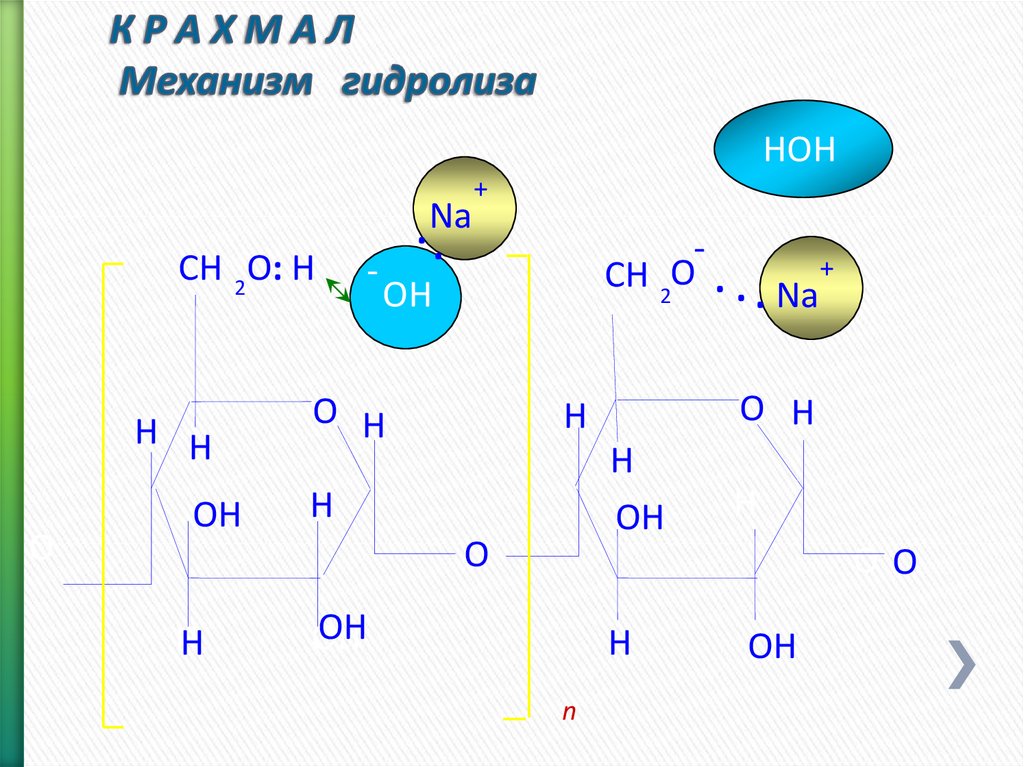
31. К Р А Х М А Л Механизм гидролиза
НОНCH 2O: H
H H
O
OH
-
.Na
.
+
CH 2O . .
ОН
O H
H
OH
O
HH
O H
H
H
. Na
+
H
OO
OH
OH
H
n
OH
32. ПРИРОДНЫЕ ПОЛИМЕРЫ
» Кукурузный крахмал» Неионный (группа-ОН)
» Средняя молекулярная масса~100,000
33.
» Применение» Контроль фильтрации
˃ Пресная вода
˃ Пластовая вода
˃ Морская вода
˃ Соленасыщенная вода
˃ Полимерные системы
» Обработка
˃ 11-22 кг/м3
34.
» Факторы, ограничивающие применение• Ферментация
• Высокий уровень кальция, высокий показатель pH
• Сохранение свойств при температурах до 107ОС
• Проблемы контроля качества
35. Крахмал
mO
Aмилопектин
CH 2 OH
Связь 1-6
O
O
CH
Aмилоза
Связь 1-4
...
H
H
OH
CH 2 OCH 2COO
2
O
H
O
H
.- .. Na
+
H
H
O
OH
H
OH
H
O
H
n
O H
OH
...
36. XC POLYMER
» Биополимер - Xanthamonas CampestriТип: неионный - анионный
Средняя молекулярная масса > 2 000 000
Комплексный разветвленный полимер
37.
CH 2OHH
CH 2OH
H
O
OH
H
O
CООМ
H
O
CH
3
O
H
CH 2
OH
H
OH
CH 2OCCH
H
O
3
H
O H
H
O
H
O
H
OH
H
H
H
OH
O H
H
O
H
O
C
H
H
OH
O
OH
n
38. XC / XCD - ПОЛИМЕР
» Применение˃ Загуститель
+ Увеличение вязкости при низкой скорости сдвига
+ Поддерживает твердую фазу во взвешенном состоянии
+ Придает раствору псевдопластические свойства
˃ Эффективен при использовании как в пресной, соленной воде,
так и в рассолах солей
Обработка - 1-6 кг/м3
39. XC / XCD - ПОЛИМЕР
» Факторы, ограничивающиеприменение
˃ Сохраняет свойства при температурах до 150ОС
˃ Является дорогостоящим продуктом
40. МОДИФИЦИРОВАННЫЕ ПОЛИМЕРЫ
МОДИФИЦИРОВАННЫЕ ЭФИРЫ ЦЕЛЛЮЛОЗЫ:» КМЦ (СМС) - Карбоксиметилцеллюлоза
» ПАЦ (РАС)– Полианионная целлюлоза
» ГЭЦ (HEC) – Гидроксиэтилцеллюлоза - (Не используется в составе
буровых растворов)
» КМК (CMS) – Карбоксиметилированный крахмал
41. ПОЛИМЕРЫ СМС (КМЦ) И РАС (ПАЦ)
» Анионные (группы – СН2СОО- )» Средняя молекулярная масса
˃ 200 000 – 225 000 (Высоковязкие)
˃ 140 000 – 175 000 (Низковязкие)
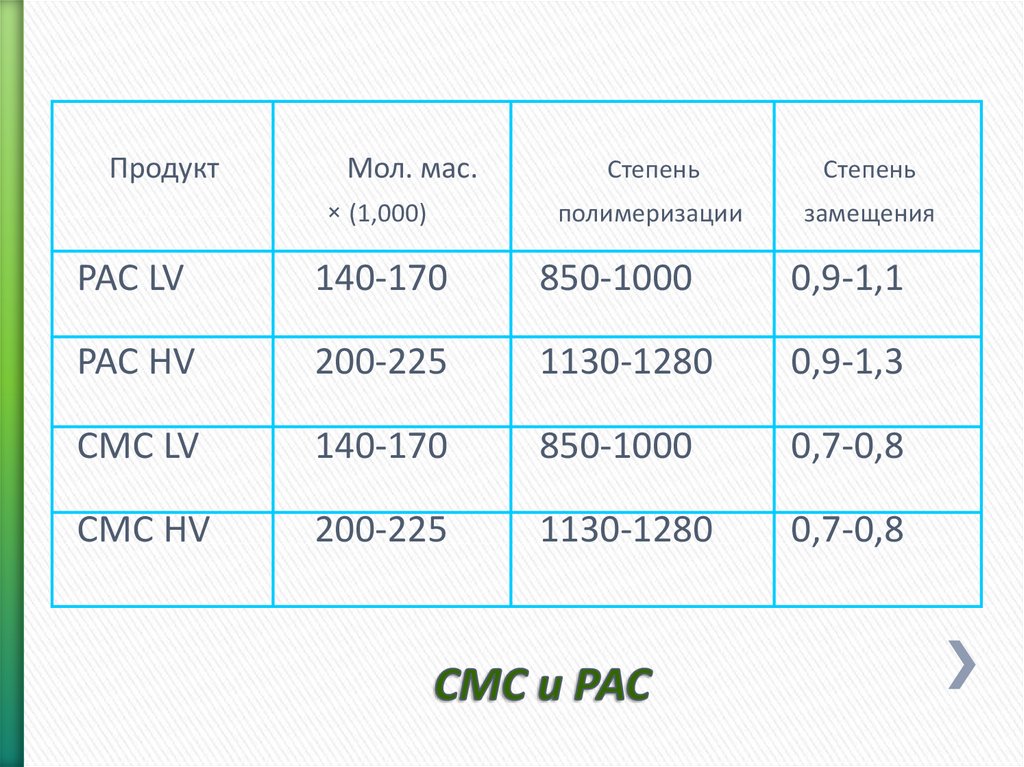
42. CMC и PAC
ПродуктМол. мас.
× (1,000)
Степень
Степень
полимеризации
замещения
PAC LV
140-170
850-1000
0,9-1,1
PAC HV
200-225
1130-1280
0,9-1,3
CMC LV
140-170
850-1000
0,7-0,8
CMC HV
200-225
1130-1280
0,7-0,8
43. CMC и PAC ФАКТОРЫ, ОГРАНИЧИВАЮЩИЕ ПРИМЕНЕНИЕ
ПродуктХлориды
Жесткость
Темп. ОС
PAC LV
Насыщ.
1,000
155
PAC HV
Насыщ.
1,000
160
CMC LV
20,000
500
150
CMC HV
20,000
500
150
44. КАРБОКСИМЕТИЛИРОВАННЫЙ КРАХМАЛ (КМК)
» Модифицированный природный» Анионный (группы – СН2СОО- )
» Mолекулярная масса 140 000 – 170 000
45. НЕС (ГЭЦ - ГИДРОКСИЭТИЛЦЕЛЛЮЛОЗА)
» Модифицированный природный» Moлекулярная масса 200 000 – 225 000
» Неионный
46. ГИДРОКСИЭТИЛЦЕЛЛЮЛОЗА
CH 2OCH 2CH 2 OHCH 2OCH 2CH 2 OH
H H
OH
O
H
O
OH
H
H
H
H
H
H
O
O
H
O
CH 2OCH 2CH 2OH
OH
n
n
47. НЕС (ГЭЦ - ГИДРОКСИЭТИЛЦЕЛЛЮЛОЗА)
ПрименениеКонтроль фильтрации
Повышение вязкости
Пресная вода, морская вода, рассолы солей
48. НЕС (ГЭЦ) ПОЛИМЕР ФАКТОРЫ ОГРАНИЧИВАЮЩИЕ ПРИМЕНЕНИЕ
» Устойчив до 105О С» Эффективность снижается при рН > 10
» Эффективность снижается в крепких рассолах
» Недостаток тиксотропных свойств
49.
Синтетические полимеры50.
» СИНТЕТИЧЕСКИЕ ПОЛИМЕРЫ:˃ Полиакрилат натрия - SP-101
˃ Частичногидролизованный полиакриламид
˃ Различные сополимеры
51. ПОЛИАКРИЛАТ НАТРИЯ
» Синтетический» Анионный
» Молекулярная масса
˃ <10 000 для дефлокулянта
˃ ~300 000 для регулятора фильтрации
52.
CH 2CH
CH 2
CH
-
COO ..
.
Na+
-.
.
COO .
CH
-.
Na+
COO ..
Na
n
+
53. SP-101 (70% AКРИАЛАТ (n)- 30% AКРИЛАМИД (m) Mолекулярная масса = 300000-500000)
CHCH
CH 2
CH 2
CH 2
CH
-
CONH
COO .
..
m
n
Na+
2
CH
CH 2
CH
CH
COO . COO .
..
..
Na +
Na +
CONH
2
2
54. (SP-101) - ПОЛИАКРИЛАТ НАТРИЯ СО СРЕДНЕЙ МОЛЕКУЛЯРНОЙ МАССОЙ
Факторы, ограничивающие применение»
Хлориды – 100 000 мг/л
»
Кальций - 400 мг/л
»
Высокое содержание твердых частиц низкой
плотности
»
Температура 205-230 ОС
55. PHPA
Чaстично Гидролизованный Пoлиакриламидили
Полиакриламид / Полиакрилат
Сополимер
56. Чaстично Гидролизованный Пoлиакриламид (PHPA)
» Moлекулярная масса - 2 – 15 млн.» Aнионный
» Поставляется в сухом или жидком виде
(разведенным в минеральных маслах)
57. Чaстично Гидролизованный Пoлиакриламид (PHPA)
» Получается в результате:˃ щелочного гидролиза полиакриламида
˃ Сополимеризации акриламида с акрилатом
58. ГИДРОЛИЗ ПОЛИАКРИЛАМИДА
CHCH
2
CH
CH
CONH
CO
+ NaОН
2
NH
2
CH
2
CH
2
2
CH
CH
CONH
COО -.
2
+ NH 3
..
Na+
59. СОПОЛИМЕР- ПОЛИАКРИЛАМИДА / ПОЛИАКРИЛАТА
CHCH 2
CH 2
CONH
n
2
COO
m
2
CH
CH
CH
CH
2
CH
-..
.
CONH
+
Na
2
CONH
2
60.
Чaстично ГидролизованныйПoлиакриламид (PHPA)
» Применение
Флокуляция твердой фазы
+ Селиктивная
+ Общая
Стабилизация/ингибирование глин
+ Адсорбция на поверхности
+ Загущение водной фазы
+ Адсорбция свободной воды
61.
Полимеры применяемыев буровых растворах
62. ГУАРОВАЯ СМОЛА
Натуральный водный коллоид полисахариднойприроды. Добывают из семян тропических
растений Гуар, произрастающих в Индии.
В настоящее время растения культивируется и в
других странах.
Образует вязкие растворы при концентрации около
1% и формирует гелеобразную структуру при рН
около 7.
Используется для загущения пресных,
минерализованных, соленасыщенных и калиевых
буровых растворов.
63. ГУАРОВАЯ СМОЛА
OHH
OH
H
O
CH
...
O
CH 2 OH
O
H
2
O
H
OH
OH
H
H
H
H
H
H
O
OH OH
H
H
O
...
O
CH 2 OH
n
64. Танины (соединение 5 молекул дигалловой кислоты с глюкозой)
OOH
C
O
HO
HO
HO
5 молекул
HO CO
OH
OH
+
CH 2OH
OH
OH
HO
O
OH
O
рН >11,5
65. Таннины
содержатся в коре, древесине, листьях,плодах (иногда семенах, корнях, клубнях)
многих растений — дуба, каштана, акации, ели,
лиственницы, эвкалипта, чае, гранатового и
хинного деревьев, сумаха, квебрахо и других;
придают листьям и плодам терпкий вкус.
Таннины являются исходным продуктом для
производства дефлокулянтов – Desco и др.
66. Лигнит (гуминовые кислоты)
СН2COOHC
O
OH
HO
OH
COOH
COOH
COOH
67. Гуминовые кислоты
являются составной частьюбурых углей, торфа и т.п. и образовались в
результате биохимических превращения
продуктов разложения органических остатков
при участии микроорганизмов, влаги и
кислорода атмосферы).
Гуминовые кислоты входят в состав
органической массы торфов (25-50%), бурых
углей (45-60 %), окисленных каменных углей (до
60%), некоторых почв (до 10%)
В результате экстракции из исходного сырья
водной вытяжки получают гуминовые
кислоты в промышленных масштабах
68. Гуминовые кислоты
» По химической структуре гуминовые кислотывысокомолекулярные (мол. масса 1300-1500)
конденсированные ароматич. соединения, в
которых установлено наличие фенольных
гидроксилов, карбоксильных, карбонильных
и ацетогрупп, простых эфирных связей и др.
Элементный состав: 50-70% С; 4-6% Н; 2535% О.
» Гуминовые кислоты являются исходным
продуктом для производства реагента
TANNATHIN
69. TANNATHIN
Реагент может использоваться в качестве понизителя водоотдачи иразжижителя в любых типах растворов на водной основе. Реагент
особенно эффективен при высоких температурах, загрязнении СО2 и
высокой жесткости раствора, где прочие реагенты теряют
эффективность. «Таннатин» часто применяется для обработки
растворов, загрязненных цементом – он снижает щелочность и
жесткость загрязненного раствора.
Рекомендуемая концентрация реагента в растворе – от 3 до 23 кг/м3.
Ввиду кислой природы реагента, рекомендуется сочетать обработку
«Таннатином» с добавлением каустика (или альтернативного
щелочного реагента) для поддержания рН раствора и увеличения
растворимости реагента. Рекомендуется добавлять 1 мешок каустика
на каждые 4 мешка «Таннатина».
При обработке соленасыщенных систем рекомендуется
прегидратировать реагент в отдельной емкости в пресной или
слабоминерализованной воде (нормальной или высокой щелочности).
Максимальная эффективность реагента достигается в растворах с
рН=9-11.
70. Лигнин (лигносульфонаты)
Н3C-ОC
C
O
O
SO3Na
OH
HO
OH
CH3
SO3Na
O
COOH
71. Лигнин (лигносульфонаты)
» Молекула лигнина состоит из продуктовполимеризации ароматических спиртов; основной
мономер — конифериловый спирт.
» Древесина лиственных пород содержит
20—30 % лигнина, хвойных — до 50 %.
» Лигнин — ценное химическое сырьё,
используемое во многих производствах, в том
числе для получения реагентов SPERSENE,
SPERSENE СF
72. SPERSENE
«SPERSENE» может использоваться в качестведефлокулянта и понизителя водоотдачи во всех типах
растворов на водной основе. Его эффективность доказана в
растворах на основе пресной, морской воде, в
соленасыщенных, в калиевых и гипсовых системах, а также при
бурении высокотемпературных скважин в растворах с низким
содержанием активной твердой фазы.
Лабораторные и промысловые испытания показали очень
высокую разжижающую эффективность продукта в присутствии
различных примесей и загрязнителей.
Рекомендуемая концентрация «SPERSENE» колеблется от 3
до 34 кг/м3 в зависимости от применяемой системы,
содержания твердой фазы и рекомендуемых параметров
раствора.
Для максимальной эффективности продукта уровень рН
необходимо поддерживать на уровне 9-11. Щелочность
регулируется каустической содой.
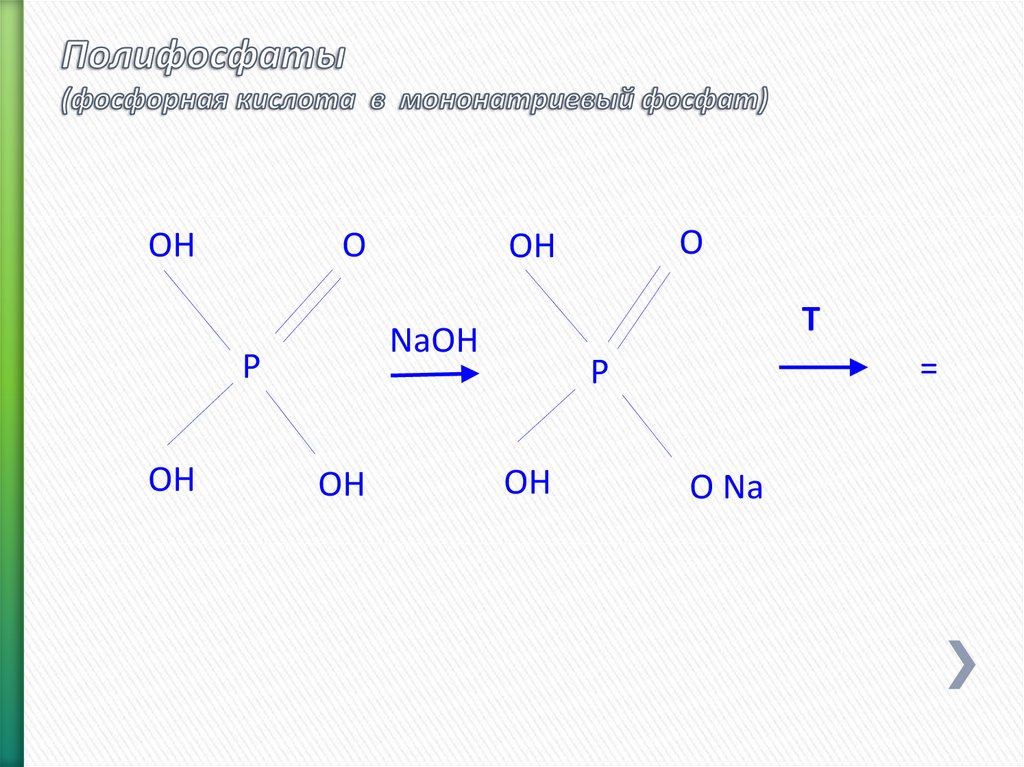
73. Полифосфаты (фосфорная кислота в мононатриевый фосфат)
OHO
OH
T
NaOH
P
OH
O
OH
=
P
OH
O Na
74. Полифосфаты (дегидропирофосфат натрия - SAPP)
OOH
O
P
=
O Na
OH
P
O
+
O Na
HOH
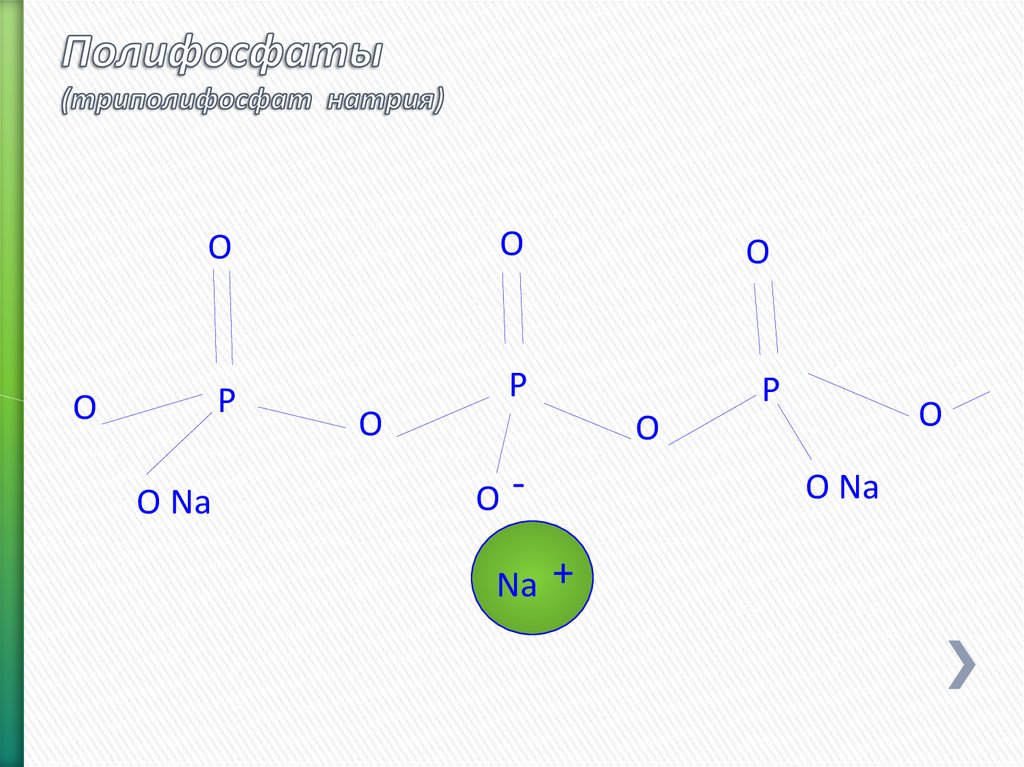
75. Полифосфаты (триполифосфат натрия)
OO
O
P
P
P
O
O Na
O
O
O
ONa +
O Na
76. HOSTADRIL 2825
77. POLYDRIL
OНСН2
С
R1
СН2
SO3 - Na+
OН
С
SO3 - Na+
n
78. РЕЗЮМЕ
» Функции зависят от:˃ Степени замещения
˃ Степени полимеризации
» Факторы, ограничивающие
применение
˃
˃
˃
˃
Температура
Наличие ионов в растворе
pH
Твердая фаза
79. Твердая фаза
» Растворимая твердая фаза, которую невозможноотфильтровать или механически удалить из
жидкой фазы
˃ Соль
˃ Сахар
» Твердые частицы (нерастворимые), удаляемые
механически или в процессе фильтрации
˃ Глины
˃ Песок
80. Глинистые твердые частицы
Обеспечивают вязкость и регулируютфильтрацию
Термоустойчивы
Пластовые глины являются загрязителями
При наличии избытка глинистой твердой
фазы возрастает необходимость и стоимость
химической обработки
Требуется разбавление раствора
81. Классификация глин
Физические свойстваРазмер частиц
Тип породы / Минералогия
˃Кристаллическая структура
˃Химический состав
82. Классификация глин по кристалической структуре
» Слоистые силикатыСмектит
Вайомингский бентонит (монтмориллонит)
и буренная порода
Иллит
Выбуренная порода
(до 1998 г относился к гидрослюдам)
Выбуренная порода
Выбуренная порода
Хлорит
Каолинит
» Игольчатые
˃ Аттапульгит
˃ Сепиолит
Солестойкие растворы
Солестойкие и термостойкие растворы
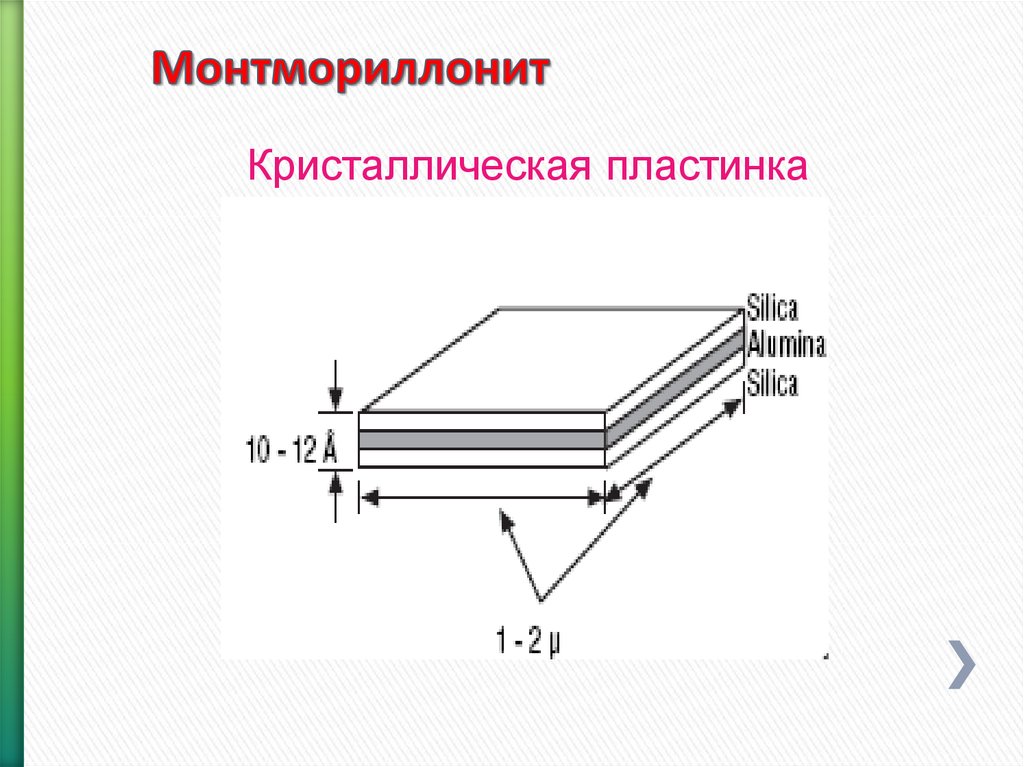
83. Слоистые силикатные глины
Глины:˃ Двухслойные
+ Слой кремнезема
+ Слой глинозема
˃ Трехслойные (например: натриевый бентонит)
+ Слой кремнезема
+ Слой глинозема
+ Слой кремнезема
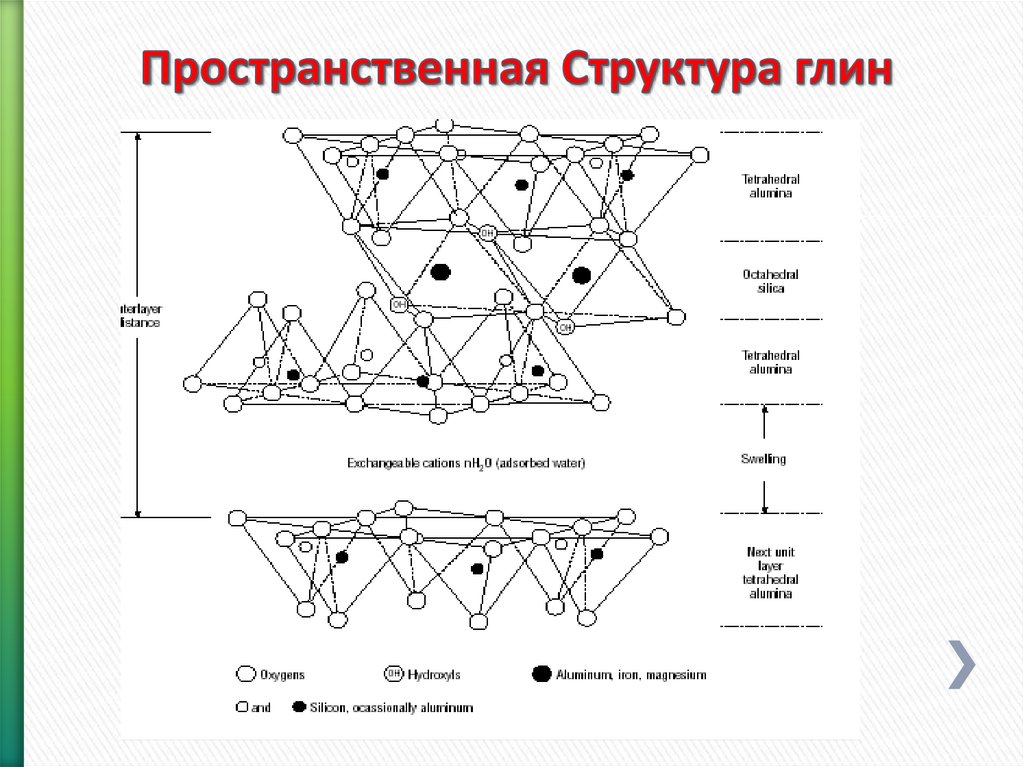
84. Структура трехслойных алюмосиликатов
85. Пространственная Структура глин
86. Слоистые силикатные глины
Глины:˃ Четырехслойные (хлорит)
+ Слой кремнезема
+ Слой глинозема
+ Слой кремнезема
+ Слой брусита
(гидроксид магния)
87. Кристаллы слоистых силикатных глин
Диаметр: ~1 микрон (1 милионная метра)Tолщина: ~10 Å (10 миллиардных метра)
Диаметр : Толщина: 1,000 : 1
Площадь поверхности / Вес: ~ 800 м2 / г
Кристаллические пластинки расположены поверхность к
поверхности в виде пачки
Расстояние между кристаллами от 7 дo 17 Å
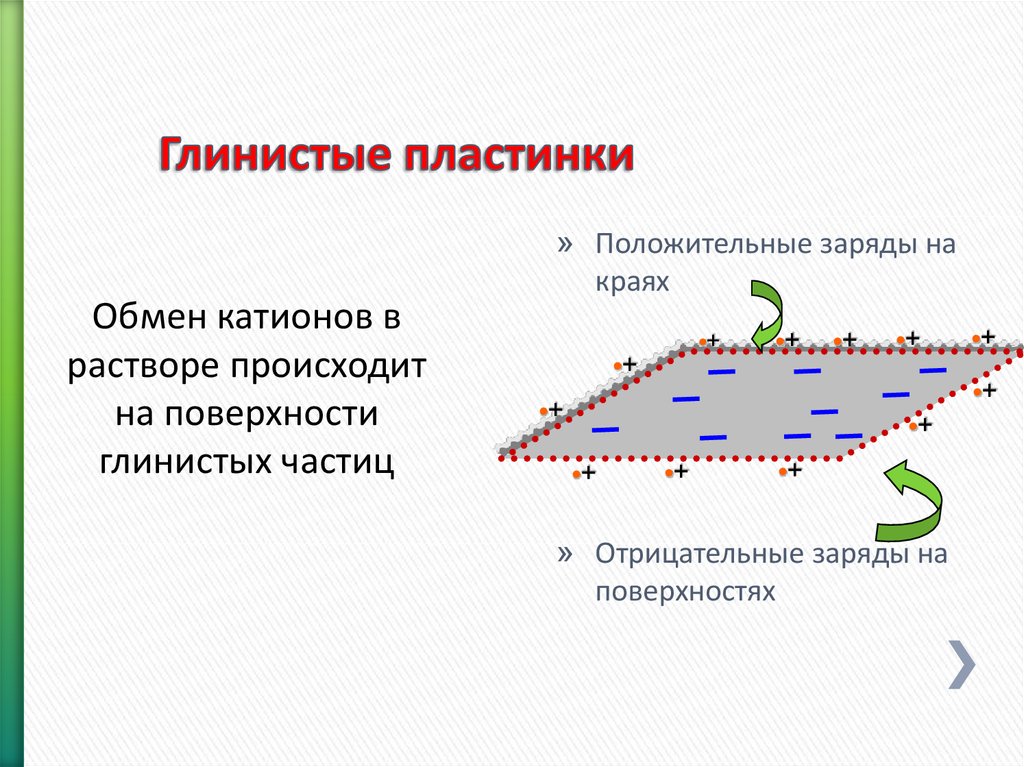
Заряды на основной поверхности в большинстве отрицательные
Заряды на краях кристаллов в основном положительные
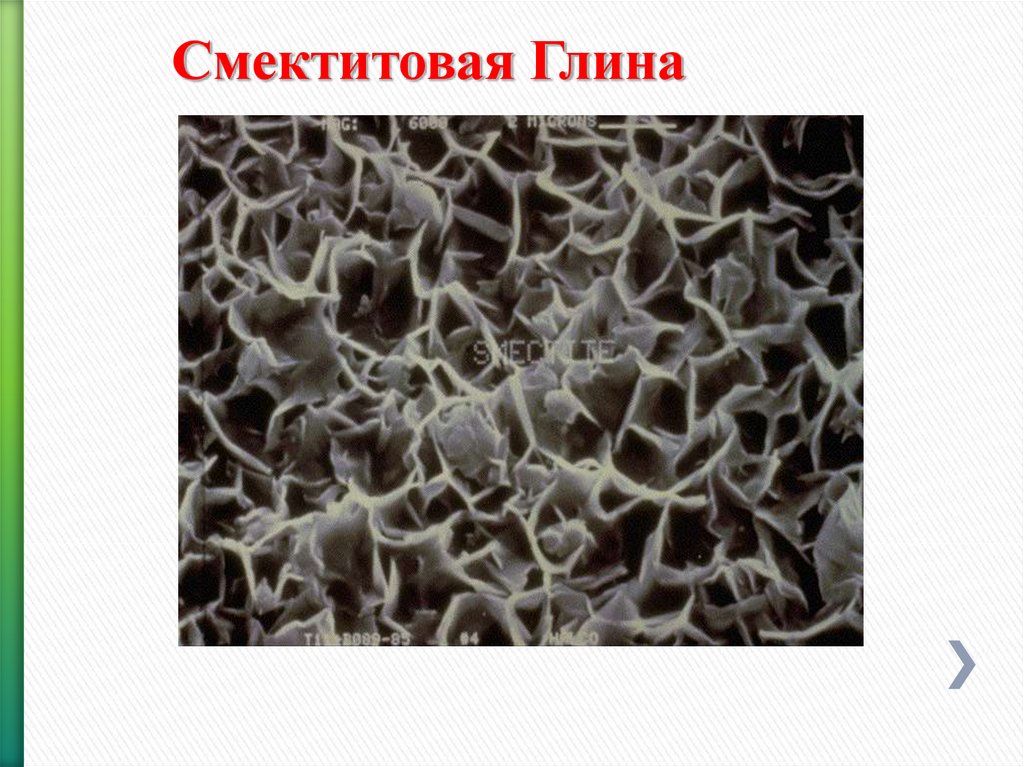
88.
Смектитовая Глина89.
Смектитовые глиныВ данное семейство входят:
»
»
»
»
»
Монтмориллониты
Гекториты
Сапониты
Нонтрониты
Фемонтмориллониты
90. Монтмориллониты
В октаэдрическом слое атомы алюминиячастично замещены на атомы магния
Поверхность имеет отрицательный заряд 0,3 –
0,6 единиц
В обменном комплексе присутствуют ионы Na+,
K+, Ca+2, Mg+2, Fe+3
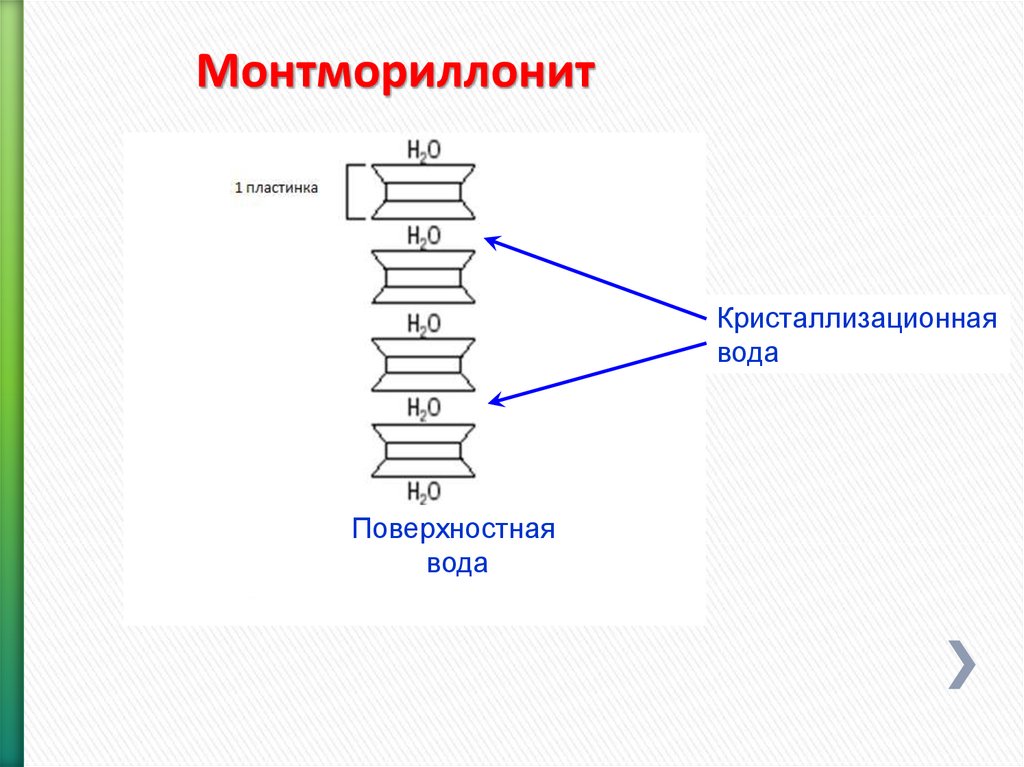
Между кристаллами прочносвязанная вода
91. Монтмориллониты
Включает:˃
˃
˃
˃
˃
Монтмориллонит натрия (Вайомингский бентонит)
Кальциевый/магниевый монтмориллонит.
Для придания раствору необходимой вязкости
требуется в 4 (четыре) раза больше, чем
натриевого
Монтмориллониты смешанного состава
Форма частиц – правильные плитки
Размером до 2 мкм
92. Монтмориллонит
Кристаллическая пластинка93.
МонтмориллонитКристаллизационная
вода
Поверхностная
вода
94.
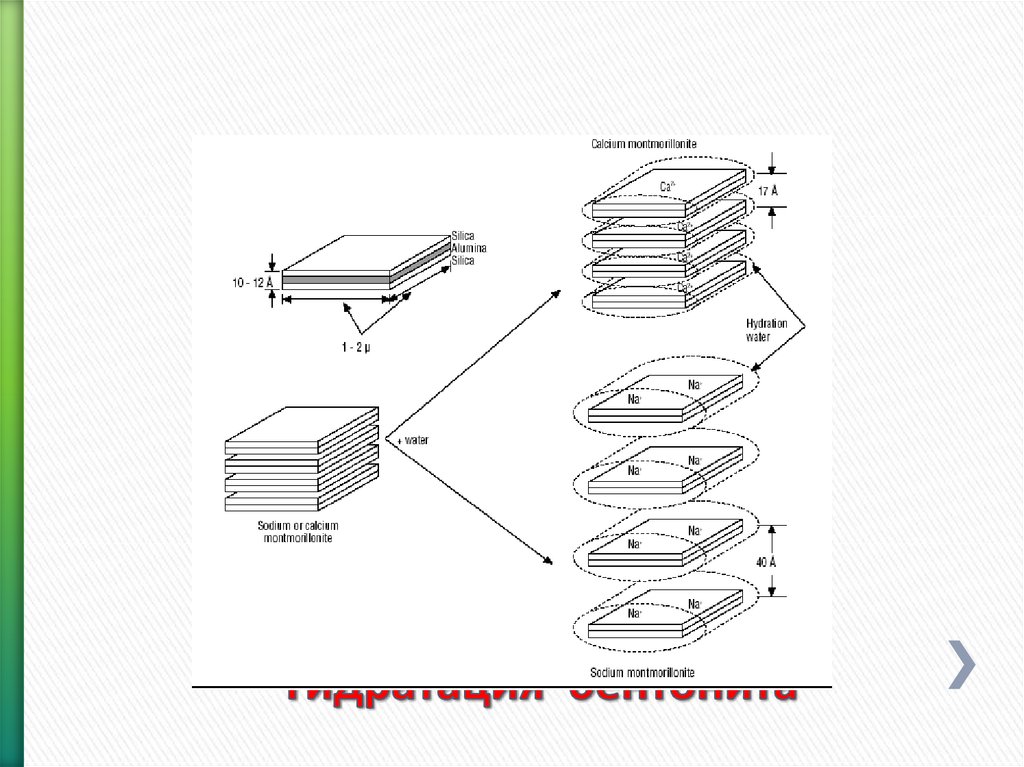
БентонитБентонит является в основном глиной
монтмориллонитового вида (не менее 70 %)
Обладает высокой способностью
гидратироваться в пресной воде
Увеличивается в объеме от 4 до 10 раз после
гидратации
95.
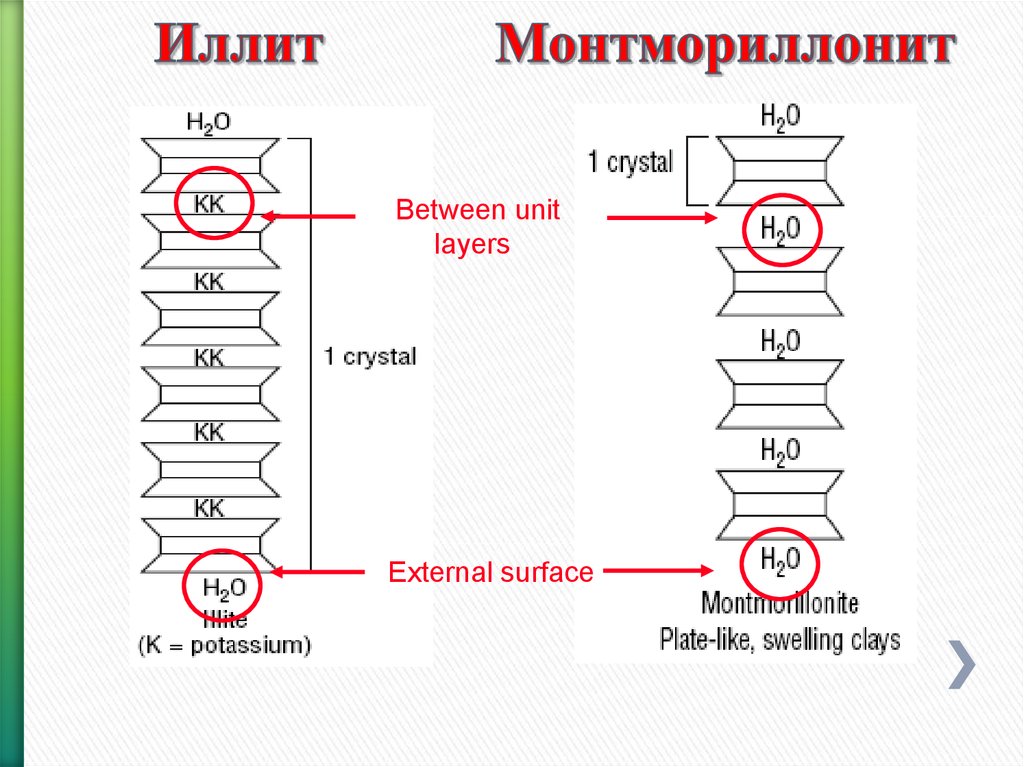
ИллитТРЕХСЛОЙНАЯ СТРУКТУРА
Относится к слюдистым минералам
В тетраэдрическом слое атомы кремния
частично замещены на атомы алюминия
Замещение кремния на алюминий меньше, чем у
настоящих слюд
В обменном комплексе присутствуют в основном
ионы K+ , но могут находиться ионы водорода,
магния, натрия
96. Иллит Монтмориллонит
Between unitlayers
External surface
97.
KaолинитДВУХСЛОЙНАЯ СТРУКТУРА
Форма частиц – шестиугольная плитка
размером до 5 мкм.
Заряды внутри структуры уравновешены, а в
решетке очень мало замещений
Между слоями сильная водородная связь
98.
KaолинитПриродный кристалл состоит из 100 слоев
(пластинок)
Набухания в пресной воде почти не
происходит
При интенсивном перемешивании
увеличивается содержание мелких частиц в
растворе
99. Аттапульгит (Палыгорскит)
100. Глинистые пластинки
Обмен катионов врастворе происходит
на поверхности
глинистых частиц
» Положительные заряды на
краях
+
+
+
+
+
+
+
+
+
+
+
+
» Отрицательные заряды на
поверхностях
101. Факторы, влияющие на ионообмен
Тип глинПорядок замещения катионов
• Размер/Тип катионов
• Разность зарядов
Концентрация катионов
102. Ионный обмен Порядок замещения
Литий
Натрий
Калий
Mагний
Кальций
Алюминий
Водород
Легкий ионный
обмен
Более тяжелый
103. Катионообменная емкость
ГлиныКатионообменная емкость
Мг-экв / 100 г
Монтмориллонит
70 – 130
Иллит
10 – 40
Каолинит
Аттапульгит
3 – 15
10 - 35
104. Катионообменная емкость
• Катионообменная емкость глины – способностьглины адсорбировать на своей поверхности
катионы
• Катионообменная емкость показывает, насколько
данная глина реакционно-активна
105. Слоистые глины подразделяются
Набухающие глины• Смектит
Не набухающий глины
• Иллит *
• Каолинит
• Хлорит
* Разная степень набухания
106. Взаимодействие глин и воды
Р = С*М-1*R*T, где
М – масса 1 моля растворенного
вещества;
С – весовая концентрация
R – универсальная газовая постоянная;
Т – абсолютная температура
107. Осмотическое давление
108. Гидратация бентонита
109. Гидратация бентонита
+H
2O
105°
+
H
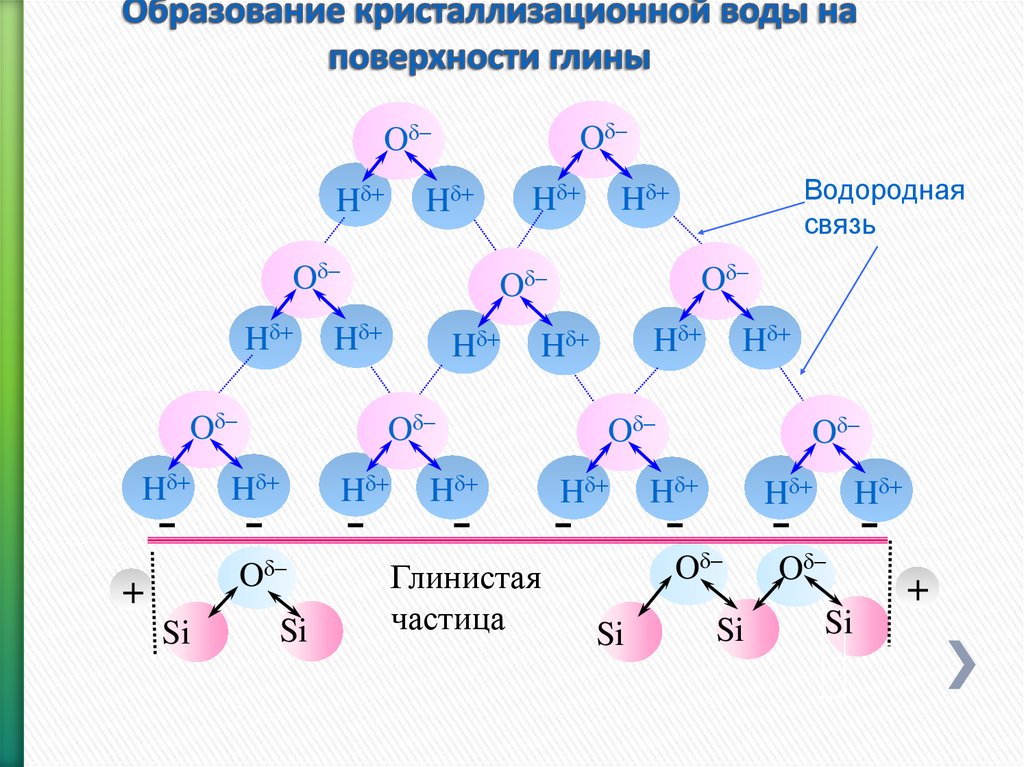
110. ВОДА, ПОЛЯРНЫЙ РАСТВОРИТЕЛЬ
Od-Od-
Hd+
OdHd+
-
+
Si
Od-
Hd+
Hd+
Hd+
-
OdSi
-
Hd+
Hd+
Od-
Hd+
Водородная
связь
Hd+
Od-
OdHd+
Hd+
Hd+
Hd+
Od-
Hd+
-
Глинистая
частица
Hd+
-
Od-
Hd+
Hd+
-
Od-
Si
Si
Hd+
-
Od-
Si
-
+
111. Образование кристаллизационной воды на поверхности глины
» АГГРЕГИРОВАННЫЕ˃ Поверхность к поверхности
» ДИСПЕРГИРОВАННЫЕ
˃ Хаотично расположены
» ФЛОКУЛИРОВАННЫЕ
˃ Поверхность к торцу
» ДЕФЛОКУЛИРОВАННЫЕ
112. Типы связей глинистых частиц
Поверхность кповерхностям
Число пластин в
пачке варьируется
Естественное
состояние глин
пластинчатого типа
или присутствие
большого количества
катионов
113. Агрегация
Частички глины хаотичнорасположены
Поверхностные заряды
влияют на их
расположение
114. Дисперсия
» Частицы не осаждаются» Причины:
˃ Броуновское движение
˃ Размер частиц очень мал
˃ Отрицательные заряды в основном на базальной
поверхности
˃ Осаждаются при флокуляции, когда увеличивается
размер флокул
115. Дисперсия глин
• Поверхность к торцу илиторец к торцу
• Обычное состояние
глинистых пластин в
растворе
• Степень флокуляции
возрастает за счет
примесей: соли, кальция,
магния, цемента, и т.п.
116. Флокуляции (коагуляция)
» Коагуляция - уменьшение электростатическогозаряда твердых частиц, позволяющее частицам
сближаться и образовывать агломераты
» Флокуляция – физико-химические связи,
формируемые между двумя или большим
количеством частиц, заставляют частицы
слипаться в крупные «флокулы»
117. Ключевые термины
Снижение электрического заряда на поверхностичастиц способствует сближению частиц
Вероятность столкновения между частицами
резко увеличивается
На близком расстоянии вступают в действие Вандер-Ваальсовы силы (межмолекулярное
взаимодействие)
118. Механизм коагуляции
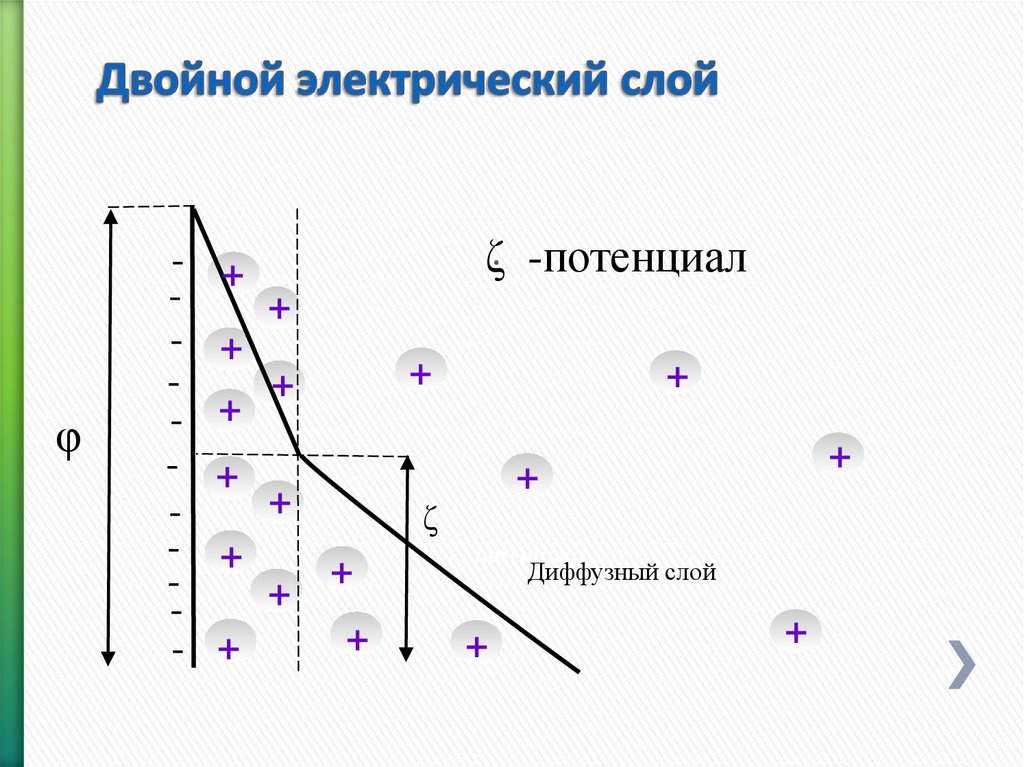
φ-
+
ζ. -потенциал
+
+
+
+
+
+
+
+
+
+
+
+
+
ζ
+
+
- потенциал
Диффузный слой
+
+
119. Двойной электрический слой
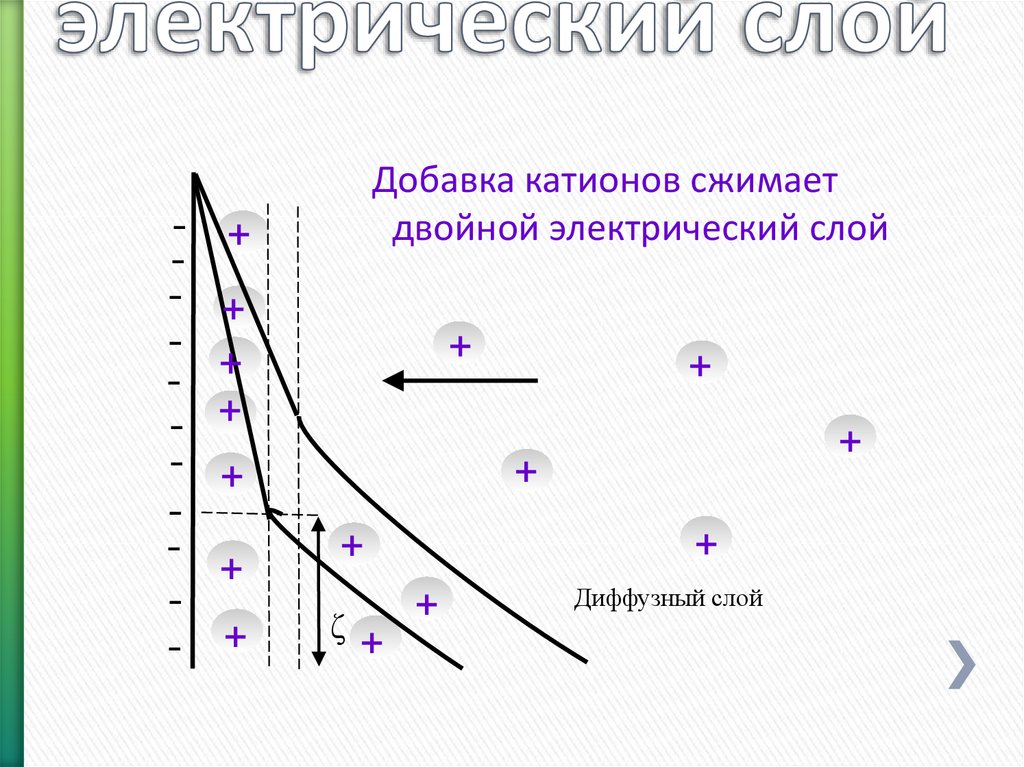
-Добавка катионов сжимает
двойной электрический слой
+
+
+
+
+
+
+
+
+
+
+
+
+
ζ +
+
Диффузный слой
120. Двойной электрический слой
Катионоактивныекоагуляторы
+
+
+
Электрическая по
природе
+
+
+
+
+ +
+
+
+
+
++
+
+
+
+
+
+
+
+
+
+ +
+
+
+
+
+
+
+
+
+
+
+
+ +
+
+
+
Частицы с отрицательным
зарядом
“Чистая
коагуляция”
относится к
одной частице
Слабая агломерация
Полностью
реверсивна
121. Механизм коагуляции
» Слипание частиц в рыхлые и пористыетрехмерные структуры произвольной
формы, с помощью
высокомолекулярных полиэлектролитов
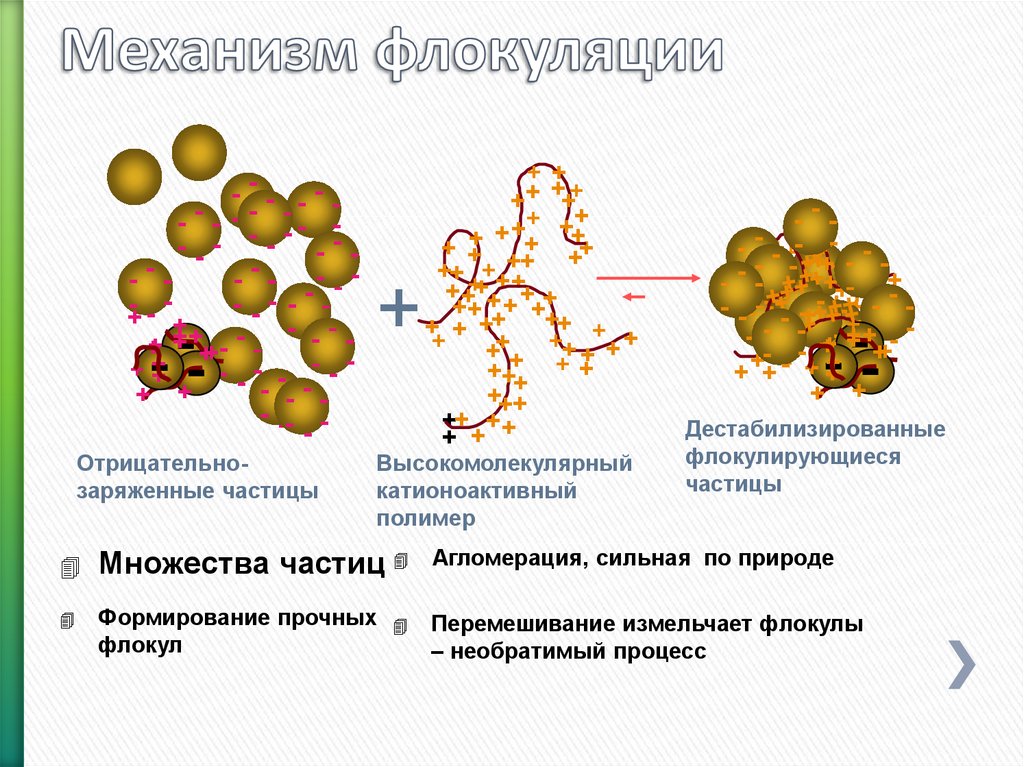
122. Флокуляция
Высокомолекулярныйкатионоактивный
полимер
----+
- +-++-+
---- - - ++- ++
+
- - -- +-+- -- ++-- +-+
+
+
+
+
- --- --+-+- -- + - - + - -- +
- -- -++-- -+- +
+-+-++
+ +
+ ++ - + +
+- +
+
+
+
+
+
Отрицательнозаряженные частицы
+
++
+
+ +++
+ ++
+
+
+
+ ++
+ +
+
++ +++++
+ ++++ + +
++ ++ ++
+
+ + +
+ ++ ++ ++ +
+
++++ + +
+++
++ ++
+ +
Дестабилизированные
флокулирующиеся
частицы
Множества частиц
Агломерация, сильная по природе
Формирование прочных
флокул
Перемешивание измельчает флокулы
– необратимый процесс
+
--- --- - - - --- - -- - ---- - - - -- - - --- - +- +
- -- -- +
+
+
+- +
+
+
--- - --- --- + +
- -- - -
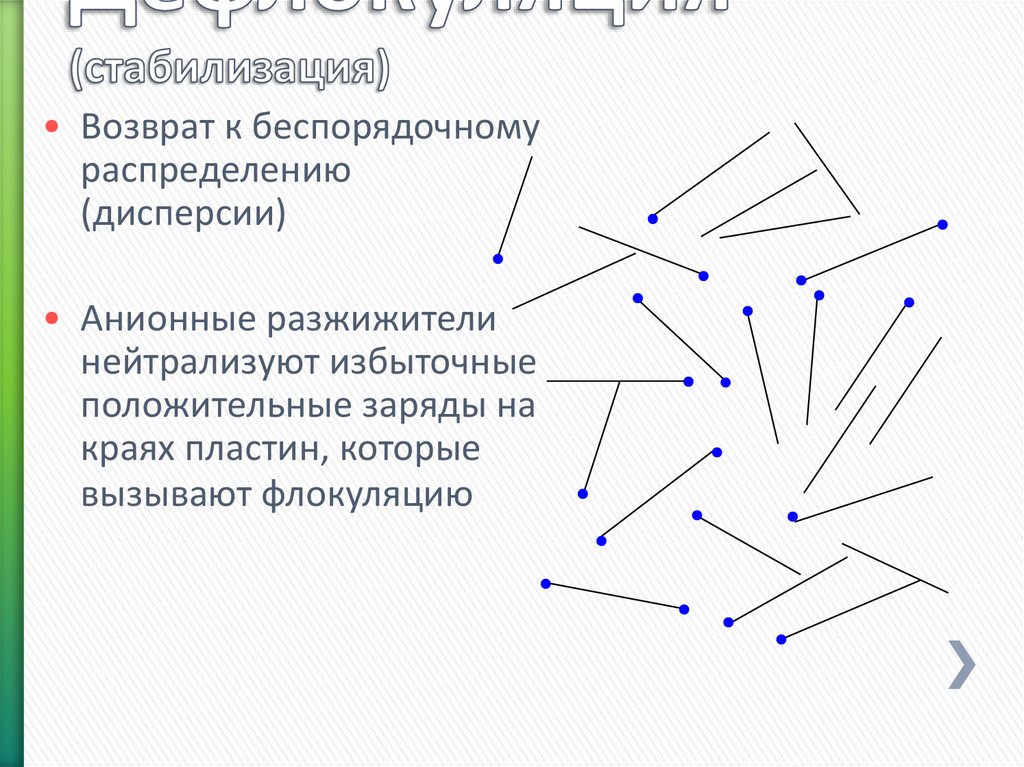
123. Механизм флокуляции
• Возврат к беспорядочномураспределению
(дисперсии)
• Анионные разжижители
нейтрализуют избыточные
положительные заряды на
краях пластин, которые
вызывают флокуляцию
124. Дефлокуляция (стабилизация)
Полимер-
+
SiSi
- +
-
-
Od-
Od-
Si
Si
-
-
125. Механизм стабилизации
Агрегация: Снижение вязкостиДисперсия: Возрастание вязкости
Флокуляция: Возрастание вязкости
Дефлокуляция: Снижение вязкости
126. Типы связей глин
Бентонит АНИ: Обработанный (Обогащенныйили Модифицированный)
• Используется в массовом бурении при забойных
температурах до 150 0С
Бентонит природный или необработанный
• Удовлетворяет требованиям АНИ без
обогащения
• Используется для бурения высокотемпературных
скважин
127. Бентонит АНИ Монтмориллонит натрия
Технические условия:Концентрат
Необработанный
бентонит
71 кг/м3
600 об/мин
PV
Обработанный
бентонит
64 кг/м3
Аттапульгит
30 и более
30 и более
10 сПз мин.
YP / PV
1,5 макс.
3,0 макс
Фильтрат,
см3
12,5 макс
15,0 макс
57 кг/м3
128. Классификация глин по АНИ
Выход – объем (м3) раствора (с вязкостью 15,0сПз), получаемый из одной тонны сухой глины.
Выход бентонита АНИ - около 16 м3 р-ра ( 15,0
сПз) с одной тонны.
Один кубометр подобного раствора будет :
˃ Содержать 2½% объема твердой фазы
˃ Содержать 5½ % массы твердой фазы
˃ Плотностью 1,03 г/см³
129. Выход раствора
Двухвалентные катионы:˃ Кальций
˃ Магний
Соли
pH
Температура
Полимеры
130. Факторы, воздействующие на выход раствора
131. Влияние рН
132. Влияние солей на вязкость
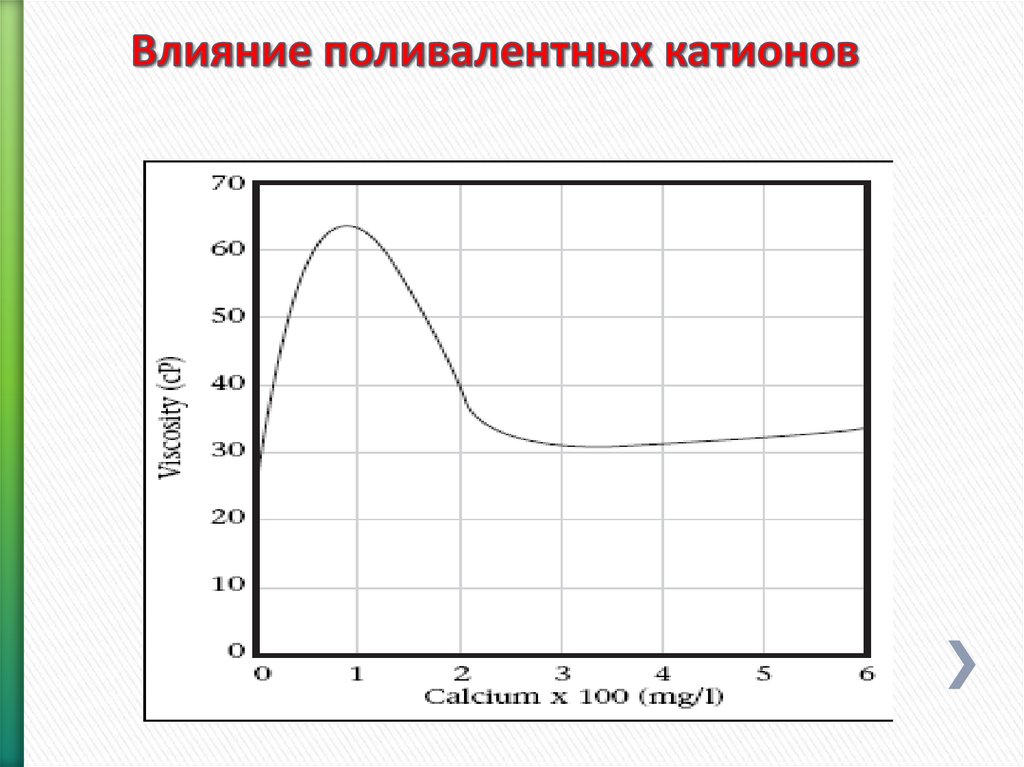
133. Влияние поливалентных катионов
» Выход раствора снижается в любойингибированной системе раствора
˃ Полимерной
˃ Калиевой
˃ Кальциевой
˃ Силикатной
˃ Гликолиевой
» Предварительная гидратация в пресной воде
улучшает свойства бентонита
134. Выход раствора
135. Гидратация бентонита в морской воде
По возможности необходимо предварительно прогидратировать бентонит в преснойводе, в емкости для приготовле-ния раствора
• Перед тем, как добавить в емкость воду, емкость следует
очистить, удалив все остатки химических реагентов и «старого
раствора»
• Довести общую жесткость воды затворения
(содержание
Ca2++Mg2+) до 100,0 мг/л и менее
• Добавить бентонит (80 –100 кг/м3)
• Добавить каустическую соду (0,5 кг/м3)
• Тщательно перемешать и хорошо продиспергировать
• Перед поступлением в активную циркуляционную систему,
прогидратированный бентонит может быть разбавлен до
необходимой вязкости
136. Предварительно гидратированный бентонит
Двухвалентные катионы:˃ Кальций
˃ Магний
Соли
pH
Температура
137. Факторы, воздействующие на выход раствора
Марка глинопорошкаВыход глинистого
раствора, м3/т
ПББ
16
ПБВ, ПБМВ
12
ПБГ
8
ПБД
5
ПБН
5
ПБМА
20
ПБМБ
16
ППД
5
ППМГ
8
ПКГД
4
ПКГН
4
Месторождение
Страна
Завод
(комбинат)
«Иджеванский
Саригюхское
Армения
бентонит»,
Ильский
Биклянское
Россия
Альметьевский
Черкасское
Украина
Константиновский
Таллалаевское
Россия
Куганакский


















































































































 chemistry
chemistry industry
industry








