Similar presentations:
Золи. Некоторые характеристики золей в химии
1.
СООБЩЕНИЕАвторы работы:
Рерих Кирилл
Беликов Владислав
11 класс
МАОУ «СОШ №24»
ГО Краснотурьинск
2.
ЗолиЗоль — высокодисперсная коллоидная
система с жидкой (лиозоль) или газообразной
(аэрозоль) дисперсионной средой, в объёме
которой распределена другая (дисперсная)
фаза в виде капелек жидкости, пузырьков газа
или мелких твёрдых частиц, размер которых
лежит в пределе от 1 до 100 нм (10−9—
10−7м).
3.
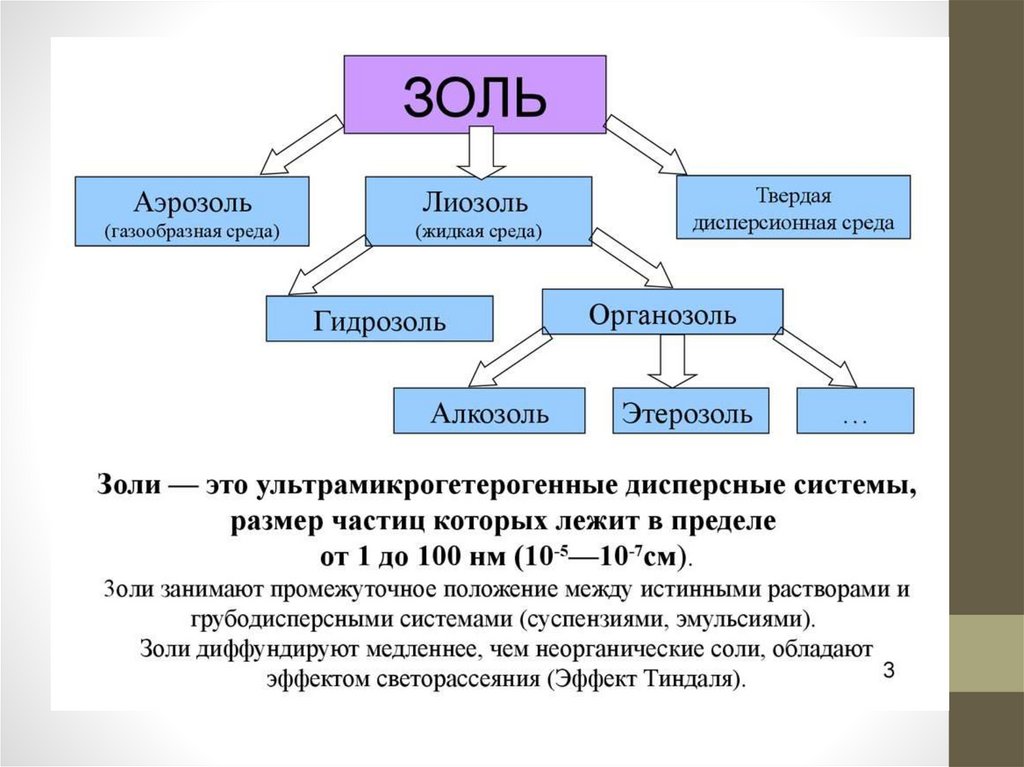
В зависимости от природы дисперсионнойсреды различают:
1. Аэрозоли — системы с газовой дисперсионной
средой (дымы и пыли).
2. Лиозоли (коллоидные растворы) — с жидкой
средой. Подразделяются на гидрозоли с водной
средой и органозоли с органической средой.
3. Твёрдые золи — системы с твёрдой
дисперсионной средой. Например, рубиновое
стекло — дисперсия золота в силикатном стекле.
Золи могут быть бесцветными или иметь окраску,
зависящую от концентрации и размера частиц
дисперсной фазы.
4.
Бездомные5.
6.
Некоторые характеристики золей в химии:занимают промежуточное положение между истинными
растворами и грубодисперсными системами
(суспензиями, эмульсиями);
диффундируют медленнее, чем неорганические соли;
обладают эффектом светорассеяния (эффект Тиндаля);
в противоположность гелям, в золях частицы дисперсной
фазы не связаны в пространственную структуру, а
свободно участвуют в броуновском движении.
Для золей характерно такое явление, как коагуляция, —
слипание коллоидных частиц с последующим
выпадением их в осадок. В результате этого процесса
коллоидный раствор превращается в суспензию или гель.
7.
Свойства золей:1. Большая удельная поверхность.
2. Адсорбция и плёнкообразование на
поверхностях раздела.
3. Агрегация как следствие взаимодействия частиц.
4. Частицы на поверхности обладают большей
энергией, чем частицы внутри фазы.
Золи занимают промежуточное положение между
истинными растворами и грубодисперсными
системами (суспензиями, эмульсиями). Они
диффундируют медленнее, чем неорганические
соли, и обладают эффектом светорассеяния (эффект
Тиндаля).
8.
Применение золей:— в химии,
— в фармацевтике,
— в военном деле.
Золи позволяют резко улучшить качественные и количественные
показатели химических реакций.
Наиболее известными каждому считаются золи, образованные в
фармацевтической промышленности (лекарственные препараты) и
пищевой: соки и нектары, мороженое, масла и растительно-сливочные
смеси, сливки и множество других подобных продуктов.
Также широкое применение золи получили в:
– резиновой;
– текстильной;
– кожевенной;
– мыловаренной;
– лакокрасочной и прочих отраслях.
Невозможно представить без коллоидных дисперсных систем
строительную отрасль и сельское хозяйство. Так, изучение почвенных
коллоидов позволяет корректировать почвенный состав, что отражается на
показателях плодородности культур, и бороться с
различными вредителями, уничтожающими урожай.
9.
ПОЛУЧЕНИЕ:Золи (коллоидные растворы) получают двумя основными методами: 1
Диспергирование. Измельчение, уменьшение размеров частиц дисперсной
фазы. Например, с помощью механического дробления или дробления
ультразвуком. 1
Конденсация. Объединение молекул и ионов в более крупные коллоидные
частицы. 1
Некоторые методы конденсации:
Физико-химическая конденсация. Вещество, из которого предполагается
получить золь, растворяют в соответствующем растворителе в присутствии
стабилизатора (или без него) и затем раствор смешивают с избытком другой
жидкости, в которой вещество нерастворимо. В результате образуется золь.
Так получают золи серы, канифоли. 2
Химическая конденсация. 2 Происходит в результате химических реакций
(восстановления, ионного обмена, гидролиза), сопровождающихся
образованием труднорастворимых в дисперсионной среде
соединений. 5 Например, золи гидроксида железа(III) и гидроксида
алюминия можно получить в результате полного гидролиза их солей. 1
10.
Некоторые примеры золей в химии:Краски, чернила.
Золь золота.
Золь серебра.
Мутная вода.
Крахмал.
Золь гидроксида железа (III). Для его получения к 20 мл
кипящей воды прибавляют 1–2 капли насыщенного раствора
FeCl3. Образуется золь вишнёво-красного цвета.
Золь парафина в воде. К 2 мл воды в пробирке добавляют
при взбалтывании 1–2 капли раствора парафина в этиловом
спирте концентрацией 1 мас.%.
Золи иодистого, бромистого и хлористого серебра. Их
получают, смешивая разбавленные растворы и беря одно
вещество в избытке.










 chemistry
chemistry








