Similar presentations:
Окислительно-восстановительные реакции
1. Тема урока: «Окислительно-восстановительные реакции»
Тема урока: «Окислительновосстановительные реакции»«
Кто-то теряет, а кто-то находит.»
2. Повторение изученного ранее
Что такое атом?Что такое ион?
Чем отличается ион от атома?
Какие типы реакций вам
знакомы?
Что такое степень окисления?
Как определять степень
окисления?
3.
Правила вычисления степени окисления(СО) элементов:
4. Задание № 1 Выполните работая в группе
Определите степени окисления атомовхимических элементов по формулам их
соединений:
H2S, O2, NH3, HNO3, Fe, K2Cr2O7
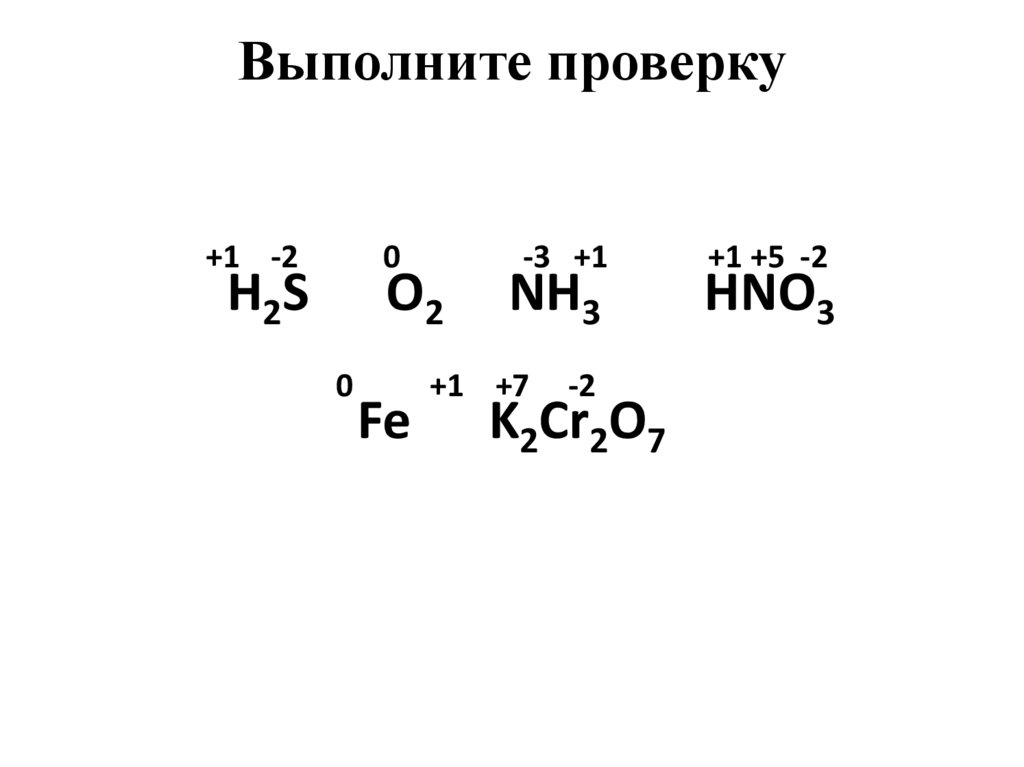
5. Выполните проверку
+1 -20
H2S
O2
0
Fe
-3 +1
NH3
+1 +7
-2
K2Cr2O7
+1 +5 -2
HNO3
6.
Расставьте степени окисления элементов в реакциях.Сравните, как ведут себя степени окисления в
процессе реакции.
+1
+1
-1
-2 +1
+1
-1
+1
-2
HCl + NaOH = NaCl + H2O
+1
-1
0
+2
-1
0
Окислительновосстановительная
2
реакция
2 HCl + Zn = ZnCl2 + H
Реакции, в которых происходит изменение степеней
окисления, называются
окислительно-восстановительными
7. Тема урока: «Окислительно-восстановительные реакции»
Тема урока: «Окислительновосстановительные реакции»«
Кто-то теряет, а кто-то находит.»
8. Цель урока:
отработать умение записывать процессы изменениястепеней окисления частиц с целью определения
коэффициентов, необходимых для уравнивания
окислительно – восстановительных реакций.
9. План
1. Повторение домашнего задания2. Актуализация знаний
3. Изучение нового материала
4. Закрепление
5. Рефлексия
6. Домашнее задание
10.
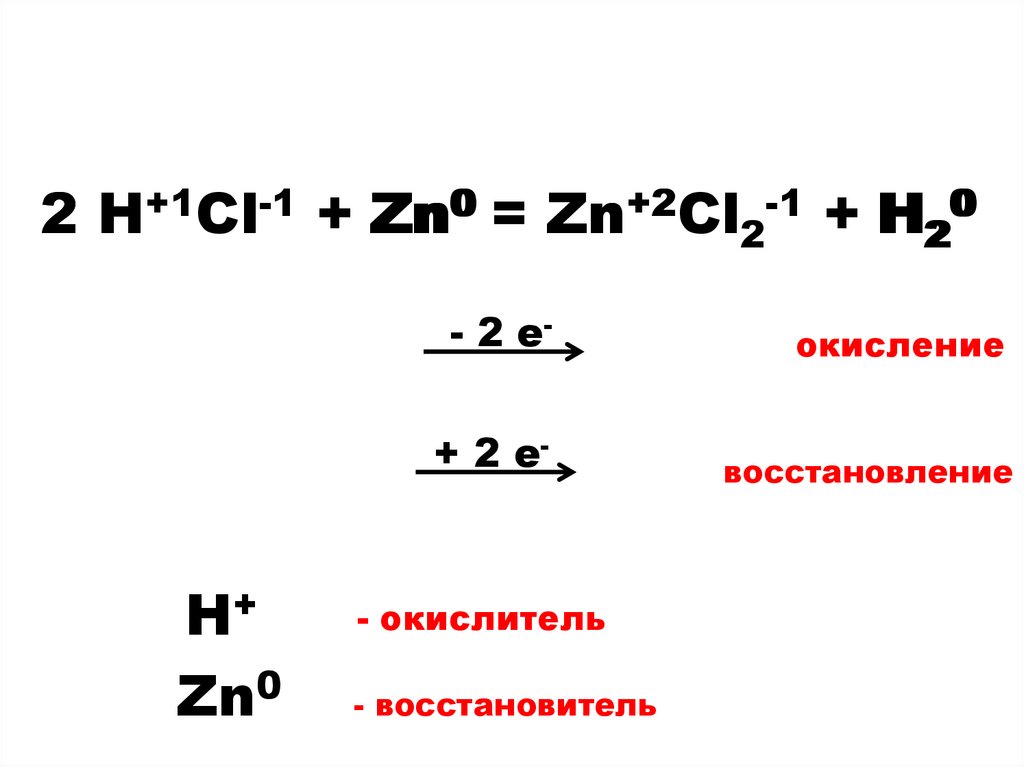
2 H++1Cl-1 + Zn0 = Zn+2Cl2-1 + H2200H+
Zn0
- 2 е-
окисление
+ 2 е-
восстановление
- окислитель
- восстановитель
11.
Окисление – процесс отдачи электронов.Восстановление – процесс присоединения
электронов.
Окислитель – элемент, принимающий
электроны.
Восстановитель – элемент, отдающий
электроны.
12.
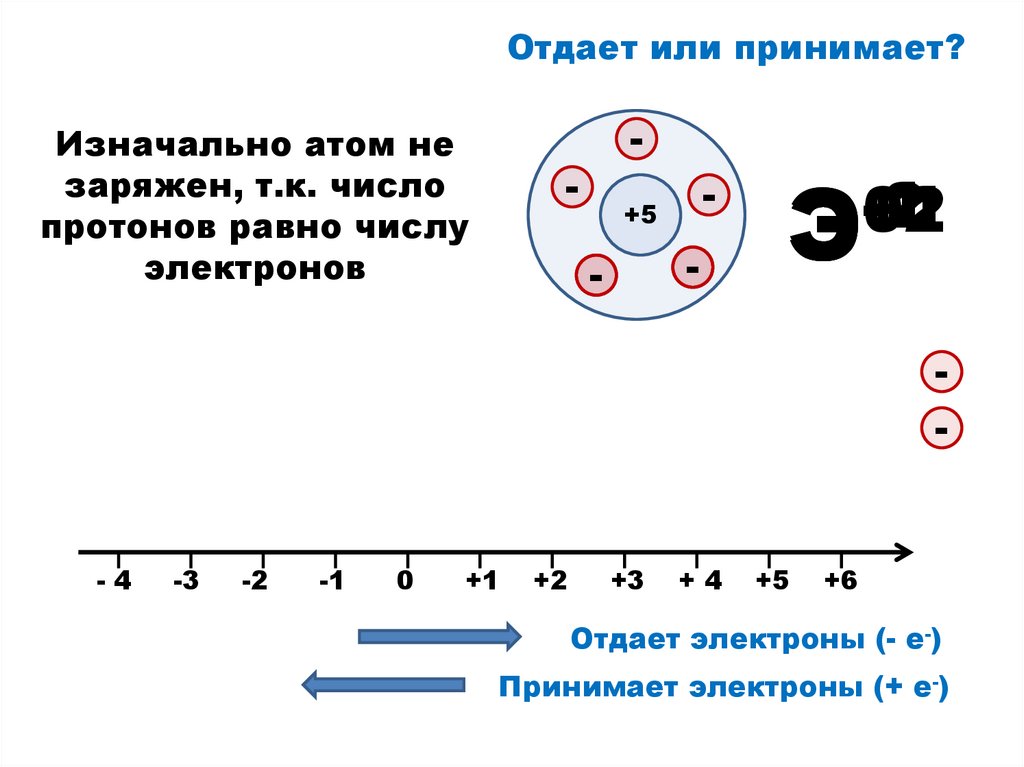
Отдает или принимает?Изначально атом не
заряжен, т.к. число
протонов равно числу
электронов
-
-
-
+5
-
-
-2
-1
+1
+2
0
Э
-
-4
-3
-2
-1
0
+1
+2
+3
+4
+5
+6
Отдает электроны (- е-)
Принимает электроны (+ е-)
13.
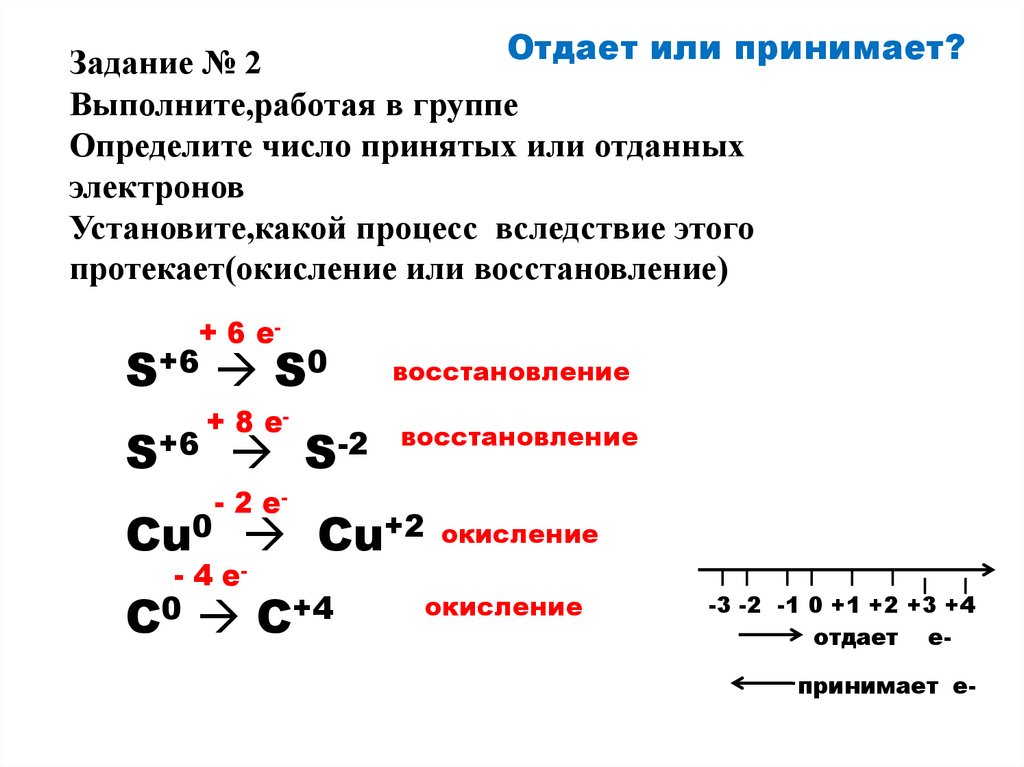
Отдает или принимает?Задание № 2
Выполните,работая в группе
Определите число принятых или отданных
электронов
Установите,какой процесс вследствие этого
протекает(окисление или восстановление)
+ 6 e-
S+6 S0
S+6
+ 8 e-
S-2
восстановление
восстановление
- 2 e-
Cu0 Cu+2 окисление
- 4 e-
C0 C+4
окисление
-3 -2 -1 0 +1 +2 +3 +4
отдает е-
принимает е-
14.
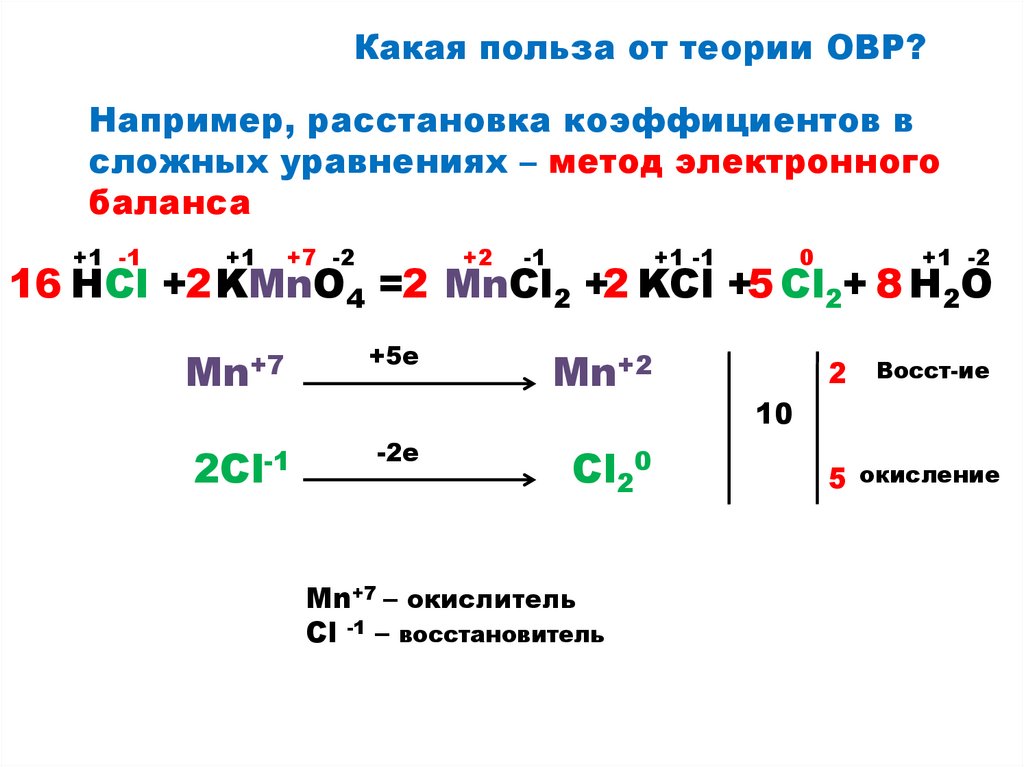
Какая польза от теории ОВР?Например, расстановка коэффициентов в
сложных уравнениях – метод электронного
баланса
+1 -1
+1
+7 -2
+2
-1
+1 -1
0
+1 -2
16 HCl +2 KMnO4 =2 MnCl2 +2 KCl +5 Cl2+ 8 H2O
Mn+7
+5е
2Cl-1
-2е
Mn+2
Cl20
Mn+7 – окислитель
Сl -1 – восстановитель
2
Восст-ие
10
5 окисление
15.
План составления уравнений ОВР иэлектронного баланса к ним
1. Записать схему реакции.
2. Определить, атомы каких элементов
изменяют степень окисления.
3. Составить электронные уравнения
процессов окисления и восстановления.
4. Подобрать общее делимое для отданных
и принятых электронов и коэффициенты
для электронных уравнений.
5. Перенести эти коэффициенты в
уравнение ОВР и подобрать коэффициенты
перед формулами других веществ.
16.
ФизкультминуткаСтих
Движения
Окислитель электроны
принимает на орбиту
На вытянутых руках
сжимаем и разжимаем
пальцы в кулачки
Но при этом электроны
атом тоже отдает
Потянулись влево и вправо
Это наш восстановитель
Поднимаем руку вверх и
раскрываем ладонь
Он реакцию дает
Хлопаем в ладоши
17.
Вспомним правила техникибезопасности
1)При работе с кислотами необходимо
помнить, что эти вещества опасны
2)Оборудование должно быть чистым
3)В пробирку не стоит помещать большое
количество вещества
4)Этикетку под ладонь
5)Крышку от открытого сосуда
необходимо переворачивать
6)Пробирку держать тремя пальцами
18.
Опыт №1Карбонат кальция+соляная кислота=
CaCO₃ + 2HCl(разб.) → CaCl₂ + CO₂↑ + H₂O
Опыт №2
Нитрат серебра + Медь=
AgNO3 + Cu → Cu(NO3)2 + Ag↓
Задание найти окислительновосстановительную реакцию и уравнять ее
методом электронного баланса
19.
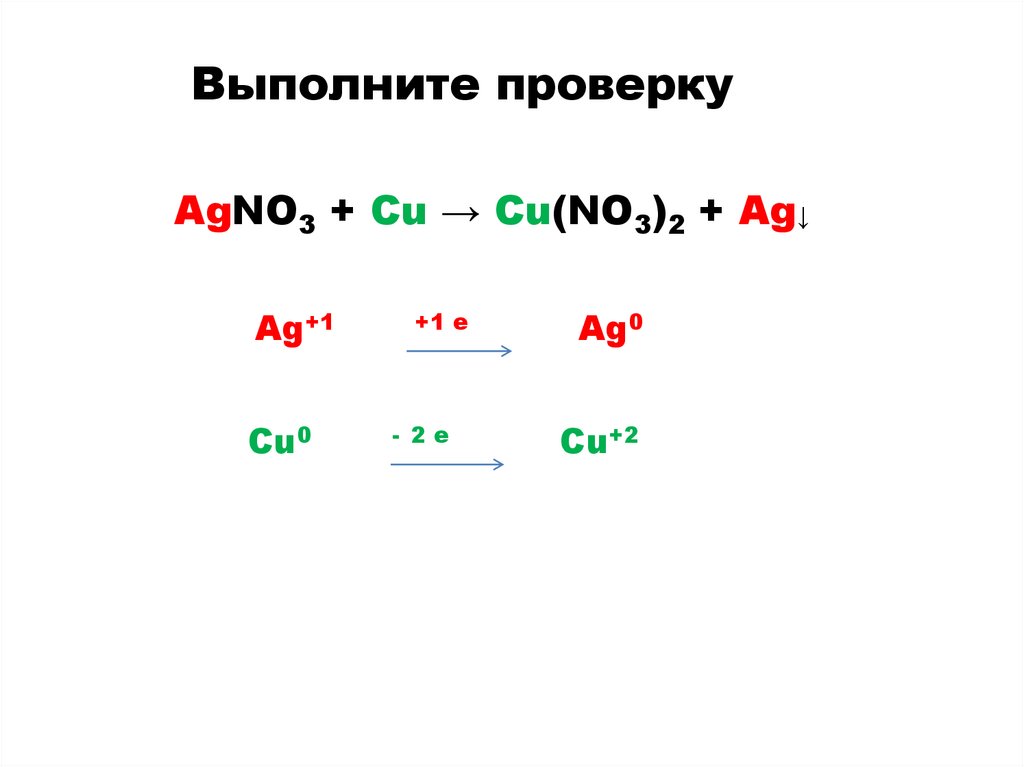
Выполните проверкуAgNO3 + Cu → Cu(NO3)2 + Ag↓
Ag+1
Cu0
+1 e
- 2e
Ag0
Cu+2
20.
ОВР в быту21.
Цель работы:Выяснить, как окислительновосстановительные реакции применяются в
быту.
22.
Горение газа на кухнеГаз метан горит бесцветным пламенем с образованием
воды и углекислого газа
СН4+2О2=СО2+2Н2О
23.
Отбеливание тканиПри обработке персолью отбеливание
происходит за счет окисления
загрязнений
2H2O2=2H2O+O2.
Для того чтобы образующийся
кислород не улетучивался
из емкости, лучше
держать ее
закрытой.
24.
Коррозия металлаПри взаимодействии железа и кислорода
образуется ржавчина.
4Fe+ 2O2= 2Fe2O3
25.
Вывод:Мы часто сталкиваемся с окислительновосстановительными реакциями в быту:
• при горении газа;
• при коррозии металлов;
• при отбеливании ткани
• при промывания ран.
26. Задание №3 Выполните, работая в группе 1. Из приведенных схем уравнений реакций выпишите те, которые можно отнести к ОВР 2.
найдите в реакциях ОВР восстановитель иукажите его степень окисления
• СаСО3
=>
СаО + СО2
• KMnO4 > K2 MnО4 + MnО2 + О2
• CuS + О2 =>
СuО + SО2
27. Выполните проверку
• KMnO4 > K2 MnО4 + MnО2 + О2О-2 Восстановитель
• CuS + О2 => СuО + SО2
S-2 Восстановитель
28.
29.
30. Домашнее задание:
Параграф 24, вопросы письменно 1,3
Подготовить сообщение на тему ОВР
в природе
























 chemistry
chemistry








