Similar presentations:
Основные положения молекулярно - кинетической теории и их опытные подтверждения
1. 10.09.2024
Основные положения молекулярнокинетической теории и их опытныеподтверждения. Масса и размер атомов и
молекул . Модели твёрдого, жидкого и
газообразного
состояний вещества
2.
Тема: «Основные положения молекулярнокинетической теории строения вещества»Молекулярная физика – раздел физики,
изучающий природу тепловых явлений на
основании внутреннего строения вещества.
Запишите Еще задолго до нашей эры, в
период
расцвета
древних
культур, возникло учение о
мельчайших
частицах,
из
которых построено любое
вещество.
Одна из древнеиндийских философских школ учила,
что вечные части вселенной состоят из четырех
элементов: воды, земли, огня и воздуха. Частички этих
элементов вечны и несотворимы, они непротяжённы, и
в то же время их разнородная природа составляет
причину протяжённости возникающих соединений этих
3. СОЗДАТЕЛИ АТОМНОЙ ТЕОРИИ
ДжонДальтон
Дмитрий
Менделеев
Амедео
Авогадро
Эрнест
Резерфорд
Древнегреческие философы Анаксагор и Демокрит (в IV веке до нашей эры)
считали, что любое вещество состоит из мельчайших неделимых частиц.
4. Из истории…
• Еще в Древней Греции, около 2,5 тысяч лет назад, былавыдвинута гипотеза о том, что вещество состоит из
мельчайших частичек – атомов и молекул.
• Основоположником идеи дискретного строения вещества
считается древнегреческий философ Демокрит,
живший около 470 года до новой эры. Демокрит считал,
что все тела состоят из бесчисленного количества
сверхмалых, невидимых глазу, неделимых частиц. "Они
бесконечно разнообразны, имеют впадины и выпуклости,
которыми сцепляются, образуя все материальные тела, а
в природе существуют только атомы и пустота».
В научную
теорию
этана
гипотеза превратилась только
Изображение
атомов
XVIII
– XIX веках.
поверхности кремния,
• Если
бы мы смогли
рассмотреть окружающие нас тела
полученное
с помощью
через
микроскоп, то увидели бы отдельные атомы и
туннельного микроскопа.
молекулы
5.
Этим вращательным движением Ломоносов объяснил тепловыеявления. Он утверждал, что «должна существовать наибольшая
степень холода, состоящая в полном покое частичек, в полном
отсутствии вращательного движения их», т. е. должен существовать
абсолютный нуль температуры. Сохранились собственноручные
рисунки Ломоносова, на которых молекулы изображены в виде
зубчатых колес.
6.
Микро- и макропараметрыМакроскопические тела (от греч. «макрос» –
большой) - это все тела, которые нас окружают:
дома, машины, вода в стакане, вода в океане и
т.д. При макроскопическом подходе к изучению
тел нас интересуют сами тела: их размеры,
объёмы, массы, энергии и т.д.
При микроскопическом подходе нас тоже
интересуют размеры, объём, масса, энергия и т.
д. Однако уже не самих тел, а тех частиц, из
которых они состоят: молекул, ионов и атомов.
МКТ объясняет явления и свойства тел с
точки
зрения
их
микроскопического
строения.
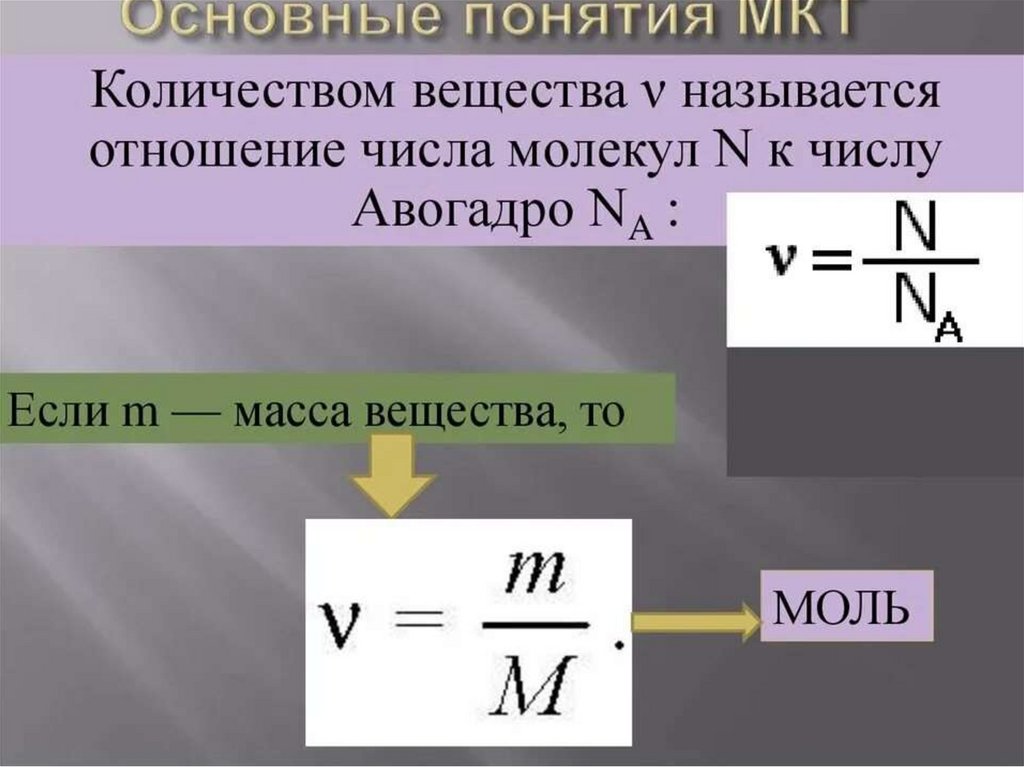
7.
В основе МКТ лежат три утверждения:1. Все вещества состоят из молекул и атомов. Молекула –
наименьшая электронейтральная частица вещества,
сохраняющая его свойства.
2. Молекулы и атомы всех веществ находятся в
непрерывном хаотическом движении, называемом
тепловым. Интенсивность этого движения возрастает
с повышением температуры.
3. Молекулы (атомы) взаимодействуют между собой.
Между ними действуют силы притяжения и
отталкивания.
Запишите
8. ПЕРВОЕ ПОЛОЖЕНИЕ
1. Все вещества – жидкие, твердые игазообразные – образованы из мельчайших
частиц – молекул, атомов, ионов.
Молекулы и атомы представляют собой
электрически нейтральные частицы. При
определенных условиях молекулы и атомы
могут приобретать дополнительный
электрический заряд и превращаться в
положительные или отрицательные ионы.
9.
10. ТРЕТЬЕ ПОЛОЖЕНИЕ
Частицы взаимодействуютдруг с другом силами,
имеющими электрическую
природу. Гравитационное
взаимодействие между
частицами пренебрежимо
мало
11.
12. Атомы
• Атомы очень малы.Их невозможно разглядеть
не только простым глазом, но и с
помощью даже самого мощного
оптического микроскопа.
• В 1951 году Эрвин Мюллер
изобрёл ионный микроскоп,
позволивший в деталях разглядеть
атомную структуру металла.
• Атомы различных химических
элементов отличаются друг от
друга.
Атом кислорода
Атом водорода
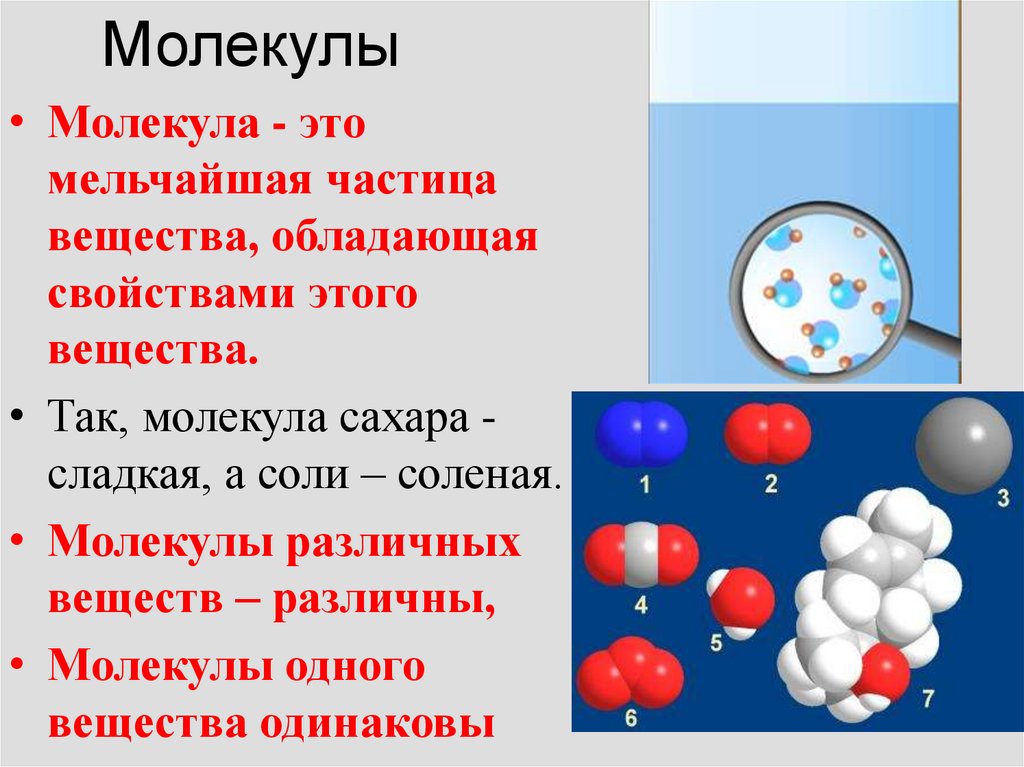
13. Молекулы
• Молекула - этомельчайшая частица
вещества, обладающая
свойствами этого
вещества.
• Так, молекула сахара сладкая, а соли – соленая.
• Молекулы различных
веществ – различны,
• Молекулы одного
вещества одинаковы
14. Взаимодействие частиц вещества
• Частицы веществ способны притягиваться друг к другу.Однако это притяжение возникает лишь тогда, когда поверхности
тел очень гладкие (для этого и понадобилась зачистка лезвием) и,
кроме того, плотно прижаты друг к другу.
• Частицы веществ способны отталкиваться друг от друга. Это
подтверждается тем, что жидкие, а особенно твердые тела очень
трудно сжать.
• Притяжение или отталкивание частиц веществ возникает лишь в
том случае, если они находятся в непосредственной близости.
• На расстояниях, чуть больших размеров самих частиц, они
притягиваются.
• На расстояниях, меньших размеров частиц, они
отталкиваются.
• Если же поверхности тел удалены на расстояние, заметно
большее, чем размер частиц, то взаимодействие между ними не
проявляется никак.
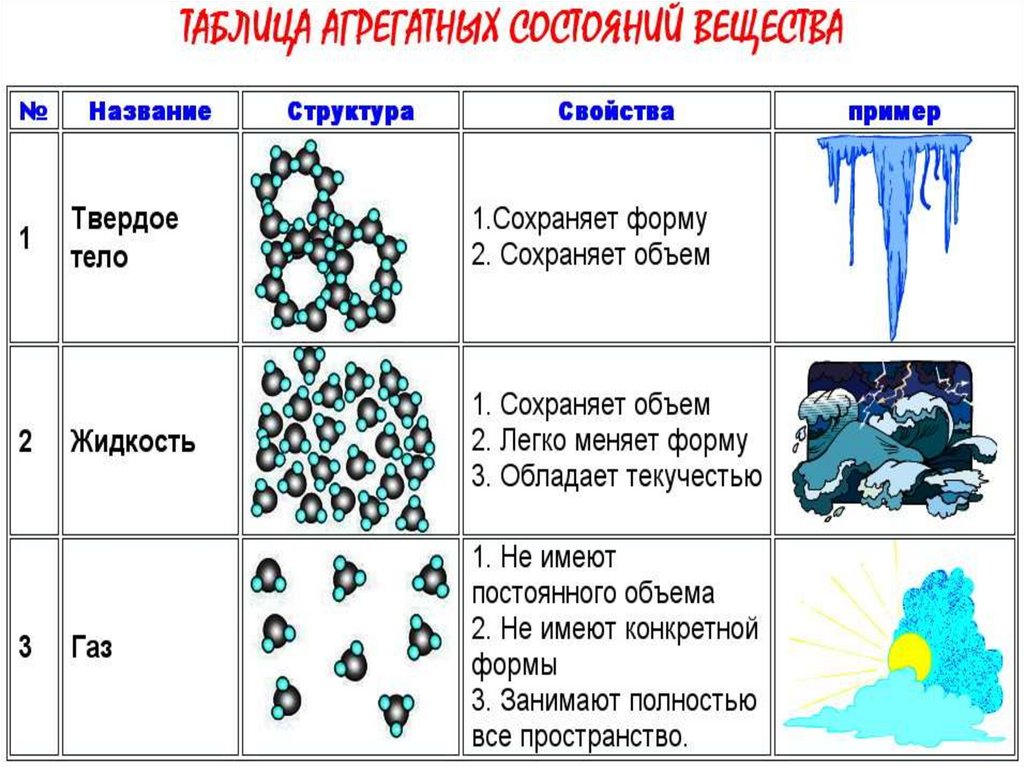
15. Модели строения газов, жидкостей и твердых
Молекулыодногостроения
и того же вещества
во всех
Модели
газов,
агрегатных состояниях одинаковы!
жидкостей и твердых
В жидкостях молекулы имеют
В твердых телах
значительно большую свободу для
молекулы совершают
теплового движения. Они не
беспорядочные
привязаны к определенным
колебания около
фиксированных центровцентрам и могут перемещаться по
(положений равновесия). всему объему жидкости. Этим
объясняется текучесть жидкостей.
В газах расстояния между
молекулами обычно
значительно больше их
размеров, каждая молекула
движется вдоль прямой
линии до очередного
столкновения с другой
молекулой или со стенкой
сосуда.
16.
17. Модели твердого,жидкого и газообразного состояний вещества
• Вещество в газообразном состоянии (газ):• Не имеет определённой формы и объёма, заполняет весь предоставленный
объём.
• Средние расстояния между молекулами намного превышают размеры самих
молекул.
• Молекулы хаотически движутся и слабо взаимодействуют друг с другом.
• Вещество в жидком состоянии (жидкость):
• Имеет собственный объём, принимает форму сосуда.
• Молекулы расположены вплотную друг к другу, но в этом расположении нет
определённого порядка.
• При хаотическом движении молекулы часто меняются местами друг с другом,
но ограничены в движении.
• Вещество в твёрдом состоянии (твёрдое тело):
• Имеет собственную форму и объём.
• В кристаллах молекулы или атомы расположены упорядоченно, вплотную
друг к другу.
• Молекулы или атомы колеблются около определённой точки и не могут
18.
19.
20. ДОМАШНЕЕ ЗАДАНИЕ
• Изучить материал конспекта.• Выучить определения и основные
положения МКТ.

















 physics
physics








