Similar presentations:
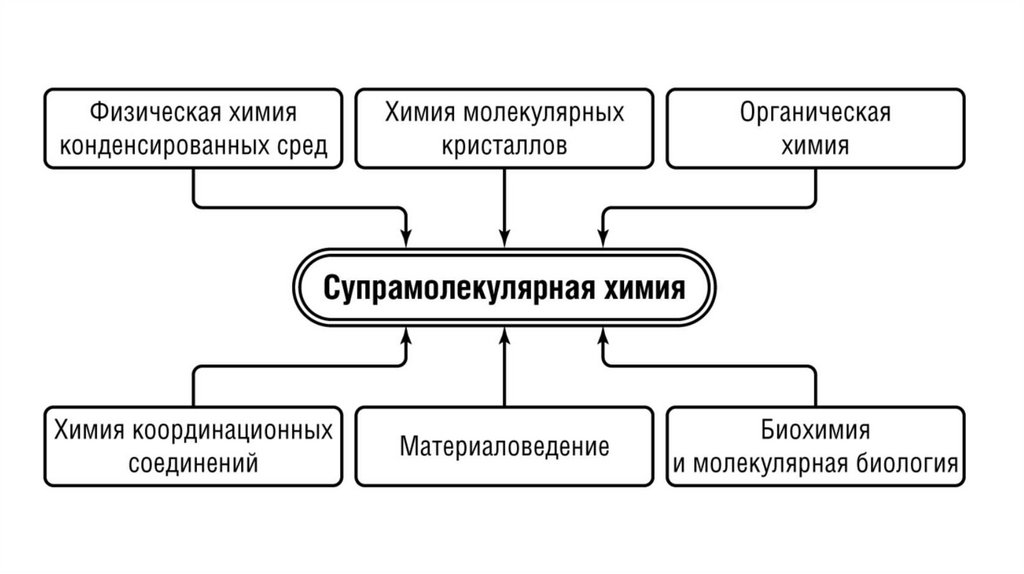
Супрамолекулярная химия. Основные понятия и термины
1.
СУПРАМОЛЕКУЛЯРНАЯХИМИЯ
ОСНОВНЫЕ ПОНЯТИЯ И ТЕРМИНЫ
Типы взаимодействий
Условия образования супрамолекулы
2.
Литература3.
4.
Супрамолекулярная химия:• Разработка высокоэффективных селективных реагентов и
катализаторов;
• Создание сенсоров различного типа;
• Синтез новых лекарственных препаратов;
• получение новых миниатюрных приборов для записи и
хранении информации
5.
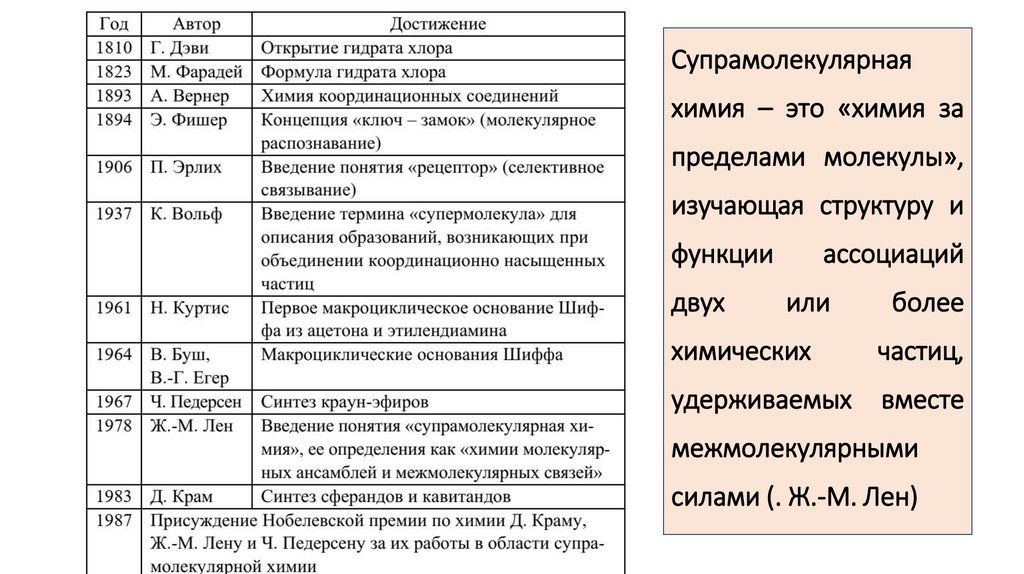
Супрамолекулярнаяхимия – это «химия за
пределами молекулы»,
изучающая структуру и
функции
двух
ассоциаций
или
более
химических
частиц,
удерживаемых
вместе
межмолекулярными
силами (. Ж.-М. Лен)
6.
Современное определениеСупрамолекулярная (надмолекулярная) химия (Supramolecular
chemistry) — междисциплинарная область науки, включающая
химические, физические и биологические аспекты рассмотрения более
сложных, чем молекулы, химических систем, связанных в единое целое
посредством
межмолекулярных
(нековалентных)
взаимодействий.
(″химия за пределами молекулы″)
• объекты классической химии — молекулы
• объекты супрамолекулярной химии —
супермолекулы и их ансамбли
6
7.
• «Супермолекулы представляют собой по отношению к молекулам тоже, что молекулы по отношению к атомам, причем роль ковалентных
связей в супермолекулах играют межмолекулярные взаимодействия»
8.
Согласно Ж.-М. Лену, супрамолекулярную химию можно разделить на две широкие,частично налагающиеся друг на друга области:
– химию супермолекул – четко обозначенных олигомолекулярных частиц, возникающих в
результате межмолекулярной ассоциации нескольких компонентов – рецептора и его
субстрата (хозяина и гостя – по другой терминологии) и строящихся по принципу
молекулярного распознавания;
–
химию
молекулярных
ансамблей
–
полимолекулярных
систем,
которые образуются в результате спонтанной ассоциации неопределенного числа
компонентов
с
переходом
в
специфическую
фазу,
имеющую
более
или
менее
четко
обозначенную
микроскопическую
организацию
и
зависимые
от
ее
природы
характеристики.
• Основные функции супермолекул: молекулярное распознавание,
превращение (катализ) и перенос.
9.
Образование супрамолекулярных ансамблей происходит за счётнековалентных, слабых взаимодействий.
Однако эти взаимодействия являются высокоспецифичными, в основе их
лежат процессы распознавания.
Другими характерными процессами в супрамолекулярной химии являются
изменение характеристик системы при специфичном связывании с другими
молекулами (реагирование), возможность специфичного переноса других
молекул через мембраны (транспорт), процессы протекания реакций между
молекулами в ансамбле (катализ) – процессы аналогичные тем, что мы
находим в биологических объектах.
10.
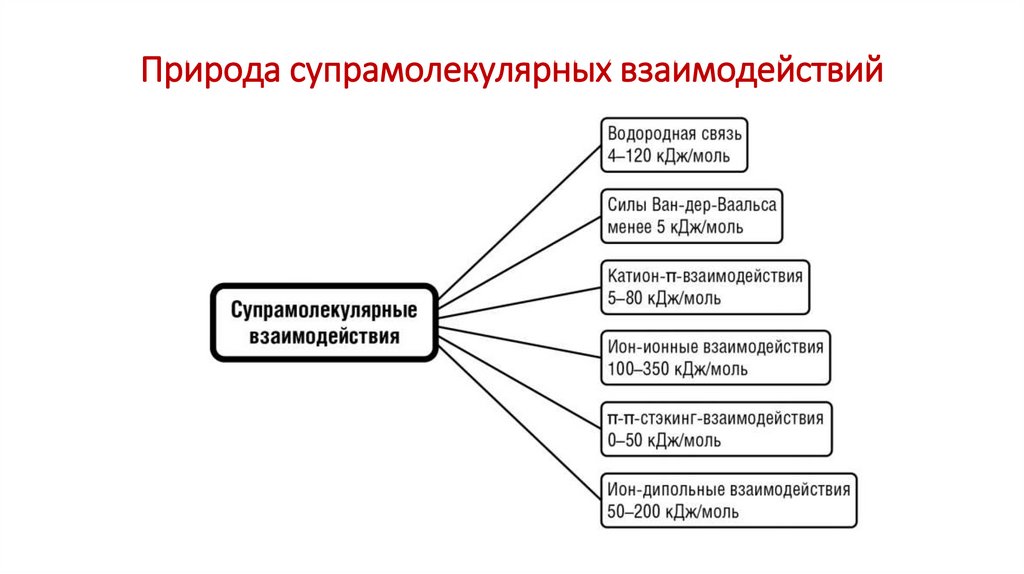
Природа супрамолекулярных взаимодействий11.
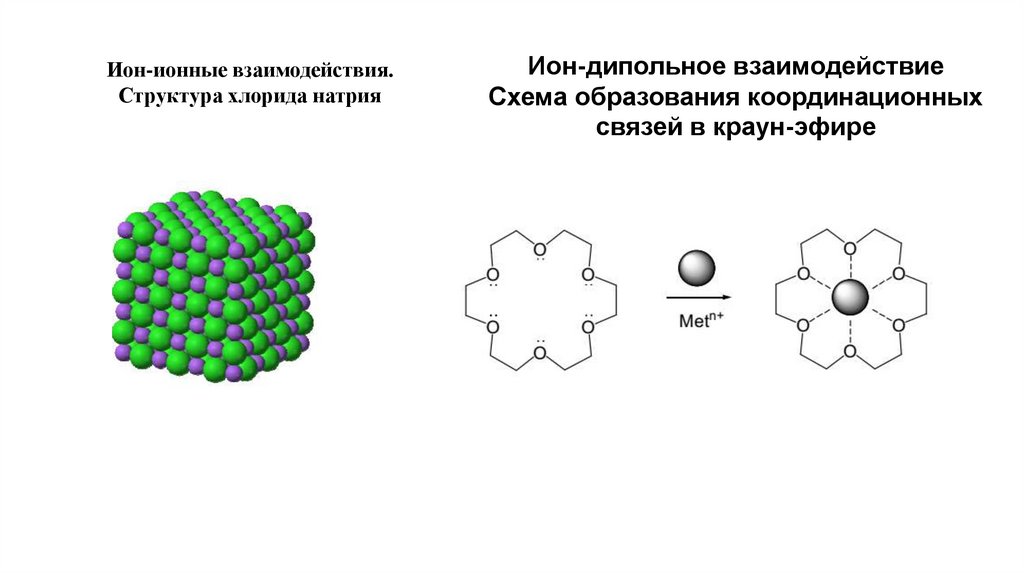
Ион-ионные взаимодействия.Структура хлорида натрия
Ион-дипольное взаимодействие
Схема образования координационных
связей в краун-эфире
12.
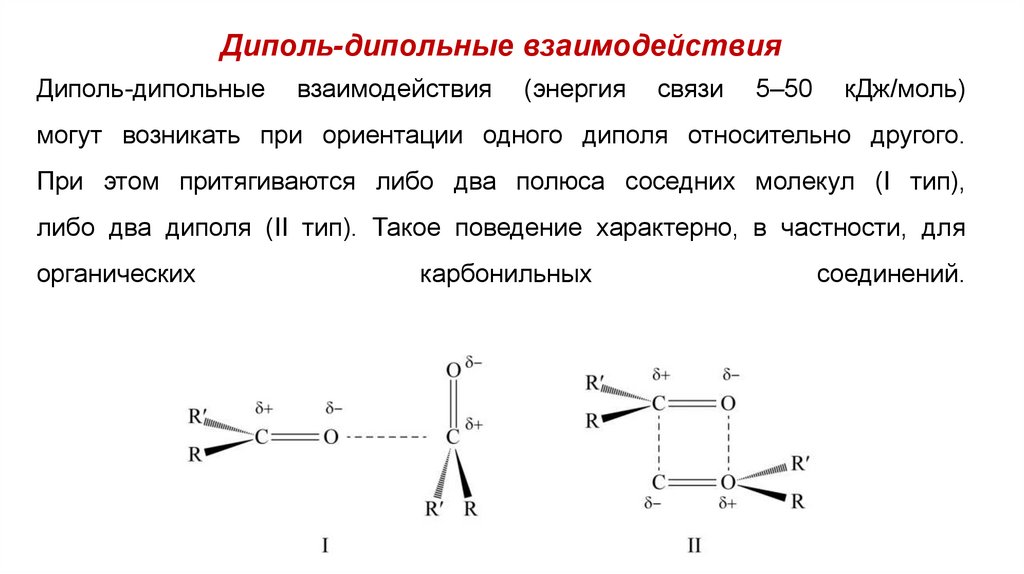
Диполь-дипольные взаимодействияДиполь-дипольные
взаимодействия
(энергия
связи
5–50
кДж/моль)
могут возникать при ориентации одного диполя относительно другого.
При этом притягиваются либо два полюса соседних молекул (I тип),
либо два диполя (II тип). Такое поведение характерно, в частности, для
органических
карбонильных
соединений.
13.
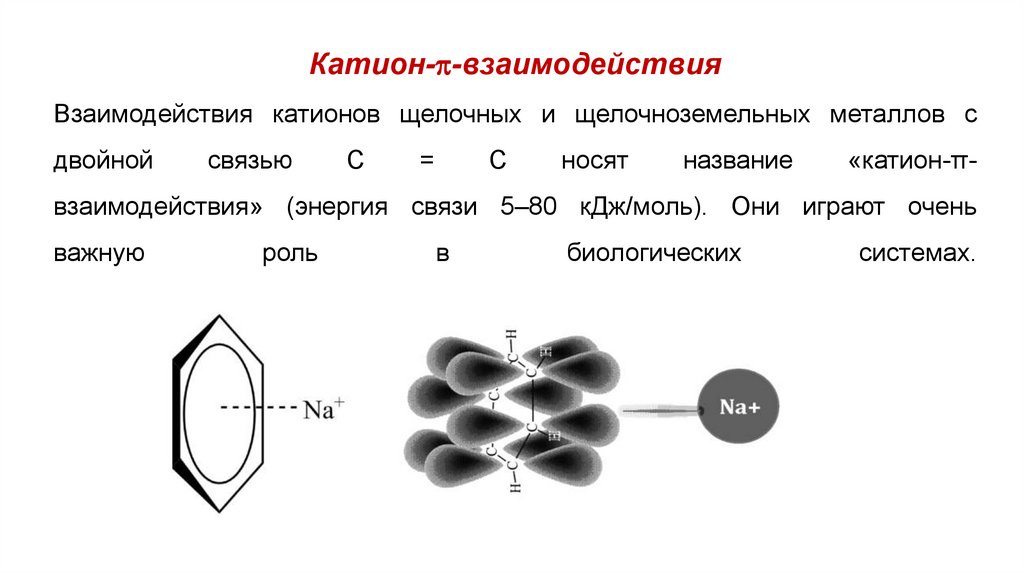
Катион- -взаимодействияВзаимодействия катионов щелочных и щелочноземельных металлов с
двойной
связью
С
С
=
носят
название
«катион-π-
взаимодействия» (энергия связи 5–80 кДж/моль). Они играют очень
важную
роль
в
биологических
системах.
14.
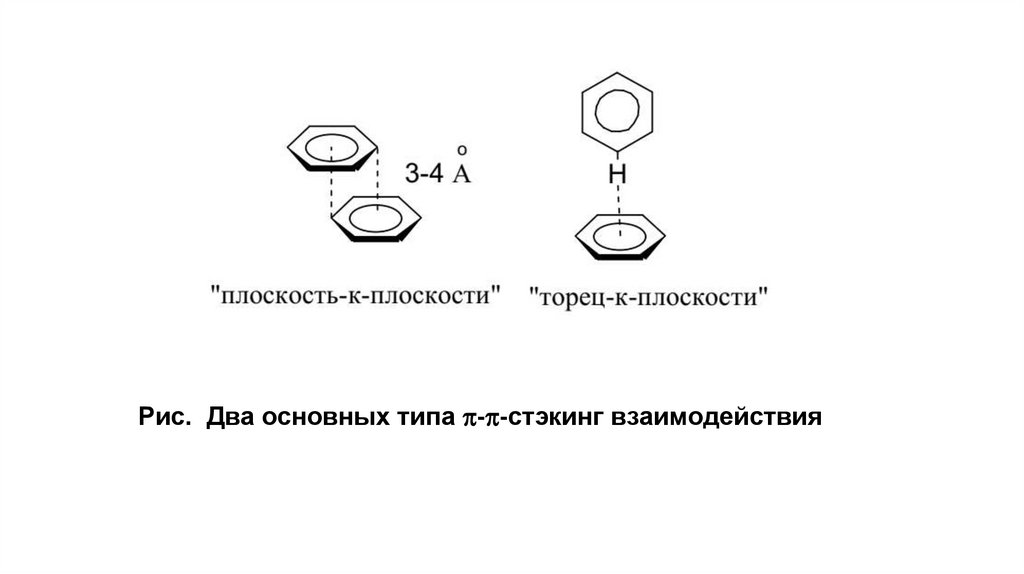
Рис. Два основных типа - -стэкинг взаимодействия15.
Водородная связь (4-120 кДж/моль) относится к числуважнейших,
структурообразующих связей, особенно в супрамолекулярной
химии.
В ряде случаев между частицами может существовать не одна
водородная связь, а несколько, причем это может быть
справдливым и для одного атома, образующего две водородные
связи (атом килорода в молекуле воды в структуре льда).
Водородная связь в значительной мере определяет
структурируемость веществ в конденсированном состоянии.
Обычны водородные связи в молекулах, содержащих связи О-Н,
N-H или F-H.
16.
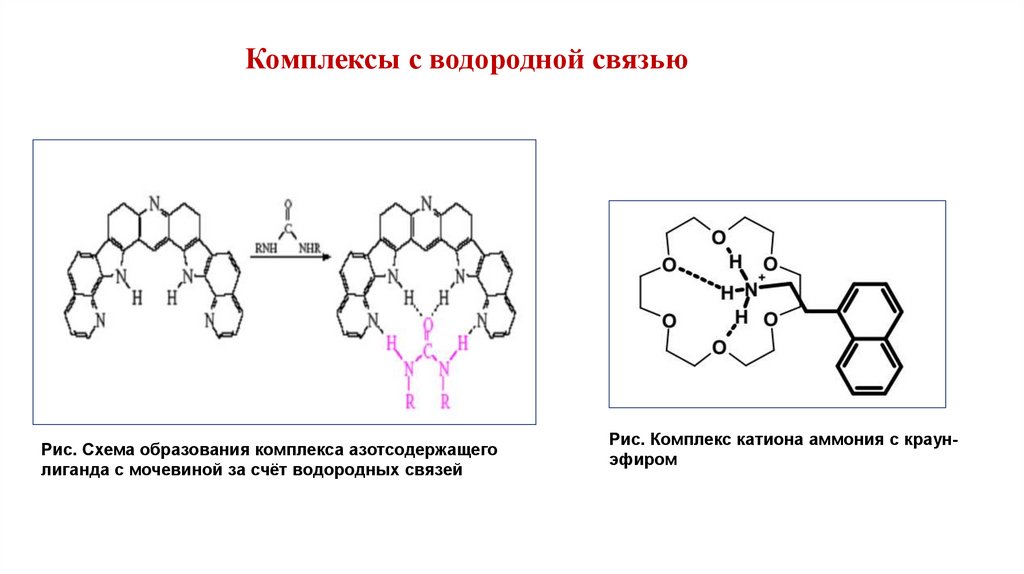
Комплексы с водородной связьюРис. Схема образования комплекса азотсодержащего
лиганда с мочевиной за счёт водородных связей
Рис. Комплекс катиона аммония с краунэфиром
17.
Под силами Ван-дер-Ваальса (< 5 кДж/моль) в иностраннойлитературе понимают слабое электростатическое
взаимодействие, возникающее благодаря поляризации
электронных облаков из-за соседства близлежащих ядер –
взаимодействия, называемые дисперсионными в традиционной
российской научной химической литературе.
Эти силы характеризуются отсутствием направленности. Они
компенсируются (при сближении) силами отталкивания
(обменно-отталкивающие силы) и они не направлены.
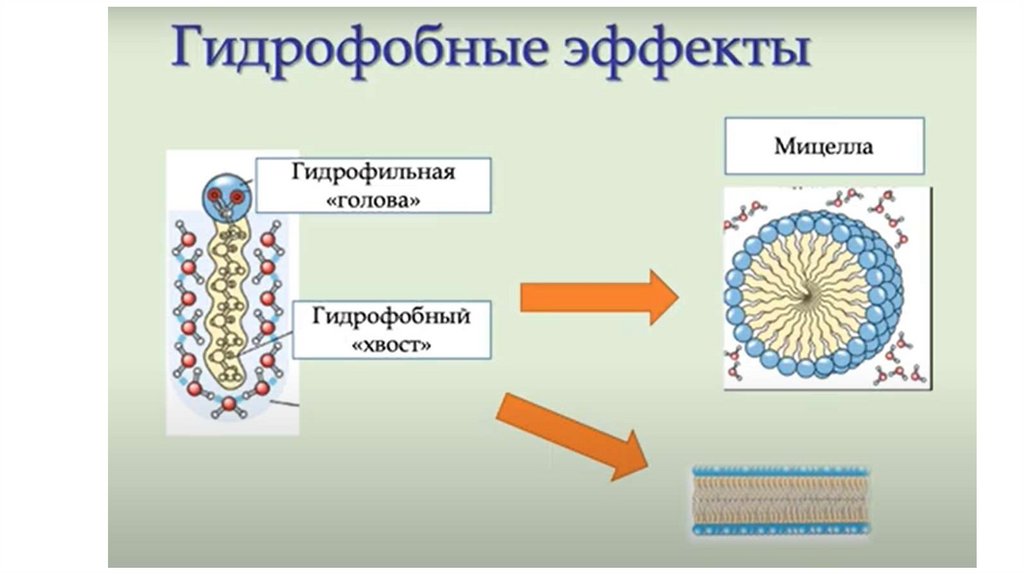
18.
Гидрофобные взаимодействия – играют определяющуюроль при получении моно- и полислоёв из органических
молекул
Образование плёнок происходит за счёт выталкивания из воды
слабосольватированных
гидрофобных молекул.
Вещества, имеющие в структуре как полярные, так и неполярные группы,
называются амфифильными. К этой группе принадлежат, например, жиры,
фосфолипиды и желчные кислоты
Вследствие гидрофобных взаимодействий амфифилы при контакте с водой
склонны образовывать структуры, у которых площадь контакта неполярной части
молекул с водой минимальна. На поверхности воды такие вещества обычно
образуют монослойные плёнки, у которых полярные группы ориентированы в
воду.
В воде амфифилы образуют протяжённые бислойные мембраны или мицеллы, у
которых полярные группы ориентированы в воду. По этому принципу построено
большинство биологических мембран. Полые мембранные пузырьки носят
название везикул. В клетках и крови такие структуры играют ключевую роль при
выполнении транспортных функций
19.
20.
Рис. структуры белкаПервичная структура белка (рис. а)
представляет собой последовательность
аминокислот.
Эта последовательность определяет
строение белка.
Вторичная структура белка (рис. б)
образуется за счёт водородных связей между
отдельными фрагментами полипептидной
цепи.
С помощью рентгеноструктурного анализа
было установлено, что стабилизация
вторичной структуры белка происходит за
счёт образования спирали, содержащей 4
аминокислоты на один виток, при участии - стэкинг- и гидрофобных взаимодействий.
Такая структура может быть отнесена к
супрамолекулярной структуре белка.
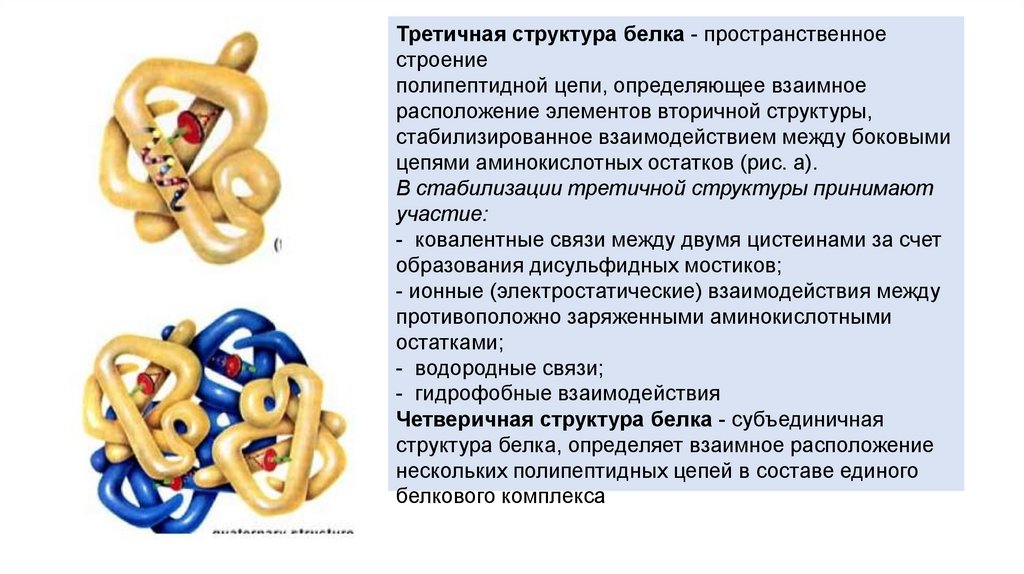
21.
Третичная структура белка - пространственноестроение
полипептидной цепи, определяющее взаимное
расположение элементов вторичной структуры,
стабилизированное взаимодействием между боковыми
цепями аминокислотных остатков (рис. а).
В стабилизации третичной структуры принимают
участие:
- ковалентные связи между двумя цистеинами за счет
образования дисульфидных мостиков;
- ионные (электростатические) взаимодействия между
противоположно заряженными аминокислотными
остатками;
- водородные связи;
- гидрофобные взаимодействия
Четверичная структура белка - субъединичная
структура белка, определяет взаимное расположение
нескольких полипептидных цепей в составе единого
белкового комплекса
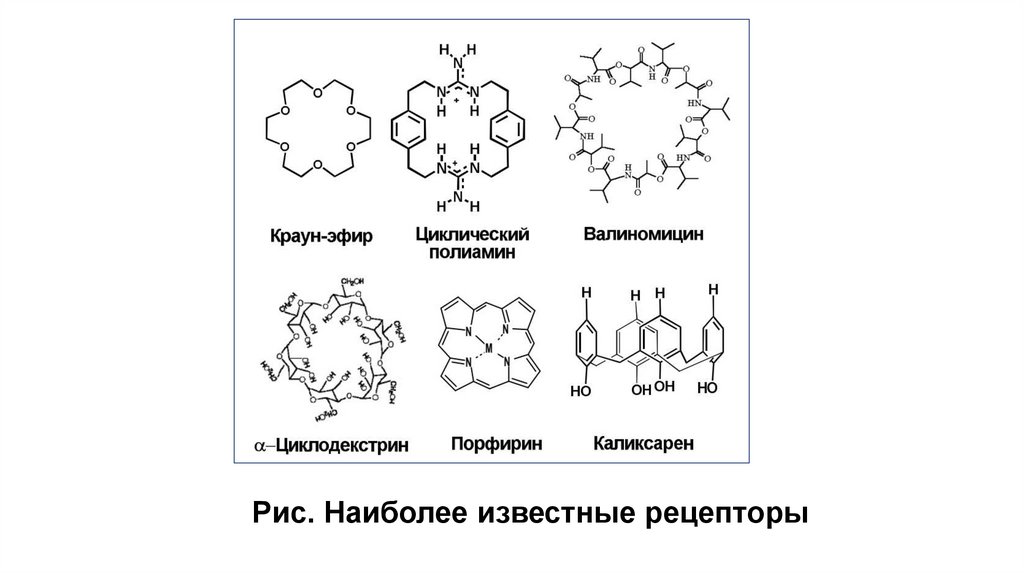
22.
Рис. Наиболее известные рецепторы23.
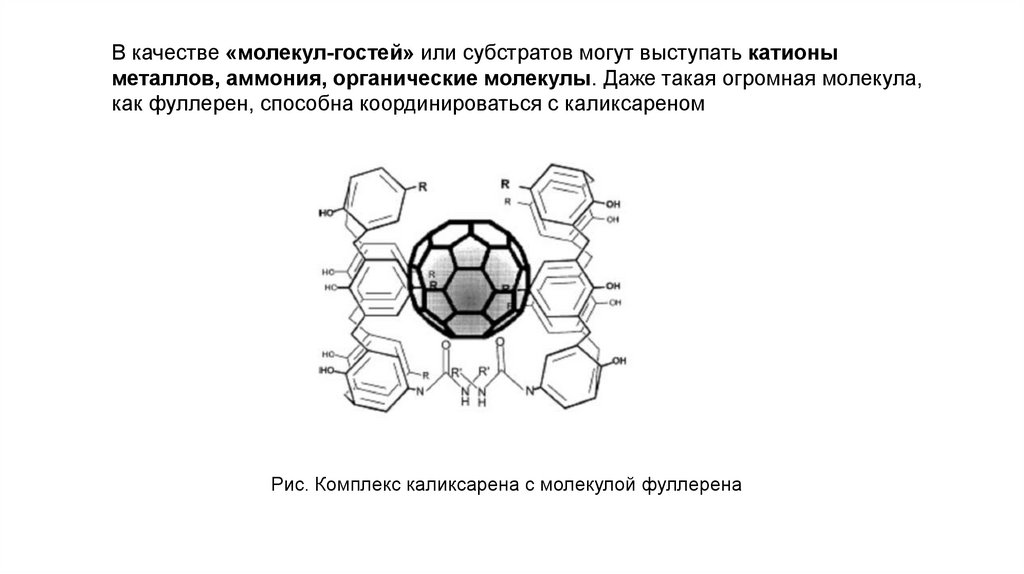
В качестве «молекул-гостей» или субстратов могут выступать катионыметаллов, аммония, органические молекулы. Даже такая огромная молекула,
как фуллерен, способна координироваться с каликсареном
Рис. Комплекс каликсарена с молекулой фуллерена
24.
• Может происходить ассоциация и с полимернымимакромолекулами, если они содержат подходящие
функциональные группы, например аминогруппы,
карбоксильные, карбонильные группы
• Известно и очень активно изучается образование
комплексов между органическими молекулами (субстраты) и
белками (рецепторы). Это процесс называется
интеркаляцией.
25.
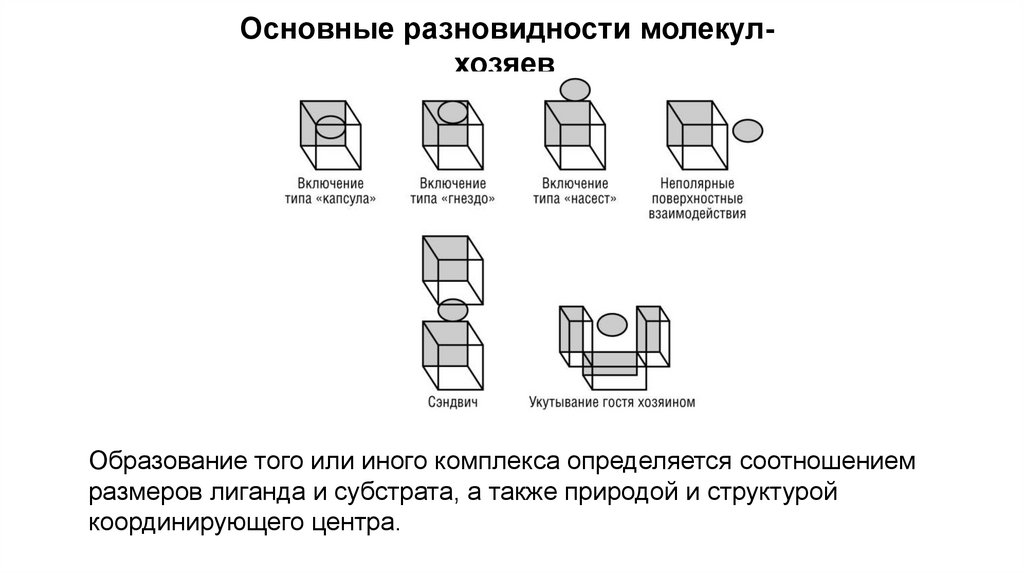
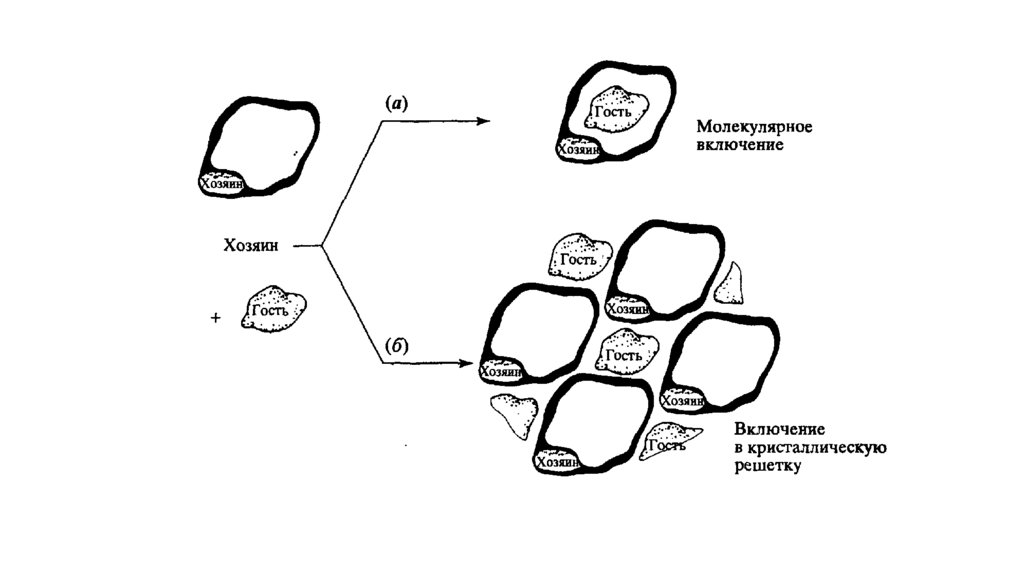
Основные разновидности молекулхозяевОбразование того или иного комплекса определяется соотношением
размеров лиганда и субстрата, а также природой и структурой
координирующего центра.
26.
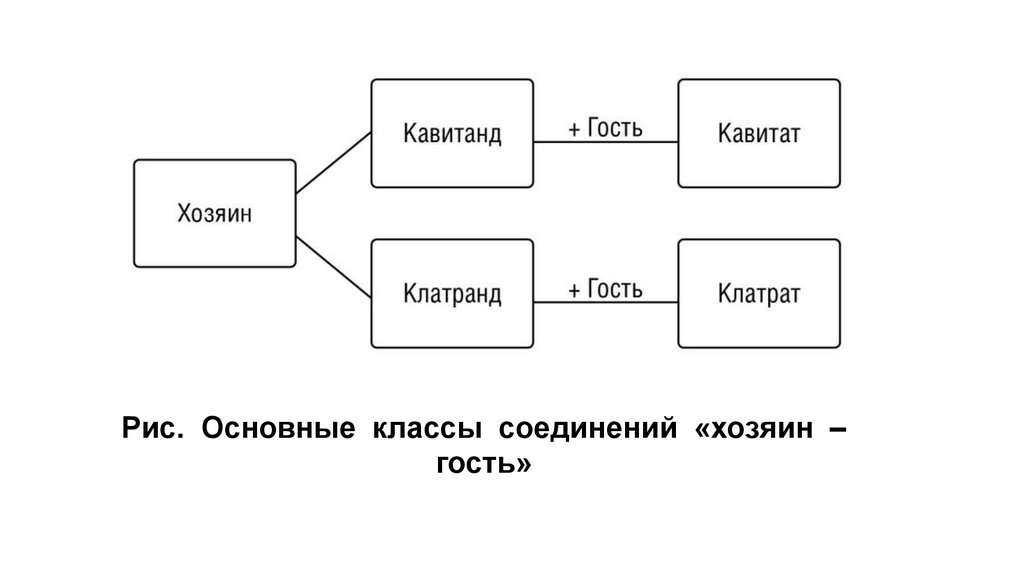
Рис. Основные классы соединений «хозяин –гость»
27.
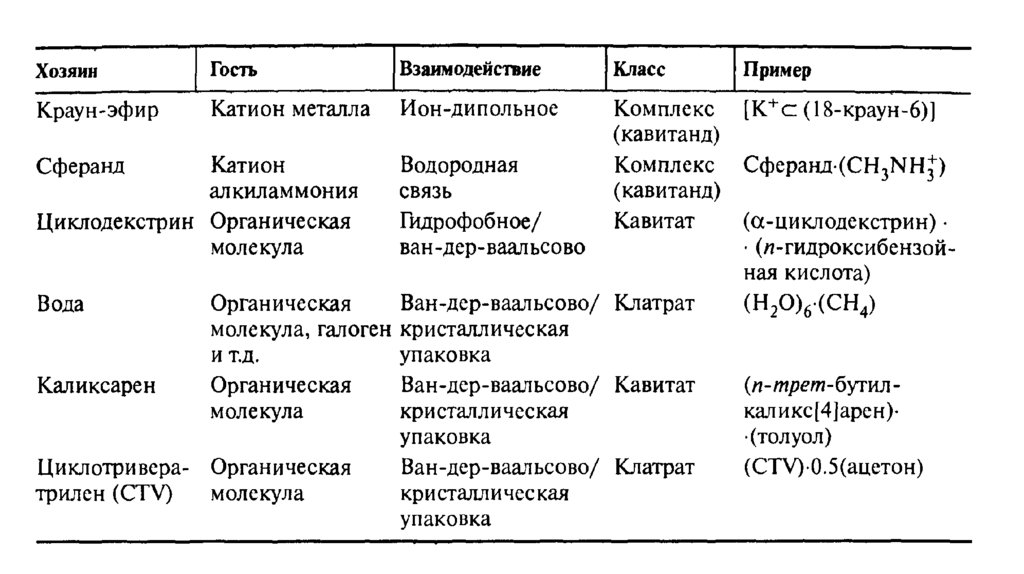
Соединения-хозяева могут быть разделены на два главных класса всоответствии
с
топологической
взаимосвязью
между
хозяином
и гостем.
- Кавитандами
называются
молекулы-хозяева
с внутримолекулярными полостями.
Способность полости связывать молекулу-гостя в этом случае –
неотъемлемое свойство хозяина и проявляется как в твердом состоянии, так
и
в
растворе.
- Клатрандами
называют хозяев с межмолекулярными полостямизазорами между двумя или более молекулами хозяина, существующими
только в кристаллическом или твердом состоянии.
- Агрегат «хозяин – гость», образованный кавитандом, называют
кавитатом,
образованный
клатрандом
–
клатратом.
28.
29.
30.
Механизм образования супрамолекулГлавное - размер и форма или геометрическая
комплементарность (геометрическая и химическая
взаимодополняемость) молекул, а не их реакционная
способность.
Химия типа «хозяин-гость»:
Размер полости хозяина
определяет размер
«желанного» гостя; чем точнее
соответствие «гость-хозяин»,
тем выше устойчивость
ансамбля.
30
31.
Механизм образования супрамолекул• Во всех супрамолекулярных системах рецептор (хозяин) содержит
молекулярные центры (точно так же как замок – замочную скважину),
нацеленные на селективное связывание определенного субстрата-«ключа»
(или «гостя»).
• В «супермолекулах» удерживание отдельных фрагментов происходит за счет
невалентных межмолекулярных взаимодействий, к которым относятся
водородные связи, электростатические силы и лиофильные-лиофобные
взаимодействия.
• Способность биологических молекул к самоорганизации и селективному
взаимодействию с другими частицами, называемая молекулярным
распознаванием основана на принципе “ключ-замок”. Причем каждому замку
соответствует строго определенный ключ.
31
32.
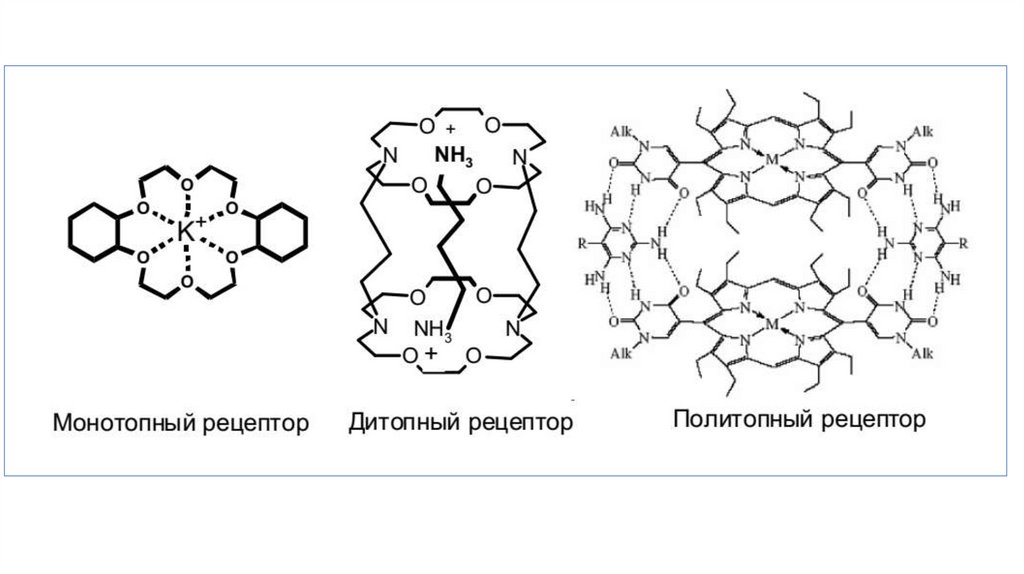
Процессы распознавания в супрамолекулярной химии итипы рецепторов
«молекулярное распознавание» Э. Фишер,1894 г. :
стерическое соответствие рецептор–субстрат по форме и
геометрии в виде образа «замочек–ключик»
33.
Образование супрамолекулы происходит при соблюдении рядаусловий:
• Пространственная комплементарность, т.е. возможность субстрату
подойти к рецептору.
• Комплиментарность
на
уровне
возможности
осуществления
взаимодействия.
Так,
если
рецептор
положительно
заряжен,
то
субстрат
должен обладать отрицательным зарядом. Донор взаимодействует с
акцептором, диполь - с диполем.
• Стабильность молекулярных ансамблей. Поскольку межмолекулярные
взаимодействия являются слабыми, то множественность взаимодействий
обеспечивает прочность межмолекулярным ансамблям.
• Эффект растворителя. Важно учитывать эффект среды, поскольку
межмолекулярные связи не должны разрушаться при взаимодействии со
средой.
• Распознавание
предполагает
комплементарность
партнеров
–
геометрическое,
природное
соответствие.
34.
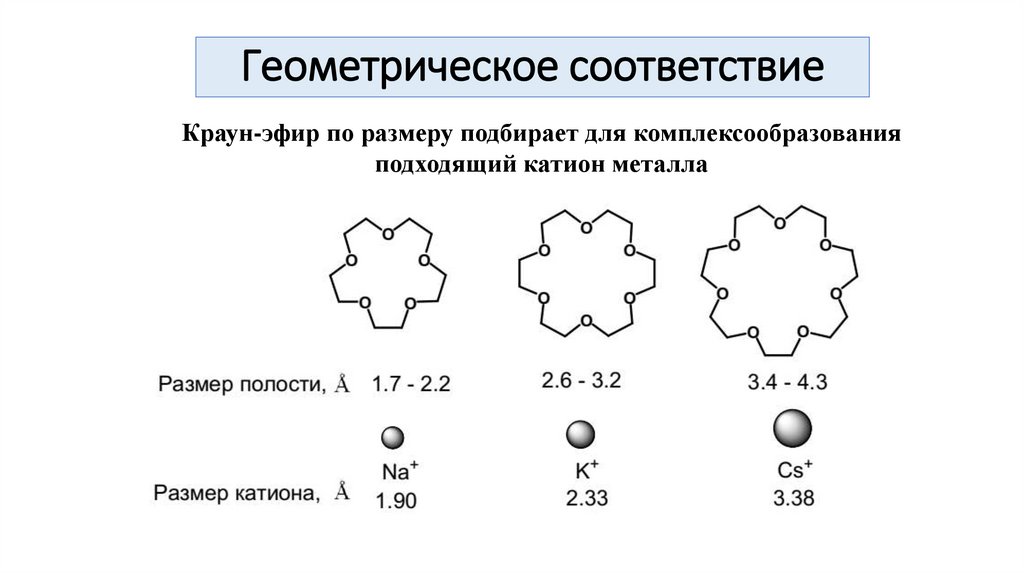
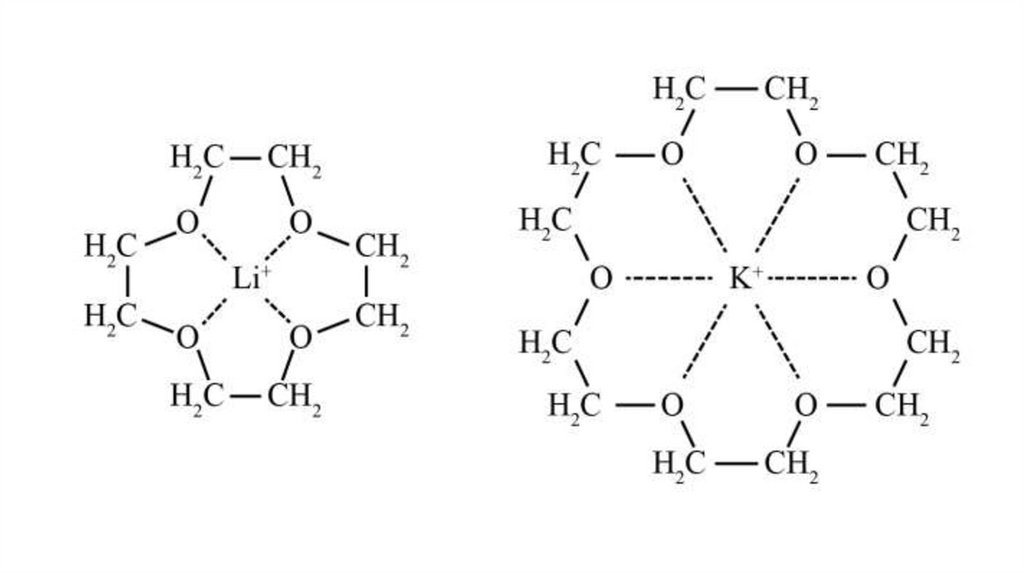
Геометрическое соответствиеКраун-эфир по размеру подбирает для комплексообразования
подходящий катион металла
35.
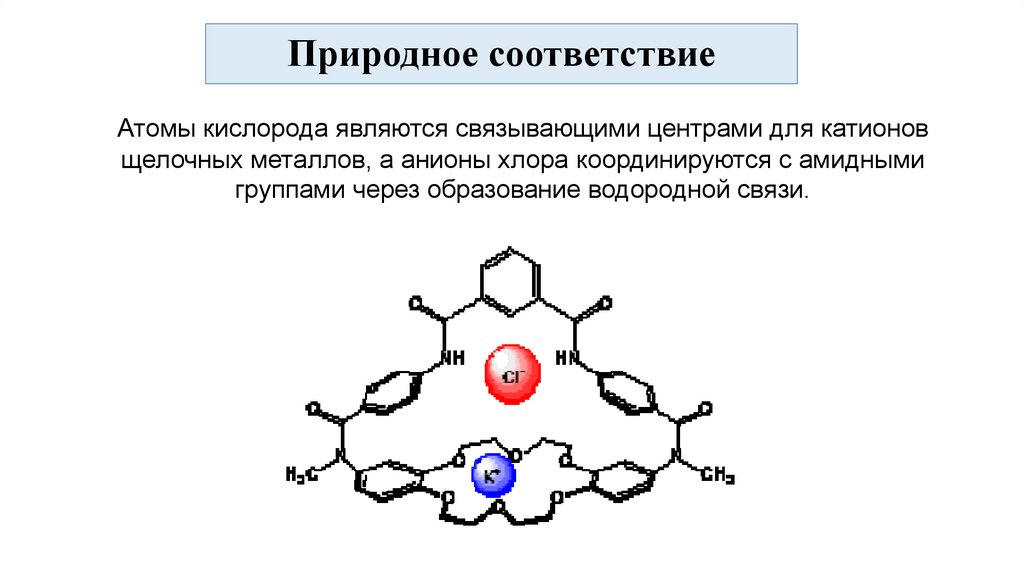
Природное соответствиеАтомы кислорода являются связывающими центрами для катионов
щелочных металлов, а анионы хлора координируются с амидными
группами через образование водородной связи.
36.
Хелатный и макроциклический эффектыВ супрамолекулярной химии хелатный эффект
проявляется при координации субстрата
открытоцепными рецепторами – подандами.
Краун-эфиры и криптанды проявляют
макроциклический эффект, который
демонстрирует более высокую устойчивость
комплексов по сравнению с хелатным
эффектом (10 4раз). Полагают, что упрочение
связывания достигается благодаря
конформационной перестройке лиганда для
осуществления «укутывания» субстрата.
Дальнейшая стабилизация комплексов
наблюдается при переходе от плоских
макроциклов к объёмным криптандам
37.
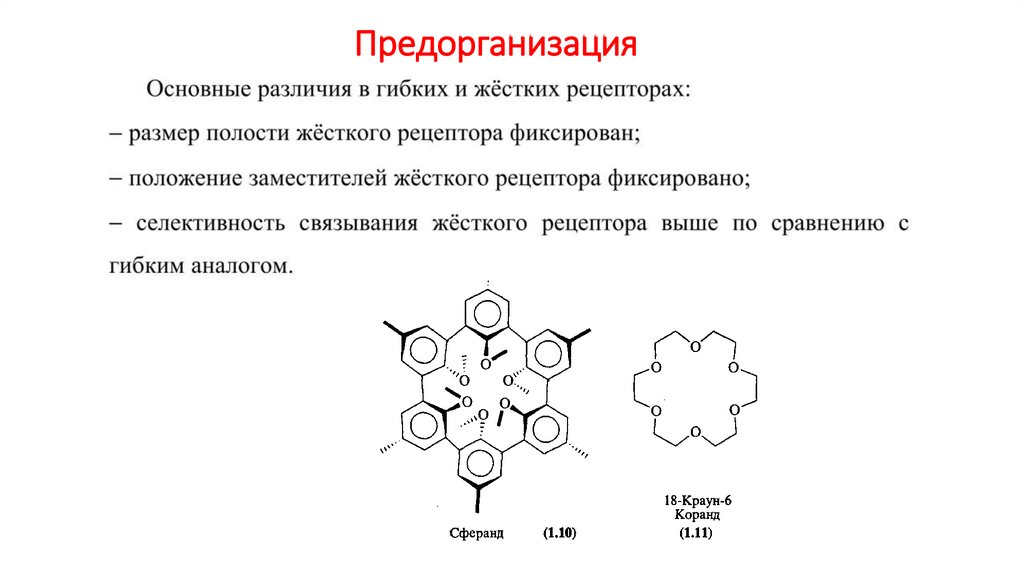
Предорганизация38.
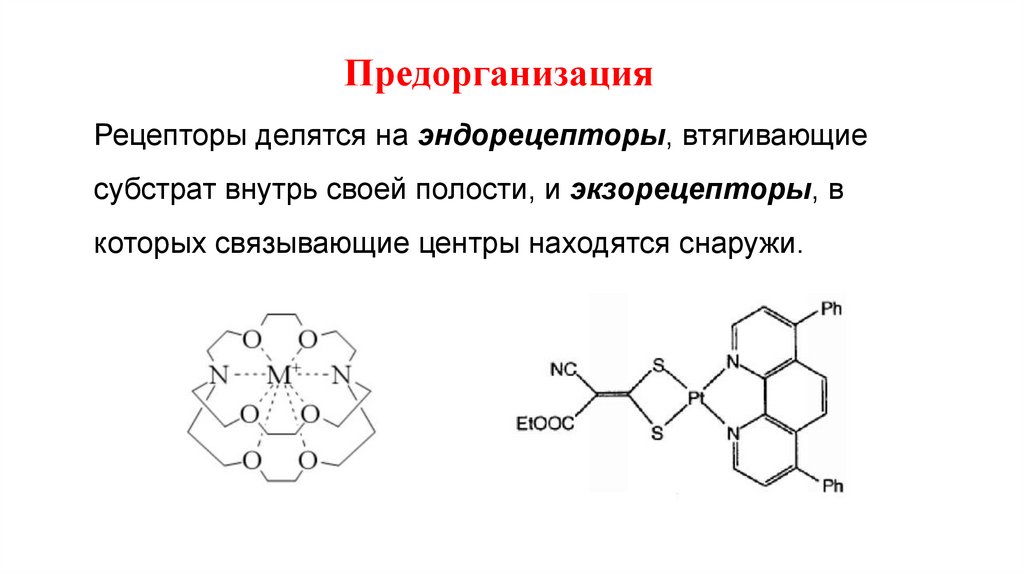
ПредорганизацияРецепторы делятся на эндорецепторы, втягивающие
субстрат внутрь своей полости, и экзорецепторы, в
которых связывающие центры находятся снаружи.
39.
40.
41.
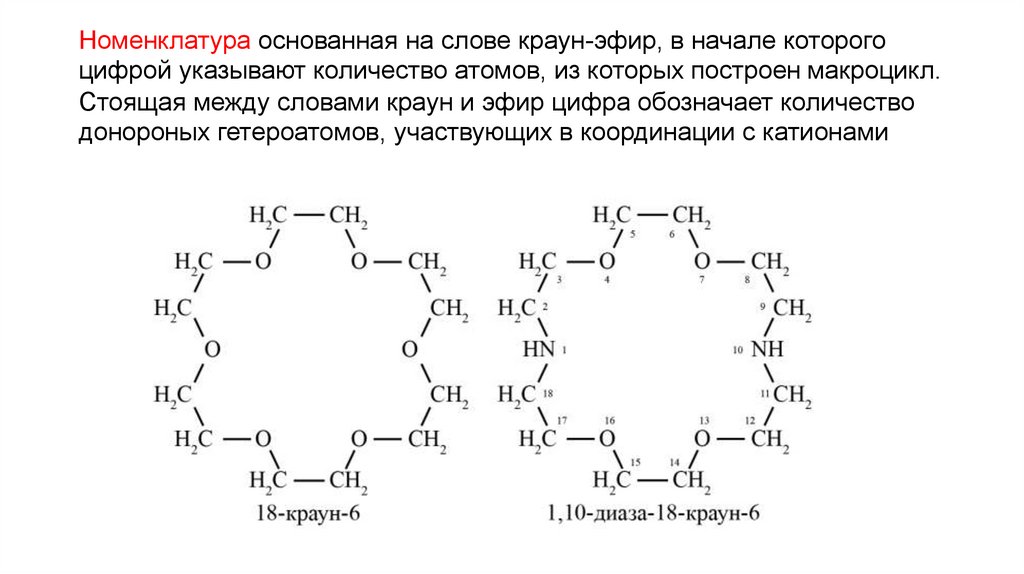
Номенклатура основанная на слове краун-эфир, в начале которогоцифрой указывают количество атомов, из которых построен макроцикл.
Стоящая между словами краун и эфир цифра обозначает количество
донороных гетероатомов, участвующих в координации с катионами
42.
43.
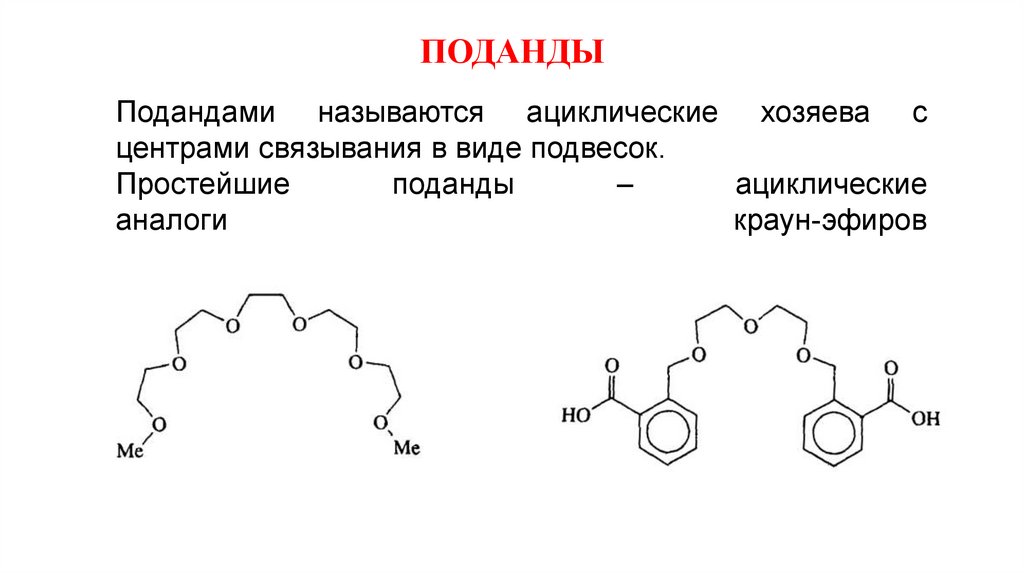
ПОДАНДЫПодандами называются ациклические хозяева с
центрами связывания в виде подвесок.
Простейшие
поданды
–
ациклические
аналоги
краун-эфиров
44.
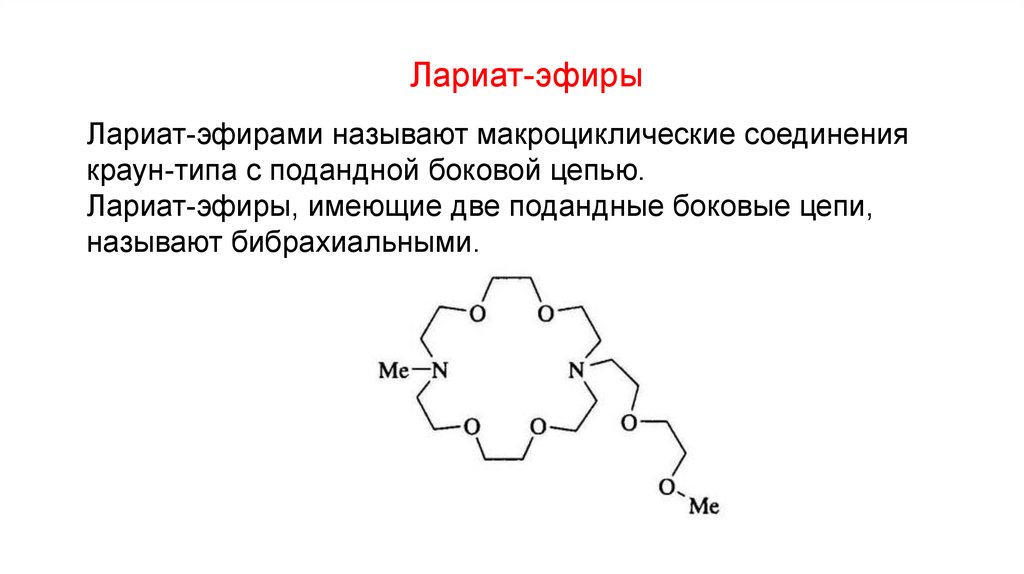
Лариат-эфирыЛариат-эфирами называют макроциклические соединения
краун-типа с подандной боковой цепью.
Лариат-эфиры, имеющие две подандные боковые цепи,
называют бибрахиальными.
45.
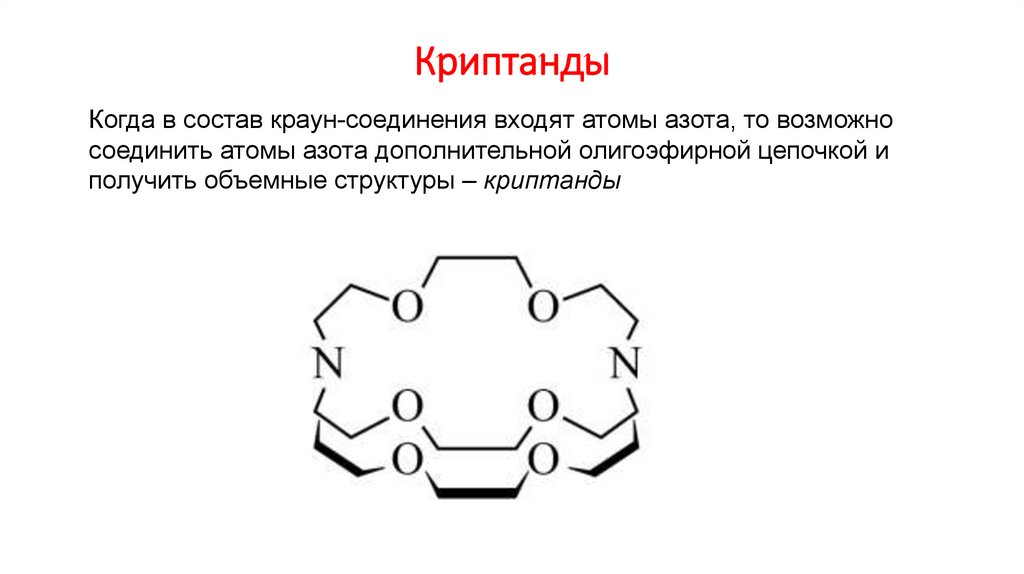
КриптандыКогда в состав краун-соединения входят атомы азота, то возможно
соединить атомы азота дополнительной олигоэфирной цепочкой и
получить объемные структуры – криптанды
46.
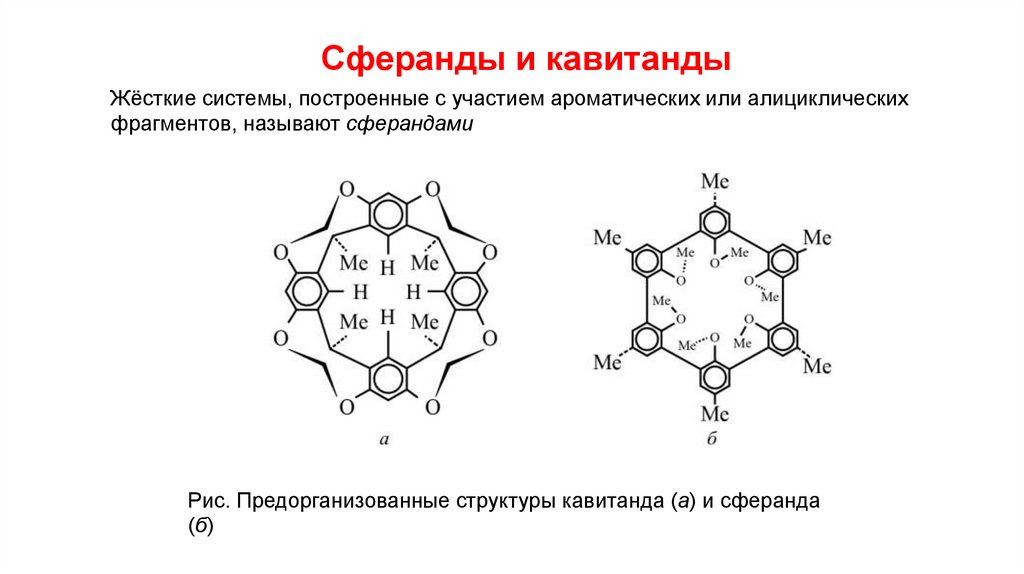
Сферанды и кавитандыЖёсткие системы, построенные с участием ароматических или алициклических
фрагментов, называют сферандами
Рис. Предорганизованные структуры кавитанда (а) и сферанда
(б)
47.
Применение краун-соединений• Реагенты для экстракции солей из водной фазы в органическую
• Процессы разделения солей.
• Концентрирование радионуклеидов.
• В хроматографии краун-эфиры используют для модификации
селикагелей.
• При проведении электрофореза на бумаге краун-эфиры вводят как
компоненты в элюирующий растворитель.
• В физико-химических методах анализа (например, при проведении
экстракционной фотометрии) в титрующий раствор добавляют краунэфир.




















 chemistry
chemistry








