Similar presentations:
Изотопы, их свойства применение
1.
изотопыих свойства
применение
2.
При изучении свойстврадиоактивных элементов было
обнаружено, что у одного и того же
химического элемента можно
встретить атомы с различной массой
ядра.
Заряд ядра при этом они имеют
одинаковый, то есть это не примеси
сторонних веществ, а то же самое
вещество
3.
В периодической системеМенделеева и данный элемент, и
атомы вещества с отличающейся
массой ядра занимают одну клетку.
Исходя из вышеперечисленного
таким разновидностям одного и того
же вещества было дано название
«изотопы».
4.
Название «изотопы» былопредложено в 1912 г
английским радиохимиком
Фредериком Содди,
который образовал его из
двух греческих слов: isos –
одинаковый и topos –
место.
5.
Изотопы– разновидностиодного и того же химического
элемента, близкие по своим
физико-химическим
свойствам, но имеющие
разную атомную массу.
6.
По принятой нейтронно-протонноймодели ядра объяснить
существование изотопов удалось
следующим образом:
ядра некоторых атомов вещества
содержат различное количество
нейтронов, но одинаковое
количество протонов.
7.
Те элементы, количество протоновкоторых нечетно, могут иметь лишь по
два стабильных изотопа.
У ряда элементов имеется только один
стабильный изотоп.
Это такие вещества как золото, алюминий,
фосфор, натрий, марганец и другие.
Такие вариации по числу стабильных
изотопов у разных элементов связано со
сложной зависимостью числа протонов и
нейтронов от энергии связи ядра.
8.
Сколько изотопов может содержать ядро?Ядро не может содержать произвольное
количество нейтронов. Соответственно,
количество изотопов ограниченно.
У четных по количеству протонов
элементов количество стабильных
изотопов может достигать десяти.
Например, олово имеет 10 изотопов,
ксенон – 9, ртуть – 7 и так далее.
9.
В природе встречаются какстабильные изотопы, так и
нестабильные
10.
Стабильные изотопы – эторазновидности химических элементов,
которые могут самостоятельно
существовать продолжительное время.
Сейчас известно около 270 стабильных
изотопов
11.
Нестабильные – радиоактивныеизотопы, ядра атомов которых
подвержены самопроизвольному
превращению в другие ядра с
испусканием различных частиц
(или процессам так называемого
радиоактивного распада).
12.
Большая часть нестабильных изотопов былаполучена искусственным путем.
Нестабильные изотопы радиоактивны, их ядра
подвержены процессу радиоактивного
распада, то есть самопроизвольному
превращению в другие ядра,
сопровождающемуся испусканием частиц или
излучений.
Практически все радиоактивные
искусственные изотопы имеют очень
маленькие периоды полураспада, измеряемые
секундами и даже долями секунд.
13.
Число нестабильных изотоповпревышает 2000.
Число радиоактивных изотопов у
многих элементов очень велико и
может превышать два десятка.
14.
Разнообразные изотопыхимических элементов находят
широкое применение в научных
исследованиях, в различных
областях промышленности и
сельского хозяйства, в ядерной
энергетике, современной биологии и
медицине, в исследованиях
окружающей среды и других
областях.
15.
Меченые атомы (изотопные индикаторы)содержат изотопы, которые по своим
свойствам (радиоактивности, атомной
массе) отличаются от других изотопов
данного элемента. Их добавляют к
химическому соединению или смеси, где
находится исследуемый элемент;
поведение меченых атомов характеризует
поведение элемента в исследуемом
процессе.
16.
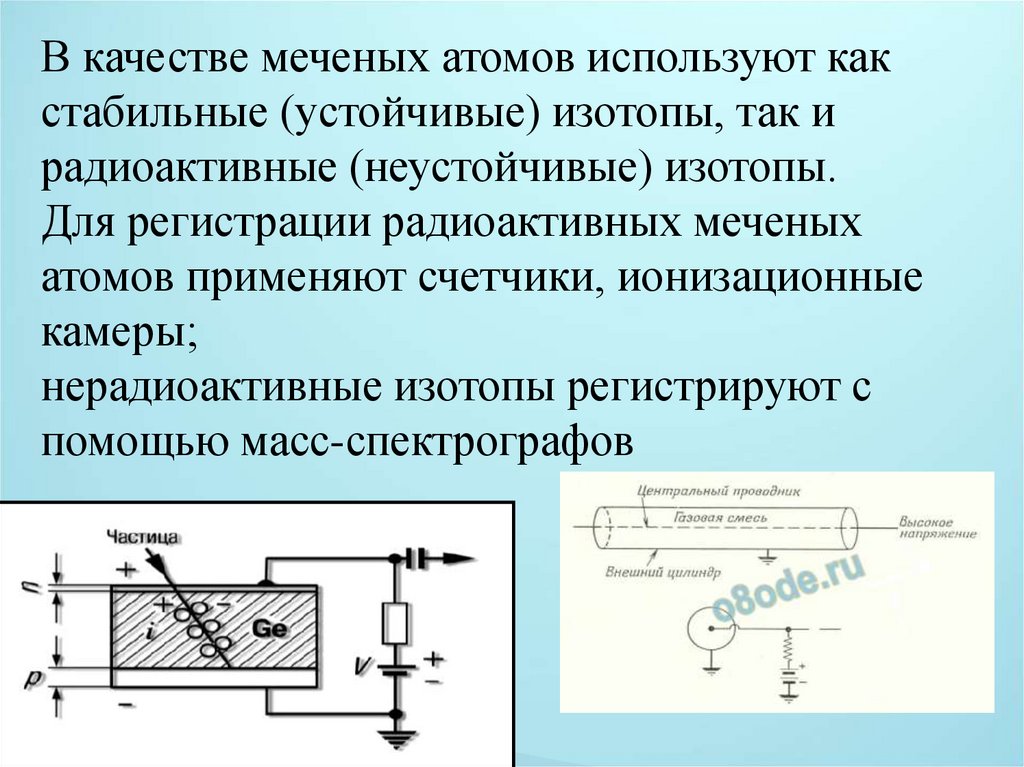
В качестве меченых атомов используют какстабильные (устойчивые) изотопы, так и
радиоактивные (неустойчивые) изотопы.
Для регистрации радиоактивных меченых
атомов применяют счетчики, ионизационные
камеры;
нерадиоактивные изотопы регистрируют с
помощью масс-спектрографов
17.
В биологии изотопы применяют длярешения как фундаментальных, так и
прикладных биологических проблем,
изучение которых другими методами
затруднено или невозможно.
Для биологии преимущество метода
меченых атомов состоит в том, что
использование изотопов не нарушает
целостности организма и его основных
жизненных отправлений.
18.
С помощью стабильных ирадиоактивных изотопов были
выяснены и детально изучены
сложные и взаимосвязанные процессы
биосинтеза и распада белков,
нуклеиновых кислот, углеводов, жиров
и др. биологически активных
соединений, а также химические
механизмы их превращений в живой
клетке
19.
Радиоактивные изотопы в археологииМетод радиоактивного углерода получил
интересное применение для определения
возраста древних предметов
органического происхождения (дерева,
древесного угля, тканей и т.д.).
Этим методом можно узнать
возраст египетских мумий,
остатков доисторических
костров
.
20.
Предельный возраст образца, которыйможет быть определён радиоуглеродным
методом — около 60 000 лет,
т. е. около 10 периодов полураспада 14C
За это время содержание 14C
уменьшается примерно в 1000 раз
(около 1 распада в час на грамм углерода).
21.
Один из наиболее известных случаевприменения радиоуглеродного метода —
исследование фрагментов Туринской
плащаницы (христианской святыни,
якобы хранящей на себе следы тела
распятого Христа), проведённый в
1988 году, одновременно в нескольких
лабораториях слепым методом.
Радиоуглеродный анализ позволил
датировать плащаницу периодом
XI — XIII веков
22.
Радиоактивные изотопы применяются вмедицине, как для постановки диагноза, так и
для терапевтических целей.
23.
Радиоактивный натрий, вводимый внебольших количествах в кровь,
используется для исследования
кровообращения.
24.
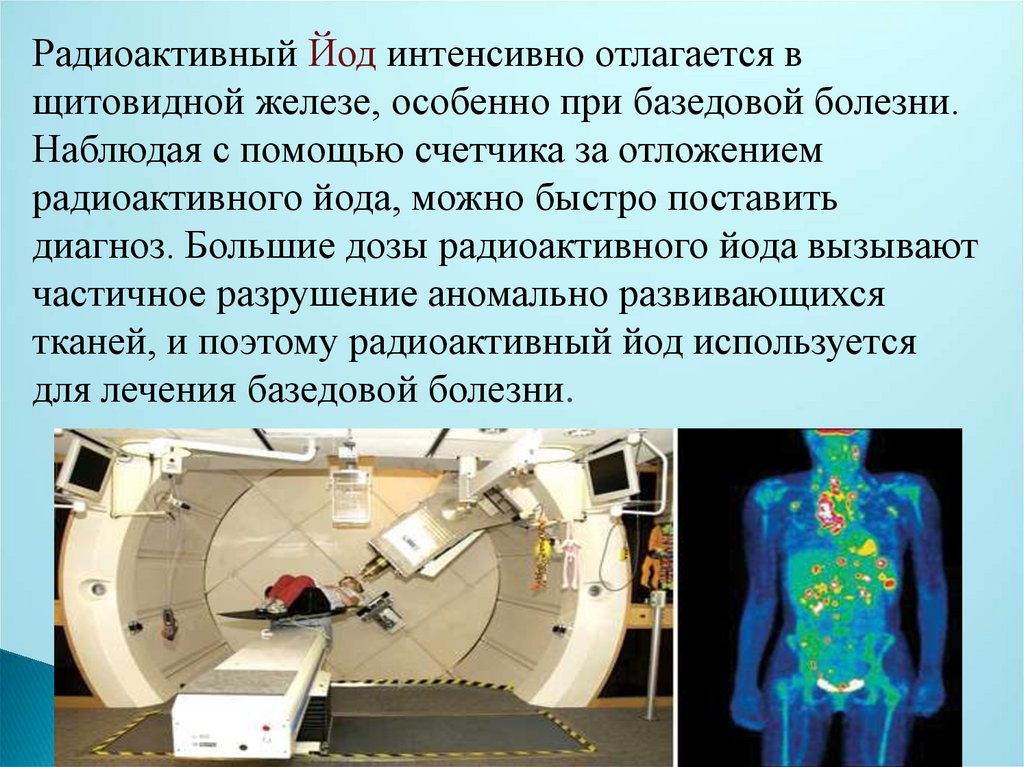
Радиоактивный Йод интенсивно отлагается вщитовидной железе, особенно при базедовой болезни.
Наблюдая с помощью счетчика за отложением
радиоактивного йода, можно быстро поставить
диагноз. Большие дозы радиоактивного йода вызывают
частичное разрушение аномально развивающихся
тканей, и поэтому радиоактивный йод используется
для лечения базедовой болезни.
25.
Интенсивное гамма-излучение кобальтаиспользуется при лечении раковых
заболеваний (кобальтовая пушка).
26.
С применением радиоактивных изотоповчрезвычайно интересные возможности
открываются перед хирургами для изучения
наркоза.
Применяется пенициллин и другие,
антибиотики однако работ, которые бы полно
освещали вопрос распределения этих
препаратов в организме, нет.
С помощью антибиотиков, меченных
радиоактивными изотопами, становится
возможным разрешить и эти вопросы.
использования радиоактивных веществ для
диагностики
27.
Применение радиоактивных изотопов впромышленности.
Одним из примеров этого может служить
следующий способ контроля износа
поршневых колец в двигателях внутреннего
сгорания.
Облучая поршневое кольцо нейтронами,
вызывают в нем ядерные реакции и делают его
радиоактивным. При работе двигателя частички
материала кольца попадают в смазочное масло.
Исследуя уровень радиоактивности масла после
определенного времени работы двигателя,
определяют износ кольца.
28.
Радиоактивные изотопы позволяют судить одиффузии металлов, процессах в доменных
печах и т. д.
Мощное гамма-излучение радиоактивных
препаратов используют для исследования
внутренней структуры металлических отливок
с целью обнаружения в них дефектов.
Батарейки для приборов
стабилизации ритмов
сердца
29.
В химической промышленности ...В резиновой промышленности с помощью
радиоактивного изотопа серы изучается механическое
и химическое поведение серы в условиях
вулканизации.
Облучение полиэтиленовых труб радиоактивными
изотопами позволяет повысит их термостойкость и
стойкость к агрессивным средам.
30.
В текстильной промышленности:С помощью радиоактивных изотопов получают
хлопчатобумажные ткани с антимикробными
свойствами;
Радиоизотопные приборы применяют для контроля массы
волокнистого слоя
Облучение текстильных материалов радиоизотопными
изотопами используется для получения
шерстоподобных свойств ткани
В деревообрабатывающей промышленности:
в результате облучения радиоактивными изотопами
мягкое дерево приобретает значительно низкую
способность собирать воду и более высокую твердость
31.
В строительной промышленности:применение радиоактивных изотопов для исследования
строительных материалов и строительных механизмов,
контроля металлических конструкций, вентиляции
и отопительных систем, а также некоторым другим
вопросам, связанным с задачами строительной
промышленности
32.
Пищевая промышленность:Радиационное облучение пищевых продуктов питания
способствует увеличению сроков хранения;
Радиоизотопные приборы применяются для измерения
уровня содержания искусственных красителей в
продукте питания;
Угольная промышленность:
Радиоизотопные приборы используются для контроля
и регулировки скиповых установок, для контроля в
угольных и породных бункерах.
33.
Все более широкое применение получаютрадиоактивные изотопы в сельском хозяйстве:
Облучение семян растений (хлопчатника, капусты,
редиса и др.) небольшими дозами гамма-лучей от
радиоактивных препаратов приводит к заметному
увеличению урожайности.
Большие дозы 'радиации вызывают
мутации у растений и
микроорганизмов, что в
отдельных случаях приводит
к появлению мутантов с новыми ценными свойствами
(радиоселекция).
34.
Так выведены ценные сорта пшеницы, фасолии других культур, а также получены высоко
продуктивные микроорганизмы,
применяемые в производстве антибиотиков.
Гамма-излучение радиоактивных изотопов
используется также для борьбы с вредными
насекомыми и для консервации пищевых
продуктов.
35.
Широкое применение получили «меченые атомы» вагротехнике.
Например, чтобы выяснить, какое из фосфорных удобрений
лучше усваивается растением, помечают различные
удобрения радиоактивным фосфором.
Исследуя затем растения на радиоактивность, можно
определить количество, усвоенного ими фосфора из разных
сортов удобрения.
36.
КриминалистикаВ 1937 г. в печати
появилось сообщение о
том, что найдена дотоле
неизвестная картина
голландца Яна Вермера
Делфтского – одного из
самых знаменитых
художников 17-того
столетия.
«Девушка с жемчужной сережкой»
37.
В ходе судебного процесса и открылось, чтокартины, "найденные" Ван Меегереном,
написаны не Вермером, а им самим.
38.
В 1972 г. наII Международной
конференции голландские
исследователи сообщили об
обнаруженных ими
посредством нейтронноактивационного и гаммаактивационного анализов
подделках античных монет.
39.
Изучая письма ИсаакаНьютона, группа
английских и американских
исследователей высказала
предположение о том, что
причина его болезни —
отравление ртутью.
40.
Производство изотоповЯдерные реакторы
Ускорители
Крупнейшие производители
ПО «Маяк»
Димитровградский НИИ
«Сибирский химический комбинат»
«Росатом»
41.
Завод разделения изотопов в ТомскеЗавода в Челябинске «Маяк»
42.
Нейтронный реактор43.
ИЗОТОПЫ44.
Применение изотопов водородаЛегкий водород используется во
множестве отраслей: в химической
промышленности, где с его помощью
ведется производство аммиака,
метанола, соляной кислоты и других
веществ;
в нефтепереработке и металлургии, где
он необходим для восстановления
тугоплавких металлов из оксидов.
45.
Также он применяется на некоторыхстадиях производственного цикла (в
производстве твердых жиров) в пищевой
и косметической промышленности.
Водород служит одним из видов ракетного
топлива и используется в лабораторной
практике в науке и на производстве.
46.
Дейтерий незаменим в ядерной энергетикекак прекрасный замедлитель нейтронов.
Он применяется в этом качестве, а также как
теплоноситель в тяжеловодных реакторах,
позволяющих использовать природный уран,
что снижает затраты на обогащение.
47.
Химические свойства тяжелого водородапозволяют использовать его в
производстве медицинских препаратов в
целях замедления выведения их из
организма.
Он также, наряду с тритием, является
компонентом рабочей смеси в
термоядерном оружии.
48. Тритий Радиоактивный изотоп водорода, получаемый искусственно облучением лития тепловыми нейтронами Тритий - бесцветный газ,
49.
Содержание в природе.Тритий образуется в верхних слоях
атмосферы в результате взаимодействия
нейтронов вторичного космического
излучения с ядрами атомов азота;
Термоядерных реакций, осуществляемых на
энергетических комплексах и при ядерных
испытаниях.
50.
Изотопы кислородаИзвестно, что в природе кислород может находиться в
виде трех изотопов 16O (99,76%), 17O (0,04%) и 18O
(0,2%).
Кислород-15O часто используется в
позитронно-эмиссионной томографии.
Наиболее стабильные изотопы имеют период
полураспада 122,24 с; 70,606 с;
Все остальные радиоактивные изотопы имеют периоды
полураспада менее 27 с; большинство из них имеют
периоды полураспада менее 83 мс
51.
КалийПриродный калий состоит из трех изотопов двух
стабильных и одного радиоактивного
Период полураспада – 1,32 года
40К содержится в живых организмах и своим
излучением создает естественное (фоновое)
облучение. Остальные радиоактивные изотопы К в
природе не встречаются.
42К используется как индикатор в аналитической
химии, биологии, медицине.
52.
ЦезийПриродный цезий состоит из одного стабильного изотопа.
Известны 23 радиоактивных изотопа цезия. Наибольшее
практическое значение имеет 137Cs.
Период полураспада 30,1 года,
В небольших количествах радиоактивные изотопы цезия
содержатся практически во всех объектах внешней
среды.
53.
Получение: Образуется при делении ядератомов тяжелых элементов при ядерных
реакциях на АЭС и при взрывах, а также
при помощи ускорителей заряженных
частиц.
Применяется в химических и
радиобиологических исследованиях, в
дефектоскопии, в радиационной
технологии137Сs используют в качестве
источника альфа-излучения.
54.
СтронцийПриродный стронций состоит из смеси
стабильных изотопов:
Наибольший токсикологический интерес
представляет 90Sr с
Периодом полураспада 28,1 года.
Чистый бета-излучатель
55.
Антропогенные источники поступленияв окружающую среду:
Стронций, образующийся в ядерных
реакторах, может поступать в
теплоноситель.
При очистке теплоносителя - в
газообразные и жидкие отходы.
В результате крупных ядерных испытаний
и аварий на АЭС.
56.
ЦерийРадиоактивные изотопы церия получают в
ядерном реакторе при делении ядер атомов
тяжелых элементов или при ядерных взрывах.
Содержание изотопов церия в неразделенной
смеси продуктов деления составляют 6 %.
-излучатель.
Применяется в медицине
Период полураспада 284,3 суток,
57.
ПлутонийСтабильных изотопов не обнаружено.
Известны радиоактивные изотопы с
массовыми числами 232-246.
Практическое значение имеют 238Pu
и 239Pu.
Период полураспада - 24360 лет
Испускает альфа- частицы
58.
Содержание в природе:239Pu в природе образуется в урановых.
Изотопы плутония получают в урановых
реакторах. Также образуется при испытаниях
ядерного оружия.
Антропогенными источниками поступления в
окружающую среду, являются испытания
ядерного оружия, некоторые этапы ядерного
топливного цикла, аварии на атомных
электростанциях, связанные с
разгерметизацией ядерных систем.
59.
Производство и переработка ядерноготоплива, захоронение радиоактивных
отходов также является источником
поступления плутония в окружающую
среду.
60.
УглеродПриродный углерод состоит из смеси двух
стабильных изотопов 12C (98,0992%) и 13С
(1,108%).
Известно 6 радиоактивных изотопов с массовыми
числами 9-11 и 14-16. Наибольшее значение с
точки зрения радиационной опасности
представляет долгоживущий изотоп 14С.
Антропогенные источники поступления 14С в
окружающую среду в основном выбросы и
сточные воды АЭС.
61.
Выброс изотопа 14С из реакторов сграфитовым замедлителем 14С
является также одним из
компонентов по регенерации ядерного
топлива.
62.
При попадании в окружающую среду 14Сучаствует в фотосинтезе, накапливается в
растениях, хорошо мигрирует по пищевым
цепочкам.
10% 14С из атмосферы поглощается наземными
биоценозами.
Остальные 90% 14C фиксируются морскими
организмами, в основном фитопланктоном.
63.
ЙодПриродный изотоп йода 127I. Известны
радиоактивные изотопы с массовыми числами
115-126, 128-141.
С точки зрения радиационной опасности интерес
представляет 131I, 132I, 133I, 129I.
Содержание в природе: образуется в реакциях
деления урана и плутония
Применение. 131I и 125I применяется в
физической химии, биологии, медицине.
64.
Содержание в природе: образуется вреакциях деления урана и плутония
Применение:
131I и 125I применяется в физической
химии, биологии, медицине.
65.
Антропогенными источникамипоступления в окружающую среду
радиоактивного йода являются ядерные
взрывы и атомные электростанции.
Йод характеризуется высокой
миграционной способностью.
66.
Поступая во внешнюю среду, онвключается в биологические цепи
миграции, становится источником
внешнего и внутреннего облучения.
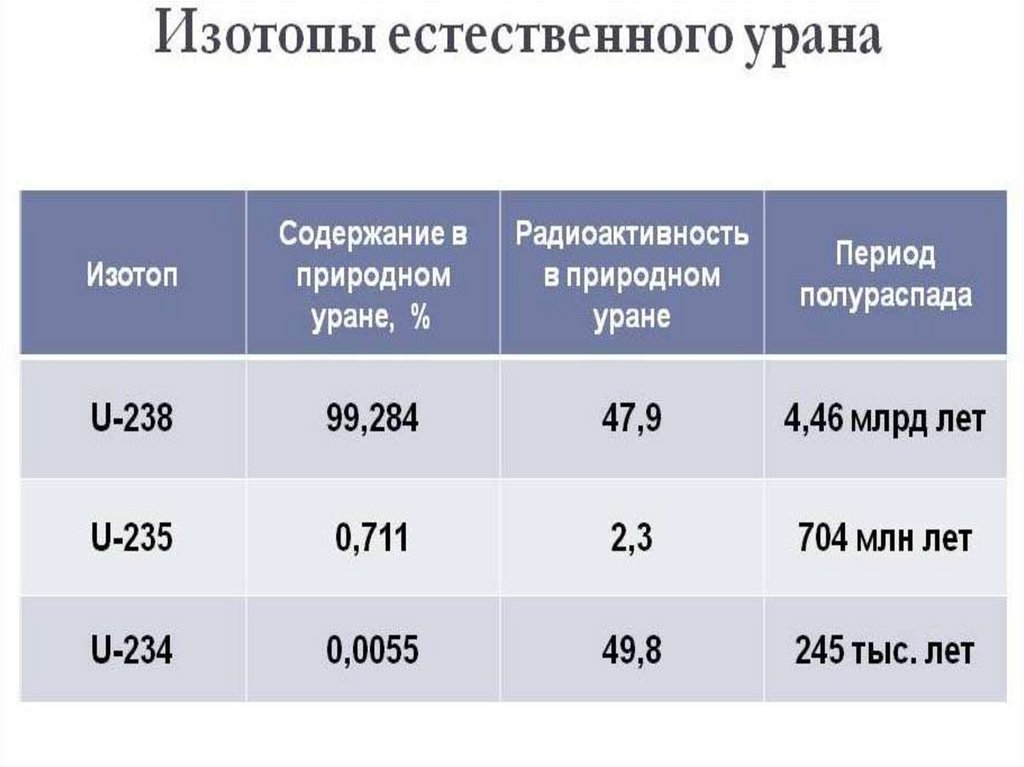
67.
Изотопы уранаНа данный момент известны 26 изотопов
урана и еще 6 возбуждённых изомерных
состояний.
В природе встречаются три изотопа
урана: 234U (0,0055 %), 235U (0,7200 %),
238U (99,2745 %)
Нуклиды 235U и 238U являются
родоначальниками радиоактивных рядов
ряда актиния и ряда радия соответственно.
68.
Нуклид 235U используется кактопливо в ядерных реакторах, а также
в ядерном оружии (благодаря тому, что в нём
возможна самоподдерживающаяся цепная
ядерная реакция).
Нуклид 238U используется для
производства плутония-239, который также
имеет чрезвычайно большое значение как в
качестве топлива для ядерных реакторов, так и
в производстве ядерного оружия.
69.
70.
71.
Применение:238U служит источником вторичного
ядерного горючего - плутония.
Соединения химического элемента ранее
использовались в качестве красителей для керамики;
В настоящее время незначительное количество
уранового стекла и изделий из него производится в
Чехии.
Также уран вводится в некоторые сорта оптических
стёкол;
В геологии — определение возраста минералов и
горных пород с целью выяснения последовательности
протекания геологических процессов.
Этим занимается геохронология.
72.
В начале XX века уранилнитрат широкоприменялся для усиления негативов и
окрашивания (тонирования) позитивов
(фотографических отпечатков) в бурый
цвет.
Сплавы железа и обеднённого урана (уран238) применяются как
мощные магнитострикционные материалы
73.
Самое известное применение обеднённого уранав качестве сердечников для бронебойных снарядов.
Впервые уран в качестве сердечника для снарядов был
применен в Третьем рейхе.
Обеднённый уран используется в современной танковой броне
(в боевом танке США M-1 «Абрамс»),
Обедненный уран используется для радиационной защиты
и балластная масса в аэрокосмических применениях, таких как
рулевые поверхности летательных аппаратов.
Материал применяется в высокоскоростных роторах
гироскопов, больших маховиках, как балласт в космических
спускаемых аппаратах и гоночных яхтах, при бурении
нефтяных скважин.




































































 physics
physics








