Similar presentations:
Введение в общую иммунологию. Неспецифические и специфические факторы защиты макроорганизма
1.
Лекции 1-3 на тему:Лектор
Третьякевич Зоя Николаевна,
доктор мед. наук, профессор
2.
ЛИТЕРАТУРА (основная)1) Иммунология [Электронный ресурс] / Хаитов Р. М. - М.
: ГЭОТАР-Медиа, 2009. http://www.studmedlib.ru/book/ISBN9785970412220.html
2) Иммунология [Электронный ресурс] / Ярилин А.А. - М. :
ГЭОТАР-Медиа, 2010. http://www.studmedlib.ru/book/ISBN9785970413197.html
3) Иммунология [Электронный ресурс]: учебник / Р. М.
Хаитов. - 2-е изд., перераб. и доп. - М. : ГЭОТАРМедиа, 2018. –
http://www.studmedlib.ru/book/ISBN9785970433 454.html
4) Иммунология : структура и функции иммунной системы
[Электронный ресурс] / Хаитов Р.М. - М. : ГЭОТАР-Медиа,
2019. Режим доступа:
http://client.studmedlib.ru/book/ISBN9785970449622.html
3.
ЛИТЕРАТУРА (дополнительная)1) Иммунология. Атлас [Электронный ресурс]: учебное
пособие / Хаитов Р.М., Ярилин А.А., Пинегин Б.В. - М.:
ГЭОТАР-Медиа, 2011. http://www.studmedlib.ru/book/ISBN9785970418581.html
2) Клиническая иммунология [Электронный ресурс] :
учебник / Земсков А.М., Земсков В.М., Караулов А.В.;
Под ред. А.М. Земскова. - М. : ГЭОТАР-Медиа, 2008.
http://www.studmedlib.ru/book/ISBN9785970407752.html
3) Клиническая иммунология и аллергология с основами
общей иммунологии [Электронный ресурс]: учебник /
Ковальчук Л.В., Ганковская Л.В., Мешкова Р.Я. - М. :
ГЭОТАР-Медиа, 2012. –
http://www.studmedlib.ru/book/ISBN9785970422410.html
4.
ЖЕЛАЕМОЕВ ДЕЙСТВИТЕЛЬНОСТИ
ПОМОГИТЕ!
ВЕТРЯНАЯ
ОСПА
ГРИПП
КИШЕЧНАЯ
ИНФЕКЦИЯ
ОРВИ
ПОМОГИТЕ !
НА
ПОМОЩЬ!
5.
• Организм человека постоянно подвергаетсявоздействию различных болезнетворных
факторов окружающей среды. В то же время
многие люди сохраняют здоровье.
• В процессе биологической эволюции человека
сформировались системы и механизмы,
защищающие его как целостность в случаях,
когда физические, химические или
биологические факторы среды могут при
взаимодействии организма с ними привести к
повреждению каких-либо его структур, что в
свою очередь вызывает их патологию.
• Термин иммунитет (лат. Immunitas) ―
свободный от чего-либо, нетронутый → то, что
не воспринимает каких-либо внешних
вмешательств.
6.
История развития иммунологии• В начале своего развития иммунология появилась как
наука о борьбе организма с инфекционными болезнями.
• Великие открытия «ранней эры» иммунологии (начало
ХХ века) были связаны с тяжелыми болезнями (оспа,
сибирская язва, бешенство, дифтерия). Наряду с
постепенным пониманием того, как именно происходит
иммунная защита организма, были разработаны
эффективные вакцины и сыворотки, которые позволили
бороться с этими заболеваниями.
• Позже, в «средние века» иммунологии (30-е ― 60-е гг.)
стало ясно, что иммунная система не только борется с
вмешательством внешних инфекционных агентов, а
вообще поддерживает индивидуальность данного
организма, не позволяя внесению клеток и тканей
другого человека и уничтожая собственные клетки,
потерявшие черты своей индивидуальности.
7.
• В «новейшую эру» иммунологии (70-е ― 90-егоды) наряду с пониманием очень тонких
процессов иммунного распознавания на уровне
молекул белков и их генов, стало ясно, что
иммунная система не является особой и
отдельной, она использует молекулы и клетки,
которые принимают участие во многих других
процессах в организме.
• На примере иммунных процессов был открыт ряд
важных общебиологических закономерностей, а
иммунологические методы стали общепринятыми
во многих других областях биологии.
• Сейчас иммунология находится на подъеме и
очень быстро развивается: каждый год приносит
новые открытия, а прежние представления
меняются, дополняются, а иногда и отвергаются,
заменяются новыми.
8.
• История иммунологии начинается с именианглийского врача Эдварда Дженнера. Первый
иммунологический эксперимент ― 14 мая 1796 года
→ Дженнер ввел в надрез на коже плеча 8-летнего
мальчика содержимое пустулы коровьей оспы.
• Дженнер сделал первый, полусознательный шаг в
понимании и использовании иммунных процессов.
(1749―1823)
9.
• Отцом иммунологии как науки считают Луи Пастера,Пастер известен многими открытиями ― он фактически
доказал микробную природу инфекционных
заболеваний и предложил меры по ослаблению и
уничтожению микробных агентов (пастеризацию).
• Пастер работал с возбудителями нескольких болезней
В 1879 году он наблюдал
что введение ослабленных
вирионов куриной холеры
предотвращает заболевание
кур. Этот подход был
позднее успешно применен
для предотвращения
сибирской язвы, бешенства
и краснухи животных. Были
разработаны принцип
прививок и их схема.
(1822―1895)
10.
• Только после этого Пастер рискнул применитьэтот принцип для лечения человека.
• В лабораторию Пастера привели мальчика,
которого покусала бешеная собака (1885 год).
И Пастер решился, пользуясь принципами
прививки животных, провести вакцинацию
этого мальчика против бешенства → мальчик
не заболел.
• Опыты Пастера принесли ему мировую славу.
В 1888 г. на деньги, собранные по
международной подписке, был открыт Институт
Пастера в Париже, который и сейчас является
известным иммунологическим центром. Позже
институты (станции Пастера) были созданы во
многих странах мира.
11.
• С 1901 года ученым, внесшим большой вклад вразвитие биологии и медицины, начали
присваивать Нобелевские премии (мировое
признание). На примере этих премий интересно
проследить за развитием иммунологии в ХХ веке,
а также представить место этой дисциплины
среди других биологических наук.
• За прошедшие годы Нобелевскую премию
присуждали 120 раз (исключая 9 лет, которые
пришлись на первую и вторую мировые войны).
Иммунологи получали ее 24 раза, т.е. 1/5 всех
выдающихся открытий в области биологии и
медицины касалась иммунологических явлений.
• Эта цифра свидетельствует о важности
иммунологии в понимании биологических
процессов.
12.
• Иммунологические исследования в ХХ, а затем XXIвеке проводились по всему миру: в Европе, Америке,
Северной Африке, Австралии и Японии.
• С помощью иммунологических исследований стали
возможными трансплантации органов и тканей.
Появились иммунологические методы, которые
сейчас применяются для решения многих
биологических задач.
• За последние годы получены новые данные о
развитии иммунной системы, механизмов регуляции
иммунного ответа, основы многих патологий
иммунной системы. В частности, благодаря высокому
уровню исследований в иммунологии, был найден
возбудитель СПИД – ВИЧ-инфекции.
• Темпы развития иммунологии дают надежду на
преодоление как СПИД, так и других опасных
заболеваний.
13.
Понятие о реактивности• Человеческий организм способен защищаться от
повреждений, бороться с патологией самостоятельно.
• В основу учения о причинах патологии
современная медицинская наука ставит понятие
«реактивность» ― способность организма при
взаимодействии с различными повреждающими
воздействиями давать защитный «ответ»,
соответствующий характеру этого патогенного
воздействия.
• В ходе эволюции у человека сложились биологические
механизмы защиты организма от вредных
воздействий, защитные реакции на них.
• Изменения в окружающей среде приводят к
изменению физиологических процессов в организме,
соответствующих новому воздействию.
14.
• Защитная реакция организма проявляется внекотором изменении его характеристик, что
позволяет сохранить жизнедеятельность организма
в целом.
• Человек без вреда для себя переносит физические
нагрузки в определенных пределах. Но отсутствие
нагрузок (гиподинамия) или перегрузки
(гипердинамия) могут привести к патологии. На
одни микроорганизмы человек не реагирует как на
вредные, хотя они болезнетворны для животных.
Другие оказывают повреждающее воздействие на
организм и приводят в действие защитные
механизмы → вызывают защитную реакцию,
которая может привести к патологии.
• В этом проявляется видовая избирательность
защитных механизмов человеческого
организма.
15.
• Состояние организма зависит от характера воздействияна него: физическое истощение, переохлаждение, стресс
могут вызвать заболевание у человека, организм
которого в нормальных условиях не реагирует на тот или
иной повреждающий фактор. А душевный подъем,
эмоциональное возбуждение могут привести к
повышению сопротивляемости организма.
• Защитные реакции различаются:
1) по степени проявления;
2) по характеру участвующих в них систем.
• До определенного порога воздействия патогенного
фактора защитные реакции не дают ему возможности
нанести повреждение организму (порог в каждом
случае индивидуален). Если же порог превышен, в
реакцию включаются приспособительные, адаптивнокомпенсаторные механизмы, осуществляющие
перестройку организма для борьбы с патогенным
фактором.
16.
• Приспособительные реакции конкретногоорганизма зависят от того, насколько защитные
механизмы приспособлены к взаимодействию с
патогеном.
• Выделяют следующие типы защитноприспособительных механизмов:
1) морфологические:
барьерные мембраны, ограждающие
защищаемые клетки, ткани или органы;
пролиферация (восстановление) клеток
пораженной ткани;
гиперплазия, т. е. количественное увеличение
клетки или ткани против нормы;
17.
2) физиологические:активация обменных процессов,
образование новых медиаторов, ферментов
или обменных циклов и дезактивация
существующих;
3) иммунологические клеточногуморальные системы, направленные на
защиту организма от воздействия других
биосистем.
18.
• Из всех типов защитно-приспособительныхмеханизмов наиболее важный ― иммунная
система. Хорошо работающая иммунная
система ― самый лучший гарант крепкого
здоровья. Это мощная внутренняя сила, которой
природа наградила все живые существа.
• Иммунная система ― организация тонкая: она
реагирует на мельчайшие изменения внутренней
и внешней среды организма.
• Давно подмечено, что человек, перенесший
опасную инфекционную болезнь, второй раз
обычно ею не заболевает.
• Невосприимчивость к повторному заражению
одной и той же инфекцией обусловлена
иммунитетом.
19.
1920.
• Иммунитет ― это невосприимчивостьорганизма к различным инфекционным
агентам, а также продуктам их
жизнедеятельности, веществам и
тканям, которые обладают
чужеродными антигенными
свойствами (например, ядам животного и
растительного происхождения).
• Однажды переболев, наш организм
запоминает возбудителя болезни, поэтому
в следующий раз заболевание протекает
быстрее и без осложнений.
21.
• Однако после длительных заболеваний,оперативных вмешательств, при
неблагоприятной экологической обстановке, в
состоянии стресса иммунная система может
давать сбои.
• Снижение иммунитета проявляется частыми
и длительными ОРВИ, хроническими
инфекционными заболеваниями
(тонзиллитом, фурункулезом, гайморитом,
кишечными инфекциями), постоянной
повышенной температурой и т.п.
22.
ИММУНИТЕТЭлиминация живых тел и веществ, несущих
признаки генетической чужеродности (АГ)
Экзогенные
антигены
Микроорганизмы:
бактерии, грибы,
простейшие, вирусы
Эндогенные
антигены
Клетки,
модифицированные вирусами,
ксенобиотиками, старением,
опухолевые клетки и др.
23.
ИММУНИТЕТ― способ защиты организма от живых тел и веществ,
которые несут в себе признаки генетически чужой
информации.
• Наиболее древний и стабильный механизм
взаимодействия ткани с любыми внешними
повреждающими факторами среды (АГ) – это фагоцитоз.
Фагоцитоз в организме осуществляется специальными
клетками – макрофагами, микрофагами и моноцитами
(клетками–предшественниками макрофагов).
• Это сложный многоступенчатый процесс захвата и
уничтожения всех попавших в ткани чужеродных для них
микрообъектов, не трогая собственные ткани и клетки.
Фагоциты, перемещаясь в межклеточной жидкости, при
встрече с АГ захватывают его и переваривают до того,
как он контактирует с клеткой.
24.
2425.
Фагоцитарный иммунитетв 1883 году открыл
ИЛЬЯ ИЛЬИЧ МЕЧНИКОВ ―
Нобелевская
премия!
(1845 ― 1916)
26.
Фагоцитоз• был положен в основу разработанной И.И.Мечниковым
теории фагоцитарной защиты организма от
болезнетворных микробов. Установлено широкое
участие макрофагов в различных иммунологических
процессах:
распознавании антигена,
регуляции иммунных процессов,
осуществлении иммунного надзора → в распознавании
и разрушении единичных измененных клеток
собственного организма, в том числе опухолевых,
в регенерации различных тканей,
в воспалительных реакциях.
• Макрофаги также вырабатывают различные вещества,
оказывающие противоантигенное воздействие.
27.
• Сцена как из научной фантастики ― клеточноерасширение макрофага, который потянулся, чтобы
захватить бактерию (псевдоподия или ложноножка)
28.
• Первый шаг в фагоцитозе заключается в том,что макрофаг распространяет псевдоподии
от своей одноклеточной формы, чтобы
захватить бактерии.
29.
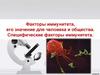
• Макрофаг пытается уничтожить компонентывторгающихся клеток
30.
• Бактерии захвачены ― в мембране макрофага.31.
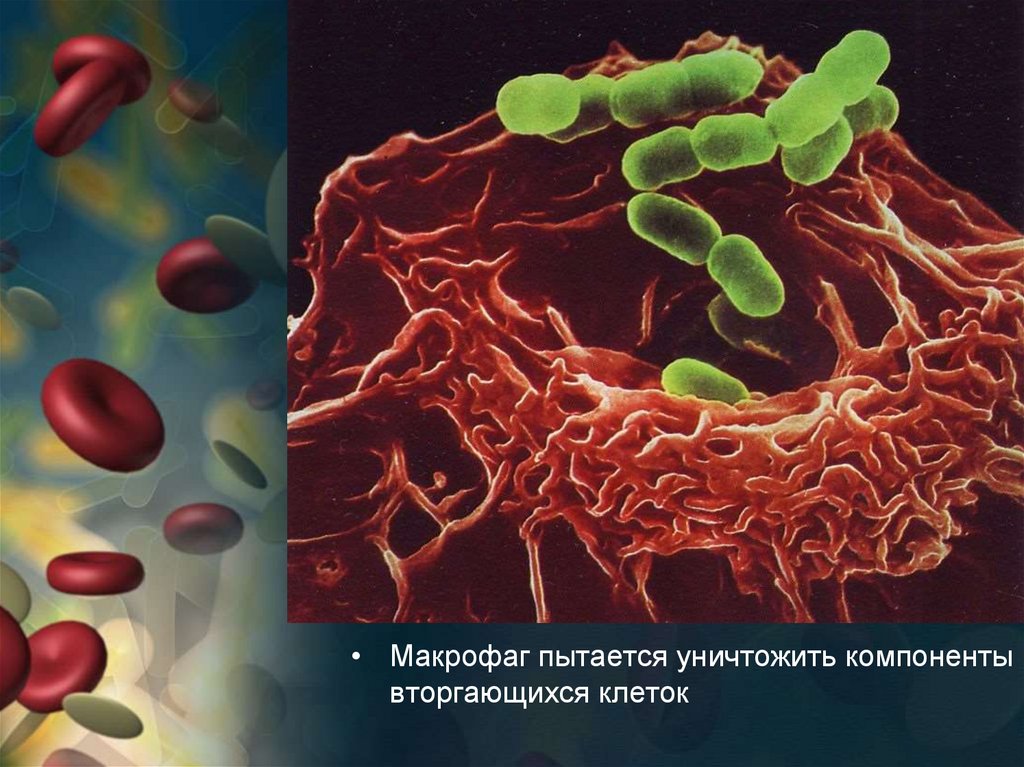
• Макрофаги(x18000),
пытаются
поглотить
капли
масла
32.
• Одна из самых больших неорганических угрозчеловечества, асбестовые волокна,
охваченные макрофагом, который, вероятно,
погибнет от трудно перевариваемой пищи.
33.
Фагоцитоз• Фагоцитоз включает несколько стадий:
1) направленное движение фагоцита к
чужеродному для ткани объекту;
2) прикрепление фагоцита к нему;
3) распознавание микроба или антигена;
4) поглощение его клеткой фагоцита (собственно
фагоцитоз);
5) умерщвление микроба с помощью ферментов,
выделяемых клеткой;
6) переваривание микроба (завершенный
фагоцитоз).
34.
Завершенный фагоцитоз• Но в некоторых случаях фагоцит не может умертвить
определенные виды микроорганизмов, которые даже
способны размножаться в нем (незавершенный фаг-з).
35.
• Именно поэтому фагоцитоз не всегда можетобеспечить защиту организма от повреждения.
• Способствует фагоцитозу наличие в организме
систем циркуляции межклеточной жидкости.
• Сосудистый транспорт межклеточной жидкости
обусловливает:
возможность более быстрой концентрации
фагоцитов в местах проникновения
повреждающего фактора в ткань;
ускорению и направленности действия
химических веществ (медиаторов),
привлекающих фагоциты в нужную точку.
36.
NB!• Таким образом, воспалительный
процесс — это местный компенсаторный
механизм, обеспечивающий
восстановление поврежденного
участка ткани, измененного в результате
взаимодействия с повреждающим
фактором любой природы.
37.
• В процессе эволюции появиласьспецифическая система защиты, которая в
отличие от локальной защиты при фагоцитозе
действует на уровне целостного организма.
• Это система иммунитета, направленная на
защиту организма от повреждающих факторов
биологического происхождения.
• Система иммунитета защищает
жизнеобеспечение всего организма, является
высоко-специализированной системой,
которая включается тогда, когда локальные
неспецифические механизмы защиты
исчерпывают свои возможности.
38.
• Изначально иммунная система предназначена дляконтроля над размножением большого количества
различных по структуре и функциям
дифференцированных клеток, а также для защиты
клеток от мутаций.
• Так возник механизм, предназначенный для
распознавания и уничтожения клеток, генетически
отличающихся от клеток организма, но настолько
схожих с ними, что механизм фагоцитоза не мог их
распознать и уничтожить, не дать им размножаться.
• Механизм иммунитета, сложившийся первоначально
для внутреннего контроля над клеточным составом
организма, в силу своей эффективности в
дальнейшем использовался против внешних
повреждающих факторов белковой природы: вирусов,
бактерий и продуктов их жизнедеятельности.
39.
• С помощью системы иммунитета формируются игенетически закрепляются:
1) реактивность организма к тем видам микробов, к
взаимодействию с которыми он не приспособлен,
2) отсутствие реакции тканей и органов к другим
видам микробов.
• Возникают видовая и индивидуальная формы
иммунитета. Обе формы могут быть:
абсолютными ─ организм и микроб
НЕ взаимодействуют непосредственно ни при
каких условиях (человек не заболевает собачьей
чумкой),
относительными ─ взаимодействие между ними
может произойти при определенных условиях,
ослабляющих иммунитет организма:
переохлаждении, голоде, перегрузке и т. п.
40.
• Функция иммунной системы заключается в том,чтобы компенсировать недостаточность
неспецифических форм защиты организма от АГ в
тех случаях, когда фагоциты не могут уничтожить
АГ, если он имеет специфические защитные
механизмы.
• Так, некоторые бактерии и вирусы могут
размножаться внутри поглотившего их макрофага,
на них в этом состоянии не действуют
антибактериальные препараты.
• Поэтому иммунная система отличается большой
сложностью, дублированием функций отдельных
элементов, включает клеточные и гуморальные
элементы, предназначенные для точного
опознания и уничтожения микробов и продуктов
их жизнедеятельности
41.
• Система является саморегулирующейся. →• Она реагирует не только на количество
микробов, но последовательно включая
свои элементы, повышает
чувствительность неспецифических
уровней защитной реакции и прекращает
иммунную реакцию в нужный момент.
• Таким образом, формирование в ходе
эволюции и всемерное совершенствование
специальной противобелковой обороны
играет огромную роль в охране здоровья
организма.
42.
• Белок ― носитель жизни. Поддержание чистотысвоей белковой структуры ― долг живой системы.
• Эта защита, поднятая в живом организме на
высочайший уровень, включает два вида защитных
сил:
1) врожденный иммунитет, носящий
неспецифический характер, т. е. направленный
вообще против любого чужеродного белка. Из
огромной армии микробов, постоянно попадающих в
наш организм, только ничтожной части удается
вызвать заболевание;
2) приобретенный иммунитет ― поразительный
защитный механизм, возникающий при жизни данного
организма и носящий специфический характер, т. е.
направленный на один конкретный чужой белок.
Иммунитет, возникший после перенесения
определенной болезни, наз. приобретенным.
43.
44.
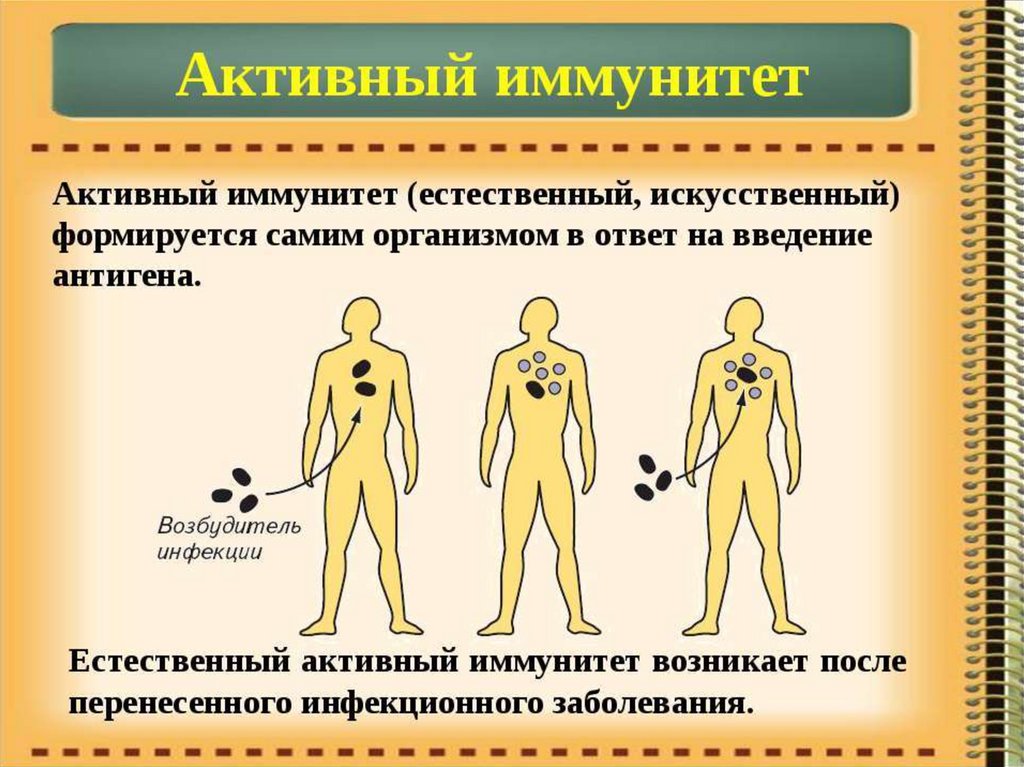
45.
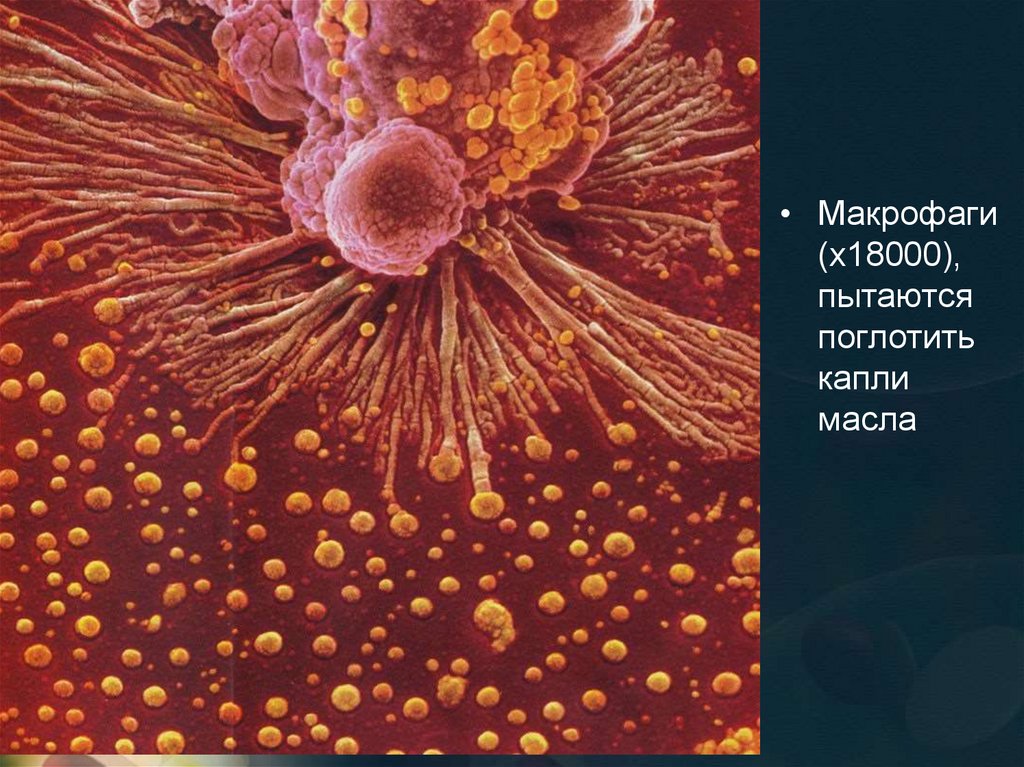
Формы иммунитетанеспецифический
специфический
макрофаги
лейкоциты
лимфоциты
антитела на
антигены
Фагоцитоз
(И.И.Мечников)
нейтрализация
46.
• Специфический иммунитет обеспечиваетсямеханизмами иммунитета и имеет
гуморальные и клеточные основы.
Чужеродные частицы ― АГ могут поселяться в
организме человека, проникнув в него через
кожу, нос, рот, глаза, уши.
• К счастью, большинство этих «врагов» при
попытке проникнуть внутрь организма
погибают. Организм человека содержит
большое количество желез и тканей, которые
по команде ЦНС вырабатывают так
называемые иммунокомпетентные клетки.
• Они же, находясь в состоянии постоянной
«боевой готовности», выполняют
определенные функции.
47.
• Иммунная система в организме человекапризвана осуществлять иммунологический
надзор ― контроль генетического
постоянства внутренней среды организма.
Главные функции иммунной системы
распознавание «своего» от «чужого»;
нейтрализация и элиминация из организма
генетически чужеродных высокомолекулярных
соединений (белки, полисахариды и др.)
48.
Иммунологическая реактивность– способность организма отвечать на иммунные
стимулы изменением жизнедеятельности.
Иммунологическую реактивность
обеспечивают:
неспецифические факторы защиты
(разнообразные по происхождению, строению и
механизмам функционирования клетки и
гуморальные вещества);
специализированная система клеток, тканей и
органов – иммунная система
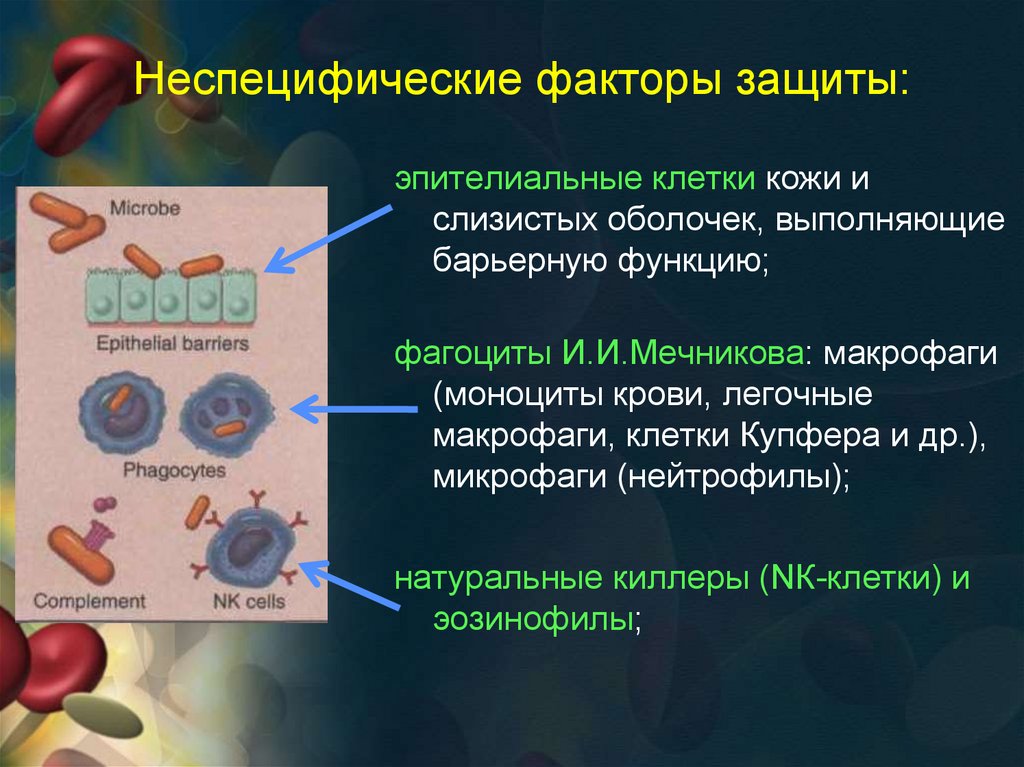
49.
Неспецифические факторы защиты:эпителиальные клетки кожи и
слизистых оболочек, выполняющие
барьерную функцию;
фагоциты И.И.Мечникова: макрофаги
(моноциты крови, легочные
макрофаги, клетки Купфера и др.),
микрофаги (нейтрофилы);
натуральные киллеры (NК-клетки) и
эозинофилы;
50.
Неспецифические факторы защиты:• гуморальные вещества, продуцируемые
клетками иммунной системы и другими
клетками:
* система комплемента;
* ферменты (лизоцим, пероксидаза и др.);
* интерфероны;
* С-реактивный белок;
* ингибиторы ферментов бактериальных
клеток;
* ингибиторы вирусов;
* бактерицидные вещества
(лактоферрин, молочная кислота и др.)
51.
Схема неспецифической защиты:ПЕРВАЯ ЛИНИЯ:
кожа → большинство возбудителей погибают
из-за прямого губительного действия
молочной кислоты и жирных кислот в секрете
потовых и сальных желез (низкая рН);
слизистые оболочки, контактирующие с
окружающей средой, покрыты слоем слизи,
которая не дает бактериям и вирусам
прикрепиться к клеткам эпителия. Они
удаляются со слизью за счет движения
ресничек, при чихании и кашле. Сама слизь
содержит много бактерицидных веществ.
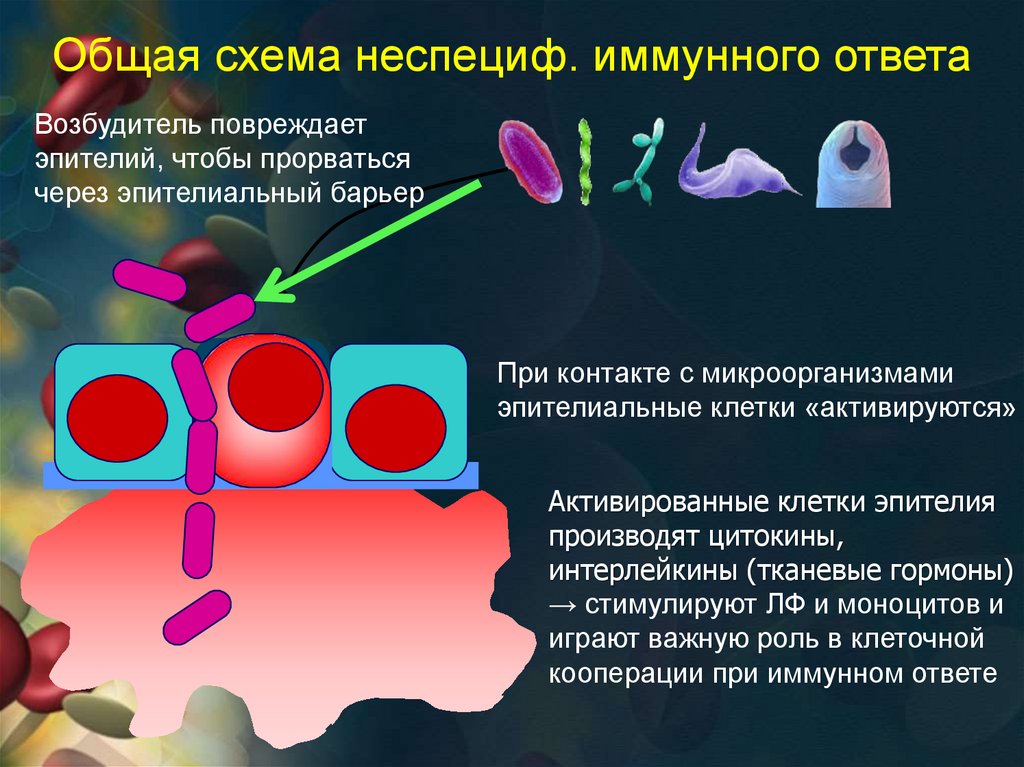
52.
Общая схема неспециф. иммунного ответаВозбудитель повреждает
эпителий, чтобы прорваться
через эпителиальный барьер
При контакте с микроорганизмами
эпителиальные клетки «активируются»
Активированные клетки эпителия
производят цитокины,
интерлейкины (тканевые гормоны)
→ стимулируют ЛФ и моноцитов и
играют важную роль в клеточной
кооперации при иммунном ответе
53.
Первая линия защиты (обороны)54.
Схема неспецифической защиты:ВТОРАЯ ЛИНИЯ:
растворимые бактерицидные факторы:
Система комплемента обеспечивает:
– реакции адгезии;
– образование биологически активных в-в;
– повреждение мембран микробных клеток;
– усиление иммунных реакций → в
комплексе с АТ убивает и лизирует клетки,
активирует все виды иммунокомпетентных
клеток.
55.
- Альтернативный путь активации. Его инициируют непосредственно поверхностные молекулы клеток микроорганизмов [факторы альтернАктивация комплемента происходит двумя
путями:
• Альтернативный путь активации. Его
инициируют непосредственно
поверхностные молекулы клеток
микроорганизмов.
* пропердин – принимает участие в
альтернативном пути активации
комплемента
56.
Комплемент усиливает фагоцитозВозбудитель →
контактирует с белками
плазмы крови
Фрагменты комплемента
опсонируются на
поверхности возбудителя
Комплемент активируется
возбудителем
Фагоцитоз опсонированных
возбудителей
57.
Схема неспецифической защиты:ВТОРАЯ ЛИНИЯ:
растворимые бактерицидные факторы:
* интерфероны (α, β, γ, δ) → препятствуют
проникновению вирусов в здоровые клетки;
* лизоцим → разрушает клеточную стенку
бактерий);
* белки острой фазы → в плазме крови при
повреждении тканей или внедрении
микроорганизмов (в т.ч. они активируют
комплемент):
– С-реактивный белок;
– альфа-1-антитрипсин;
– церуллоплазмин и др;
58.
Схема неспецифической защиты:ВТОРАЯ ЛИНИЯ:
натуральные киллеры (особые фагоциты)
и эозинофилы: они НЕ поглощают
объекты, подлежащие уничтожению, а,
нападая на них, выделяют биологически
активные вещества, разрушающие объекты
нападения (натуральные киллеры →
пораженные вирусами клетки; эозинофилы
→ гельминтов)
Неспецифические факторы защиты
являются филогенетически более
древними и обеспечивают первый
уровень защиты организма от различных
неблагоприятных воздействий.
59.
60.
Cпецифическая иммуннаяреактивность
• Комплекс факторов специфической
защиты включается в работу только после
контакта с генетически чужеродным
материалом, в результате чего
формируется специфический иммунный
ответ.
• Ее обеспечивает специализированная
система клеток тканей и органов, которую
называют иммунной системой.
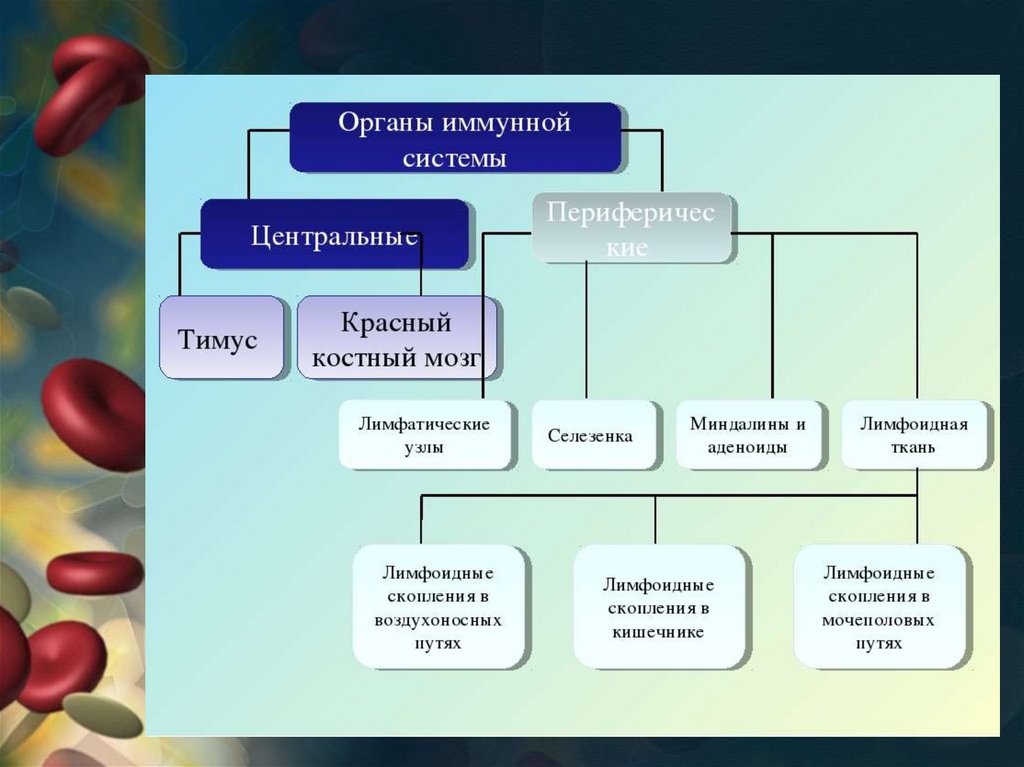
61.
ИММУННАЯ СИСТЕМА― это совокупность всех
лимфоидных органов и
скоплений лимфоидных
клеток организма.
К ней относятся:
вилочковая железа (тимус);
селезенка;
лимфатические узлы;
групповые лимфатические
фолликулы (пейеровы бляшки) и др.
лимфоид. скопления (GALT);
лимфоциты костного мозга и
периферической крови.
62.
• Общая масса этой «диффузнойсистемы» у взрослого человека
составляет ~ 1,5-2 кг, общее число
лимфоидных клеток – 1012.
• Иммунная система – это такая же
самостоятельная система
организма, как и все остальные, но
она имеет ряд особенностей,
которые существенно отличают ее от
других физиологических систем
организма.
63.
Особенности иммунной системы:1. Иммунная система дискретна, т.к.
располагается в разных частях тела.
2. Клетки иммунной системы постоянно
рециркулируют в организме в системе
кровотока.
3. Иммунная система обладает уникальной
способностью вырабатывать
специфические антитела –
иммуноглобулины (Ig), различные по
своей специфике в отношении каждого
антигена.
64.
Основная функция иммунной системы― распознавание и уничтожение
проникших извне или
находящихся в организме
генетически чужеродных клеток,
включая микроорганизмы, ткани,
белки и др., т.е. – обеспечение
иммунитета
65.
ИММУНИТЕТ― это способ защиты
организма от живых тел и
веществ, несущих на себе
признаки генетической
чужеродности
Р.В.Петров
66.
6667.
68.
Центральный орган иммунной системы –вилочковая железа (thymus)
• оказывает регулирующее влияние на функцию
всех органов иммунной системы.
• Он формируется раньше других органов
иммунной системы (на 6-й неделе беремен-ти),
но уже с 15 лет подвергается обратному
развитию. Тимус невелик ― наибольший (~25 г)
– он во время полового созревания.
К 60 годам значительно уменьшается и весит
всего 6 г: у взрослых почти полное замещение
его жировой клетчаткой.
• Иногда тимус не претерпевает возрастной
инволюции → при снижении активности коры
надпочечников и недостатке гормонов. Тогда
развиваются: восприимчивость к инфекциям и
интоксикациям, развитие опухолевых
процессов.
69.
ТИМУС• Чем более длительно
функционирует тимус, тем
дольше живет организм.
• Главное ― тимус – место
созревания и дифференцировки
Т- лф, затем заселяющих
периферические органы
иммунитета.
• В вилочковой железе наряду с
образованием Т-лф
продуцируются тимозин и
тимопоэтин – гормоны,
обеспечивающие
дифференцировку Т-лф и
играющие определенную роль в
клеточных иммунных реакциях .
70.
7071.
Лимфоузлы• Лимфоузлы – периферические органы иммунной
системы, которые расположены по ходу
лимфатических сосудов.
• Главное назначение – задержание и
предотвращение распространения АГ, что
осуществляется за счет Т- и В-лф. Лимфоузлы
содержат преимущественно Т-лф (до 65 %), а В-лф
синтезируют АТ, когда иммунная система только
созревает, особенно у детей первых лет жизни.
• Лимфоузлы ― своеобразный фильтр для
микроорганизмов, переносящихся лимфой.
Микроорганизмы проходят через кожу или слизистые
оболочки → в лимфатические сосуды → по ним
проникают в лимфатические узлы, где
задерживаются и уничтожаются.
72.
ЛимфоузлыФункции лимфатических узлов:
1) барьерная – они первыми реагируют на контакт с
повреждающим агентом;
2) фильтрационная – в них осуществляется задержка
проникающих с током лимфы микробов, инородных
частиц, опухолевых клеток;
3) иммунная – связана с выработкой в лимфатических
узлах В-лимфоцитов и иммуноглобулинов;
4) синтетическая – синтез специального
лейкоцитарного фактора, который стимулирует
размножение клеток крови;
5) обменная – лимфатические узлы принимают участие
в обмене жиров, белков, углеводов и витаминов.
73.
Лимфоидная ткань, ассоциированнаясо слизистыми оболочками
• располагается под слизистой оболочкой.
• Сюда относятся аппендикс, лимфоидное
кольцо, аденоиды, лимфатические фолликулы
кишечника. Скопления лимфоидной ткани в
кишечнике – пейеровы бляшки.
• Эта лимфоидная ткань является барьером на
пути проникновения микробов через слизистые
оболочки.
74.
• Функции лимфоидных скоплений в кишечнике иминдалинах:
1) распознавательная – общая площадь поверхности
миндалин у детей очень большая (~ 200 см2). Здесь
происходит постоянное взаимодействие АГ и клеток
иммунной системы.
Именно отсюда информация о чужеродном агенте
следует в центральные органы иммунитета: тимус и
костный мозг;
2) защитная – на слизистой оболочке миндалин и
пейеровых бляшек в кишечнике, в аппендиксе
расположены Т- и В-лф, лизоцим и др. вещества,
обеспечивающие защиту. Кроме того, в пейеровых
бляшках синтезируются АТ, особенно SIgA,
обеспечивающие местный иммунитет слизистых
оболочек.
75.
Селезенка• Селезенка имеет строение, близкое к строению
вилочковой железы. В селезенке образуются
гормоноподобные вещества, участвующие в
регуляции деятельности макрофагов. Здесь
происходит фагоцитоз поврежденных и старых
эритроцитов.
• Функции селезенки:
1) синтетическая – именно в селезенке
осуществляется синтез Ig классов М и G в ответ на
попадание АГ в кровь или лимфу. В ткани селезенки
содержатся Т- и В-лф (до 65% В-лф, → синтез АТ)
2) фильтрационная – разрушение и переработка
чужеродных для организма в-в, поврежденных
клеток крови, красящих соединений и чужеродных
белков.
76.
Выделительная система• Благодаря ей организм очищается от микробов,
продуктов их жизнедеятельности и токсинов.
• Нормальная микрофлора организма ―
совокупность микроорганизмов, населяющих кожу и
слизистые оболочки здорового человека. Эти микробы
обладают способностью противостоять защитным
механизмам самого организма, но они НЕ способны
проникать в ткани.
• Большое влияние на интенсивность иммунного ответа
в органах пищеварения оказывает нормальная
микрофлора кишечника. Она подавляет развитие
болезнетворной микрофлоры.
• Нормальная микрофлора влагалища ―
молочнокислые бактерии, которые создают кислую
среду, препятствующую развитию патогенной
микрофлоры.
77.
Выделительная система• Внутренняя среда отграничена от внешнего мира
кожей и слизистыми → механический барьер. В
эпителии кожи и слизистых клетки очень прочно
связаны между собой межклеточными контактами.
• Мерцательный эпителий дыхательных путей
удаляет бактерии и частицы пыли благодаря
колебанию ресничек (мукоциллиарный клиренс).
• В коже ― сальные и потовые железы. В их
секрете содержатся молочная и жирная кислоты →
понижают pH кожи. Тормозят размножение
бактерий перекись водорода, аммиак, мочевина,
желчные пигменты, содержащиеся в поте.
78.
Выделительная система• Слезные, слюнные, желудочные, кишечные и
прочие железы, секреты которых выделяются
на поверхность слизистых оболочек, интенсивно
борются с микробами:
1) они их просто механически смывают;
2) некоторые секреторные жидкости имеют такой
pH, который повреждает или разрушает
бактерии;
3) в слюнной и слезной жидкостях содержится
фермент лизоцим, который непосредственно
разрушает бактерии.
79.
Красный костный мозг– источник самоподдерживающейся
популяции мультипотентных стволовых
клеток и поставщик полипотентных
стволовых клеток для всех ростков
кроветворения и лимфопоэза.
• Стволовые клетки, выходя из костного
мозга в кровоток и циркулируя в организме,
поступают в тимус и др. лимфоидные
органы, в которых происходит их
лимфопоэтическая дифференцировка с
образованием Т- и В-лимфоцитов.
80.
ЛИМФОЦИТЫ• Лимфоциты – главные фигуры в
иммунологическом надзоре. В костном мозге
предшественники лимфоцитов делятся на две
крупные ветви.
• Одна из них (у млекопитающих) заканчивает
свое развитие в костном мозге, а у птиц – в
специализированном лимфоидном органе –
бурсе (сумке) Фабрициуса. Это В-лимфоциты.
Их 20 – 30%.
81.
Лекция 3 на тему:Лектор
Третьякевич Зоя Николаевна,
доктор мед. наук, профессор
82.
Т-лимфоциты• Другая часть лимфоцитов из костного мозга
переселяется в тимус. Эта ветвь – Т-лф.
В норме их 50 – 60%.
• Это популяция лимфоцитов,
дифференцировка и созревание которых
зависят от тимуса. Они отличаются от др.
лимфоцитов наличием на поверхности
мембран рецепторов, которых нет на других
популяциях клеток, а также
функционированием.
• На мембране Т-лф – рецепторы, связывающие
эритроциты барана, а также рецепторы к
антигенным детерминантам CD2+ и CD3+.
83.
Т-имфоциты• В тимусе происходит селекция
Т-лф, имеющих рецепторы к
собственным тканям.
• Проникая из костного мозга в
тимус, стволовая клетка под
влиянием гормонов превращается
сначала в тимоцит (клетку –
предшественницу Т-лф), а затем,
проникая в селезенку или
лимфатические узлы,
превращается в зрелый,
иммунологически активный Тлимфоцит.
• После завершения развития в
тимусе часть зрелых Т-лф
продолжает находиться в
мозговом слое.
84.
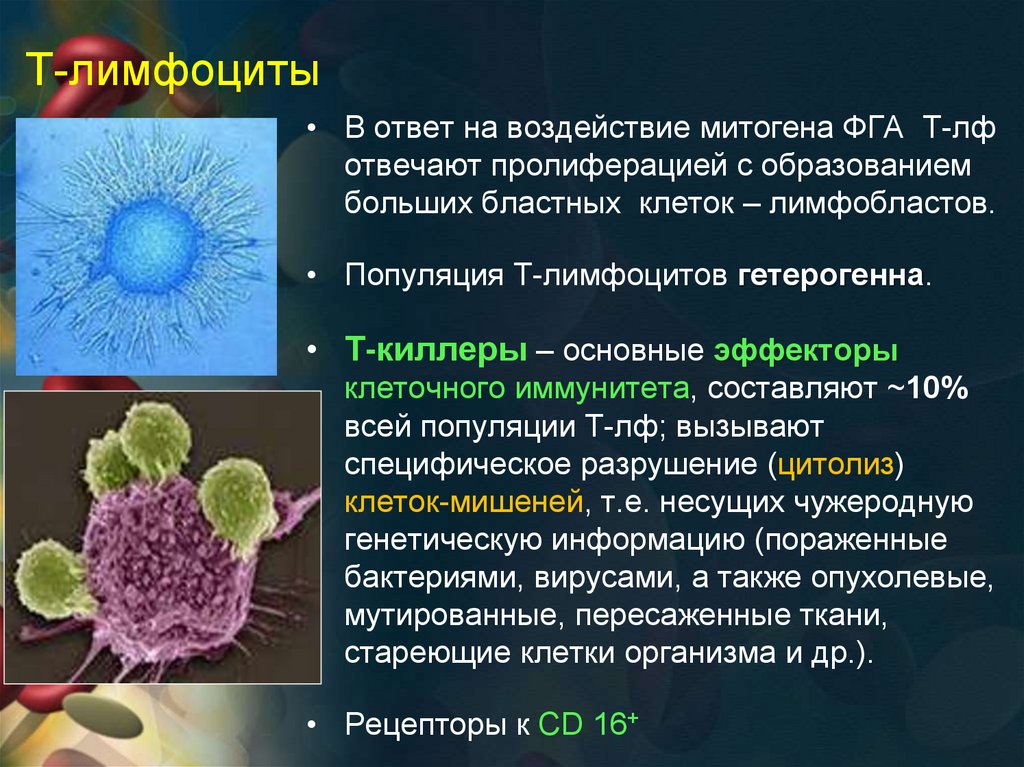
Т-лимфоциты• В ответ на воздействие митогена ФГА Т-лф
отвечают пролиферацией с образованием
больших бластных клеток – лимфобластов.
• Популяция Т-лимфоцитов гетерогенна.
• Т-киллеры – основные эффекторы
клеточного иммунитета, составляют ~10%
всей популяции Т-лф; вызывают
специфическое разрушение (цитолиз)
клеток-мишеней, т.е. несущих чужеродную
генетическую информацию (пораженные
бактериями, вирусами, а также опухолевые,
мутированные, пересаженные ткани,
стареющие клетки организма и др.).
• Рецепторы к CD 16+
85.
• T-клеткикиллерыокружили
большую
раковую
клетку
86.
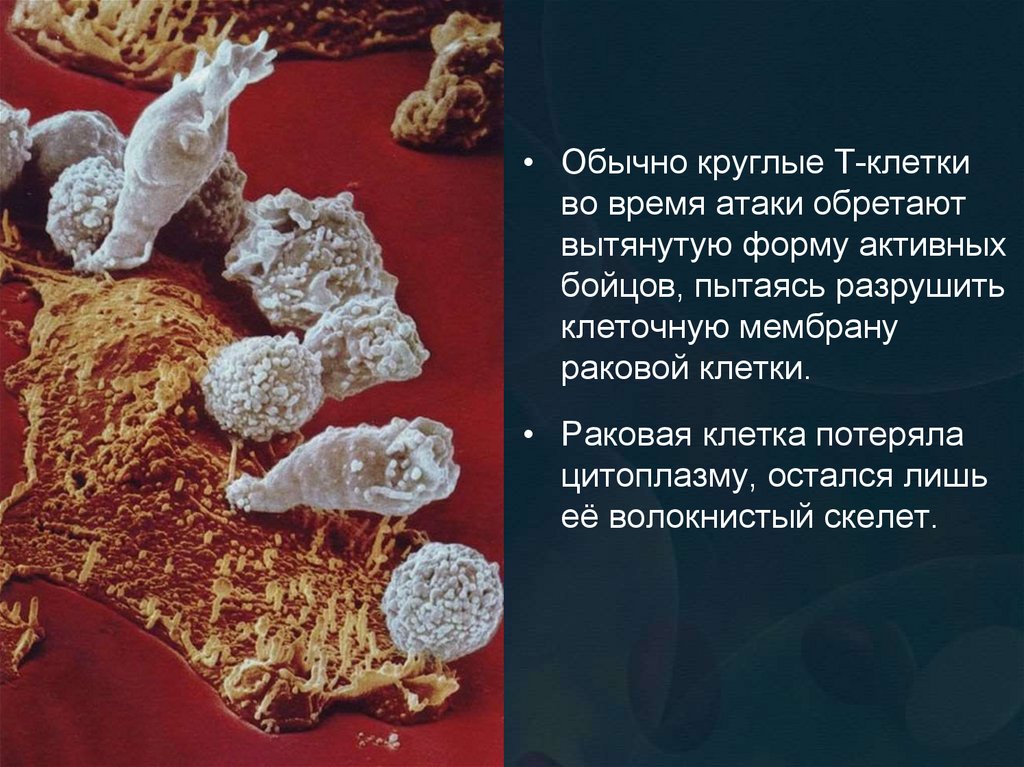
• Обычно круглые Т-клеткиво время атаки обретают
вытянутую форму активных
бойцов, пытаясь разрушить
клеточную мембрану
раковой клетки.
• Раковая клетка потеряла
цитоплазму, остался лишь
её волокнистый скелет.
87.
Регуляторную функцию выполняют:Т-хелперы / индукторы ─ организуют иммунный
ответ, распознавая АГ и воздействуя на В-лф на
расстоянии → давая сигнал для синтеза АТ против
появившегося в организме АГ. Они секретируют
интерлейкин-2, воздействующий на В-лф, и γ-ИФ
(лимфокины).
В периферической крови их до 60–70% общего
числа Т-лф. Рецепторы к CD4+.
Т-хелперы (CD4) распознают антиген в комплексе с
локализованными на мембране клеток-мишеней
антигенами МНС II класса.
Т-хелперы, выделяя интерлейкины, стимулируют
пролиферацию и дифференцировку Т- и Влимфоцитов.
88.
Среди них различают:Т-хелперы первого типа (Th1), выделяющие
ИЛ-2, ИЛ-12, ИФН-γ, ФНО-α – обеспечивают
реакции Т-клеточного иммунитета.
Т-хелперы второго типа (Th2),
секретирующие ИЛ-4, ИЛ-5, ИЛ-10, ИЛ-13 –
стимулируют синтез антител, т.е.
гуморальное звено иммунной системы.
89.
Т-супрессоры / цитотоксики ─ограничивают силу иммунного ответа,
контролируют активность Т-киллеров.
При небходимости блокируют
деятельность Т-хелперов и В-лф,
подавляя избыточный синтез АТ,
которые могут вызывать аутоиммунную
реакцию, т. е. обратиться против
собственных клеток организма.
Т-супрессоры составляют 18–20% от Тлф периферической крови. Рецепторы к
CD8+.
90.
• В отличие от В-лф, Т-лф (в основном Т-хелперы/индукторы) при помощи своих рецепторов
распознают не только чужое, но и измененное
свое, т. е. чужеродный АГ должен быть
представлен ― чаще всего макрофагами в
комплексе с собственными белками организма.
• Иммунорегуляторный индекс (ИРИ)
CD4+/CD8+ = 1,5―2,0
• ТГЗТ – эффекторы реакций
гиперчувствительности замедленного типа — Тлф, которые взаимодействуют с АГ →
сенсибилизированные, выделяют растворимые
факторы — лимфокины, которые имеют
существенное значение для проявления и
регуляции клеточных иммунных реакций.
91.
• Кроме четырех основных видов, существуют идругие виды Т-лф, в том числе Т-лф
иммунологической памяти, сохраняющие и
передающие информацию об АГ.
• При повторной встрече с этим АГ они
обеспечивают его распознавание и тип
иммунного ответа.
• Т-лф, выполняя функции клеточного иммунитета,
кроме того, облегчают и направляют действие
неспецифической системы: синтезируют и
секретируют :
медиаторы (лимфокины), которые активируют
или замедляют деятельность фагоцитов,
медиаторы с цитотоксическим и
интерфероноподобным действиями.
92.
Схема трансформациииммунокомпетентных кллеток
93.
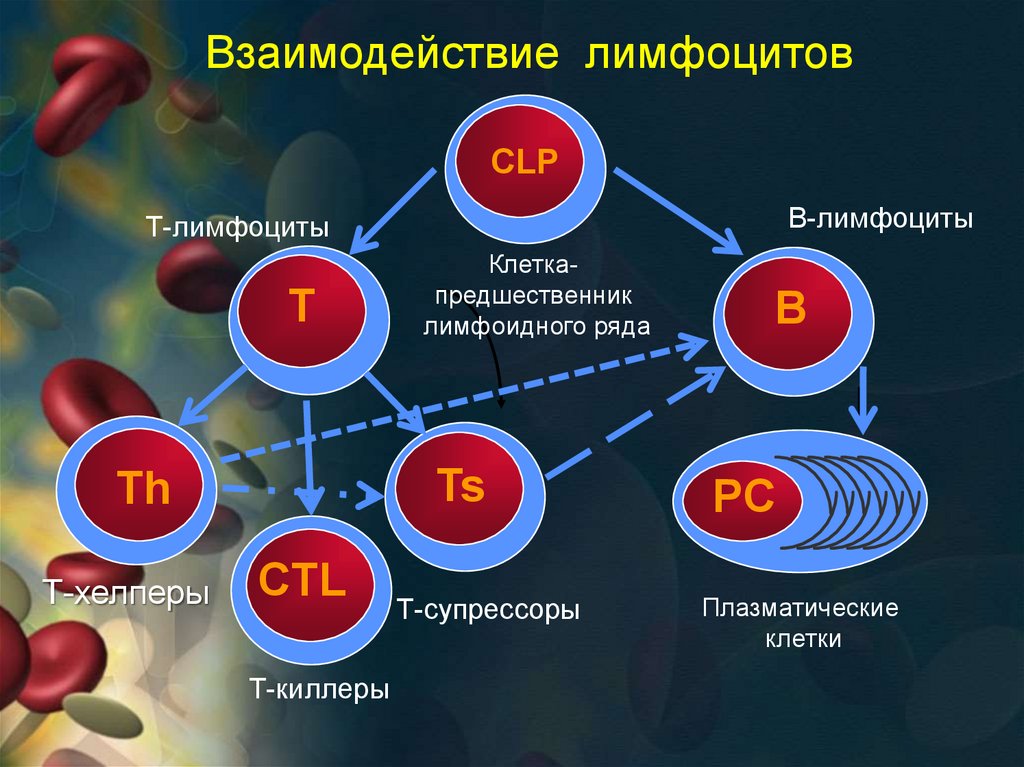
Взаимодействие лимфоцитовCLP
В-лимфоциты
Т-лимфоциты
T
Ts
Th
Т-хелперы
Клеткапредшественник
лимфоидного ряда
CTL
Т-киллеры
Т-супрессоры
B
PC
Плазматические
клетки
94.
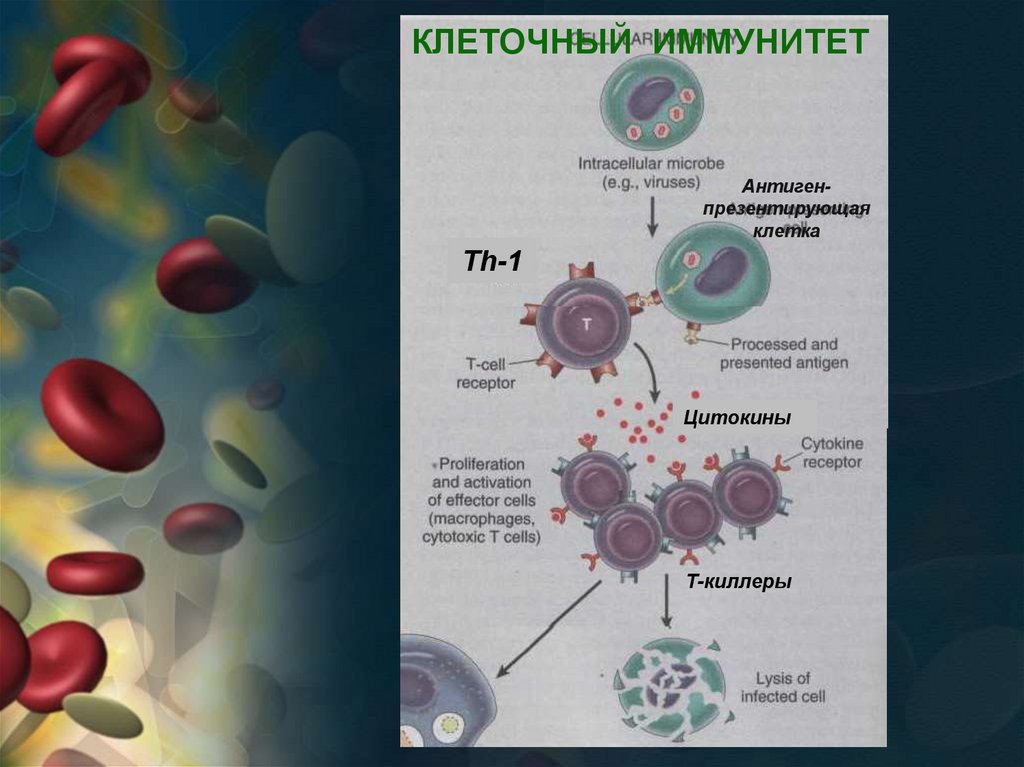
95.
КЛЕТОЧНЫЙ ИММУНИТЕТАнтигенпрезентирующая
клетка
Th-1
Цитокины
Т-киллеры
96.
Другие лейкоциты• Одно из названий нейтрофилов (микрофагоциты)
указывает на их возможность фагоцитировать
микроорганизмы, но в меньших количествах, чем это
делают макрофаги. Нейтрофилы защищают организм
от проникновения бактерий, грибов и простейших.
Они ликвидируют погибшие клетки тканей, удаляют
старые эритроциты и очищают раневую поверхность.
• При оценке развернутого анализа крови признаком
воспалительного процесса является сдвиг
лейкоцитарной формулы влево с увеличением числа
нейтрофилов.
• Эозинофилы принимают участие в уничтожении
паразитов (выделяют специальные ферменты,
которые оказывают на них повреждающее действие),
в аллергических реакциях.
97.
Макрофаги• Макрофаги (фагоциты) – «пожиратели» инородных
тел, самые древние клетки иммунной системы.
Происходят из моноцитов.
• Первые стадии развития они проходят в костном
мозге, а затем покидают его в виде моноцитов и
короткое время циркулируют в крови.
• Из кровяного русла они попадают во все ткани и
органы, где изменяют свою округлую форму
→дендритные клетки. Именно в таком виде они
приобретают подвижность и способны прилипать к
любым потенциально чужеродным телам.
• Они распознают некоторые чужеродные вещества и
сигнализируют о них Т-лф, а те в свою очередь – Влф → В-лф начинают продуцировать АТ против того
агента, о котором «сообщили» клетка-фагоцит и Т-лф
98.
• Оседлые макрофаги можно найти практически во всехтканях и органах человека, что обеспечивает
равносильный ответ иммунной системы на любой АГ,
попавший в организм.
• Макрофаги ликвидируют не только микроорганизмы и
чужеродные химические яды, но и погибшие клетки или
токсины (эндотоксины). Миллионы макрофагов
окружают их, поглощают и растворяют, чтобы вывести
из организма.
• Уменьшение фагоцитарной активности клеток крови
способствует:
1) развитию хронического воспалительного
процесса и возникновению агрессии против
собственных тканей (появлению аутоиммунных
процессов);
2) дисфункции разрушения и выведения из
организма иммунных комплексов.
99.
100.
Клетки иммунной системы и ихфункции
101.
В-лимфоциты –• Это самостоятельная популяция лимфоцитов,
созревание и дифференцировка которых
происходит в групповых лимфатических
фолликулах.
• Они несут на поверхности мембран IgG, IgА,
IgМ, IgE, IgD, рецепторы к CD19, 22+, С3компоненту комплемента. Пролиферация В-лф
в бластные клетки (лимфобласты) происходит
под действием липополисахарида,
выделенного из кишечной палочки или
сальмонелл.
• Покинув костный мозг, В-лф короткое время
циркулируют в кровяном русле, затем
происходит внедрение их в периферические
органы. Срок жизни этих В-лф – всего 7-10 дней.
102.
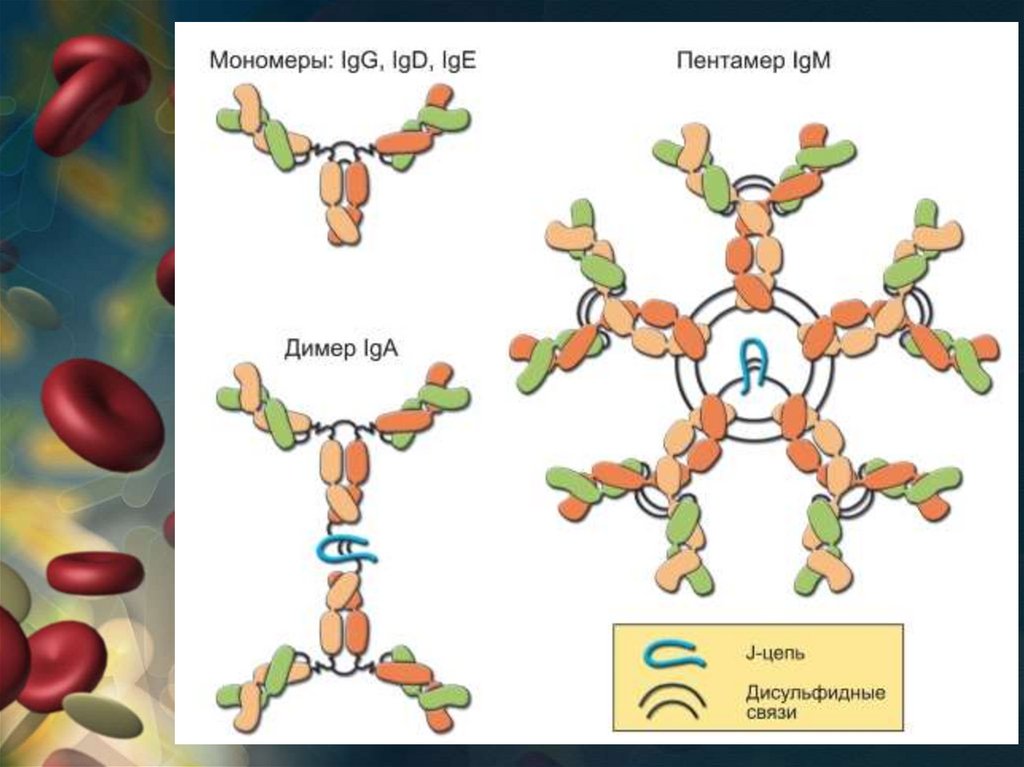
В-лимфоциты• Плазматические клетки способны
синтезировать иммуноглобулины, которые в
зависимости от физико-химических свойств
подразделяются на 5 классов: G, А, М, Е и D.
• Разнообразие В-лф формируется уже во время
внутриутробного развития, причем каждый из
них направлен против определенного
антигена.
• Первоначально В-лф синтезируют ІgM. При
созревании только 10% В-лф продолжают
синтезировать ІgM, 70% переключаются на
синтез IgG, а 20% – на синтез IgА.
103.
В-лф также состоят из нескольких субпопуляций:
1) В1-лф – предшественники плазмоцитов,
синтезирующие IgM без взаимодействия с Т-лф;
2) В2-лф – предшественники плазмоцитов,
синтезирующие Ig всех классов в ответ на
взаимодействие с Т-хелперами. Они
обеспечивают гуморальный иммунитет на АГ,
распознаваемые Т-хелперами;
3) В3-лф (К-клетки или В-киллеры), разрушают
клетки-АГ, покрытые АТ;
4) В-супрессоры тормозят функцию Т-хелперов,
5) В-лимфоциты памяти, сохраняя и передавая
память об АГ, стимулируют синтез
определенных Ig при повторной встрече с АГ.
104.
105.
• Особенность В-лф → их специализия наконкретных АГ.
• При взаимодействии В-лф с АГ, встреченным
впервые, образуются плазмоциты,
выделяющие АТ именно против этого АГ.
→ Образуется клон В-лф, ответственный за
реакцию с этим конкретным АГ.
• При повторной реакции размножаются и
синтезируют АТ только В-лф, направленные
против этого АГ. Другие клоны В-лф не
участвуют в реакции.
106.
• В-лф непосредственно не участвуют вборьбе с АГ.
• Под влиянием стимулов от фагоцитов и Тхелперов/индукторов они
трансформируются в плазмоциты, которые и
синтезируют АТ (Ig), обезвреживающие АГ.
NB!
• Иммуноглобулины – белки сыворотки
крови и других жидкостей организма,
которые действуют как АТ,
связывающиеся с АГ и
обезвреживающие их.
107.
ИММУНОГЛОБУЛИНЫ• Иммуноглобулины (АТ) представляют собой
белковую молекулу. Они соединяются с
чужеродным веществом и образуют иммунный
комплекс, циркулируют в крови и располагаются
на поверхности слизистых оболочек.
• Главная особенность АТ – способность
связывать строго определенный АГ. Например,
при кори в организме начинает вырабатываться
«противокоревой» иммуноглобулин, против
гриппа – «противогриппозный» и т. д.
• Выделяют 5 следующих классов
иммуноглобулинов: IgM, IgG, IgA, IgD, IgE.
108.
109.
IgM• IgM наиболее древние, являются
тяжелыми иммуноглобулинами.
Различают 2 субкласса — IgM1 и IgM2 –
низкоактивные, которые появляются
первыми после антигенного
раздражения.
• Период их полураспада у человека — 5
дней. Имеют 10 валентностей, составляя
10% всех классов иммунных глобулинов.
• К этому классу относятся АТ против
полисахаридов микроорганизмов и
вирусов, ревматоидный фактор и др.
• Содержание в сыворотке крови
0,5-2,0 г/л.
ММ 900 000 D.
110.
IgM• Синтезируется при первичном
иммунном ответе; повышение их титра
в крови говорит об остром
воспалительном процессе.
• IgM играют важную защитную роль при
проникновении бактерий в кровь на
ранних стадиях инфекции.
• IgM обладают способностью:
связывать комплемент;
преципитировать, агглютинировать и
лизировать АГ.
111.
IgG• IgG составляют основную массу
сывороточных Ig (~75%), ММ 150 000 D.
• Высокоактивные, синтезируются позднее IgM.
В основном образуются при повторной
иммунизации. Имеют 4 субкласса – IgG1, G2,
G3, G4, двухвалентны. Период полураспада
достигает 23 дней.
• Это АТ против АГ различной природы. Они в
основном выполняют антибактериальные
функции и образуют АТ против
полисахаридов бактериальных оболочек, а
также антирезусные АТ, обеспечивают
реакцию кожной чувствительности и
связывания комплемента.
• Они способны:
нейтрализовать токсины,
вызывать агглютинацию и лизис микробов. →
112.
IgG• Они образуют комплексы с АГ на
поверхности бактериальной клетки, затем
к ним присоединяются др. белки плазмы
(комплемент) → бак. клетка лизируется.
• IgG участвуют в возникновении некоторых
аллергических реакций.
• Являются главным защитным фактором у
ребенка первых недель жизни, т. к.
проходят через плацентарный барьер в
сыворотку крови плода. При естественном
вскармливании IgG из молока матери
через слизистую кишечника проникают в
кровь новорожденного.
• Концентрация в сыворотке крови в
пределах 8−16 г/л
113.
IgA также высокоактивны. Известны 2субкласса - IgA1 и IgA2. Образуются при
антигенном раздражении. Составляют от 15
до 30% всех иммуноглобулинов. их в
сыворотке крови 1,4 – 4,0 г/л (~1,5-2,5).
ММ 300 000 D. Имеют период полураспада
около 6 суток.
IgA
• Различают 3 типа IgA:
1 – сывороточный мономерный IgA,
составляющий до 80% всех IgA сыворотки,
2 – сывороточный димерный IgА,
3 – секреторный SIgA → Они относительно
независимы от сывороточной системы,
подавляют прикрепление микробов к слизистым
оболочкам, обладают мощной противовирусной
активностью.
.
114.
IgAIgA не преципитируют растворимые АГ, не
агглютинируют и не лизируют
корпускулярные АГ микроорганизмов.
• К IgA относятся АТ против вирусов,
инсулина (при сахарном диабете),
тиреоглобулина (при хроническом
тиреоидите).
• IgA, особенно SIgA, находятся на слизистых
оболочках. В слюне они составляют 85%
всех Іg. Именно SIgA :
активируют комплемент по
альтернативному пути, стимулируя
опсонизацию и лизис бактерий;
препятствуют адгезии бактерий к
эпителиальным клеткам → предупреждают
развитие хронич. местного воспаления.
115.
IgD• IgD содержатся в сыворотке крови в
концентрации 0,03 – 0,04 г/ л. (< 1%)
ММ 160 000 – 180 000 D.
Период полураспада 4 дня.
• Не связывают комплемента и не
связываются с тканями.
• Биологическая функция IgD НЕ выяснена.
Считают, что:
IgD служат Ig-рецепторами В-лимфоцитов
на одной из стадий их дифференцировки;
что они участвуют в аутоиммунных
процессах организма.
• Есть сведения об увеличении их при
некоторых инфекционных заболеваниях,
остеомиелите, бронхиальной астме и т. п.
116.
IgEIgE в сыворотке крови здорового
человека очень мало – 0,02- 0,5 г/л.
ММ 190 000 D.
Период полураспада 2,5 дня.
• IgE не связывают комплемента.
• Участвуют в реакциях ГНТ.
Могут связывать АГ на слизистых
оболочках → высвобождение гистамина
→ усиление проницаемости сосудов.
• Поэтому в норме IgE выполняют
защитную функцию в слизистых
оболочках.
117.
IgEIgE взаимодействуют с рецепторами,
которые располагаются на тучных
клетках и базофилах. В результате
происходит высвобождение гистамина и
др. медиаторов аллергии, вследствие
чего развивается аллергическая
реакция.
• При повторном контакте с аллергеном
взаимодействие IgE происходит на
поверхности клеток крови, →
анафилактическая аллергическая
реакция.
118.
• Если АГ проникают черезэпителиальный барьер → они
связываются со спец. IgЕ (реагины)
→ сигнал для дегрануляции тучных
клеток → они высвобождают
вазоактивные амины и
хемотаксические факторы.
Это вызывает приток в место
нахождения АГ циркулирующих
IgG, комплемента, нейтрофилов,
базофилов, действие которых
непосредственно направлено
против проникшего агента.
• Помимо реакций аллергии, IgE
принимают участие в обеспечении
противоглистного иммунитета.
119.
120.
121.
Современная схемаиммуногенеза
122.
НУЛЕВЫЕ КЛЕТКИ• Клетки, не имеющие маркеров Т- и В-лф открыты
в 1973 г.
• Их популяция является весьма разнородной, она
включает естественные киллеры (NK-клетки),
составляющие до 10% всех лимфоцитов крови.
Типичным маркером клеток-киллеров является
низкоаффинный рецептор Fc-фрагмента IgG
(CD16) и молекула адгезии СD56.
• Эти клетки играют важную роль в механизмах
врожденного иммунитета, уничтожая
злокачественные клетки, инфицированные
вирусами, и чужеродные клетки.
123.
НУЛЕВЫЕ КЛЕТКИ• Часть нулевых клеток является
антителозависимой популяцией с
киллерными функциями и свойствами
естественных или нормальных (натуральных)
киллеров.
• Антителозависимые киллеры (К- клетки)
встречаются в периферической крови
человека в количестве 1,5-2,5%.
Предназначены для уничтожения
злокачественных клеток, трансплантатов с
помощью IgG, выполняющих роль связующего
элемента между мишенью и киллером, а
также имеют некоторые другие качества.
124.
Вещества с защитными комплексами• Лизоцим присутствует во всех жидкостях
организма: в слезах, слюне, сыворотке крови.
Образуется клетками крови. Это
антибактериальный фермент, который способен
растворить оболочку микроба и вызвать его
гибель. При воздействии на бактерии лизоциму
необходима поддержка еще одного фактора
естественного иммунитета – системы комплемента.
• Комплемент ― группа белковых соединений,
участвующих в цепочке иммунных реакций.
Комплемент подготавливает бактерии к поглощению
макрофагами. Система комплемента состоит из
девяти групп сложных биохимических соединений.
По изменению концентраций какого-либо из них
можно судить о месте возможной патологии в звене
иммунитета.
125.
Вещества с защитными комплексами• Интерфероны обеспечивают
противовирусный иммунитет, повышают
устойчивость клеток к воздействию вирусов,
тем самым препятствуют их размножению в
клетках. Они продуцируются в основном
лейкоцитами и лимфоцитами.
• Результат их действия → образование
вокруг очага воспаления барьера из клеток,
не инфицированных вирусом.
126.
NB!• Таким образом, иммунная система ― это
очень сложная высокоспециализированная
система клеток и органов, которые выполняют
важную функцию защиты организма от
генетически чужеродных веществ и факторов.
• Функции иммунной системы у человека
основаны на взаимосвязанных, коррелятивных
взаимодействиях центральных и
периферических органов и клеток иммунной
системы.
127.
Основные свойства иммунной системыВысокая специфичность – селективное связывание
АТ с конкретным АГ (один АГ ─ одно АТ ─ один клон
Лф).
Высокая степень чувствительности ─
иммунокомпетентные клетки распознают АГ на уровне
отдельных молекул. Взаимодействие «АГ─АТ» ─ одна
из наиболее чувствительных биологических реакций.
Иммунологическая индивидуальность ─ для
каждого организма характерен свой генетически
контролируемый тип иммунного ответа. Основной
постулат иммунногенетики ─ «конкретность
иммунного ответа».
Клональный тип организации иммунокомпетентных
клеток ─ способность в пределах отдельного клона
отвечать только на одну антигенную
детерминанту.
128.
Иммунологическая память ─ способностьиммунной системы (клеток памяти) отвечать
ускоренно и усиленно на повторное введение
АГ.
Иммунная толерантность ─ специфическая
неотвечаемость на АГ, в т.ч. на аутоантигены.
Нарушение этого свойства —→ срыв
толерантности, развитие аутоиммунной
патологии.
Высокая способность ИС к регенерации ─
свойство ИС к поддержанию гомеостаза Лф за
счет пополнения пула «наивных» клеток и
контроля популяции клеток памяти. Нарушение
гомеостаза (лимфопения) лежит в основе
многих заболеваний, прежде всего
иммунодефицитных.
129.
Способность клеток ИС к рециркуляции ─перемещение клеток через кровеносную и
лимфатическую систему в норме и при патологии
(воспаление) —→ единство и целостность ИС.
«Двойное распознавание» антигена Тлимфоцитами ─ уникальная способность Т-лф
раcпознавать чужеродные антигенные пептиды в
ассоциации с собственными молекулами комплекса
HLA. Механизм высоко специализирован и
отсутствует в др. системах организма.
Неразборчивость иммунной системы ─
Иммунные механизмы не всегда работают во благо,
они могут оказывать иммуноаггрессивное действие
в собственном организме → аллергические, аутоиммунные, иммунокомплексные заболевания и др.
130.
Регуляторное действие на др. системы организма─ иммунная система через прямые межклеточные
контакты и опосредованно через огромное к-во
медиаторов (цитокины, хемокины, гормоны тимуса,
пептиды и др.) оказывает регуляторное
воздействие практически на все системы
организма. Нарушение этих механизмов лежит в
основе многих заболеваний человека, часто с
поражением органов и тканей, формально не
включаемых в ИС (поражение суставов, печени,
кожи, ЦНС и др.) Современная иммунология
большое внимание уделяет изучению роли
цитокинов в межсистемных регуляторных процессах.
• Таким образом, иммунная система, наряду с
нервной и эндокринной, является одной из
интегрирующих систем регуляции,
действующих на уровне целого организма.






















































































































 medicine
medicine