Similar presentations:
Вычисление массовой доли растворенного вещества. 8 класс
1. МБОУ «СОШ №6» г Сафоново Смоленская область Урок химии 8 класс «ВЫЧИСЛЕНИЕ МАССОВОЙ ДОЛИ РАСТВОРЕННОГО ВЕЩЕСТВА»
МБОУ «СОШ №6»г Сафоново Смоленская область
Урок химии
8 класс
«ВЫЧИСЛЕНИЕ МАССОВОЙ ДОЛИ РАСТВОРЕННОГО
ВЕЩЕСТВА»
Подготовила
Учитель химии
Ефимова Елена Викторовна
2. Ответьте на мои вопросы, выбрав нужную:
•Какой формулой выражается массовая доля?•А как определить массу растворенного вещества?
•В каких единицах выражается массовая доля?
•Сколько будет в долях 50%? 20%? 85%? 5%?
А где в жизни мы можем использовать названные вами
формулы?
3. Выбери формулу
1) φ = Vвещества ·100%Vсмеси
2) m = n · M
3) mвещества= ω· mраствора
100%
4) n = V
Vm
5) ω = mвещества ·100%
mраствора
6) Vвещества = φ · mсмеси
100%
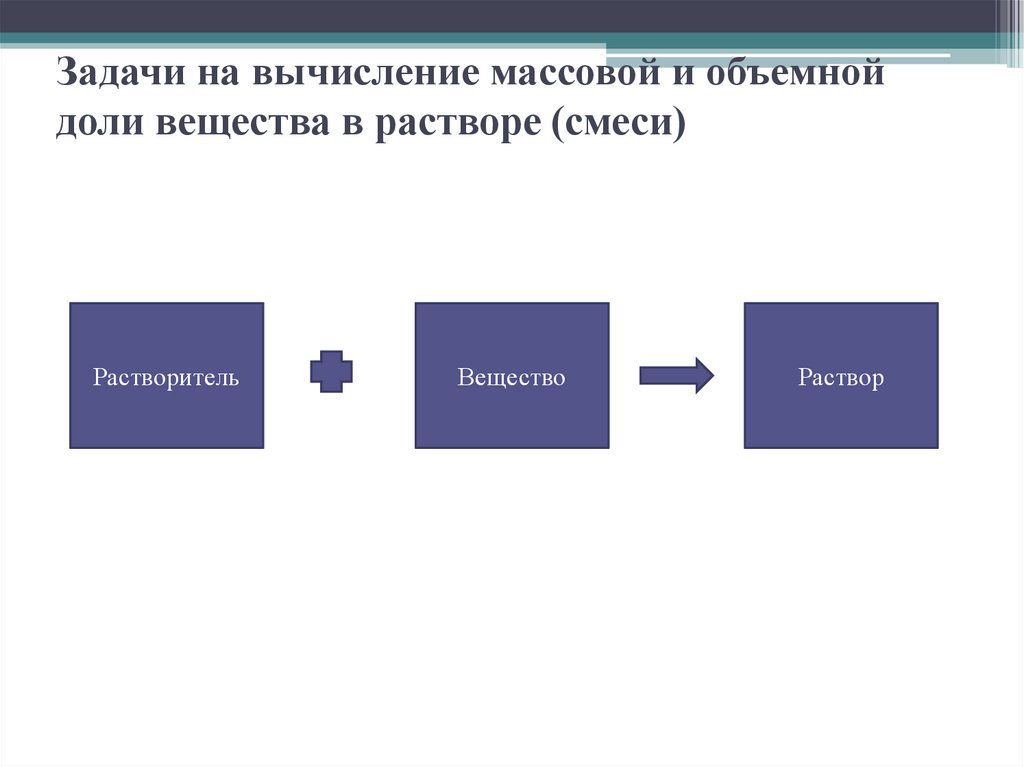
4. Задачи на вычисление массовой и объемной доли вещества в растворе (смеси)
РастворительВещество
Раствор
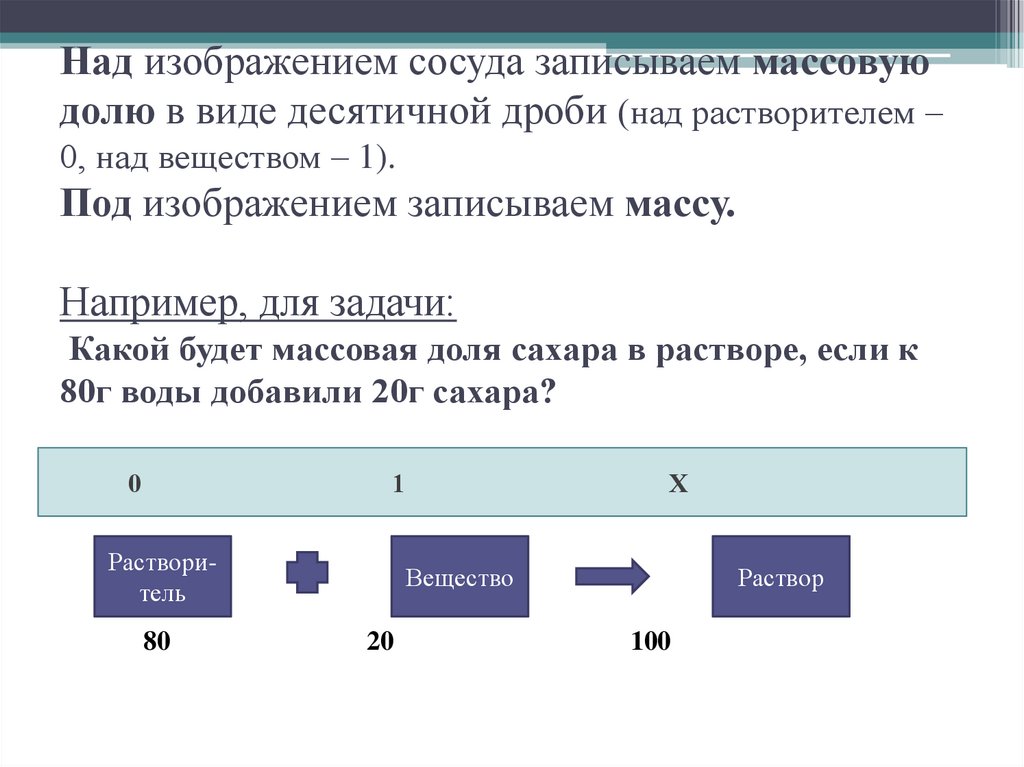
5. Над изображением сосуда записываем массовую долю в виде десятичной дроби (над растворителем – 0, над веществом – 1). Под
изображением записываем массу.Например, для задачи:
Какой будет массовая доля сахара в растворе, если к
80г воды добавили 20г сахара?
0
1
Растворитель
80
Х
Вещество
20
Раствор
100
6. m1·ω1+m2·ω2=(m1+m2)·ω3, то есть: 80·0+20·1=100·х 20=100х Х=20/100=0,2 или 20%
0Растворитель
80
1
Х
Вещество
20
Раствор
100
m1·ω1+m2·ω2=(m1+m2)·ω3, то есть:
80·0+20·1=100·х
20=100х
Х=20/100=0,2 или 20%
7. ЗАДАЧА Какую массу воды следует выпарить из 600г 5%-го раствора соли, чтобы получить ее 30%-ный раствор?
0,05Раствор
600
0
0,3
Вода
Новый
раствор
Х1
Х2
Составляем уравнение:
600 · 0,05=Х1 · 0 + Х2 ·0,3
30=0,3 Х2
Х2 =100г (масса оставшегося раствора)
600-100=500г (масса воды)
8. ЗАДАЧА
• Рассчитайте массу воды и солянойкислоты, которые надо взять для
получения 500г 5%-го раствора.
9. Команда 1 Для дезинфекции ран используется 5%-ный раствор марганцовки. Какую массу марганцовки и воды надо взять для
Команда 1Для дезинфекции ран используется 5%ный раствор марганцовки. Какую массу
марганцовки и воды надо взять для
приготовления 200г раствора?
Марганцовки 10г, воды 190г
10. Команда 2 В домашней аптечке всегда есть 3%-ный раствор «зеленки». Сколько красителя бриллиантового зеленого надо растворить в
спирте, чтобы получить 10,25г«зеленки»?
0,3г красителя
11. Команда 4 Если вы любите сладкий чай, то на 1 стакан (250 г воды) добавляете две чайные ложки сахара (по 5 г каждая). Какая
массовая доля сахара в чае?3,8 %
12. Команда 5 Чтобы кожа была белой и гладкой, принято принимать соленые ванночки для лица и рук. Какую массу соли и воды надо
взять, чтобы получить 500г соленогораствора с массовой долей соли 1%?
5г соли, 495г воды
13. «Что мы знаем о растворах»,
14.
МБОУ «СОШ №6» г Сафоново Смоленской области
Конспект урока химии
«ВЫЧИСЛЕНИЕ МАССОВОЙ ДОЛИ РАСТВОРЕННОГО ВЕЩЕСТВА»
для 8 класса
Подготовила:
Ефимова Елена Викторовна
учитель химии
15. Рефлексия
Я узнал много нового.
Мне это пригодится в жизни.
На уроке было над чем подумать.
На возникшие у меня вопросы я получил
ответы.
• На уроке работал добросовестно и цели урока
достигнуты.
16. Список использованных источников информации: Геращенко И.И. Решение задач на растворы. Журнал «Химия в школе», №5, 1994.
Список использованных источников информации:Геращенко И.И. Решение задач на растворы. Журнал
«Химия в школе», №5, 1994.
Фадеев Г.Н. Задачи и тесты для самоподготовки по
химии6 пособие для ученика и учителя. – М.: БИНОМ.
Лаборатория знаний, 2008.














 chemistry
chemistry








