Similar presentations:
Обратимость химических реакций. Химическое равновесие. Принцип Ле Шателье
1.
Обратимость химических реакций.Химическое равновесие. Принцип
Ле Шателье
2.
ПРИМЕР (книга с.104)2 CO(г.) + O2 (г.) ← 2CO2 (г.) + Q
•реакция соединения
•ОВР
•экзотермическая
•обратимая
•не каталитическая
•гомогенная
3.
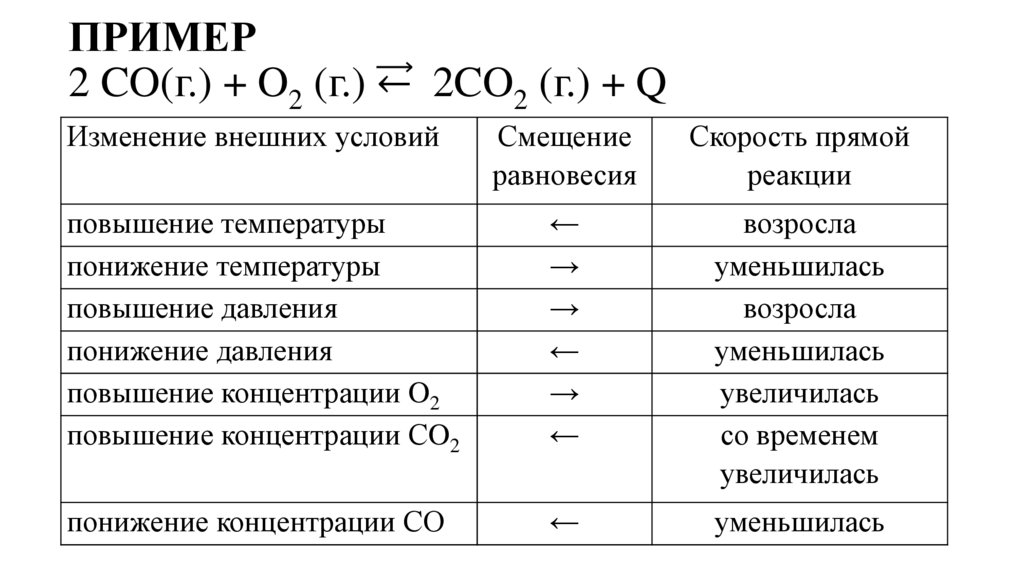
ПРИМЕР2 CO(г.) + O2 (г.) ← 2CO2 (г.) + Q
Изменение внешних условий
Смещение
равновесия
Скорость прямой
реакции
повышение температуры
понижение температуры
повышение давления
понижение давления
повышение концентрации O2
повышение концентрации СO2
←
→
→
←
→
←
возросла
уменьшилась
возросла
уменьшилась
увеличилась
со временем
увеличилась
понижение концентрации СО
←
уменьшилась
4.
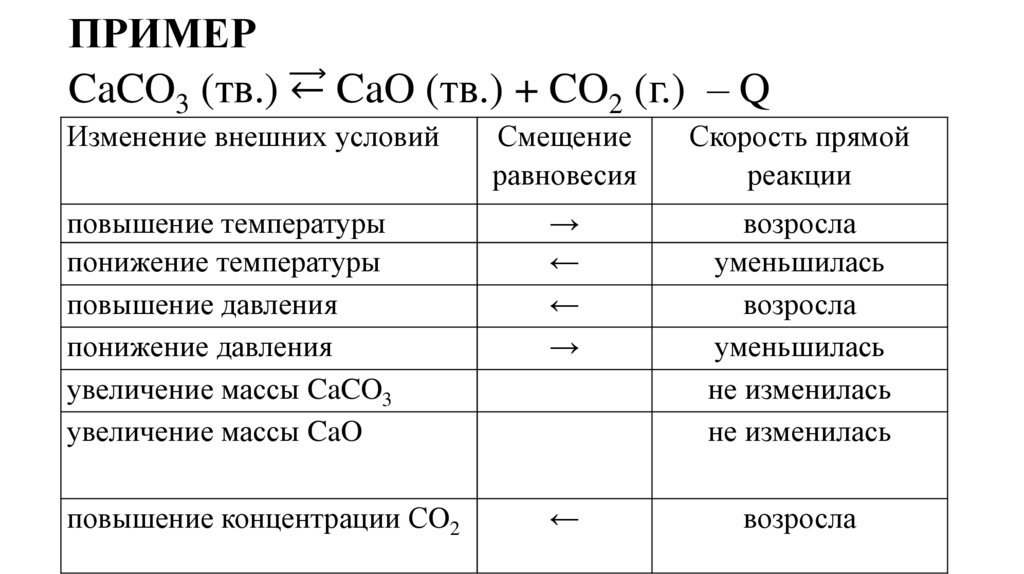
ПРИМЕРCaCO3 (тв.) ← CaO (тв.) + CO2 (г.) – Q
Изменение внешних условий
Смещение
равновесия
Скорость прямой
реакции
повышение температуры
понижение температуры
повышение давления
понижение давления
увеличение массы CaCO3
увеличение массы CaO
→
←
←
→
возросла
уменьшилась
возросла
уменьшилась
не изменилась
не изменилась
повышение концентрации СO2
←
возросла
5.
В какую сторону сместится равновесиеобратимой
реакции
N2 (г.) + 3H2 (г.) ⃪ 2NH3 (г.) + Q ,
если:
а) понизить давление;
б) повысить температуру;
в) увеличить концентрацию водорода;
г) применить катализатор?
6.
В какую сторону сместится равновесиеобратимой
реакции
2SO2 (г.) + O2 (г.) ⃪ 2SO3 (г.) + Q ,
если:
а) повысить давление;
б) понизить температуру;
в) увеличить концентрацию сернистого газа;
г) уменьшить концентрацию кислорода?
7.
В какую сторону сместится равновесиеобратимой
реакции
Fe3O4 (тв.) + 4H2 (г.) ⃪ 3Fe (г.) + 4 H2O (г.) – Q ,
если:
а) понизить температуру;
б) повысить давление;
в) увеличить концентрацию водорода;
г) добавить катализатор?
8.
В какую сторону сместится равновесиеобратимой
реакции
N2 (г.) + O2 (г.) ⃪ 2NO (г.) - Q ,
если:
а) увеличить концентрацию азота;
б) увеличить концентрацию NO;
в) понизить давление;
г) понизить температуру?
9.
В какую сторону сместится равновесиеобратимой
реакции
N2 (г.) + 3H2 (г.) ⃪ 2NH3 (г.) + Q ,
если:
а) повысить давление;
б) повысить температуру;
в) уменьшить концентрацию азота;
г) применить катализатор?
10.
В какую сторону сместится равновесиеобратимой
реакции
2SO2 (г.) + O2 (г.) ⃪ 2SO3 (г.) + Q ,
если:
а) понизить давление;
б) понизить температуру;
в) уменьшить концентрацию сернистого газа;
г) уменьшить концентрацию кислорода?








 chemistry
chemistry








