Similar presentations:
Основные понятия и законы химии
1.
Основные понятия и законыхимии
2.
Химия – наука о веществах, их строении,свойствах и превращениях.
Физические свойства вещества –
агрегатное состояние, плотность,
растворимость, температура плавления
и кипения, цвет, запах и т.д
3.
Агрегатное состояниеТвердое: сахар C12H22O11; соль NaCl ; S ; Al
Жидкое: H2O ; C6H6 ; H2SO4
Газообразное: O2 ; CO2 ; CH4
Изменение агрегатного состояния вещества –
это пример физических явлений, в результате
которых не образуются новые вещества!!!!!
4.
Химические свойства вещества – этоспособность данного вещества превращаться
в другие вещества.
Превращение одних веществ в другие
называются химическими реакциями.
В результате реакции всегда образуются новые
вещества.
Реагент
Продукты реакции
5.
Признаки химических реакций• Изменение цвета
• Образование осадка
BaCl2 + H2SO4 = BaSO4 + 2HCl
• Выделение газа
Na2CO3 + 2HCl = 2NaCl + CO2 + H2O
• Выделение теплоты
H2SO4 + 2NaOH = Na2SO4 + 2H2O +Q
6.
Простые и сложные вещества.Аллотропия.
7.
Простые вещества – это вещества, которыесостоят из атомов одного элемента.
• Молекулярное строение: H2;O2;N2;F2 ;Cl2;Br2;I2
• Атомное строение: металлы (Fe; Cu; Na …)
и некоторые неметаллы ( С ; Si …)
• Благородные газы: He; Ne; Ar; Kr; Xe ;Rn
Их атомы химически не связаны друг с другом!!!!
8.
Сложные вещества – это вещества, которыесостоят из атомов различных элементов.
Сложные вещества называют химическими
соединениями.
Пример: HCl ; H2O ; NaCl ; C6H12O6 …..
9.
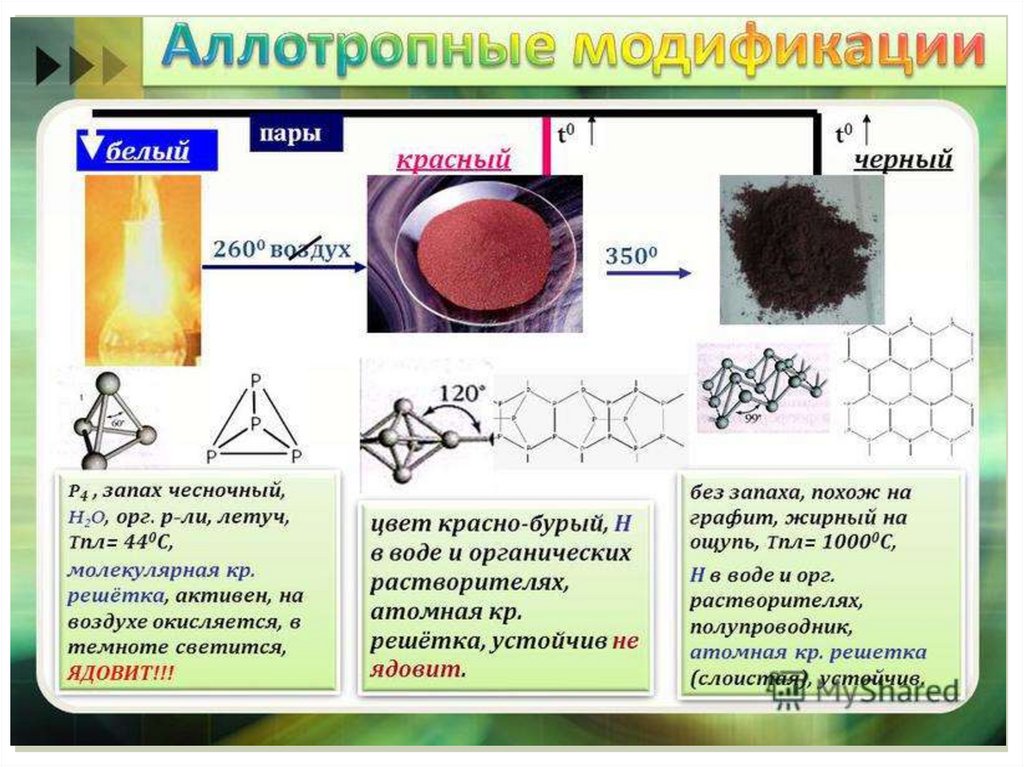
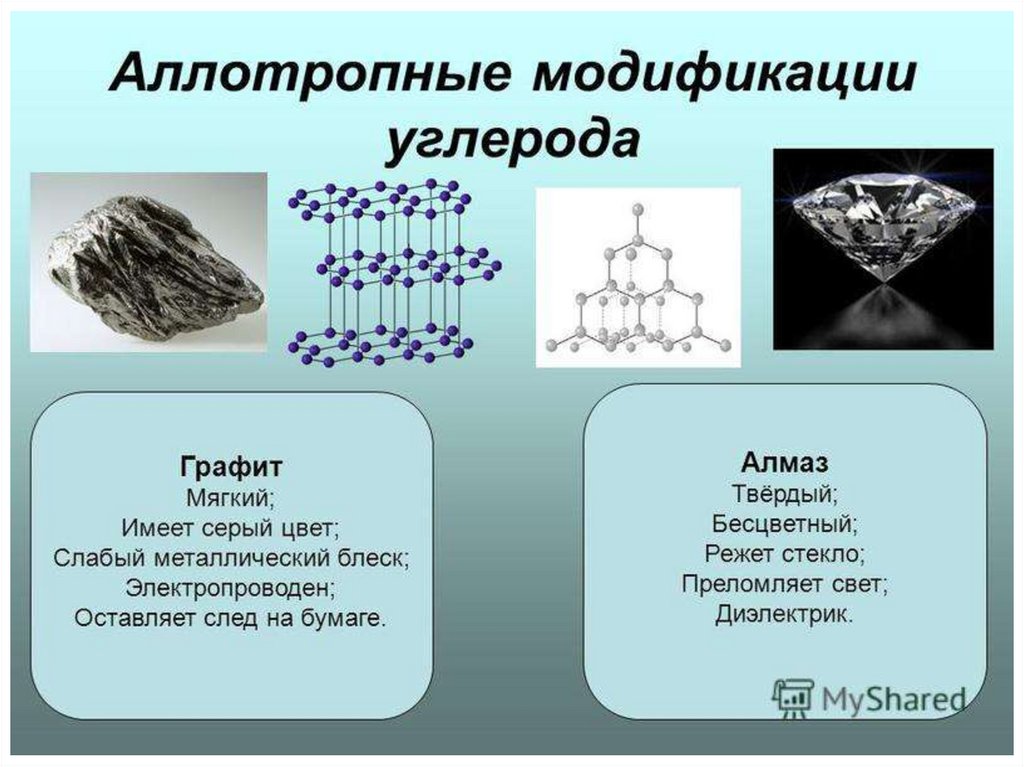
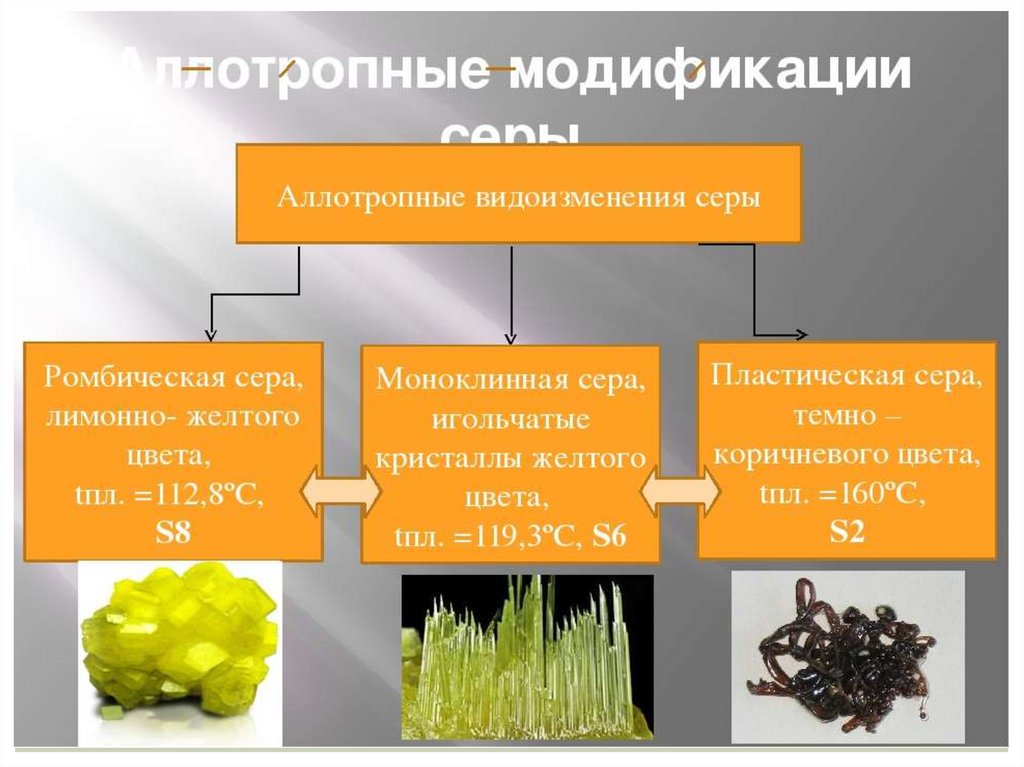
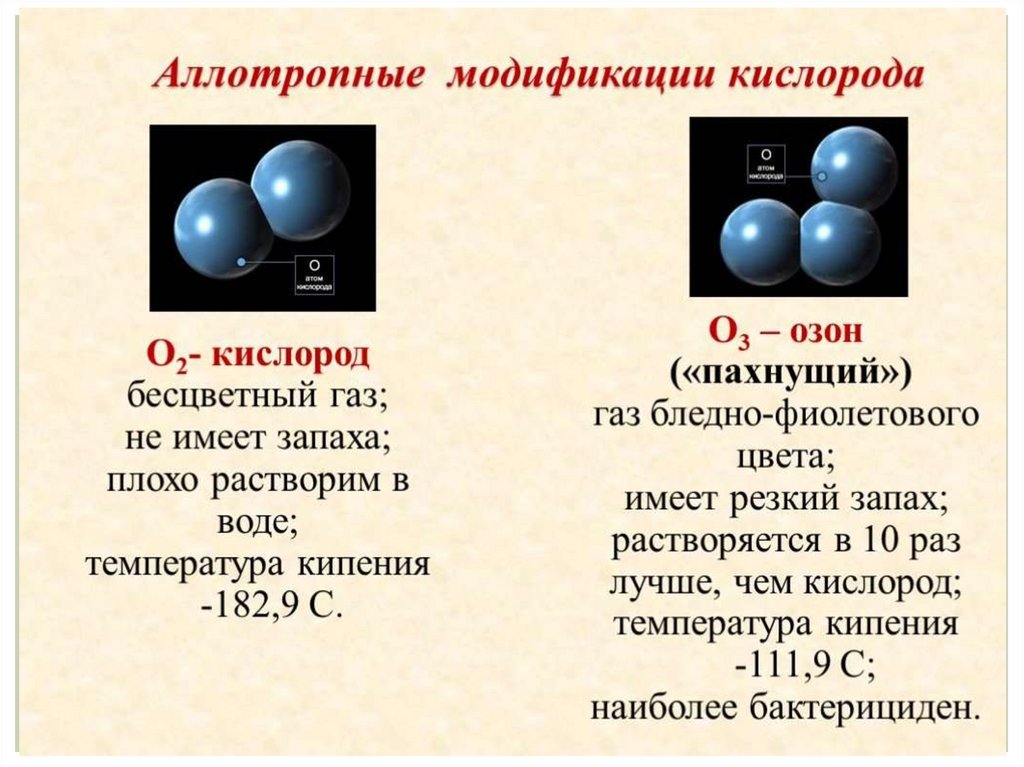
АллотропияАллотропия – это явление образования нескольких
простых веществ одним элементом.
Разные простые вещества, которые образуются
одним и тем же химич.элементом, называются –
аллотропными видоизменениями
(модификациями).
Они отличаются друг от друга составом молекул
10.
11.
12.
13.
14.
Измерения в химии15.
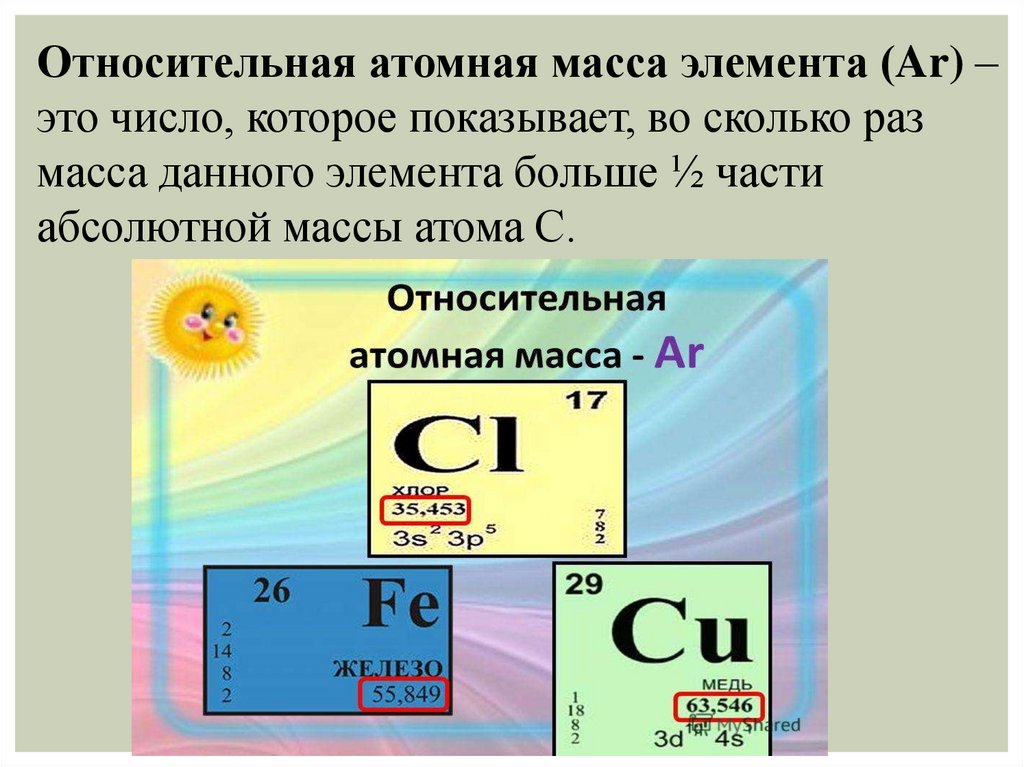
Относительная атомная масса элемента (Ar) –это число, которое показывает, во сколько раз
масса данного элемента больше ½ части
абсолютной массы атома С.
16.
Относительная молекулярная масса (Mr) равна сумме относительных атомных масс всехатомов, образующих молекулу вещества.
17.
Массовая доля (W)химического элементав данном веществе равна отношению относит
атомной массы данного элемента,
умноженной на число его атомов в молекуле,
к относительной молекулярной массе
вещества.
18.
Моль. Количество вещества.Закон Авогадро.
Масса вещества выражается в кг, г или других единицах.
Единицей количества вещества является моль.
Моль – это количество вещества, которое содержит
столько молекул (атомов) этого вещества, сколько
атомов содержится в 12 г углерода.
Число атомов или молекул, содержащихся в одном моле
любого вещества, называется постоянной Авогадро.
19.
20.
21.
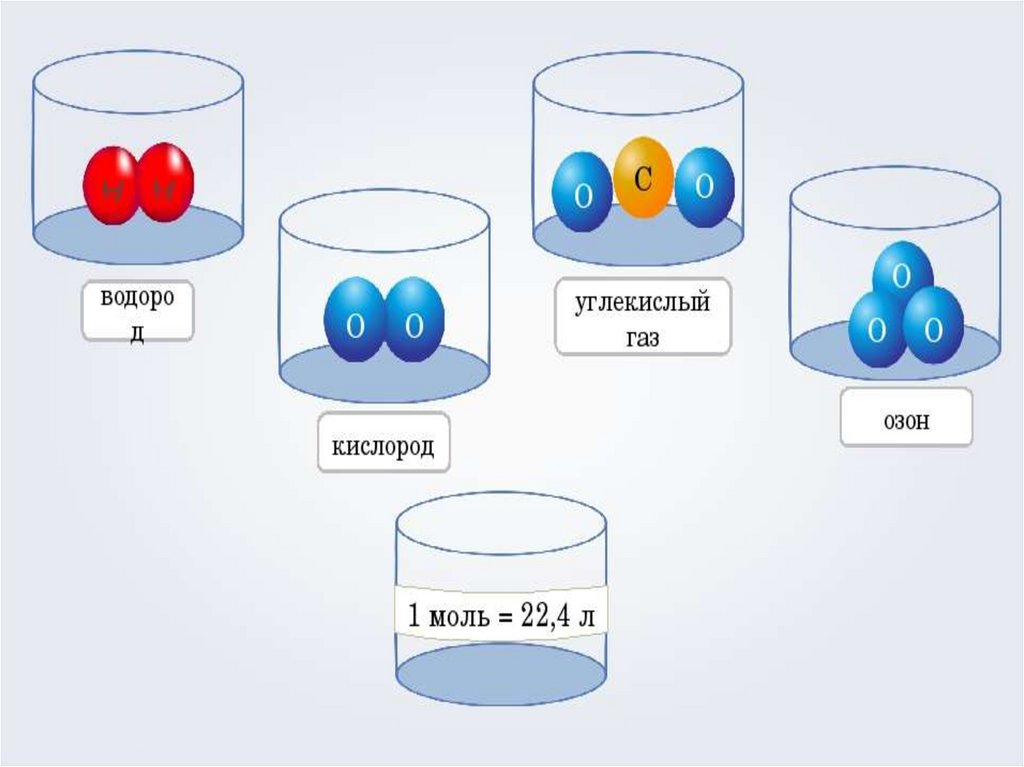
В равных объемах различных газов при одинаковыхвнешних условиях (t и p ) содержится одинаковое
число молекул N (Закон Авогадро)
N1 = N2
Одинаковое число молекул различных газов при
одинаковых условиях занимает одинаковый объем V
V1 = V2
Объем одного моля газа называется его молярным
объемом Vm
22.
23.
24.
Строение атома25.
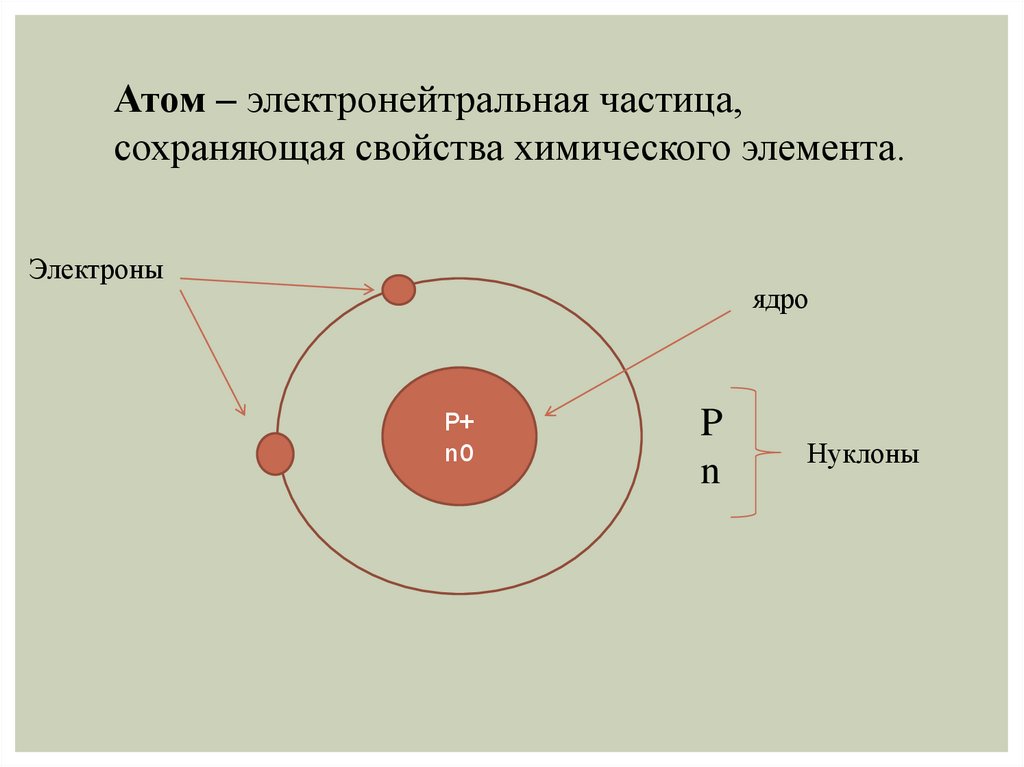
Атом – электронейтральная частица,сохраняющая свойства химического элемента.
Электроны
ядро
P+
n0
P
n
Нуклоны
26.
В 1913 г. анг.физик Г. Мозли установил, что:Порядковый номер
элемента (z)
= числу протонов = числу электронов
в ядре (p)
в атоме (e)
Для нахождения нейтронов ядре необходимо:
Массовое число (А) = число протонов + число нейтронов
27.
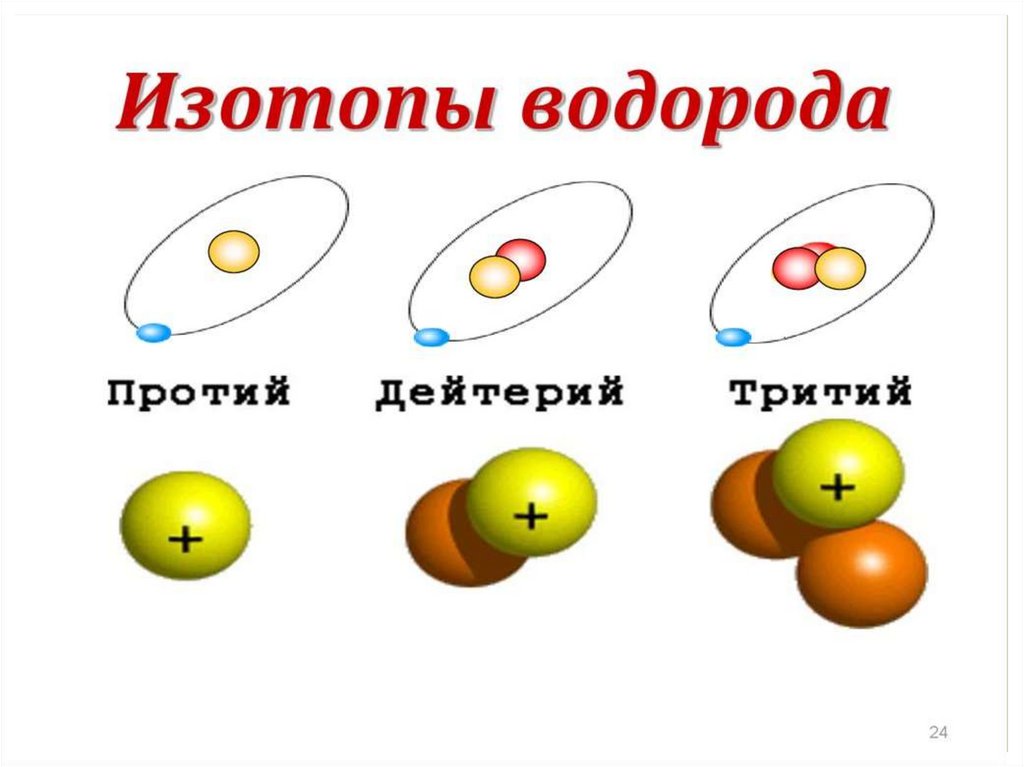
ИзотопыИзотопы – атомы одного элемента, имеющие
одинаковый заряд ядра, но разные массовые числа.
Изотопы содержат одинаковое число протонов,
но разное число нейтронов.




















 chemistry
chemistry








