Similar presentations:
Белки – природные полимеры. Химические свойства белков
1.
«Жизнь есть способсуществования белковых тел»
Ф. Энгельс.
Учитель химии ГБОУ СОШ №489
Жирова Л.Ю.
2. Белки – природные полимеры
Цель урокаИзучить:
состав
строение белков
свойства белков
функции
3. Основа жизни
Наиболее важнымисоединениями, которые
входят в состав живых
организмов, являются
белки (протеины).
Белки служат
основой всего
живого на нашей
планете.
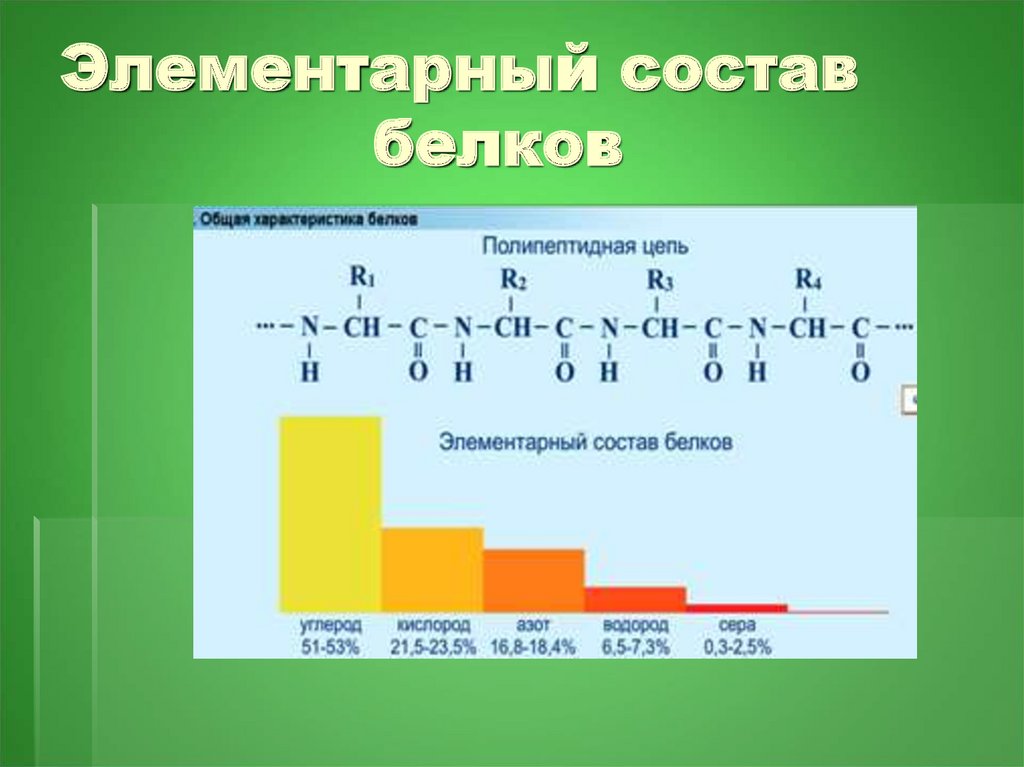
4. Элементарный состав белков
5. Белки – природные полимеры
Белки образованы всего двадцатьюразными аминокислотами, общая
формула которых:
R – CHNH2 – COOH
Внимание! Все аминокислоты белков
– это альфа-аминокислоты.
Полимерные цепи белков состоят
из десятков тысяч, миллионов и
больше остатков аминокислот.
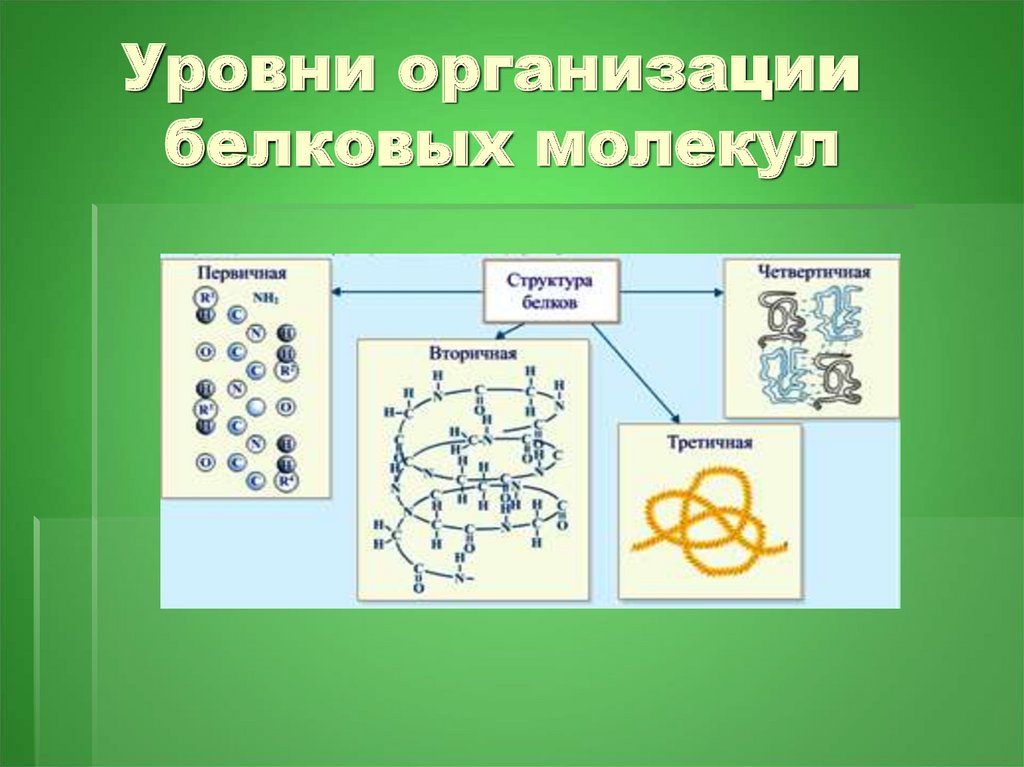
6. Уровни организации белковых молекул
7.
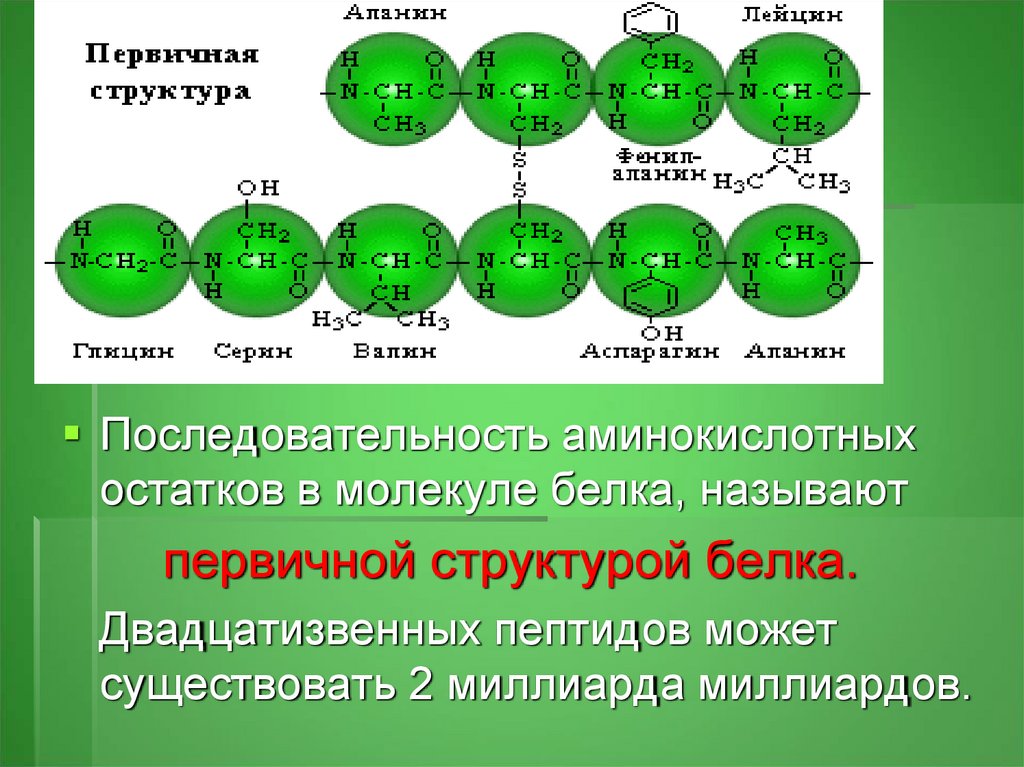
Последовательность аминокислотныхостатков в молекуле белка, называют
первичной структурой белка.
Двадцатизвенных пептидов может
существовать 2 миллиарда миллиардов.
8.
Для белковых тел характерныогромные молекулярные массы.
У вируса желтухи шелковичного червя Мr = 916000000
Отсюда и почти макроразмеры некоторых молекул белков.
(при Мr = 350000 длина молекул0,3 мкм, а при Мr = 1000000000 –1мм
Длинная молекула не может
быть строго линейной. В
результате изгибания и
сворачивания молекулы
образуется спиралевидная структура.
9.
В молекулах белковимеют место ионные
взаимодействия
между
карбоксильными и
аминогруппами
различных
аминокислотных
остатков, а также
образуются
дисульфидные
мостики. Эти
взаимодействия
приводят к появлению
третичной структуры.
Третичная структура
миоглобина.
(размер молекулы 4,5 Х
3,5 Х 2,5 нм)
10.
Белки смолекулярной массой
больше 50000 состоят
из нескольких
полипептидных
цепей, каждая из
которых имеет
первичную,
вторичную и
третичную структуры.
Глобула
Говорят, что такие белки обладают
четвертичной структурой.
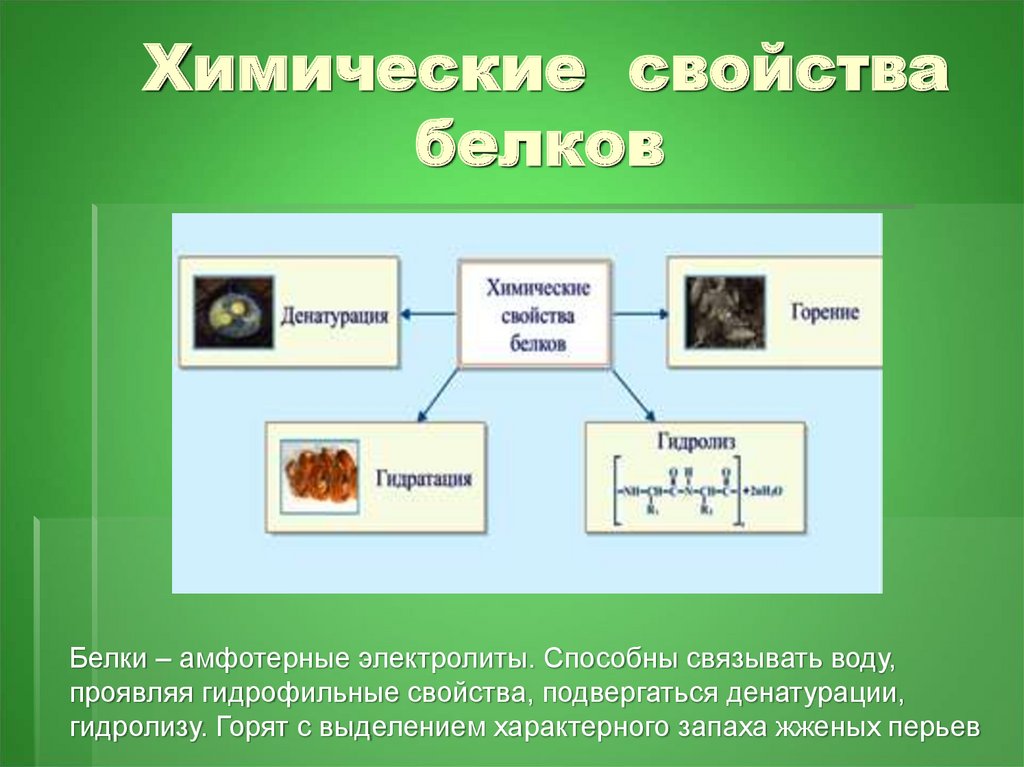
11. Химические свойства белков
Белки – амфотерные электролиты. Способны связывать воду,проявляя гидрофильные свойства, подвергаться денатурации,
гидролизу. Горят с выделением характерного запаха жженых перьев
12.
Разрушение структурыбелка –денатурация
Какими по вашему могут быть
причины денатурации белков?
13. Причины денатурации белков
Повышение температурыВлияние солей тяжелых металлов
Влияние алкоголя
14. Схема гидролиза трипептида
Гидролиз – это расщепление белка на отдельныеаминокислоты под действием ферментов или в водных
растворах кислот и щелочей.
15.
Качественные реакции на белкиКсантопротеиновая
реакция
При действии
азотной кислоты –
белки окрашиваются
в желтый цвет.
Биуретовая реакция
С солями меди (II) в
присутствии
щелочи белки дают
фиолетовую
окраску. Это
качественная
реакция на
пептидную группу.
16. Функции белков
СтроительнаяФерментативная (каталитическая)
Транспортная
Защитная
Двигательная
Регуляторная
Запасающая
Токсическая
Энергетическая
17. Ответьте на вопросы:
В чем причина несовместимоститканей при пересадке
Для каждого организма характерен свой
органов от одного организма к другому?
индивидуальный набор белков
протеины
Научное название белков.
Из чего построены молекулы белков? Из остатков аминокислот
4
Сколько структур белка существует?
вторичная
Структура белка, свернутая в спираль?
Как называется четвертичная структура белка? глобула
пептидная
Как называется связь - NH – CO - ?
денатурация
Разрушение структуры белка.
Реакции, определяющие наличие белка?
Ксантопротеиновая, биуретовая
Пищевые продукты с большим содержанием белка.
Самая неустойчивая структура белка?
четвертичная














 biology
biology








