Similar presentations:
Закономерности изменения свойств элементов в периодах и группах. Химия. 8 класс
1.
Закономерности изменениясвойств элементов
в периодах и группах
Химия 8 класс
2.
Особенности строения атомов металловНа внешнем энергетическом уровне –
от 1 до 3 электронов.
На внешнем уровне у Sn, Pb, Bi, Po
–от 4 до 6 электронов.
Валентные электроны слабо связаны с
ядром.
Сравнительно большие радиусы и
небольшая электроотрицательность.
Радиусы атомов
Li+3 )2)1;
Na+11 )2)8)1;
K+19 )2)8)8)1;
Mg+12 )2)8)2;
Al+13 )2)8)3;
3.
Особенности строения атомов неметалловНа внешнем уровне имеют от 4 до 8
электронов.
Расположены в главных
подгруппах 4 - 8 групп.
Небольшой радиус атомов и
большое значение
электроотрицательности.
Si+14 )2)8)4
P+15 )2)8)5
О+8 )2)6
Cl+17 )2)8)7
4.
Периодическое изменение свойствэлементов
Металлические свойства – это способность атомов
отщеплять внешние (валентные) электроны.
23
- 1е-
0
Na
11
23
11
2 8 1
+
Na
2
8
Неметаллические свойства – это способность атомов
притягивать электроны на внешнюю электронную оболочку.
-
+ 1е
35,5
17
Cl
2
8 7
35,5
Cl
17
2
8 8
5.
I А группа3
Li
3 период
2 1
Na
11
Mg
12
28 1
2
K
19
2 13
Al
2 8 3
Металлические свойства
убывают
1.Увеличивается заряд
атомных
ядер. ядер.
1.Увеличивается
заряд
атомных
2 8 8 1
Rb
37
Cs
55
Металлические свойства
элементов
1
1
2.Увеличивается
электронов
2.Число электронов число
на внешнем
уровне на
постоянно. уровне.
внешнем
3.Число
энергетических
уровней
3.Увеличивается
число энергетических
уровней.
постоянно.
4.Увеличивается
атома.
4.Радиус
атомарадиус
уменьшается.
Металлические свойства
возрастают.
6. Неметаллические свойства элементов
В периодах слева направо:Элементы 2 периода
7
Li
+3
+3
9
0
2 11
11 0
0
Be
+4
+4
2 22
B
+5
+5
12 0
2 33
C
+6
+6
14 0
2 44
N
+7
16 0
O
+7 2 55 +8
+8
2 6
6
19 0
20
+9
+10 2 88
2 77 +10
F
+9
0
Ne
1.Увеличивается заряд атомных ядер.
2.Увеличивается число электронов на внешнем уровне.
3.Число энергетических уровней постоянно.
4.Радиус атома уменьшается.
Неметаллические свойства возрастают.
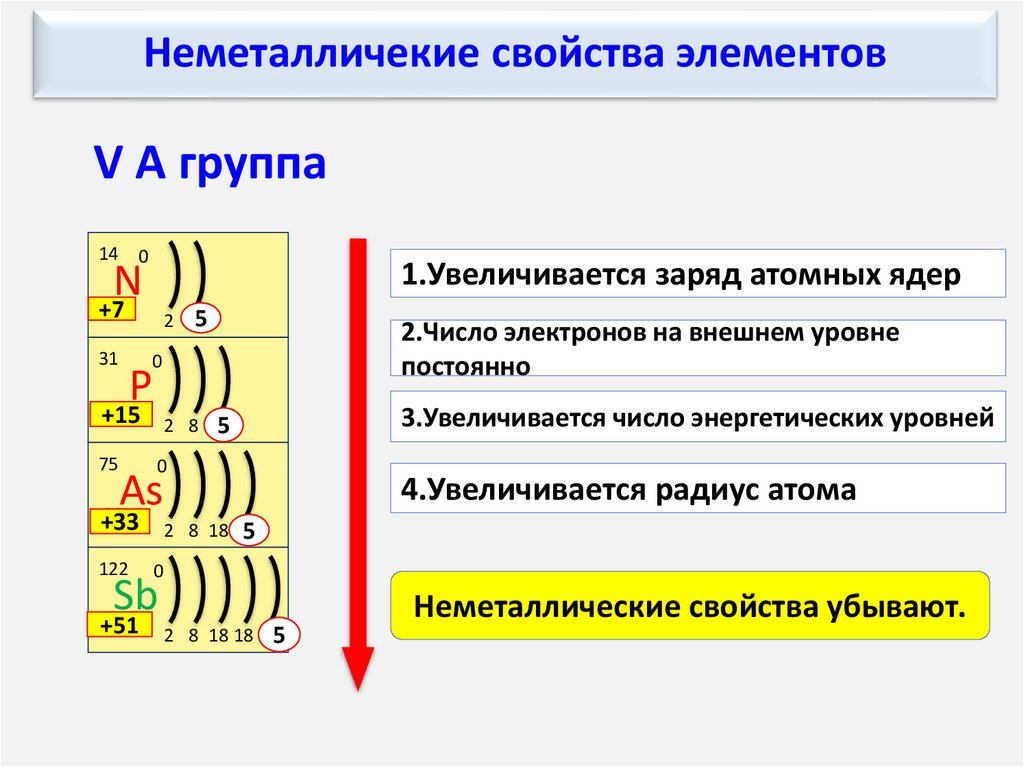
7. Неметалличекие свойства элементов
V А группа14 0
1.Увеличивается заряд атомных ядер
N
+7
+7
31
2 55
0
P
+15
+15
2 8 55
75
0
+33
2 8 18 55
122
0
As
+33
Sb
+51
+51
2 8 18 18 55
2.Число электронов на внешнем уровне
постоянно
3.Увеличивается число энергетических уровней
4.Увеличивается радиус атома
Неметаллические свойства убывают.
8.
Выводы о взаимосвязи строения атомов и свойствхим. элементов
свойства хим. элементов, расположенных в порядке возрастания
заряда ядра, изменяются периодически потому, что периодически
повторяется сходное строение внешнего электронного слоя атомов
элементов.
9.
Выводы о взаимосвязи строения атомов и свойствхим. элементов
плавное изменение свойств элементов в пределах одного периода можно
объяснить постепенным увеличением числа электронов на внешнем слое
атомов.
10.
Выводы о взаимосвязи строения атомов и свойствхим. элементов
завершение внешнего электронного слоя атома приводит к резкому скачку в
свойствах, при переходе от галогена к инертному элементу;
появление нового внешнего электронного слоя – причина резкого скачка в
свойствах при переходе от инертного элемента к щелочному металлу.
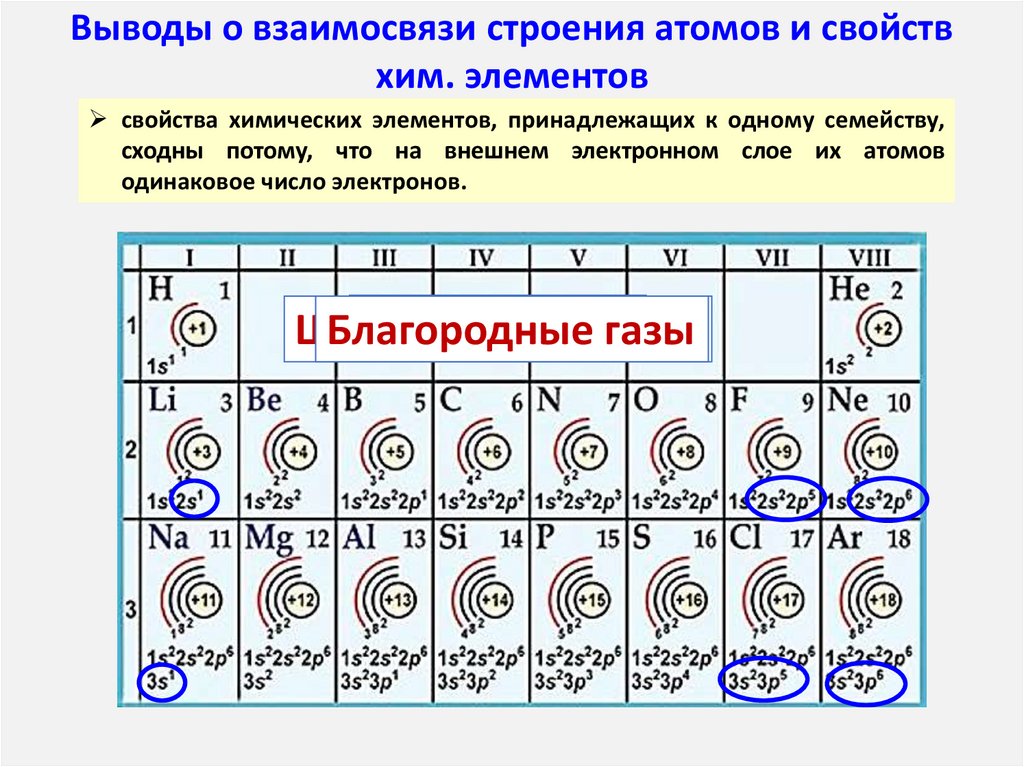
11.
Выводы о взаимосвязи строения атомов и свойствхим. элементов
свойства химических элементов, принадлежащих к одному семейству,
сходны потому, что на внешнем электронном слое их атомов
одинаковое число электронов.
Галогены
Щелочные
Благородные
металлы
газы
12. Повторение Задание: заполните пропуски.
В периодах слева направо:убывают
металлические свойства____________________
возрастают
а неметаллические свойства_________________,
потому что:
увеличивается заряд атомных ядер
а)_______________________________________
увеличивается число электронов на внешнем уровне
б)___________________________________________________
число энергетических уровней постоянно
в)________________________________________
г)________________________________________
радиус атома уменьшается
В А группе сверху вниз:
возрастают
металлические свойства____________________
убывают
а неметаллические свойства_________________,
потому что:
увеличивается заряд атомных ядер
а)___________________________________
число электронов на внешнем уровне постоянно
б)____________________________________________________
увеличивается число энергетических уровней
в)____________________________________________________
радиус атома увеличивается
г)_____________________________________
Проверка
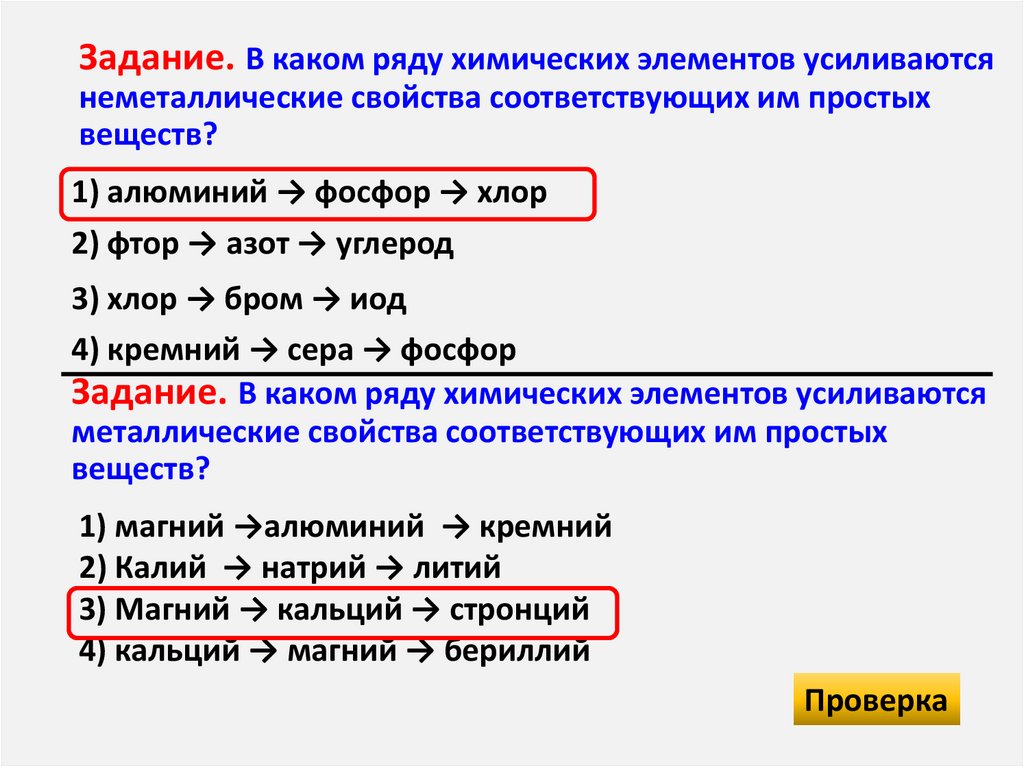
13. Задание. В каком ряду химических элементов усиливаются неметаллические свойства соответствующих им простых веществ?
1) алюминий → фосфор → хлор2) фтор → азот → углерод
3) хлор → бром → иод
4) кремний → сера → фосфор
Задание. В каком ряду химических элементов усиливаются
металлические свойства соответствующих им простых
веществ?
1) магний →алюминий → кремний
2) Калий → натрий → литий
3) Магний → кальций → стронций
4) кальций → магний → бериллий
Проверка
14. Задание: поставьте знак «больше» или «меньше», если речь идет о неметаллических свойствах.
B<
S
>
>
P
Cl
>
Se
Проверка
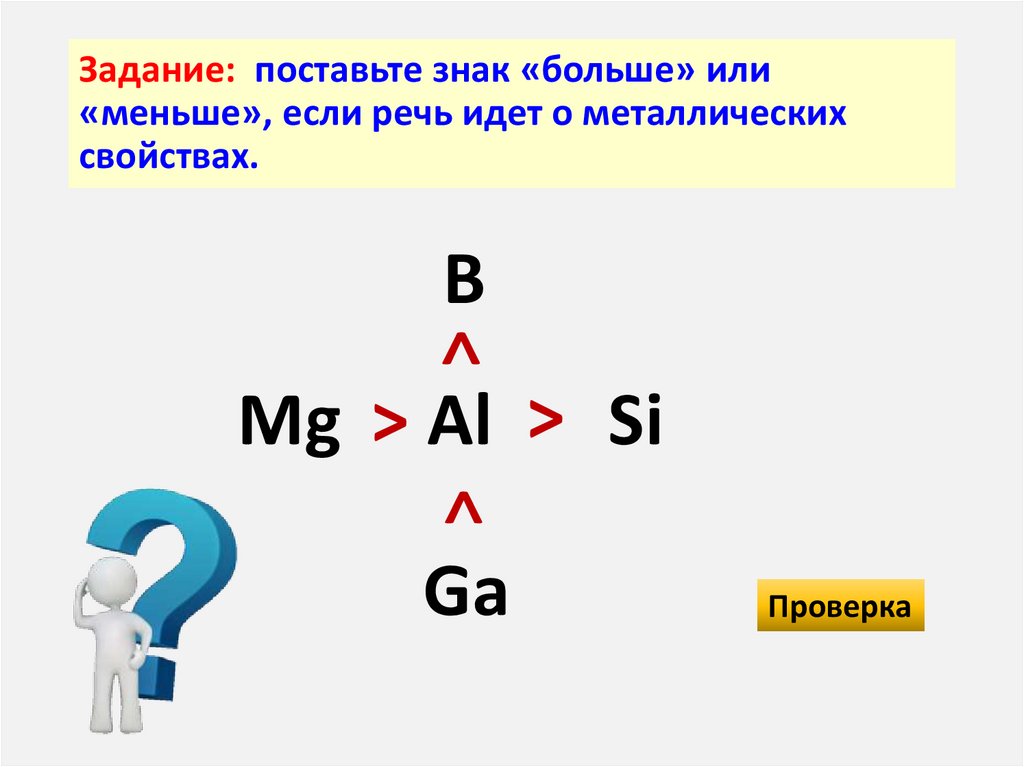
15. Задание: поставьте знак «больше» или «меньше», если речь идет о металлических свойствах.
B<
>
Mg > Al > Si
Ga
Проверка
16. Интернет-ресурсы
• Таблица Д.И. Менделееваhttps://yandex.ru/images/search?pos=608&p=11&img_url=https%3A%2F%2Fimages.pond5.com%2Fp
eriodic-table-elements-footage-022025113_prevstill.jpeg&text=таблица%20менделеева&rpt=simage
• Строение атома кальция, хлора https://foxford.ru/wiki/himiya/osobennosti-stroeniya-i-svoystvmetallov
• Радиусы атомов http://www.pvsm.ru/images/2017/03/24/udivitelnye-vulkanicheskie-molnii-11.jpg
• Вопросительный знак http://1.bp.blogspot.com/8m6Lk0zUMUc/VAnF3C0ofjI/AAAAAAAACzA/xyV8phVh3as/s1600/question_mark.jpg












 chemistry
chemistry








