Similar presentations:
В царстве «Рыжего дьявола». Урок-путешествие. 9 класс
1. В царстве «Рыжего дьявола»
Урок-путешествие9 класс.
2. «Знать – значит победить» А.Н.Несмеянов
Цели урока:Познакомиться с сущностью химической и
электрохимической коррозии;
Рассмотреть способы защиты от коррозии;
Объяснить процессы, протекающие на
поверхности металлов;
Научиться практически защищать металлы
от коррозии.
3. Графический диктант
1 вариант2 вариант
Для Меди (Си)
Для калия (К)
1. Это активный щелочной металл.
2. Металл занимает 2 место по теплопроводности.
3. Самый мягкий металл.
4. Входит в состав бронзы.
5. На внешнем энергетическом уровне 2 электрона.
6. Металл взаимодействует с водой.
7. Металл не взаимодействует с водой.
8. Вытесняет железо из растворов его солей.
4. Графический диктант
9.10.
11.
12.
13.
14.
Металлом можно воспользоваться для получения
серебра из его соли.
Может вытеснять цинк из его соли.
В реакциях с галогенами является окислителем.
При хранении на открытом воздухе быстро окисляется.
Раствор соли этого металла используют для борьбы с
вредителями сада.
Легко режется ножом.
Проверяем.
5. Ключ для проверки
1 2 3 4 5 6 7 8 9 10 11 12 13 14I вариант:0 1 0 1 0 0 1 0 1 0 0 0 1 0
II вариант:1 0 1 0 0 1 0 0 0 0 0 1 0 1
Без ошибок – «5»;
1-2 ошибки – «4»;
3-5 ошибок - «3».
6. Станция «Информационная»
КОРРОЗИЯ – это разрушение металлов исплавов под действием внешней среды.
КОРРОЗИЯ – это окислительновосстановительный процесс, при котором
атомы металла переходя в ионы. В роли
окислителя, как правило, выступают О2 и
Н+.
Коррозия – от латинского corrodere –
разъедать.
7. Станция «Информационная»
КоррозияХимическая
(протекает в средах не
проводящих
электрический ток)
4Fe+3O2+6H2O=4Fe(OH)3
Коррозия железа и
образование ржавчины
Электрохимическая
(протекает в средах при
возникновении электрического
тока)
А(+)на железе
на меди К(-)
Fe0-2e=Fe2+
2H++2e=H20
Коррозия железа, находящегося
в контакте с медью
8. Станция «Историческая»
Люди издавна гадали:Как металлы уберечь?
И теорию создали, Вот о ней как раз и речь!
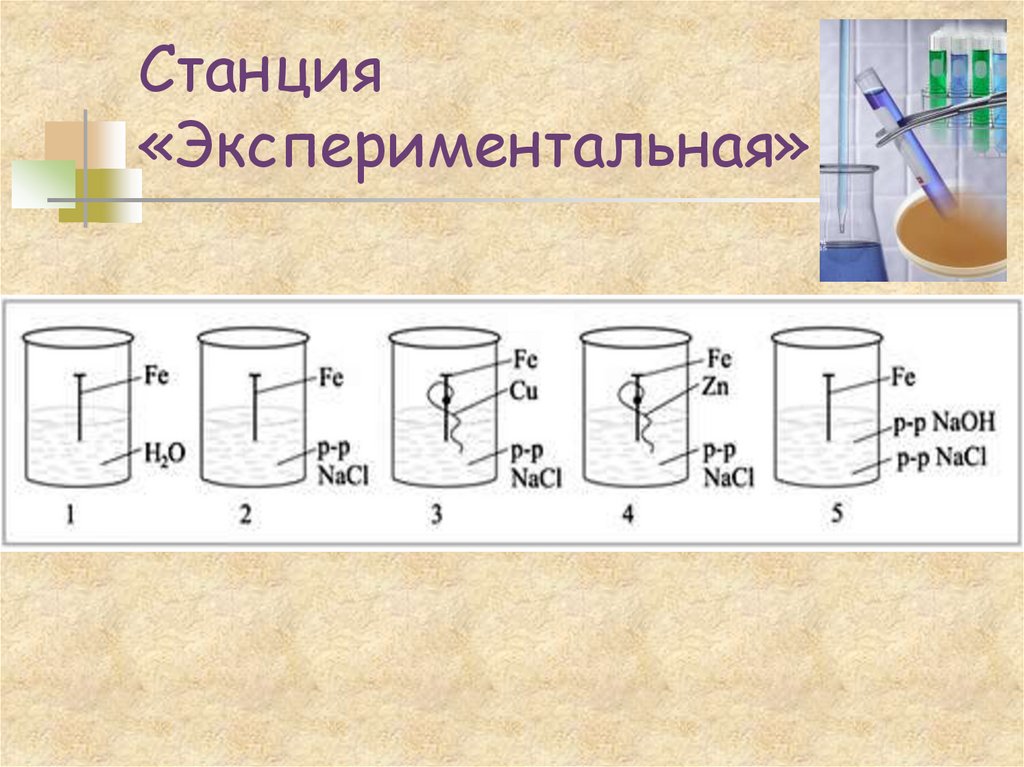
9. Станция «Экспериментальная»
10. Станция «Практическая»
Способы защиты металлов откоррозии:
Шлифование поверхностей.
11. Станция «Практическая»
Способы защиты металлов откоррозии:
Использование легированных сталей
12. Станция «Практическая»
Способы защиты металлов откоррозии:
Нанесение защитных покрытий:
1. Неметаллических (лаки, эмали, смазка, масла)
13. Станция «Практическая»
Способы защиты металлов откоррозии:
Нанесение защитных покрытий:
2. металлических (покрытие одного металла
слоем другого)
Например никелирование, лужение, хромирование.
14. Станция «Практическая»
Способы защиты металлов откоррозии:
Нанесение защитных покрытий:
3. Химических:
• Воронение,
• Оксидные пленки,
• Полимерные пленки
• И другие…
15. Станция «Практическая»
Способы защиты металлов откоррозии:
Электрохимические методы
1. Протекторная защита- к металлической
конструкции присоединяется кусок более активного
металла, который служит анодом и разрушается.
16. Станция «Практическая»
Способы защиты металлов откоррозии:
Электрохимические методы:
2. Катодная защита- конструкция присоединяется к
внешнему источнику тока (так защищают трубы
нефтепроводов и газопроводов)
17. Станция «Практическая»
Способы защиты металлов откоррозии:
Обработка среды
(В котельных установках из воды удаляется
кислород.)
18. «Стоп! Красный свет!»
Коль хотите домой возвратиться,То придется вам всем потрудиться.
Если сделана будет работа,
Я открою из царства ворота!
Рыжий дьявол
19. «Стоп! Красный свет!»
Вопросы:1.
2.
3.
4.
5.
6.
Что такое коррозия?
Какие виды коррозии вы знаете?
Когда и кем была создана теория коррозии
металлов?
Как можно замедлить коррозию?
Почему луженный бак в местах повреждения быстро
ржавеет, а оцинкованный при тех же условиях не
разрушается?
Почему рядом с золотой коронкой на зубах не
рекомендуют ставить стальную?
20. Домашнее задание
§ 10Вопросы 2, 3, 6.



















 chemistry
chemistry








