Similar presentations:
Составление формул химических соединений
1. МОУ средняя общеобразовательная школа с. Минаевки Асиновского района Томской области
Выполнил:учитель химии первой
квалификационной категории
Суцкель Татьяна Михайловна
2.
1. Орг. момент. Создание ситуации успеха2.аСтепень окисления
б.определи степень окисления х.э.
3. Таблица растворимости
4.Алгоритм составления формул соединений
5.Проверь себя.(составьте формулы)
6.Номенклатура химических соединений
7а.Самоконтроль (тест)
7.бРефлексия
8. Закрепляем(домашнее задание) наличие компьютера
3.
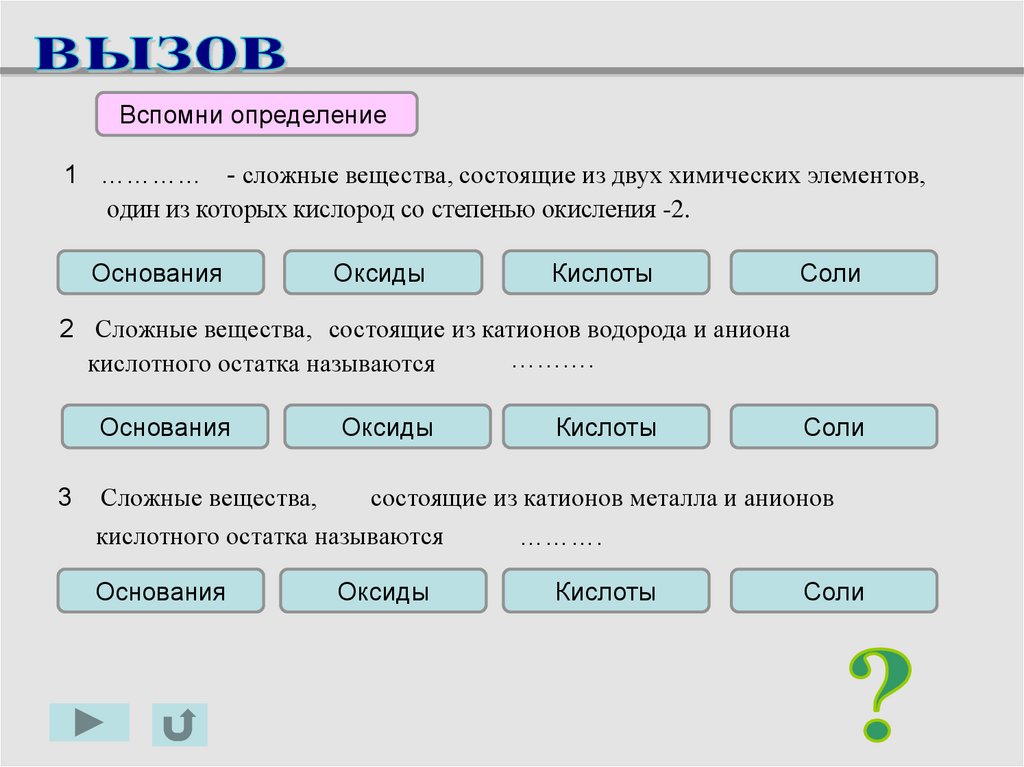
Вспомни определение1 …………
Оксиды - сложные вещества, состоящие из двух химических элементов,
один из которых кислород со степенью окисления -2.
Основания
Оксиды
Кислоты
Соли
2 Сложные вещества, состоящие из катионов водорода и аниона
……….
кислотного остатка называются
кислотами.
Основания
3
Оксиды
Кислоты
Соли
Сложные вещества,
состоящие из катионов металла и анионов
кислотного остатка называются
солями.
……….
Основания
Оксиды
Кислоты
Соли
4.
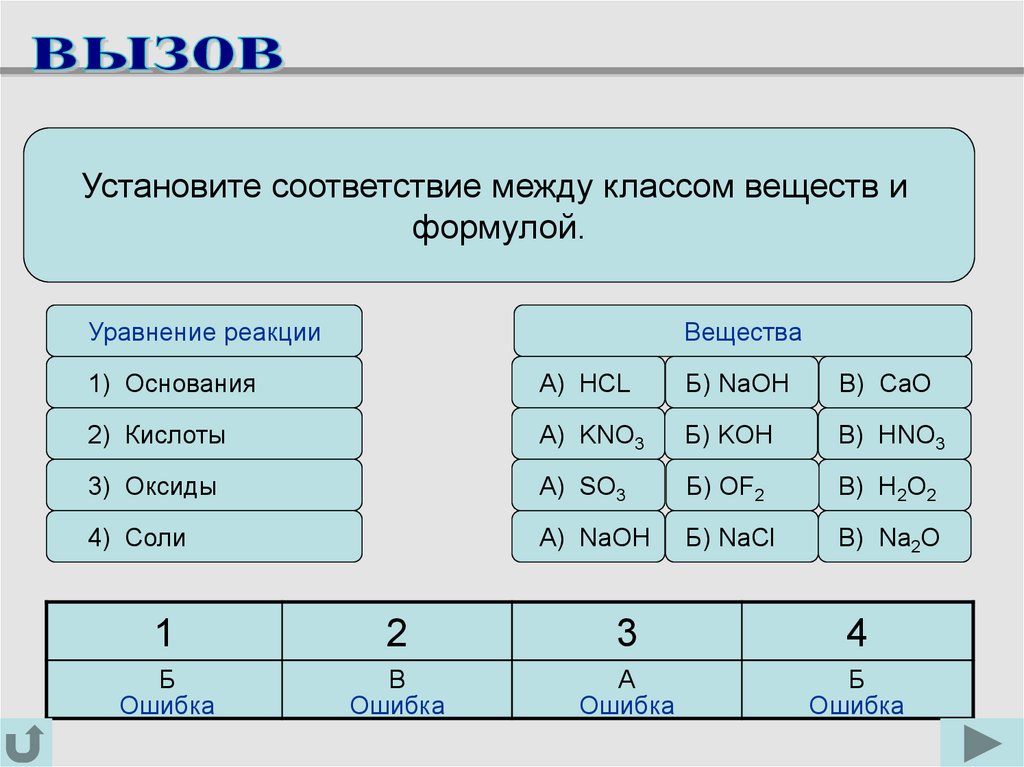
Установите соответствие между классом веществ иформулой.
Уравнение реакции
Вещества
1) Основания
А) HCL
Б) NaOH
В) CaO
2) Кислоты
А) KNO3
Б) KOH
В) НNO3
3) Оксиды
А) SO3
Б) OF2
В) Н2O2
4) Соли
А) NaOH
Б) NaCl
В) Na2O
1
2
3
4
Б
Ошибка
В
Ошибка
А
Ошибка
Б
Ошибка
5.
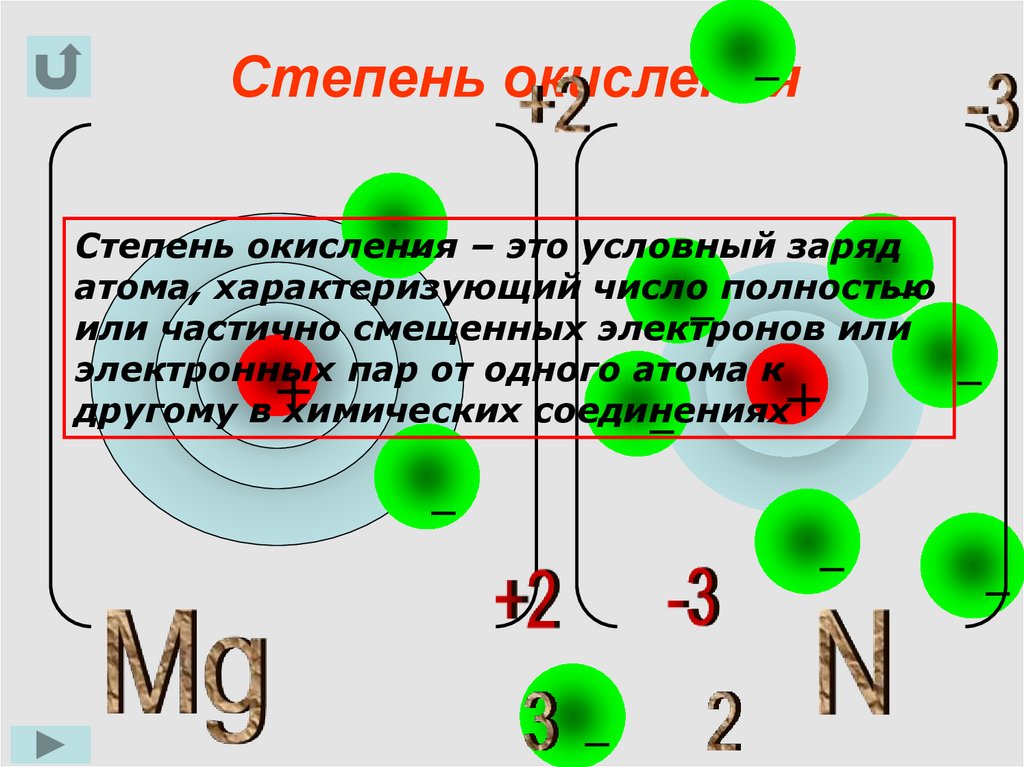
Степень окисленияСтепень окисления – это условный заряд
атома, характеризующий число полностью
или частично смещенных электронов или
электронных пар от одного атома к
другому в химических соединениях
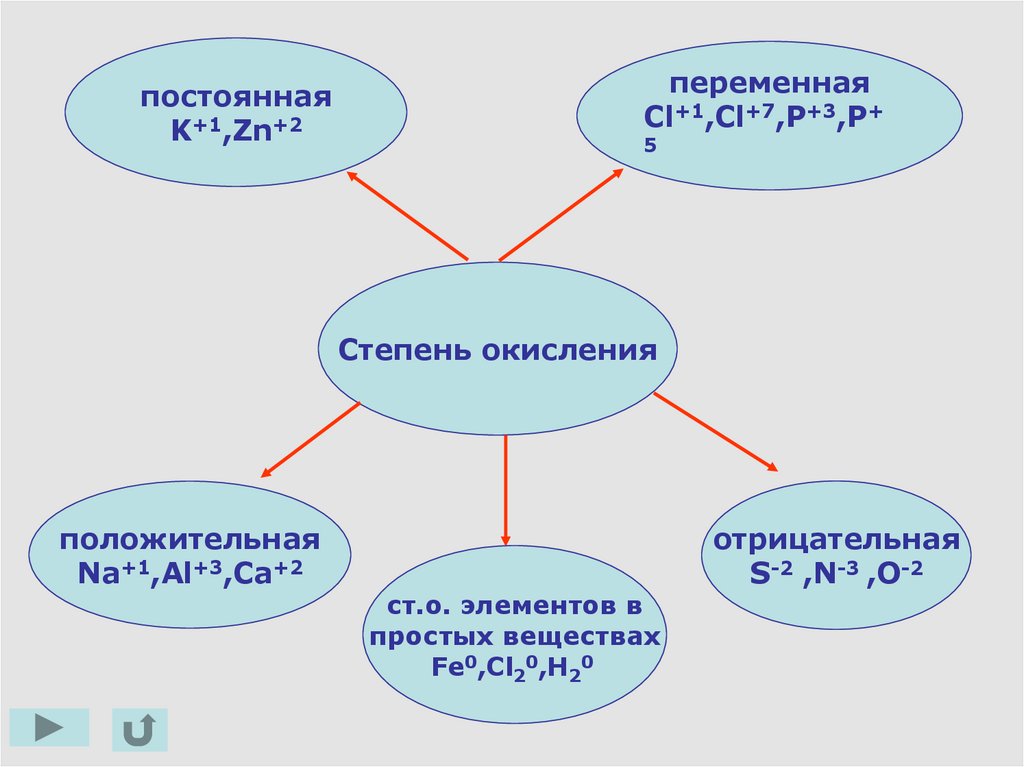
6.
постояннаяK+1,Zn+2
переменная
Cl+1,Cl+7,P+3,P+
5
Степень окисления
положительная
Na+1,Al+3,Ca+2
ст.о. элементов в
простых веществах
Fe0,Cl20,H20
отрицательная
S-2 ,N-3 ,O-2
7. Какие степени окисления у серы?
S+16 )))2
2
6
2
4
0
1s 2s 2p 3s 3p 3d
2 8 6
_
2 неспар. е ст.о. -2
3s2
S*
3s2
3p4
3p4
3d0
H2S
3d1
_
4 неспар. е ст.о. +4
SO2
_
6 неспар. е ст.о. +6
S**
3s2
3p3
3d2
SO3
8. Определите степени окисления элементов
Al2O3Ca3N2
K2Se
P2O5
Cl2O7
As2O3
Al2+3O3-2
Ca3+2N2-3
K2+1Se-2
P2+5O5-2
+7
-2
Cl2 O7
+3
-2
As2 O3
9.
Подставь индексы в формулу. Если ион сложный,По наименьшему
Определите степени
общему
окисления
кратному атомов
рассчитываем
или
а индекс
Найдите
Записать
больше
для них
единицы,
рядом
наименьшее
знаки
то возьми
элементов
общее
ионкратное
в скобки!
заряды ионов
индексы
и подпишите их
Шаг 1
НОК = 6
+2
2
Шаг 2
-3
3
Са Р
6 : =3
Шаг 3
Шаг 4
Шаг 5
6 :
=2
НОК ?
10.
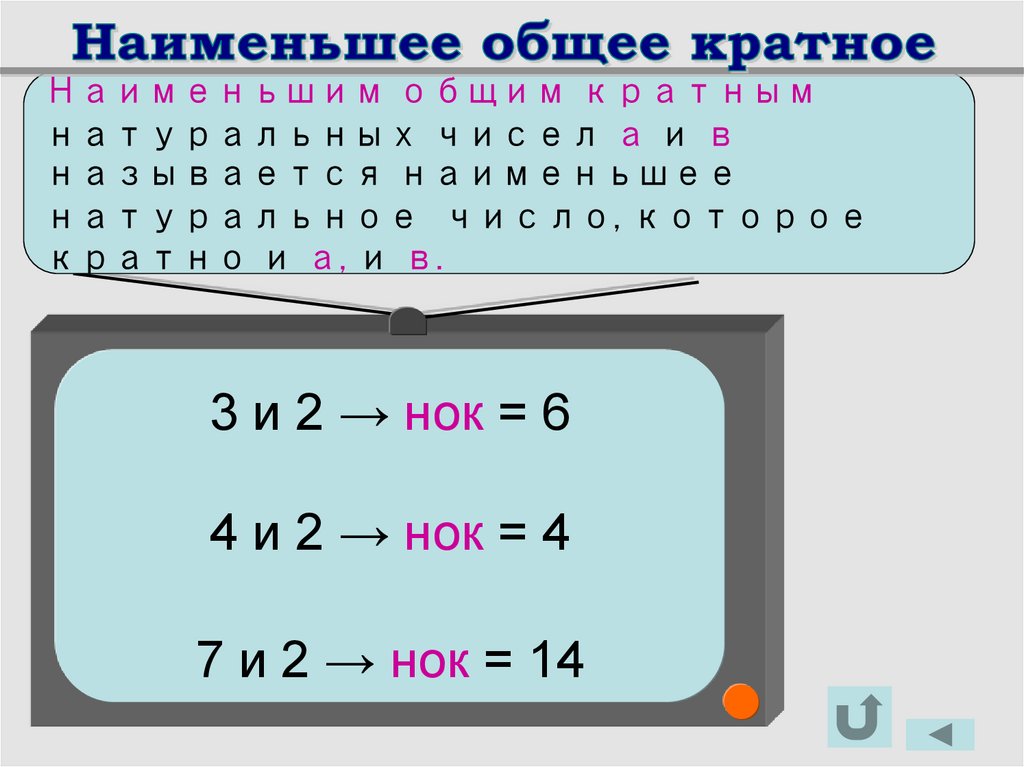
Наименьшим общим кратнымнатуральных чисел а и в
называется наименьшее
натуральное число, которое
кратно и а, и в.
3 и 2 → нок = 6
4 и 2 → нок = 4
7 и 2 → нок = 14
11.
2+3+
+и
2---- 2+
Ba
Al
Na
+
3+
+
2+
+
и
и
NO
Br
S
3Ca
OH
Al
Ca
KKNa
иииNO
иOH
иOH
P
Cl
I 33
1
2
3
4
5
6
7
8
9
10
12. Номенклатура химических соединений
Как строятся названия бинарных соединений?CO2 – диоксид углерода или оксид C(IV)
FeCl3 – трихлорид железа или хлорид Fe(III)
SnCl4 – тетрахлорид Sn или хлорид Sn(IV)
AlJ3 – трииодид Al или иодид алюминия
Ответы:
Задание: назовите химические соединения.
MgBr2 -–…
дибромид Mg или бромид Mg
MgBr
… или … … …
2
SO3 -–…
триоксид S или оксид S (VI)
SO
… или … … …
3
Al2S
S3 -–…
трисульфид Al или сульфид Al
Al
… или … …
2 3
PCl5 -–…
пентахлорид Р или хлорид Р (V)
PCl
… или … … …
5
13.
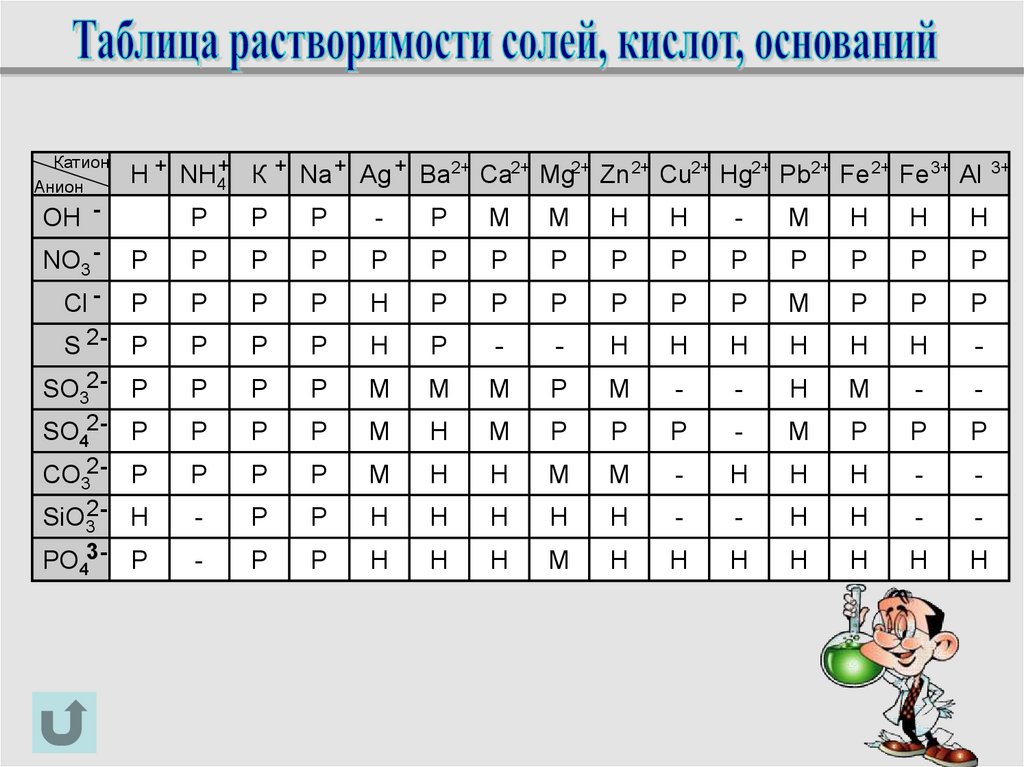
КатионАнион
Н + NH4+ К + Nа + Ag + Ва2+ Cа2+ Mg2+ Zn 2+ Cu2+ Hg2+ Pb2+ Fe 2+ Fe 3+ Al
OH -
Р
Р
Р
-
Р
М
М
Н
Н
-
М
Н
Н
Н
NO3 -
Р
Р
Р
Р
Р
Р
Р
Р
Р
Р
Р
Р
Р
Р
Р
Cl -
Р
Р
Р
Р
Н
Р
Р
Р
Р
Р
Р
М
Р
Р
Р
S 2- Р
Р
Р
Р
Н
Р
-
-
Н
Н
Н
Н
Н
Н
-
SO32- Р
Р
Р
Р
М
М
М
Р
М
-
-
Н
М
-
-
SО42- Р
Р
Р
Р
М
Н
М
Р
Р
Р
-
М
Р
Р
Р
CO32- Р
Р
Р
Р
М
Н
Н
М
М
-
Н
Н
Н
-
-
SiO32- Н
-
Р
Р
Н
Н
Н
Н
Н
-
-
Н
Н
-
-
РО43- Р
-
Р
Р
Н
Н
Н
М
Н
Н
Н
Н
Н
Н
Н
3+
14.
11
2
2
3
3
4
4
5
6
5
7
8
6
9
7
10
Высшие
оксиды
ЛВС
I
H
II
Li
1,007
3
Литий
Na
6,939
11
22,98
Натрий
K
19
39,10
Калий
Cu
29
63,54
Медь
Rb
37
Рубидий
85,47
Ag
47
107,86
Серебро
Cs
55
Цезий
196,96
Fr
III
1
Водород
79
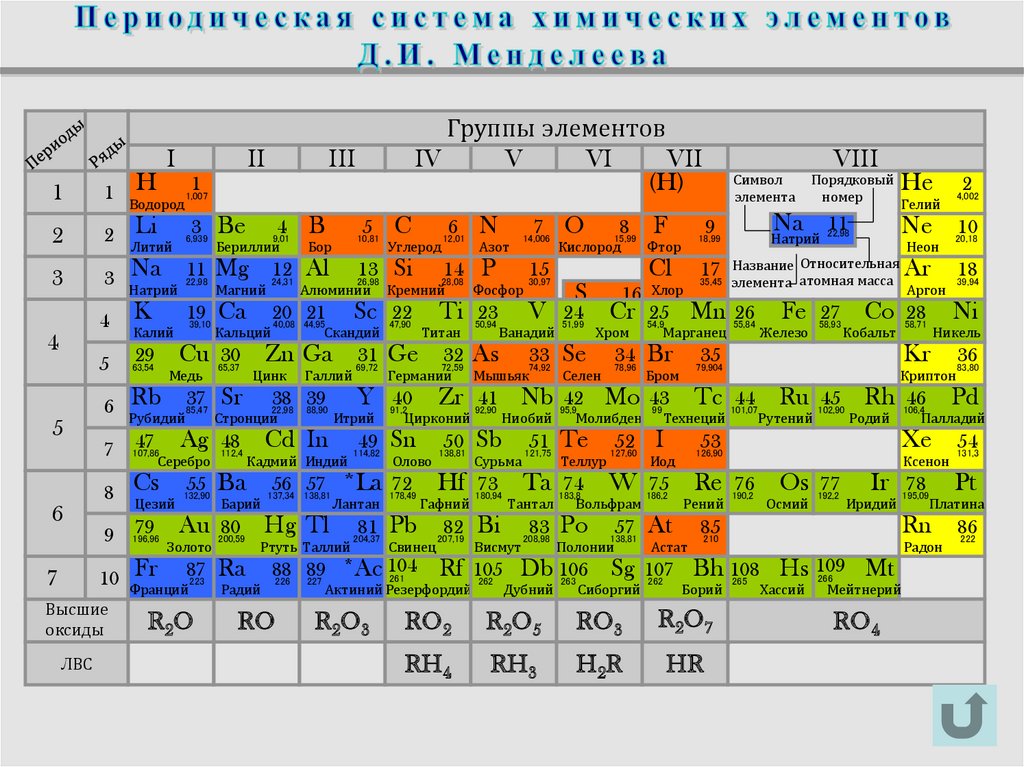
Группы элементов
IV
V
VI
VII
(H)
132,90
Au
Золото
87
223
Франций
R2O
Be
4
B
9,01
Бериллии
Бор
Mg
12
Al
24,31
Магний
Ca
Кальций
Алюминии
Скандий
Цинк
Sr
31
Галлий
38 88,90
39
22,98
Y
Cd In
56 57
Барий
137,34 138,81
49
*La
81
Ртуть Таллий
Ra
Радий
88
89
226
227
RO
114,82
Лантан
Hg Tl
80
69,72
Итрий
Кадмий Индий
Ba
200,59
Sc
20
21
40,08 44,95
Стронции
48
112,4
13
26,98
Zn Ga
30
65,37
5
10,81
204,37
C
6
Углерод
Si
12,01
14
28,08
Кремний
Ti
22
47,90
P
Фосфор
Zr
40
Цирконий
Sn
50
Олово
138,81
72
Hf
Гафний
Pb
Свинец
82
207,19
261
Актиний Резерфордий
30,97
V
23
As
91,2
O
8
15,99
Кислород
Ванадий
33
74,92
Мышьяк
Nb
41
92,90
Ниобий
Sb
51
Сурьма
Ta
73
180,94
Тантал
Bi
83
Висмут
105
262
121,75
208,98
S
16
Cr
32,06
24
Сера
51,99
Хром
Se
34
78,96
Селен
42
95,9
Mo
Молибден
Te
Теллур
74
183,8
52
127,60
W
Вольфрам
Po
57
138,81
Полонии
Db 106 Sg
Дубний
F
Фтор
263
Сиборгий
17
35,45
Хлор
Mn
25
54,9
Марганец
Br
VIII
Порядковый
номер
Na
9
Натрий
18,99
Cl
15
32
72,59
Германии
14,006
Азот
50,94
*Ac 104 Rf
R 2O 3
7
Титан
Ge
178,49
N
Символ
элемента
He
Ne
11
22,98
26
Fe
Железо
Tc
Технеций
I
Kr
44
101,07
Ru
Рутений
45
102,90
Rh
Родий
Re
75
Рений
At
Астат
107
262
76
190,2
Os
Осмий
77
192,2
Ir
Иридий
R2O 5
RO3
R2O 7
RH4
RH3
H 2R
HR
Платина
Радон
265
Хассий
266
Мейтнерий
RO4
54
131,3
Pt
78
195,09
Rn
Bh 108 Hs 109 Mt
RO2
Палладий
Ксенон
85
210
Борий
36
83,80
Pd
46
106,4
Xe
53
186,2
Никель
Криптон
126,90
Иод
Ni
28
58,71
35
43
99
18
39,94
Аргон
Кобальт
79,904
Бром
20,18
Ar
Co
27
58,93
10
Неон
Название Относительная
элемента атомная масса
55,84
2
4,002
Гелий
86
222
15.
1. Степень окисления – этовеличина:
а) переменная,
б) постоянная,
в) постоянная и переменная.
16.
2. Высшая степень окисленияфосфора равна:
а) номеру группы, т.е. 5,
б) нулю,
в) трем.
17.
3. Вещество, формула которогоР2О5, называется
а) оксид фосфора,
б) пентаоксид фосфора (V),
в) оксид фосфора (V) или
пентаоксид фосфора
18.
4. Степень окисления хлораравна -1 в:
а) Cl2O3,
б) PCl5,
в) Cl2.
19.
5. Состав диоксида серывыражается формулой
а) SO2,
б) SO,
в) SO3.
20. Рефлексия
1.На уроке я работал-активно/пассивно
2.Своей работой на уроке я
-доволен /недоволен
3.Урок для меня показался
-коротким / длинным
4.За урок я
-не устал / устал
5.Мое настроение
-стало лучше/стало хуже
6.Материал урока мне был
-понятен / не понятен
-полезен / бесполезен
-интересен / скучен
7.Домашнее задание мне
кажется
-легким / трудным
сегодня я узнал…
было интересно…
было трудно…
я выполнял задания…
я понял, что…
теперь я могу…
я почувствовал, что…
я приобрел…
я научился…
у меня получилось …
я смог…
я попробую…
меня удивило…
урок дал мне для жизни…
мне захотелось узнать…
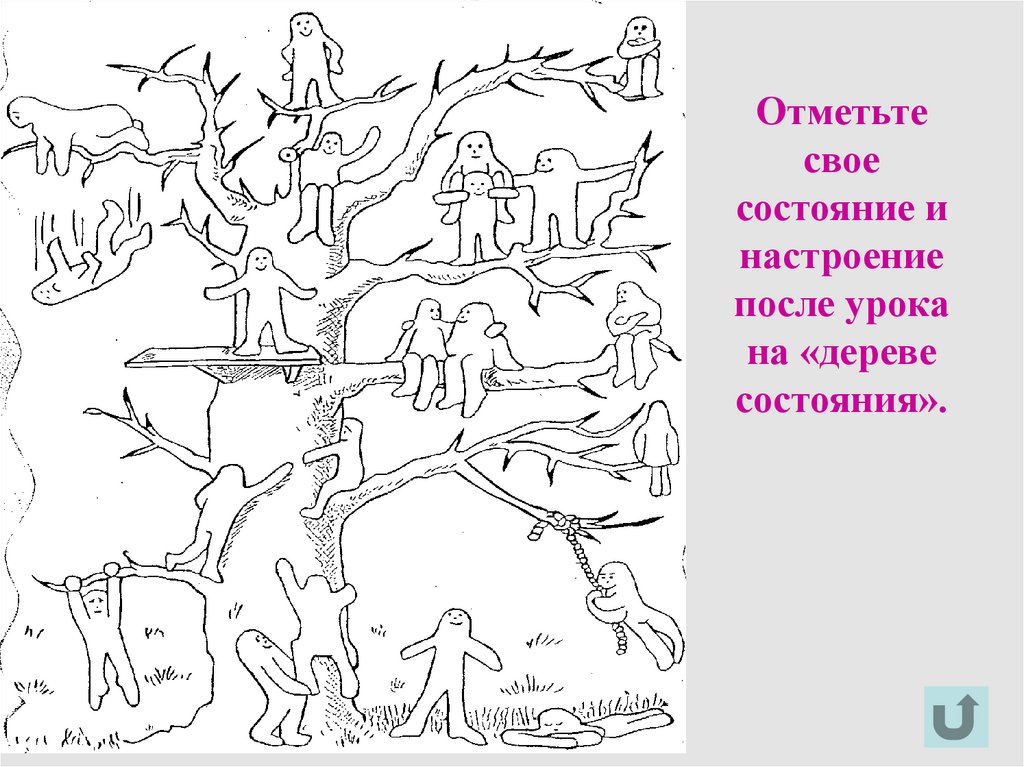
21. Отметьте свое состояние и настроение после урока на «дереве состояния».
22.
http://files.school-collection.edu.ru/dlrstore/c3cf20ae-3d55babf-b8cb4f41b66a35ef/00120068356132562.htm23.
http://files.school-collection.edu.ru/dlrstore/6129acbf-f0d2-b9f50043-cecbe934e509/00120068413911834.htmhttp://files.school-collection.edu.ru/dlrstore/7649825b-15a5-8aca-4b7f0268739dba6e/00120068411849824.htm
http://files.school-collection.edu.ru/dlrstore/84174a2a-cdc2-2d0f-a79d1590e71ca374/00120068409867814.htm
http://files.school-collection.edu.ru/dlrstore/0ab6ce97-4185-11dbb0de-0800200c9a66/ch08_19_02.swf
http://files.school-collection.edu.ru/dlrstore/0ab71cb6-4185-11dbb0de-0800200c9a66/ch08_21_01.swf
24.
СПАСИБО ЗАУРОК !















 chemistry
chemistry








