Similar presentations:
Преимущество статинов компании KRKA в России
1. Преимущество статинов компании KRKA в России
Вводный семинар для новыхсотрудников компании KRKA
Москва, июнь - 2005 г.
2. Разработка статинов компании KRKA …
1996 - ловастатин (ХОЛЕТАР®)1999 – симвастатин (ВАЗИЛИП®)
2002 – аторвастатин (АТОРИС®)
3.
KRKA - единственная компаниявыпускающая 3 статина
таблетки 10, 20 и 40 мг
симвастатин
таблетки 20 и 40 мг
ловастатин
таблетки 10 и 20 мг
аторвастатин
4.
симвастатинтаблетки по 10 мг, 20 мг и 40 мг
Вазилип®. Ваш сердечный друг
5.
В бесконечной борьбе с болезнями, в стремлении ксчастливой жизни и долголетию люди ищут себе
союзника, сердечного друга, всегда готового прийти на
помощь.
Вазилип = долголетие (симвастатин продлевает жизнь)
Долголетие = море (море - бессмертно; это абсолютное здоровье)
Море = дельфин (дельфин – символ моря, дружбы и дружелюбия)
Дельфин = Вазилип
6.
Надежный путь к целитаблетки по 10 мг и 20 мг
аторвастатин
7.
Имидж Аториса8.
Имидж Холетара9. Новаторский метод выделения ловастатина получил патентную защиту в Европе и в России
10. Собственный новаторский метод синтеза симвастатина получил патентную защиту в США и Европе
11. Окончательный результат развития компании КРКА – это Европейское качество
Сертификат соответствияЕвропейской
Фармакопеи
(CoS - Certificate of
Suitability – Сертификат
соответствия)
Выдается Европейским
директоратом
управления качеством
(EDQM – European
Directorate for Quality
Management)
12.
В своем качестве, безопасности иэффективности генерические препараты
компании KRKA эквивалентны оригинальным
Химическая эквивалентность это:
Такая же активная субстанция, такой же чистоты, стабильности и
других фармакологических и химических свойств
Фармацевтическая эквивалентность это:
Такая же активная субстанция (химическая эквивалентность) в такой
же фармацевтической форме, в такой же дозе и при таком же пути
введения (могут отличаться форма таблетки, цвет, неактивные
ингредиенты, упаковка, сроком хранения....)
Терапевтическая эквивалентность:
Фармацевтическая эквивалентность и биоэквивалентность
медицинских продуктов в соответствии со стандартами GMP и
другими международными стандартами
Vir: http://www.fda.gov
13.
Качество активной субстанции было доказанонесколькими аналитическими методами
VWD1 A, Wavelength=238 nm (E:\181200\SIM11120\013-0701.D)
25
-5
8
10
min
15
10
5
4.695
20
3.931 - lovastatin
6
2.914 - simvastatin acid
4
2.027
2
1.520
0
ZOCOR tablets
(MSD)(MSD)
Зокор
табл.
10.939 - dimer simva.
0
7.360 - acet. ester
7.502 - dehydrosimva.
mAU
6.448
5
6.749
6.915
10
5.232 - placebo
0.627 - placebo
3.374 - simvastatin acid
15
5.580 - simvastatin
20
tablets
Вазилип табл. KRKA
(KRKA)
0.368
25
7.719 - dehydrosimva.
6.006 - simvastatin
VWD1 A, Wavelength=238 nm (E:\1050C\170599\170599D\VAS16039\011-0801.D)
mAU
0
-5
0
2
4
6
8
10
min
14.
Вазилип биоэквивалентеноригинальному симвастатину
Исследование биоэквивалентности множественных доз
15.
Концентрация аторвастатинав плазме (нг/мл)
Аторис биоэквивалентен
оригинальному аторвастатину
Средние концентрации аторвастатина в плазме
(линейный график)
Время (часы после приема)
Аторис
Липримар
16. Клинические исследования – важная дополнительная ценность препаратов компании KRKA
Более чем 130 000 пациентов были включены впостмаркетинговые исследования в 22 странах мира, которые
продемонстрировали эффективность и безопасность статинов
компании KRKA.
1637 пациентов включены в мета-анализ исследований
препарата Вазилип в 10 странах
INTER – ARS (международное, мультицентровое, двойное
слепое, рандомизированное исследование препарата Аторис в
сравнении с оригинальным аторвастатином) - доказанная
терапевтическая эквивалентность
17.
ВАЗИЛИП – сегодня один из ведущихгенерических симвастатинов в
Европе.
ВАЗИЛИП – первый
генерический
симвастатин в Европе в
1999 г.
Симвастатин компании
KRKA одобрен к
применению в 43
странах мира.
18.
Аторис – самый перспективныйгенерический аторвастатин в Европе.
АТОРИС – первый
генерический
аторвастатин в Европе в
2002 г.
Единственный
генерический
аторвастатин с
доказанной клинической
эквивалентностью
Аторвастатин компании
KRKA одобрен к
применению в 15 странах
Европы.
19.
Достижения компании KRKAKRKA – лидер среди генерических компаний
производящих статины в Центральной,
Восточной и Юго-Восточной Европе.
KRKA – надежный партнер врачей и пациентов.
20.
Статины KRKA - огромныйклинический опыт
В 2004 году миллион пациентов
были пролечены статинами
компании KRKA (Аторис и
Вазилип).
Статины KRKA вносят важный
вклад в лечение и профилактику
кардиоваскулярных
заболеваний как
высококачественные,
эффективные, и доступные для
большинства пациентов
препараты.
21. Механизм действия статинов
• Влияние на липиды• Плеотропные эффекты
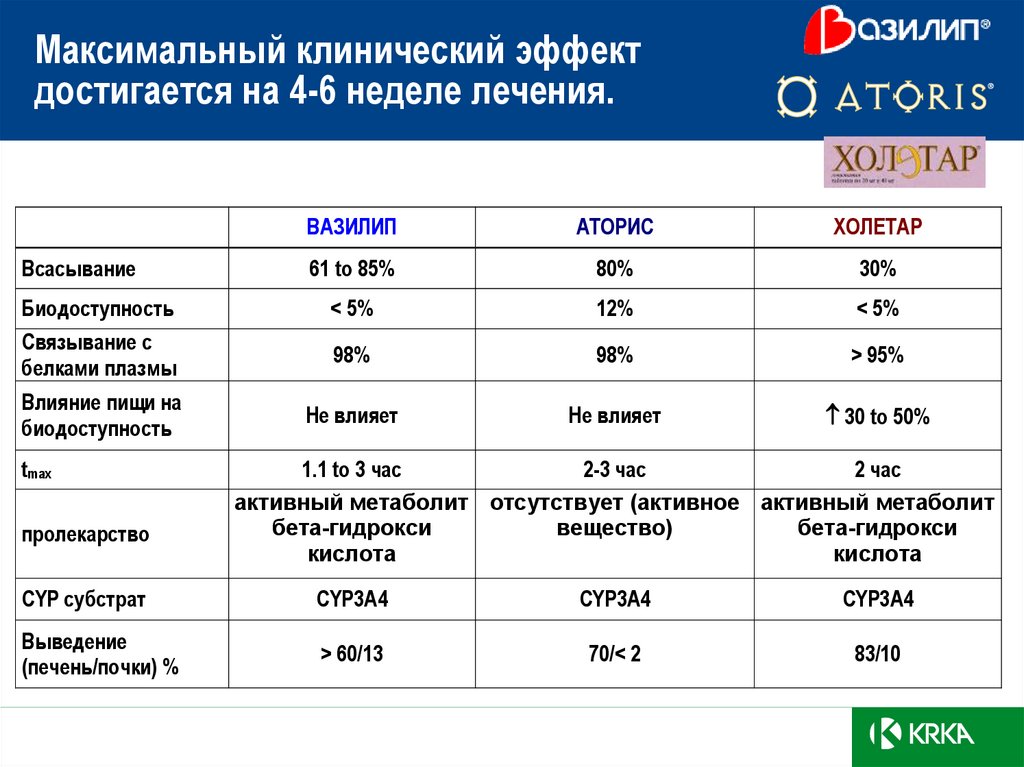
22. Максимальный клинический эффект достигается на 4-6 неделе лечения.
ВсасываниеБиодоступность
Связывание с
белками плазмы
Влияние пищи на
биодоступность
tmax
пролекарство
ВАЗИЛИП
АТОРИС
ХОЛЕТАР
61 to 85%
80%
30%
< 5%
12%
< 5%
98%
98%
> 95%
Не влияет
Не влияет
30 to 50%
1.1 to 3 час
2-3 час
2 час
активный метаболит отсутствует (активное активный метаболит
бета-гидрокси
вещество)
бета-гидрокси
кислота
кислота
CYP субстрат
CYP3A4
CYP3A4
CYP3A4
Выведение
(печень/почки) %
> 60/13
70/< 2
83/10
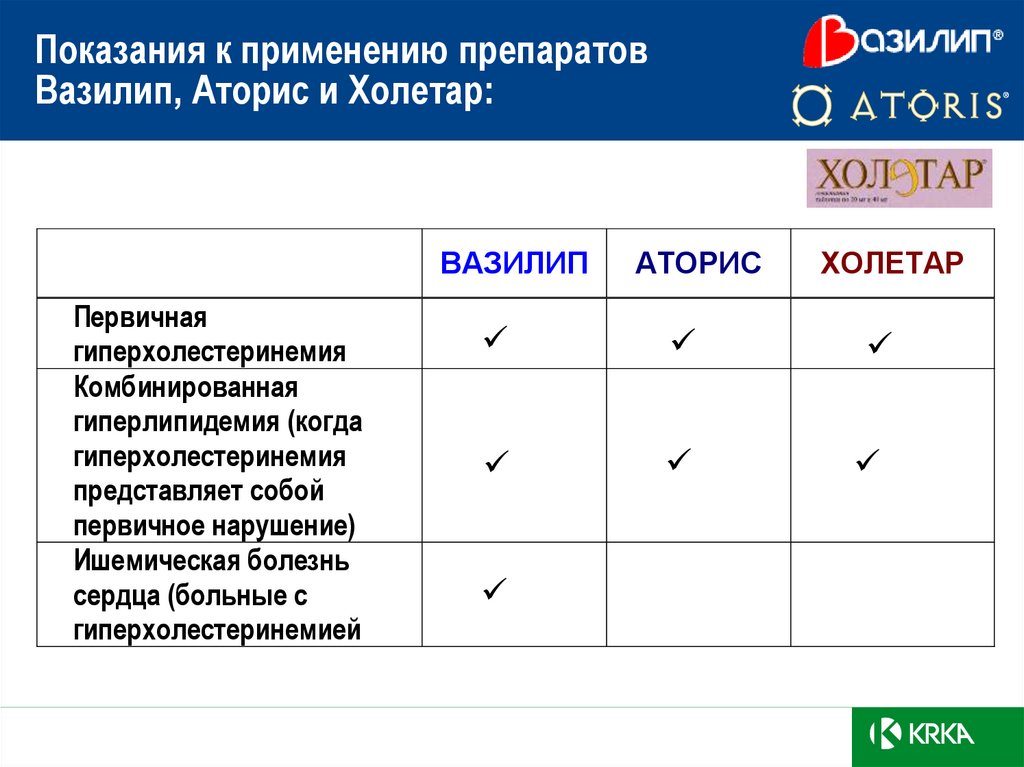
23. Показания к применению препаратов Вазилип, Аторис и Холетар:
Первичнаягиперхолестеринемия
Комбинированная
гиперлипидемия (когда
гиперхолестеринемия
представляет собой
первичное нарушение)
Ишемическая болезнь
сердца (больные с
гиперхолестеринемией
ВАЗИЛИП
АТОРИС
ХОЛЕТАР
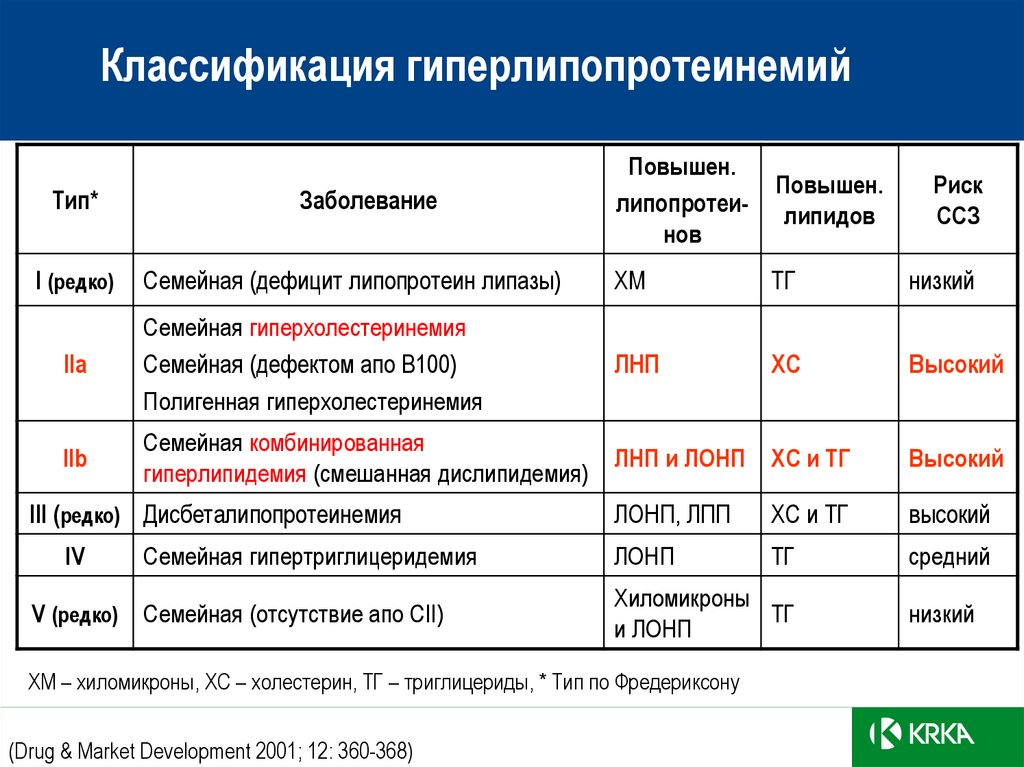
24. Классификация гиперлипопротеинемий
Повышен.липопротеинов
Повышен.
липидов
Риск
ССЗ
Тип*
Заболевание
I (редко)
Семейная (дефицит липопротеин липазы)
ХМ
ТГ
низкий
IIa
Семейная гиперхолестеринемия
Семейная (дефектом апо B100)
Полигенная гиперхолестеринемия
ЛНП
ХС
Высокий
IIb
Семейная комбинированная
ЛНП и ЛОНП ХС и ТГ
гиперлипидемия (смешанная дислипидемия)
III (редко) Дисбеталипопротеинемия
IV
Семейная гипертриглицеридемия
V (редко) Семейная (отсутствие апо СII)
ЛОНП, ЛПП
ХС и ТГ
высокий
ЛОНП
ТГ
средний
Хиломикроны
ТГ
и ЛОНП
низкий
ХМ – хиломикроны, ХС – холестерин, TГ – триглицериды, * Тип по Фредериксону
(Drug & Market Development 2001; 12: 360-368)
Высокий
25.
Вазилип, Аторис, Холетарпротивопоказаны при:
VASILIP
ATORIS
HOLETAR
Повышенной
чувствительности к
статинам
Печеночного заболевания в
активной фазе
Необъяснимых, постоянно
повышенных уровней
трансаминаз в сыворотке
Беременности и кормления
грудью
Заболеваний скелетных
мышц
26. Доказательная база по Вазилипу
27. 1593 пациентов включены в клинические исследования
ЗаконченыПродолжа
ются
Предрегистрационное исследование
Международное, мультицентровое, двойное слепое, сравнительное (70 пациентов)
Пострегистрационные исследования
Чешское – мультицентровое, открытое, сравнительное (55 пациентов)
Словенское – мультицентровое, открытое (312 пациентов)
Литовское – мультицентровое, открытое, вторичная профилактика (30 пациентов)
Хорватия – мультицентровое, открытое (66 пациентов)
Латвийское – мультицентровое, открытое, вторичная профилактика (67 пациентов)
Российское – мультицентровое, открытое, вторичная профилактика (167 пациентов)
Румынское – мультицентровое, открытое, вторичная профилактика (57 пациентов)
Украинское – мультицентровое, открытое, вторичная профилактика (96 пациентов)
Эстонское – мультицентровое, открытое, вторичная профилактика (30 пациентов)
Белорусское – мультицентровое, открытое, вторичная профилактика (43 пациента)
Словенское – мультицентр., открытое, исследование безопасности (400 пациентов)
СербоМакедоноЧерногорское – мультиц., открытое, втор. проф. (100 пациентов)
Польское – мультицентровое, открытое (100 пациентов)
1593 всего пациентов
993
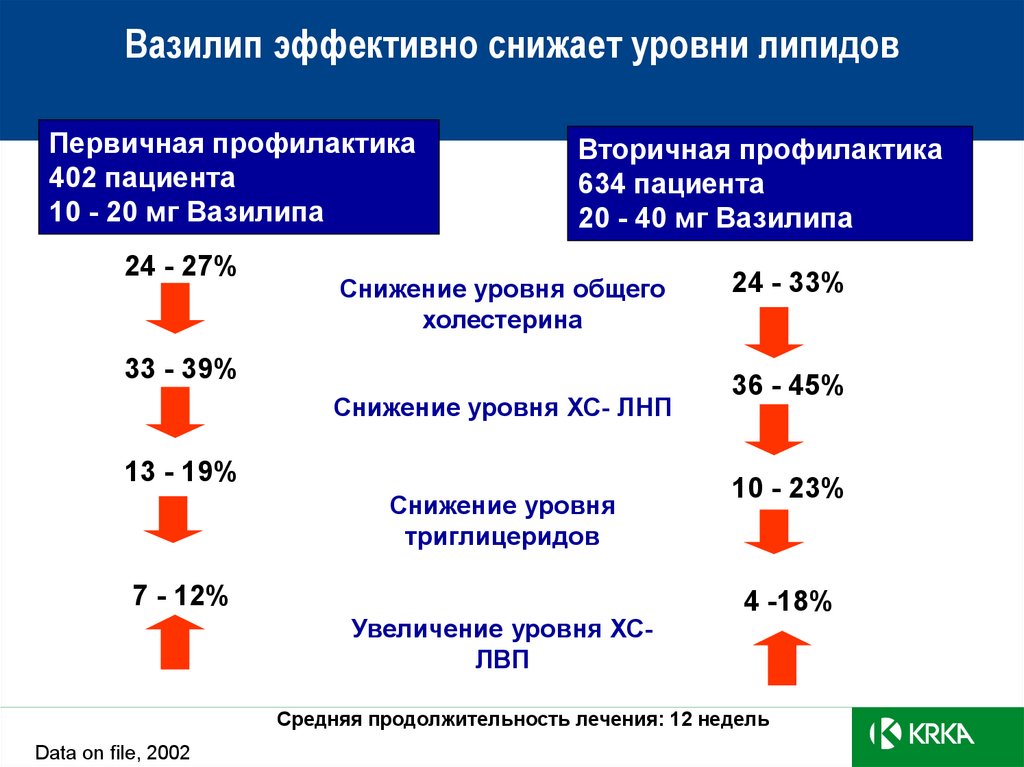
28. Вазилип эффективно снижает уровни липидов
Первичная профилактика402 пациента
10 - 20 мг Вазилипа
24 - 27%
Вторичная профилактика
634 пациента
20 - 40 мг Вазилипа
Снижение уровня общего
холестерина
33 - 39%
Снижение уровня ХС- ЛНП
13 - 19%
Снижение уровня
триглицеридов
7 - 12%
Увеличение уровня ХСЛВП
24 - 33%
36 - 45%
10 - 23%
4 -18%
Средняя продолжительность лечения: 12 недель
Data on file, 2002
29.
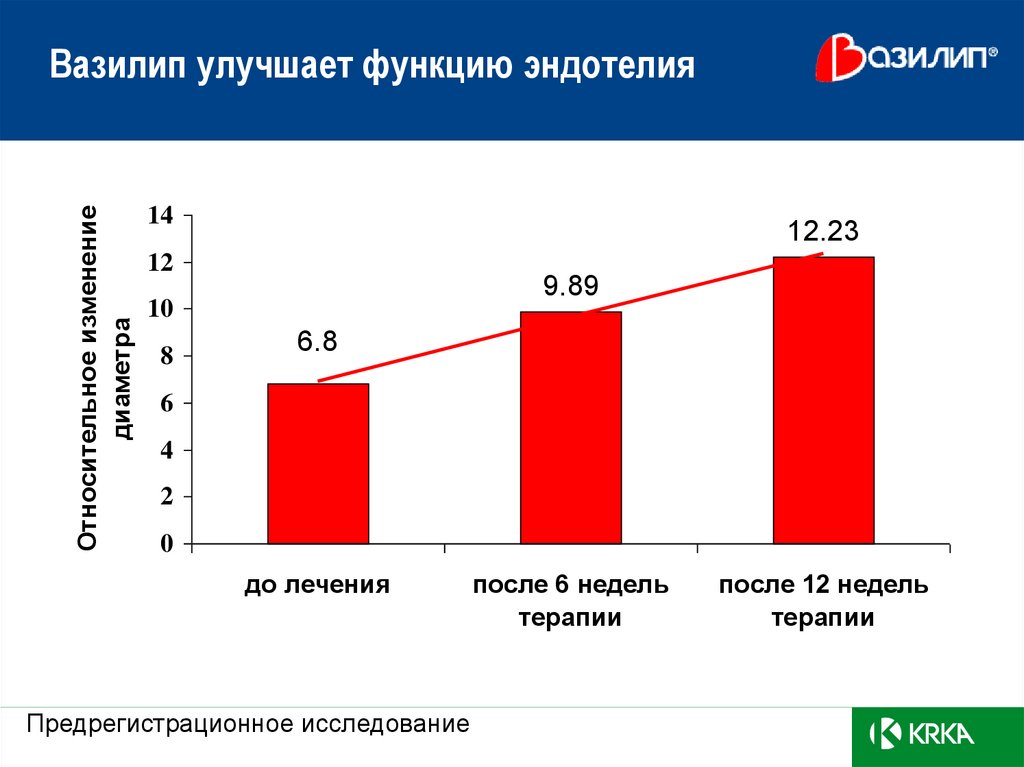
Относительное изменениедиаметра
Вазилип улучшает функцию эндотелия
14
12.23
12
9.89
10
8
6.8
6
4
2
0
до лечения
Предрегистрационное исследование
после 6 недель
терапии
после 12 недель
терапии
30.
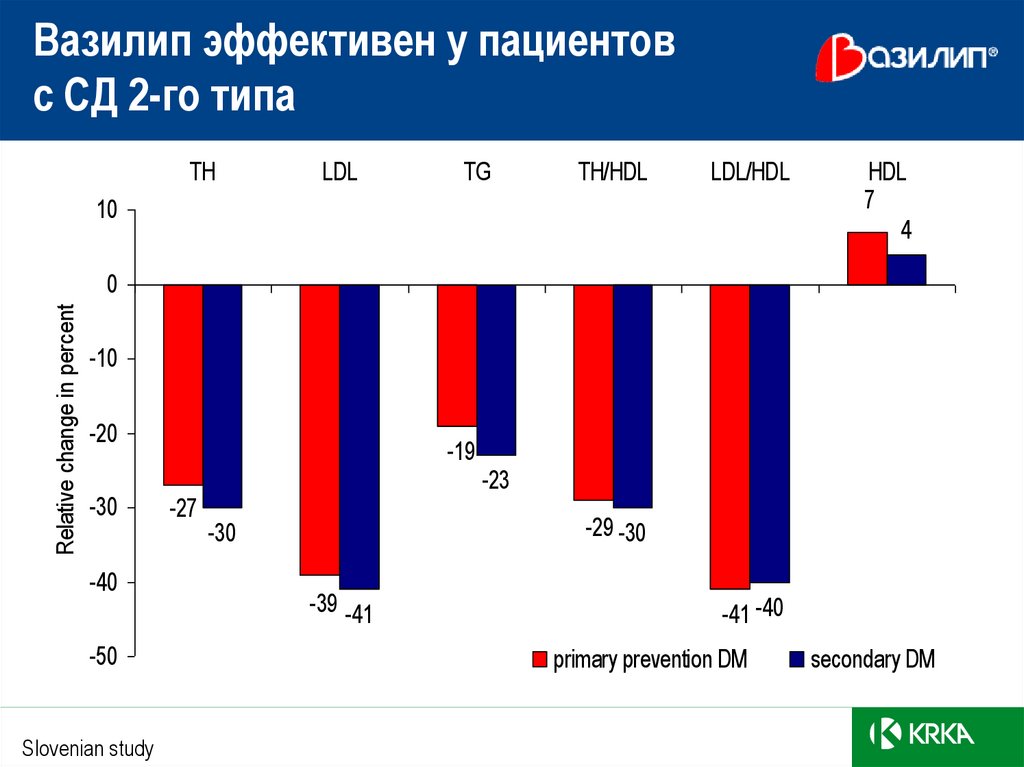
Вазилип эффективен у пациентовс СД 2-го типа
TH
LDL
TG
TH/HDL
LDL/HDL
10
HDL
7
4
Relative change in percent
0
-10
-20
-30
-40
-50
Slovenian study
-19
-27
-23
-29 -30
-30
-39 -41
-41 -40
primary prevention DM
secondary DM
31.
Симвастатин как правило хорошопереноситься пациентами
Наиболее часто встречаются нарушения со
стороны ЖКТ:
запор (2.5 5.7%)
тошнота (1.2 4.4%)
вздутие живота (2 3.4%)
боль в животе (2.5 2.8%)
диспепсия (0.7 2.9%)
диарея (2.9%)
рвота
В прекращении лечения нуждаются только 0,4%
пациентов
32. Вазилип исключительно хорошо переноситься
Ни у одного пациента не было зарегистрировано увеличение АЛТ ИАСТ более, чем в 3 раза выше нормы.
Ни у одного пациента не было зарегистрировано увеличение КФК
более, чем в 10 раз выше нормы.
Во всех исследованиях только у 11 (1,11%) пациентов лечение
было прекращено преждевременно в связи с развитием побочных
эффектов. Ни в одном из этих случаев не была диагностирована
миопатия.
Анализ включал 993 пациента получавших лечение Вазилипом
Data no file, 2004
33.
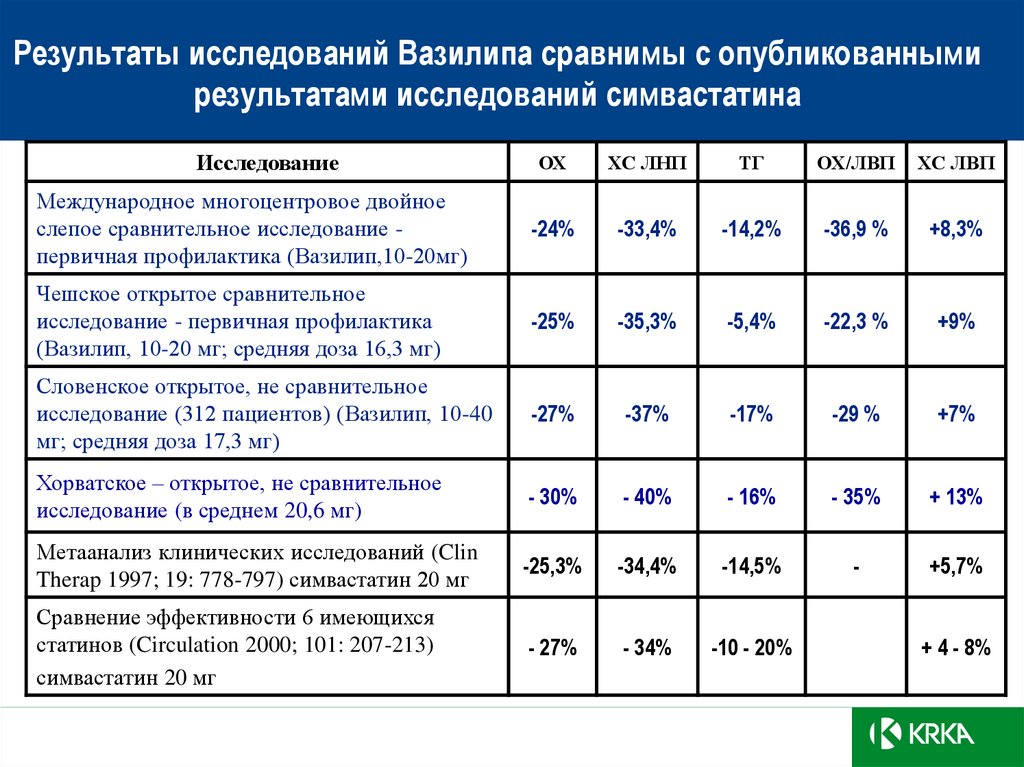
Результаты исследований Вазилипа сравнимы с опубликованнымирезультатами исследований симвастатина
Исследование
ОХ
ХС ЛНП
ТГ
ОХ/ЛВП
ХС ЛВП
Международное многоцентровое двойное
слепое сравнительное исследование первичная профилактика (Вазилип,10-20мг)
-24%
-33,4%
-14,2%
-36,9 %
+8,3%
Чешское открытое сравнительное
исследование - первичная профилактика
(Вазилип, 10-20 мг; средняя доза 16,3 мг)
-25%
-35,3%
-5,4%
-22,3 %
+9%
Словенское открытое, не сравнительное
исследование (312 пациентов) (Вазилип, 10-40
мг; средняя доза 17,3 мг)
-27%
-37%
-17%
-29 %
+7%
Хорватское – открытое, не сравнительное
исследование (в среднем 20,6 мг)
- 30%
- 40%
- 16%
- 35%
+ 13%
Метаанализ клинических исследований (Clin
Therap 1997; 19: 778-797) симвастатин 20 мг
-25,3%
-34,4%
-14,5%
-
+5,7%
Сравнение эффективности 6 имеющихся
статинов (Circulation 2000; 101: 207-213)
симвастатин 20 мг
- 27%
- 34%
-10 - 20%
+ 4 - 8%
34. Вазилип принимается один раз в день
Начальная доза припервичной профилактике
10 мг
Начальная доза при
вторичной профилактике
20 мг
Максимальная доза
80 мг*
* У больных получающих лечение циклоспорином, рекомендуемая начальная
доза 5 мг, максимальная суточная доза Вазилипа составляет 10 мг.
35. Доказательная база по Аторису
36.
Надежный путь к целитаблетки по 10 мг и 20 мг
аторвастатин
Мультицентровое
клиническое исследование
Эффективность и безопасность Аториса у пациентов с
гиперлипидемией и повышенным абсолютным
коронарным риском: сравнение с оригинальным
аторвастатином
37. Дизайн: рандомизированное, двойное слепое в параллельных группах, мультицентровое, сравнительное исследование Аториса и
оригинального аторвастатинаn = 57
Аторис 20/40 mg
ХС ЛНП - больше 3
ммоль/л
M 35 – 65 лет
Ж 45 – 65 лет
ACR более чем 9.51%
(PROCAM calculator)
n = 117
Аторис 10/20 mg
Период 3
Период 2
Период 1
10/20 mg
20/40 mg
Рандомизация после 4
недель приема плацебо
Оригинальный
аторвастатин
n = 60
12 недель
Slovenia, Poland, Czech Republic 2004
38. Аторис значительно и терапевтически эквивалентно снижает ХС ЛНП в сравнении с оригинальным аторвастатином
ммоль/л5
4
Зависимое снижение
4.49
4.46
37.8%
4.35
4.24
2.92
3
Аторис
2
2.89
2.75
2.65
оригинальный
а т орва ст а т и н
1
p < 0.001
0
плацебо
ста р то в ы е зн а че н и я
Slovenia, Poland, Czech Republic 2004
посл е 6 не д е л ь
посл е 1 2 не д е л ь
38.4%
39.
Сравнительная эффективностьв снижении других липидных параметров
Относительные изменения (%)
ОХ
10
5
0
-5
-10
-15
-20
-25
-30
-35
-40
ТГ
ХС ЛВП
ВЧ СРБ
apo B/apo A 1
3.3 3.5
-4
-20.4
-16.8
-19
-30.3 -29.2
Аторис
Slovenia, Poland, Czech Republic 2004
Оригинальный аторвастатин
-37.7 -36.1
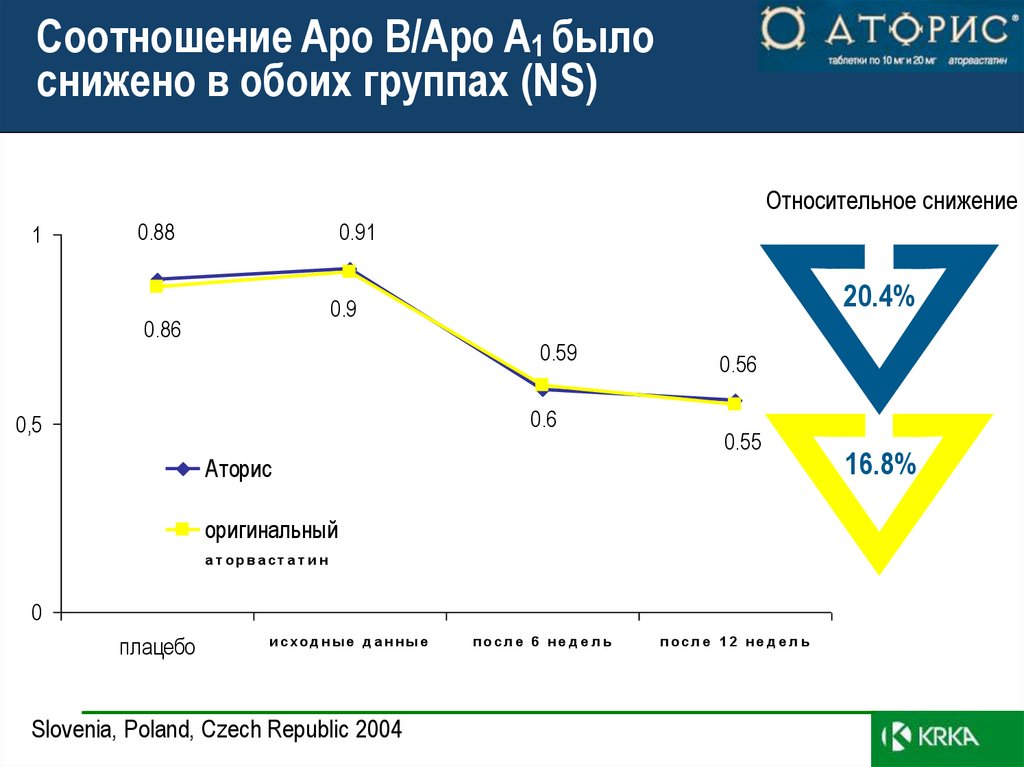
40. Соотношение Apo B/Apo A1 было снижено в обоих группах (NS)
Относительное снижение1
0.91
0.88
20.4%
0.9
0.86
0.59
0.6
0,5
Аторис
0.56
0.55
оригинальный
а т орва ст а т и н
0
плацебо
исход ные д а нные
Slovenia, Poland, Czech Republic 2004
посл е 6 не д е л ь
посл е 1 2 не д е л ь
16.8%
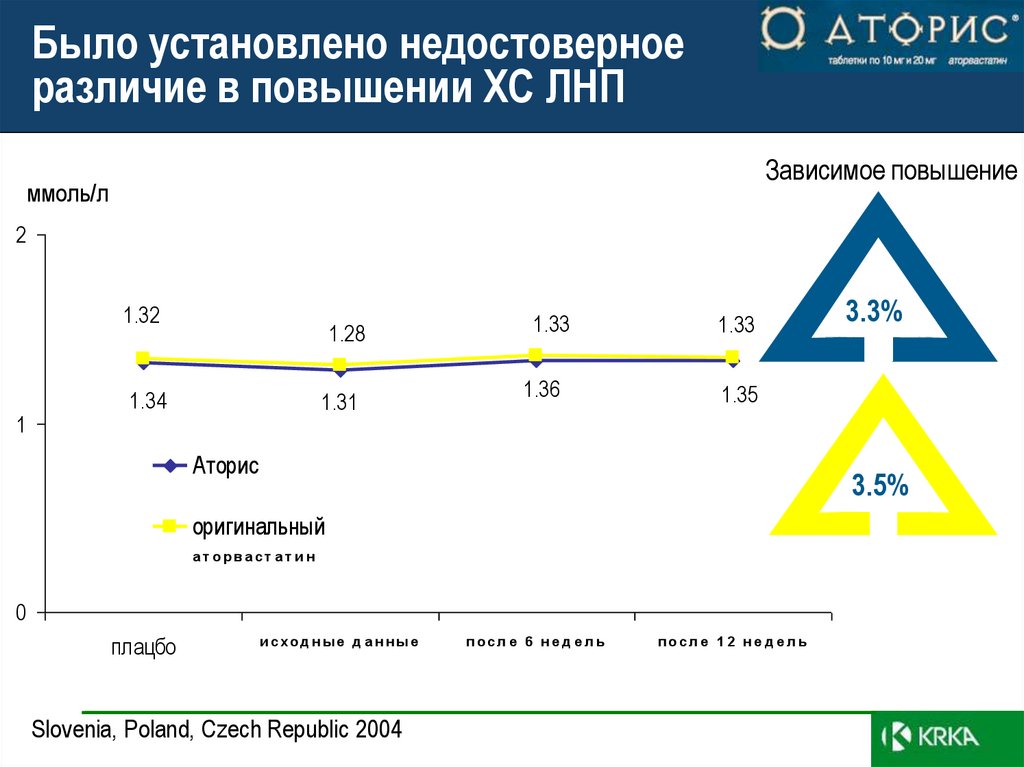
41. Было установлено недостоверное различие в повышении ХС ЛНП
Зависимое повышениеммоль/л
2
1.32
1
1.28
1.34
1.31
1.33
1.33
1.36
1.35
Аторис
3.5%
оригинальный
а т орва ст а т и н
0
плацбо
3.3%
исход ные д а нные
Slovenia, Poland, Czech Republic 2004
посл е 6 не д е л ь
посл е 1 2 не д е л ь
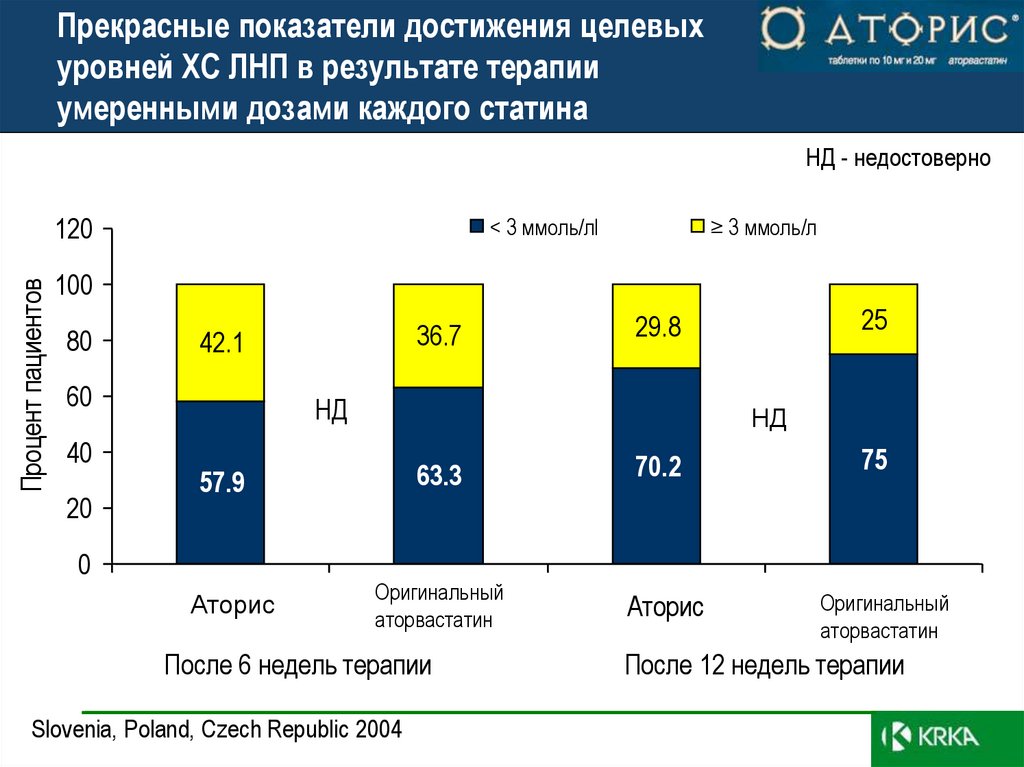
42. Прекрасные показатели достижения целевых уровней ХС ЛНП в результате терапии умеренными дозами каждого статина
НД - недостоверноПроцент пациентов
120
< 3 ммоль/лl
≥ 3 ммоль/л
100
80
42.1
60
40
20
36.7
25
29.8
НД
НД
57.9
63.3
70.2
75
Аторис
Оригинальный
аторвастатин
Аторис
Оригинальный
аторвастатин
0
После 6 недель терапии
Slovenia, Poland, Czech Republic 2004
После 12 недель терапии
43. Исходные дозы аторвастатина составили 20 мг у пациентов, нуждающихся в снижении ХС ЛНП более, чем на 45%.
Аторис, стартовые дозы20 mg
Оригинальный аторвастатин,
20 mg стартовые дозы
11.7%
8.8%
10 mg
10 mg
88.3%
91.2%
Средние дозы во второй и третий период исследования
Период 2
Период 3
Аторис
10.9 мг
16 мг
Оригинальный аторвастатин
11.2 мг
15.7 мг
Slovenia, Poland, Czech Republic 2004
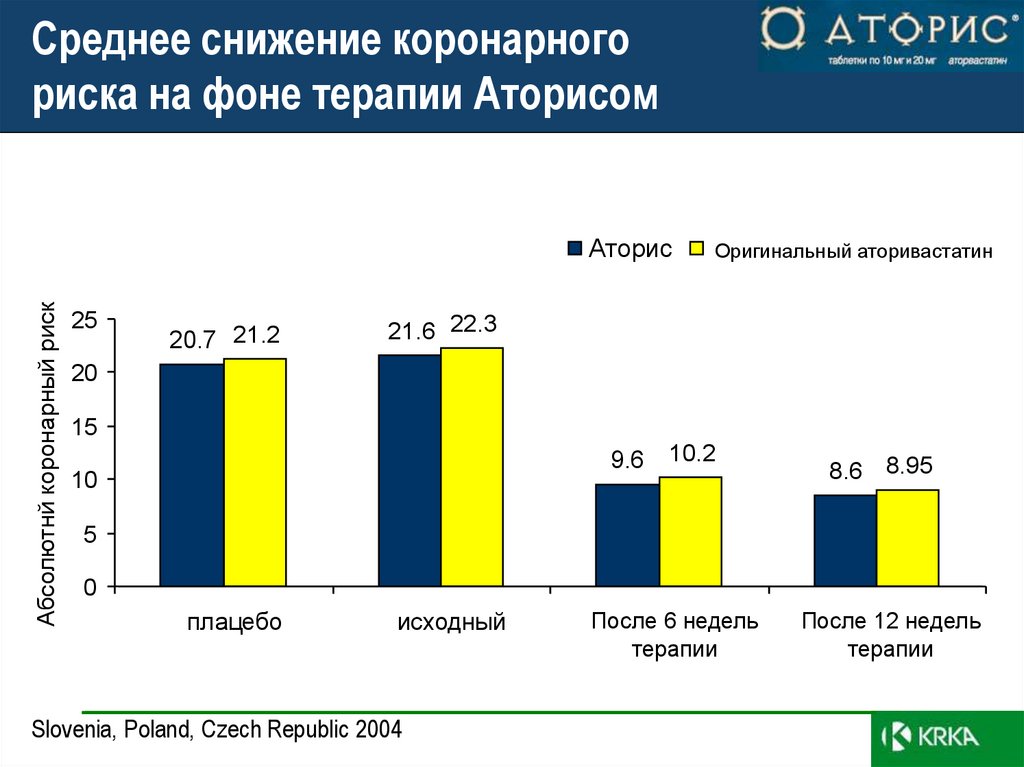
44. Среднее снижение коронарного риска на фоне терапии Аторисом
Абсолютнй коронарный рискАторис
25
20.7 21.2
Оригинальный аторивастатин
21.6 22.3
20
15
9.6
10
10.2
8.6 8.95
5
0
плацебо
исходный
Slovenia, Poland, Czech Republic 2004
После 6 недель
терапии
После 12 недель
терапии
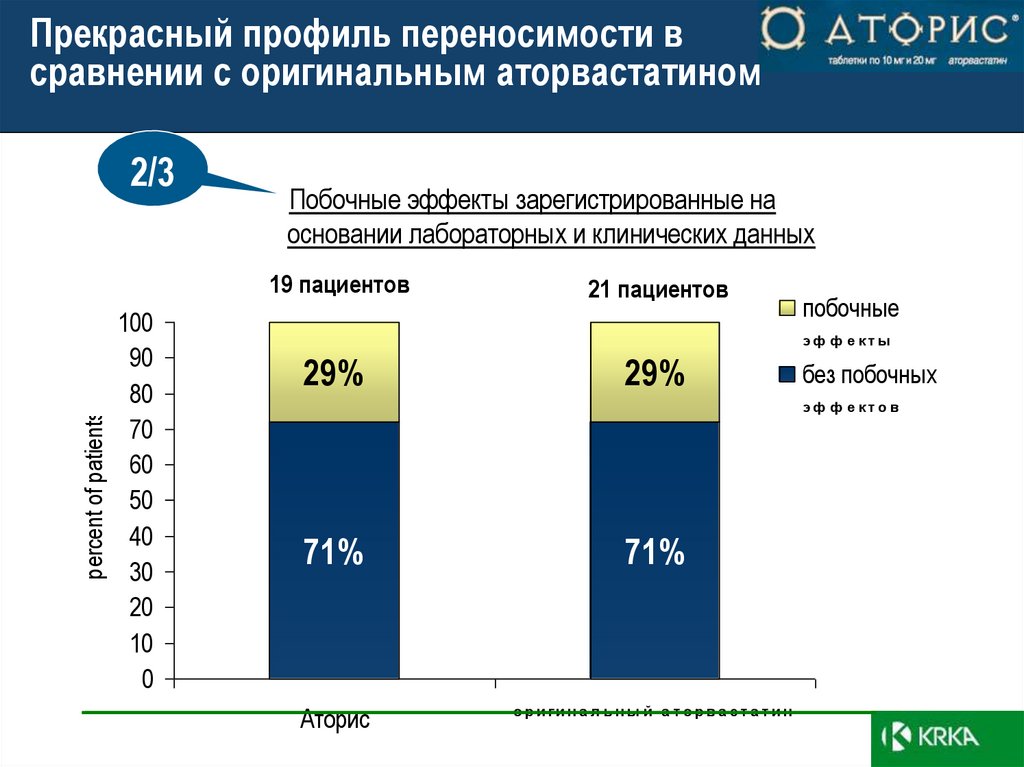
45. Прекрасный профиль переносимости в сравнении с оригинальным аторвастатином
2/3Побочные эффекты зарегистрированные на
основании лабораторных и клинических данных
percent of patients
19 пациентов
100
90
80
70
60
50
40
30
20
10
0
21 пациентов
побочные
эф ф е кты
29%
29%
без побочных
эф ф е ктов
71%
71%
Аторис
о р и ги н а л ь н ы й а т о р в а с т а т и н
46. Прекрасный профиль переносимости в сравнении с оригинальным аторвастатином
Переносимость Аториса полностью сопоставима соригинальным аторвастатином.
Ни у одного пациента терапия Аторисом не была
прервана по причине развития побочных эффектов.
Две третьи зарегистрированных побочных реакций
были несерьезными, незначительное увеличение
лабораторных показателей возвращалось к
исходному значению до окончания периода
исследования.
Slovenia, Poland, Czech Republic 2004
47. Средние показатели АЛТ
kat/l0,7
0,6
0,5
0.53
0.52
0,4
0.56
0.54
0.55
0.49
0.6
0.56
0,3
Аторис
0,2
оригинальный
0,1
а т о р ва с т а т и н
0
плацебо
исходны е да нны е
после 6 не де ль
после 1 2 не де ль
48. Средние показатели АСТ
kat/l0,5
0,45
0,4
0,35
0,3
0,25
0,2
0,15
0,1
0,05
0
0.41
0.39
0.44
0.4
0.42
0.4
0.44
0.43
Аторис
оригинальный
а т о р ва с т а т и н
плацебо
исходны е да нны е
после 6 не де ль
после 1 2 не де ль
49. Средние показатели КФК
kat/l3
2,5
2
2.26
2
1,5
2.42
1.99
2.57
2.46
2.21
1.99
Аторис
1
0,5
оригинальный
а т о р ва с т а т и н
0
плацебо
исходны е да нны е
после 6 не де ль
после 1 2 не де ль
50. Ключевое сообщение
Аторис биоэквивалентен сравниваемому аторвастатинуИспытанная терапевтическая эквивалентность
Аторис значительно и терапевтически эквивалентно снижает ХС ЛНП в
сравнении с оригинальным аторвастатином
Сравнительная эквивалентность в снижении других липидных
параметров
Прекрасная терапевтическая эффективность в
достижении целевых уровней липидов на невысоких
средних дозах Аториса к конце исследования.
Прекрасный профиль переносимости Аториса в
сравнении с оригинальным аторвастатином.
51.
Надежный путь к целиДоказанная
терапевтическая
эквивалентность
52.
Аторис принимают один раз в день,независимо от приема пищи, в одно и
то же время
Рекомендуемая начальная доза 10 мг в день.
Максимальная доза Аториса – 80 мг в день.
Значимый эффект отмечается после двух недель
лечения, а максимальный эффект достигается через
четыре недели.
53. Холетар принимается один раз в день, вечером во время еды
При умеренной гиперхолестеринемии,требующей снижения уровня холестерина ЛНП на
20% или более, начальная доза составляет 20 мг
в сутки с вечерным приемом пищи.
При тяжелой гиперхолестеринемии (уровень
общего холестерина в плазме превышает 7,8
ммоль/л) начальная доза должна составлять 40
мг в сутки.
Суточную дозу можно увеличить до 80 мг, в
один или два приема.
Таблетки следует принимать во время ужина.
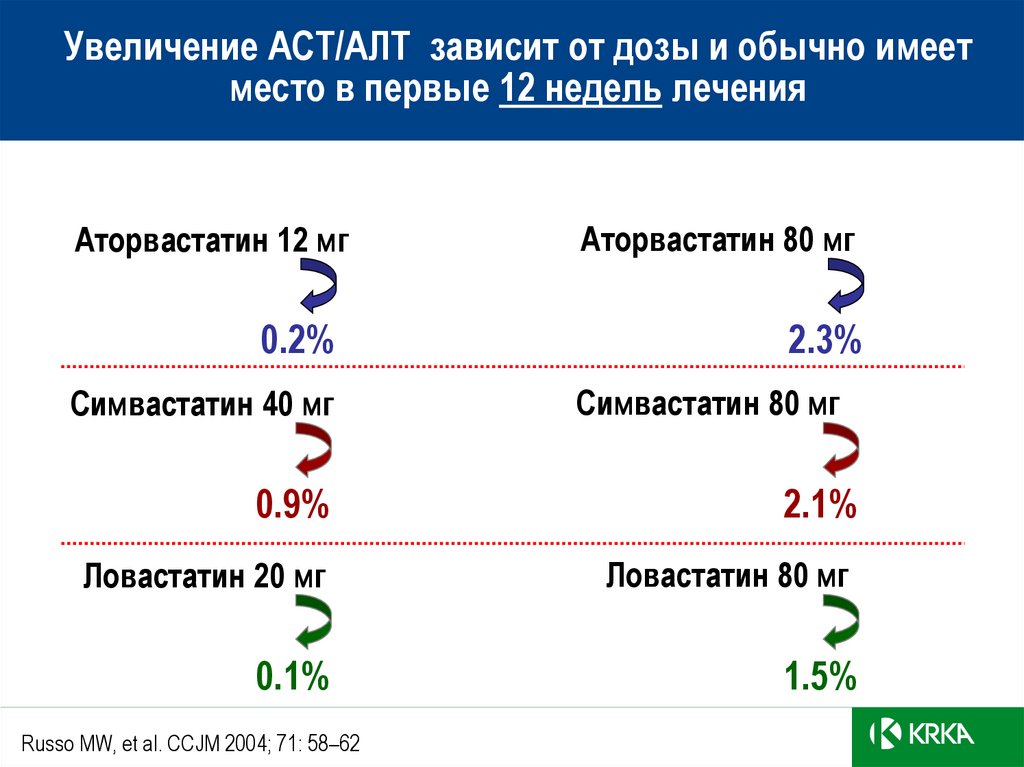
54.
Увеличение АСТ/АЛТ зависит от дозы и обычно имеетместо в первые 12 недель лечения
Аторвастатин 12 мг
Аторвастатин 80 мг
0.2%
2.3%
Симвастатин 40 мг
Симвастатин 80 мг
0.9%
2.1%
Ловастатин 20 мг
Ловастатин 80 мг
0.1%
1.5%
Russo MW, et al. CCJM 2004; 71: 58–62
55.
Важным, но очень редким побочным эффектомявляется поражение мышц (миопатия)
Миалгия (жалобы на боли
в мышцах без подьема КФК)
В клинических
исследованиях от
1% до 5%
Talamini MA. JAMA 2003; 289: 1681–1690
Мышечная боль,
снижает качество
жизни пациентов и
комплайнс
Составляет до 25% от
всех побочных
эффектов при приеме
статинов.
56.
Важным, но очень редким побочным эффектомявляется поражение мышц (миопатия)
Пациенты с умренным увеличением
показателей КФК могут не иметь никаких
клинических симптомов
3 to 5%
Клинически важные миозиты определяются:
болью в мышцах с уровнем КФК более чем в 10 раз
выше верхней границы нормы
CK – creatinine kinase
ULN – upper limit of normal
Talamini MA. JAMA 2003; 289: 1681–1690
57.
Важным, но очень редким побочным эффектомявляется поражение мышц (миопатия)
Случай фатального рабдомиолиза
0,15 летальных исходов на 1
миллион назначений
Talamini MA. JAMA 2003; 289: 1681–1690
58.
Холетар, Вазилип и Аторис - продукт работы отделанаучных исследований и разработок компании КРКА.
Препараты имеют результаты исследований на
биоэквивалентность и клинический опыт
эффективного и безопасного применения.
Они являются наиболее значимыми препаратами в
первичной и вторичной профилактики заболеваний
связанных с атеросклерозом.












































 medicine
medicine








