Similar presentations:
Горіння полімерів і металів
1.
ГОРІННЯ ПОЛІМЕРІВ І МЕТАЛІВПлан лекції
Вступ
1. Загальні поняття та класифікація полімерів.
2. Основні закономірності процесу горіння
пластмас.
2.1. Загальні закономірності горіння
полімерних матеріалів.
2.2. Способи зниження горючості полімерів і
виробів на їх основі.
3. Горіння металів.
2. 1. ЗАГАЛЬНІ ПОНЯТТЯ ТА КЛАСИФІКАЦІЯ ПОЛІМЕРІВ
Полімери - високомолекулярні речовини змолекулярною масою більше за 5000 а. од., молекули
яких складаються із ланцюгів (мономерів), що багато
разів повторюються.
Пластмаса - матеріал, що складається з полімерів або
їх сумішей з органічними і неорганічними
речовинами, здатний набувати за певних умов
пластичного стану і під впливом деформуючих
навантажень певну форму із збереженням її після
припинення впливу.
3.
До складу пластмас крім полімерів входять:Наповнювачі - непластичні речовини, яки сприяють
підвищенню механічної міцності, теплостійкості,
зниженню горючості. (пісок, гіпс, оксиди і солі деяких
металів і т.д.)
Пластифікатори - матеріали, що збільшують
пластичність матеріалу і полегшують формування.
Стабілізатори – матеріали, що сприяють збереженню
властивостей пластмас захищають від окислювання, дії
УФ опромінення (уповільнюють старіння).
4.
Полімери, макромолекули яких складаються змономеру одного виду, називають
гомополімерами, а з двох і більшого числа
різних мономерів – сополімерами.
Класифікація полімерів
1.за походженням;
2.за складом ланцюга;
3.за структурою макромолекули;
4.за способом отримання;
5.за поведінкою при нагріванні.
5.
За походженнямприродні
(целюлоза,крохмаль,
казеїн)
синтетичні
штучні
(полістирол, поліетилен,
поліуретан, поліамід)
(віскоза,
ацетатний шовк)
За складом основного ланцюга
карболанцюгові - основні полімерні ланцюги
побудовані тільки з атомів вуглецю;
гетероланцюгові - основні полімерні ланцюги
містять гетероатоми (кисень, азот, фосфор, сірку і
ін.);
елементоорганічні - основні ланцюги макромолекул
містять такі елементи як силіцій, алюміній, титан,
бор, свинець, олово і інші
6.
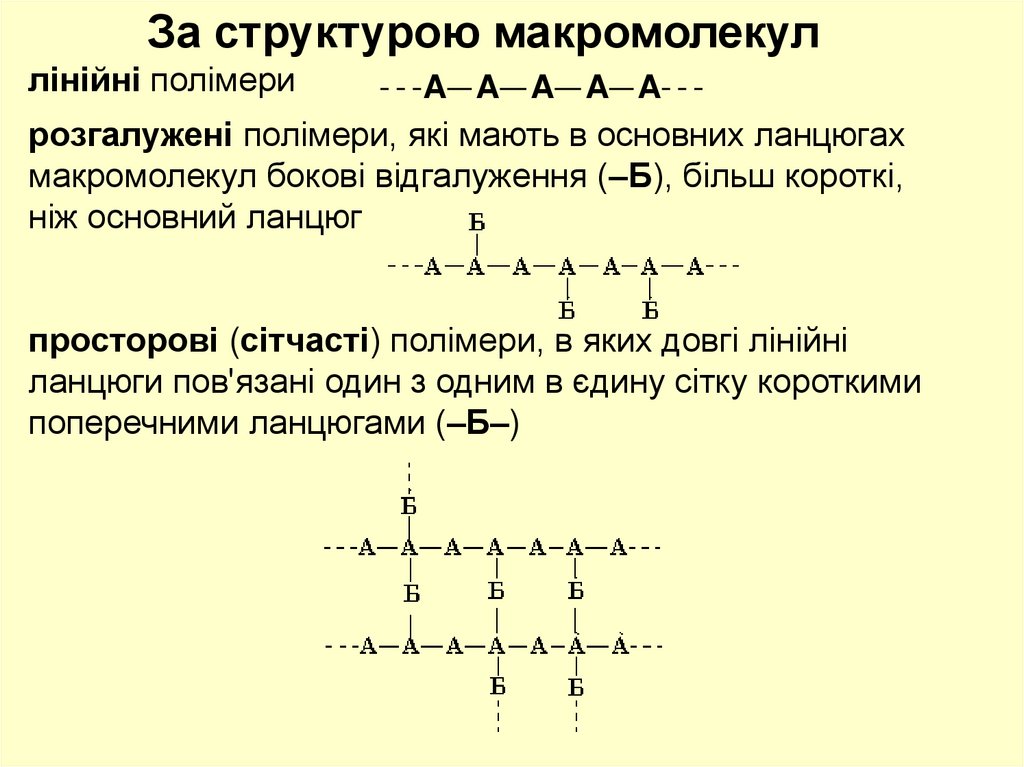
За структурою макромолекуллінійні полімери
A A A A A
розгалужені полімери, які мають в основних ланцюгах
макромолекул бокові відгалуження (–Б), більш короткі,
ніж основний ланцюг
просторові (сітчасті) полімери, в яких довгі лінійні
ланцюги пов'язані один з одним в єдину сітку короткими
поперечними ланцюгами (–Б–)
7.
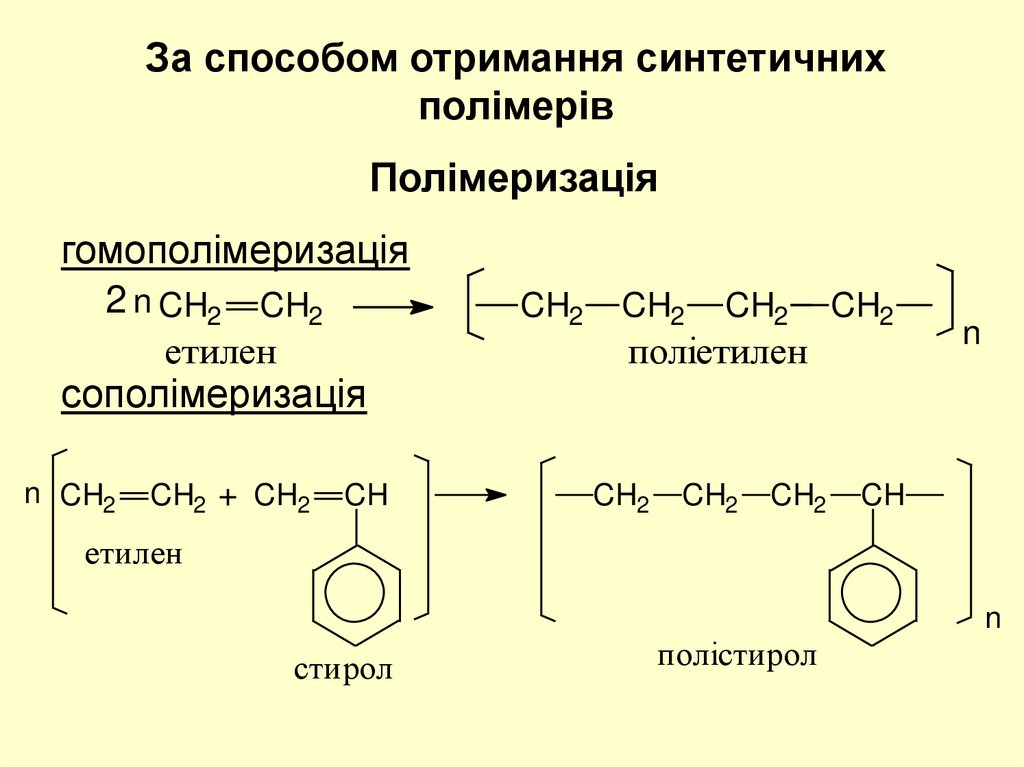
За способом отримання синтетичнихполімерів
Полімеризація
гомополімеризація
2 n CH2 CH2
етилен
сополімеризація
n CH2
CH2 + CH2
CH
CH2
CH2
CH2
поліетилен
CH2
CH2
CH2
CH2
n
CH
етилен
n
стирол
полістирол
8.
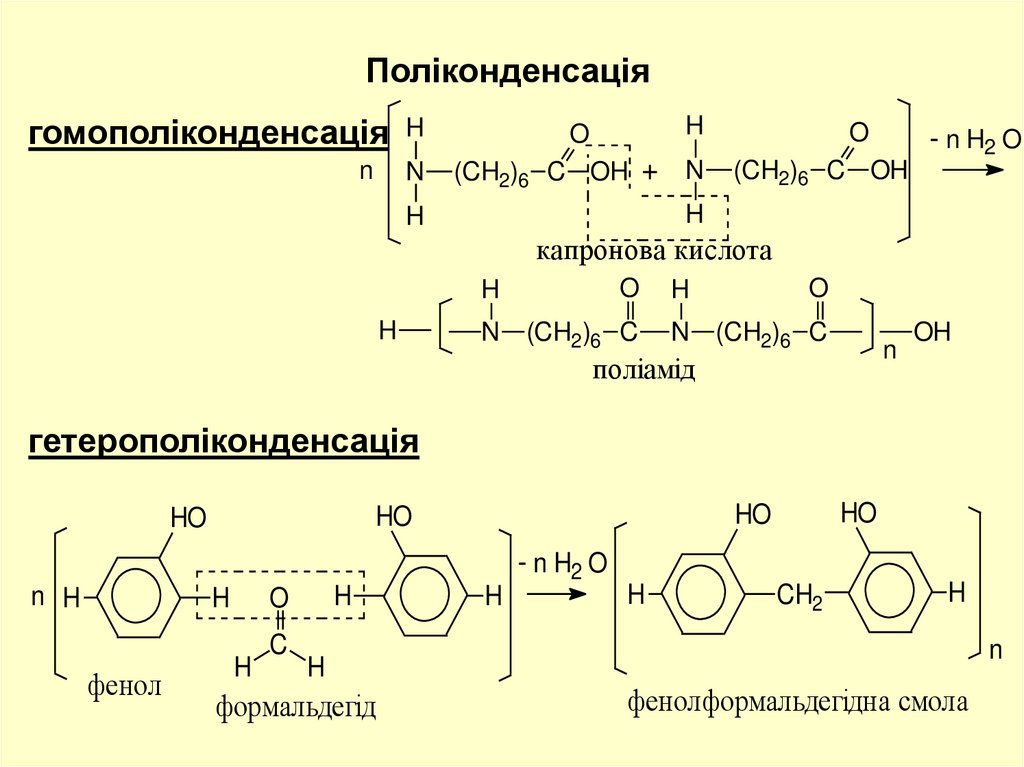
Поліконденсаціягомополіконденсація H
n
N
H
O
(CH2)6 C OH +
N
O
- n H2 O
(CH2)6 C OH
H
H
капронова кислота
H
H
O
H
O
N
(CH2)6 C
N
(CH2)6 C
n
поліамід
OH
гетерополіконденсація
- n H2 O
n H
H
фенол
H
O
H
C
HO
HO
HO
HO
H
H
CH2
H
n
H
формальдегід
фенолформальдегідна смола
9.
За поведінкою при нагріванніТермопластичні полімери (термопласти). Полімери,
властивості яких зворотно змінюються при
багаторазовому нагріванні і охолоджуванні.
(поліетилен, поліпропілен, полістирол)
мають лінійну структуру, низькою температурою
розм'якшення (80-100оС)
Термореактивні полімери (реапласти). Полімери з
просторовою або розгалуженою структурою, при
термічному впливі їх молекули розкладаються и
властивості змінюються безповоротно (гума,
фенолформальдегідна смола
10. ОСНОВНІ ЗАКОНОМІРНОСТІ ПРОЦЕСУ ГОРІННЯ ПЛАСТМАС
2.1. Загальні закономірності горіння полімернихматеріалів
Всі полімери відносяться до ТГМ, що газифікуються
Термопласти, отримані полімеризацією, мають лінійну
структуру і відносяться до ТГМ 1-го роду, При
горінні товщина рідкого шару на горизонтальній
поверхні становить 10 - 20 мм, а на вертикальній - 12 мм. В умовах пожежі для даних полімерів
характерні явища розтікання розплаву і
краплепадіння
11.
Термореактивні полімери (реапласти), отриманніметодом поліконденсації, мають розгалужену або
сітчасту структуру, відносяться до ТГМ 2-го роду,
горять в гомогенному і гетерогенному режимі, здатні до
тління. (пінополіуретани, фенопласти, спінені гуми)
Стадії розкладання і горіння полімерів
1. Нагрівання до температури плавлення (розкладання);
2. Деструкція речовини (розрив зв'язків С-Н, С-Наl, С-О,
деполімеризація;
3. Нагрів газоподібних продуктів розкладання і їх
додатковий крекінг;
4. Запалення летючих продуктів розкладання, стадія
гомогенного горіння.
5. У разі утворення залишку вуглецю, гетерогенне
горіння.
12. Відмінні особливості горіння полімерів
1. Через велику молекулярну масу полімери невипаровуються, а розкладаються, і тому не мають
певних температур кипіння і плавлення.
2. Велика густина задимлення;
3. Режим горіння (гомогенний, гетерогенний)
залежить від структури макромолекули та складу
пластмас;
4. Велика теплотворна здатність, і відповідно, висока
температура горіння;
5.Можливість розтікання та краплепадіння при
горінні термопластів;
6.Висока токсичність продуктів розкладання і
горіння.
13. 2.2. Способи зниження горючості полімерів
1. Захист полімерів за рахунок утворення на поверхні негорючоїсклоподібної плівки під дією високої температури на деякі
компоненти пластмас (борна кислота, бура, сполуки фосфору і
інші), яка погіршує підведення окислювача і відведення
продуктів піролізу;
2. Модифікація полімерів реакційноздатними сполуками, які
спричиняють зміну структури полімеру з метою сповільнення
його розкладання і інгібірування полум'яних реакцій (обрив
радикально-ланцюгових реакцій горіння за допомогою
продуктів деструкції);
3. Введення негорючого наповнювача (гіпсу, оксидів деяких
металів, силіцію, різних солей);
4. Введення в композицію антипіренів, які сприяють зміні
механізму реакцій деструкції полімерів і збагаченню газової
фази негорючими речовинами (Н2О, СО2, НСl і ін.).
14. 3. ОСОБЛИВОСТІ ГОРІННЯ МЕТАЛІВ
Горючими є ті метали, які можуть самостійно горітина повітрі після впливу джерела запалювання
середньої потужності.
Метали на пожежах можуть горіти суцільною масою
(калій, кальцій, натрій, магній) або у вигляді
ошурок, порошків (алюміній, титан і ін.).
Початковою стадією горіння металу є утворенням
поверхневої оксидної плівки.
Характер утвореної плівки (рихла або щільна)
визначає подальший характер горіння
15.
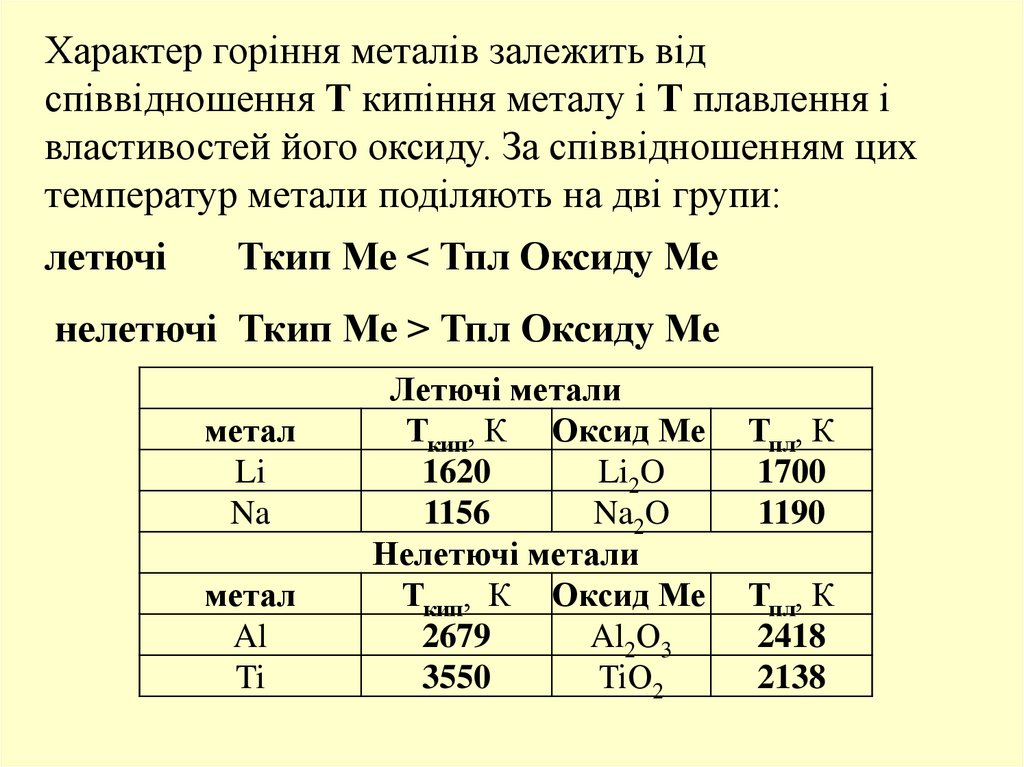
Характер горіння металів залежить відспіввідношення Т кипіння металу і Т плавлення і
властивостей його оксиду. За співвідношенням цих
температур метали поділяють на дві групи:
летючі
Ткип Ме < Тпл Оксиду Ме
нелетючі Ткип Ме > Тпл Оксиду Ме
метал
Li
Na
метал
Al
Ti
Летючі метали
Ткип, К Оксид Ме
1620
Li2O
1156
Na2O
Нелетючі метали
Ткип, К Оксид Ме
2679
Al2О3
3550
TiО2
Тпл, К
1700
1190
Тпл, К
2418
2138
16.
Горіння летючих металівОкисна плівка є пористою не ізолює поверхню
металу від окислення і виходу парів металу на
поверхню.
При дії ДЗ на поверхню Ме оксидна плівка
залишається твердою а Ме під оксидною плівкою
плавиться і переходить в рідкий стан.
Пара Ме дифундує крізь пористу оксидну плівку у
повітря, і по досягненні НКМПП займається,
встановлюється гомогенне горіння.
Утворення білого щільного диму є візуальною
ознакою горіння летючих металів
17.
Горіння нелетючих металівНа поверхні Ме утворюється щільна оксидна
плівка, яка ускладнює подальше окислення.
При дії ДЗ Ме плавитися, але концентрація парів
металу в повітрі менше, ніж НКМПП. Подальше
нагрівання призводить до розплавлення оксидної
плівки в розплаві металу. На поверхню виходить
нагрітий до високої температури метал, який
починає горіти на межі розділу фаз.
Горіння відбувається в гетерогенному режимі.
Ткип таких металів більша, ніж їх Тгор.
18.
особливості горіння металів1. Режим горіння залежить від властивостей окисної плівки
2. Горіння може відбуватися в середовищі продуктів горіння
органічних речовин:
Na + H2O = NaOH + 0,5 H2
2Na + CO2 = Na2O + CO
3. Метали горять з виділенням великої кількості енергії і
випромінюванням. Температура їх горіння 2500 - 3500 К.
У зв'язку з цим
ЗАБОРОНЕНО ГАСІННЯ МЕТАЛІВ:
а) ВОДОЮ внаслідок її розкладання на водень і кисень;
H2O = H2 + 0,5O2
б) CO2 розкладається на вуглець і кисень.
CO2 = С + O2
в) АЗОТОМ взаємодіє з металом з утворенням нітридів металів.
Li3N, K3N, Na3N, Mg3N2
19.
Завдання на самопідготовку:1. Демидов, Шандыба, Щеглов - Горение и
свойства горючих веществ. С. 148-156;
2. Демидов, Саушев - Горение и свойства
горючих веществ. С. 225-232;
3. Підготуватися до лаб. роботи №8















 chemistry
chemistry








