Similar presentations:
Алкадиены. Физические и химические свойства
1.
Алкадиены2.
Алкадиены – ациклические углеводороды,содержащие в молекуле, помимо одинарных связей,
две двойные связи между атомами углерода.
3.
Алкадиены – ациклические углеводороды,содержащие в молекуле, помимо одинарных связей,
две двойные связи между атомами углерода.
Общая формула CnH2n-2
4.
Изомерия1) Структурная изомерия: изомерия углеродного
скелета
2-метилбутадиен-1,3
(изопрен)
5.
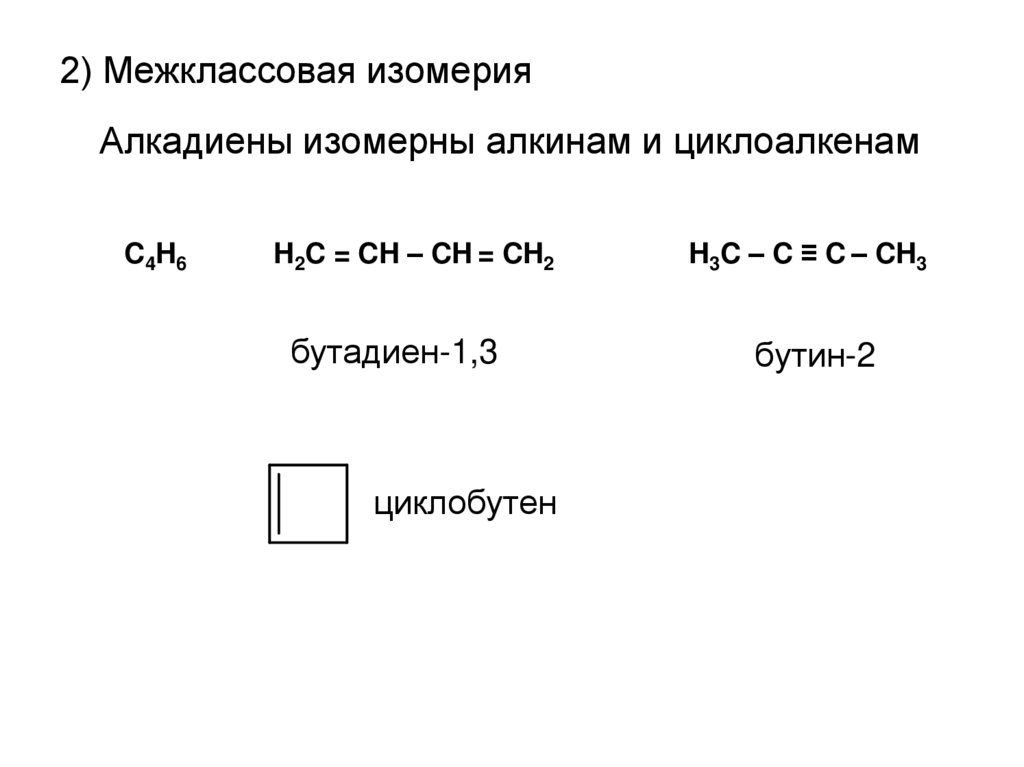
2) Межклассовая изомерияАлкадиены изомерны алкинам и циклоалкенам
C 4H 6
H2C = CH – CH = CH2
H3C – C ≡ C – CH3
бутадиен-1,3
бутин-2
циклобутен
6.
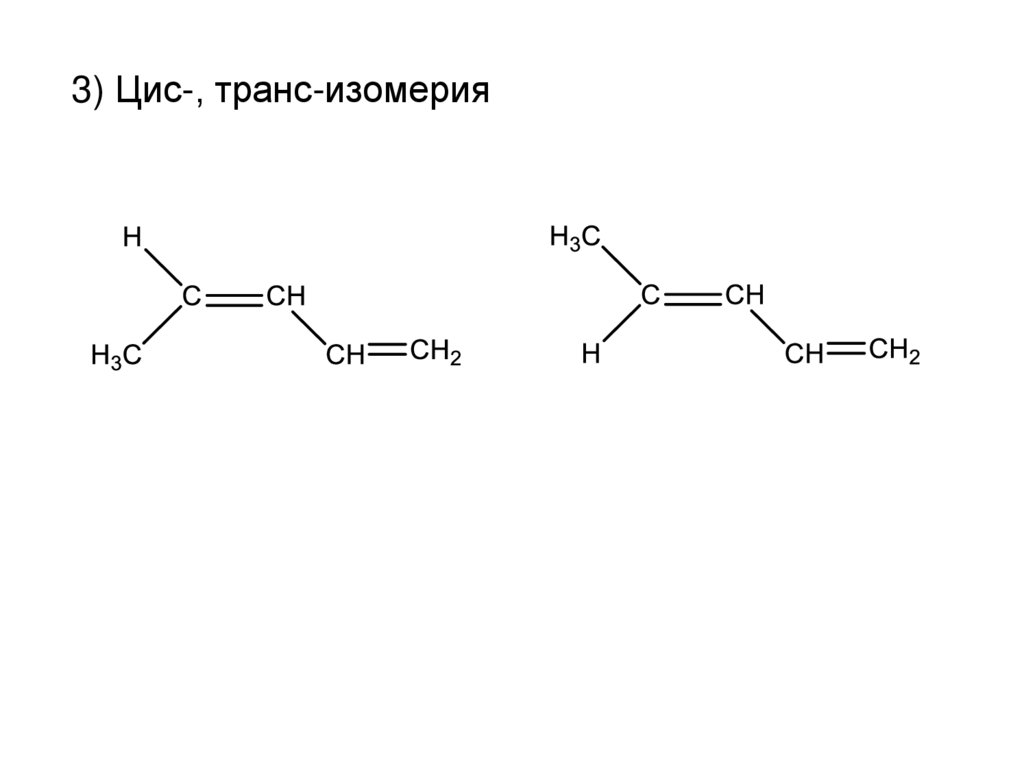
3) Цис-, транс-изомерия7.
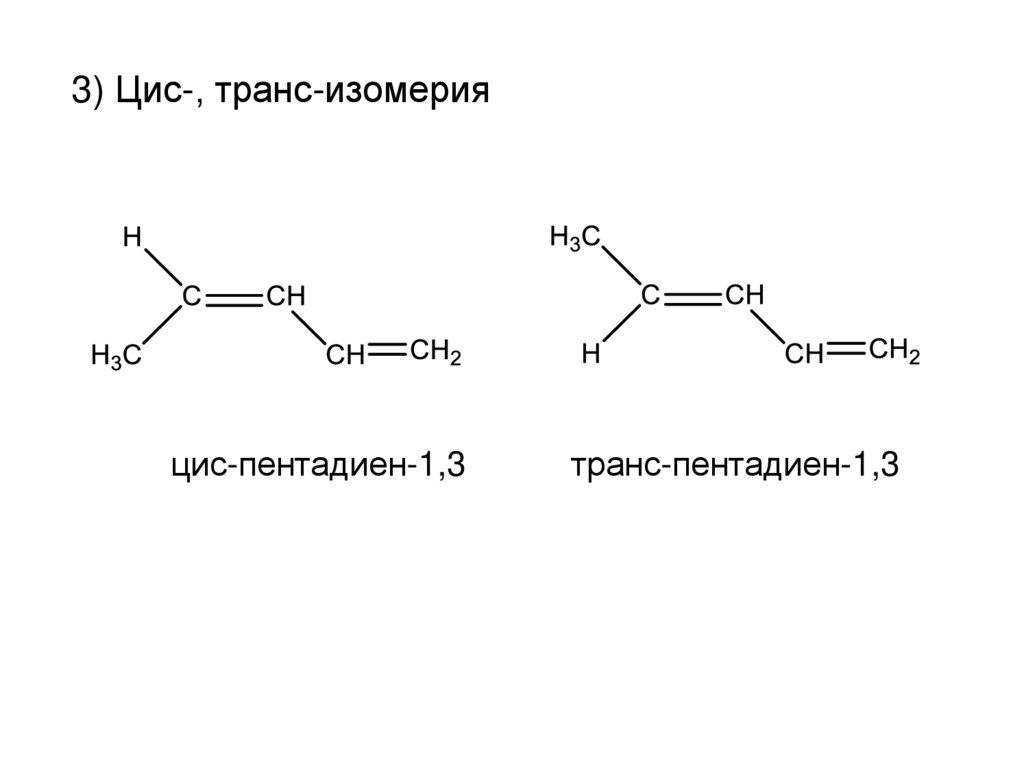
3) Цис-, транс-изомерияцис-пентадиен-1,3
транс-пентадиен-1,3
8.
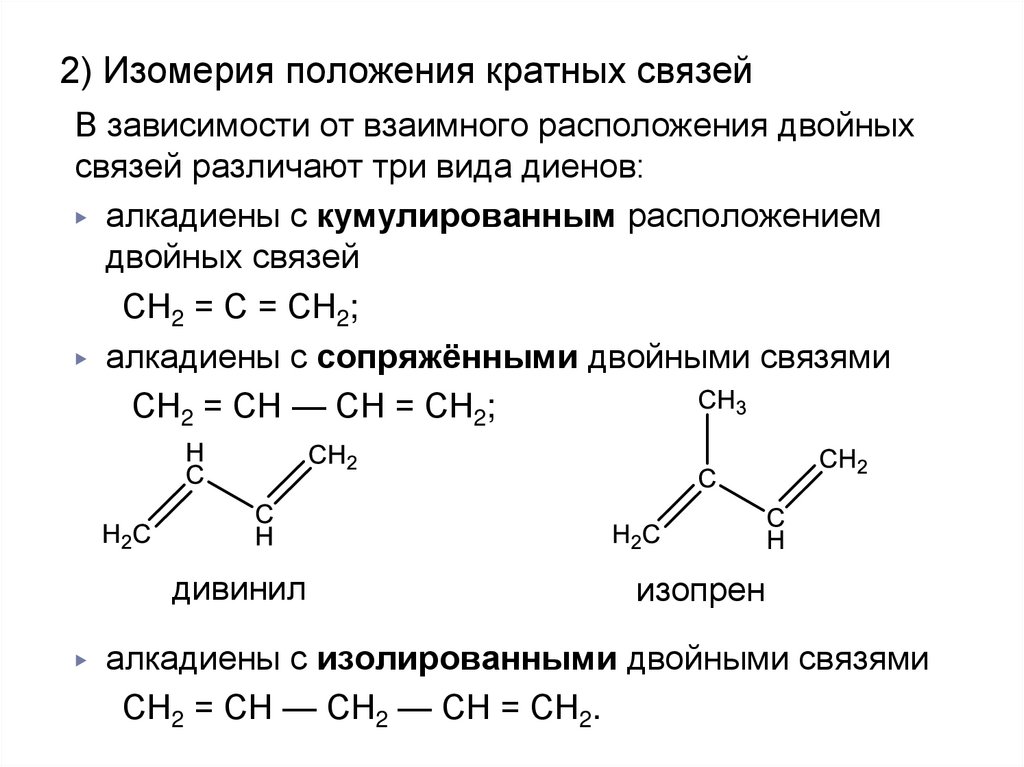
2) Изомерия положения кратных связейВ зависимости от взаимного расположения двойных
связей различают три вида диенов:
▶ алкадиены с кумулированным расположением
двойных связей
СН2 = С = СН2;
▶ алкадиены с сопряжёнными двойными связями
СН2 = СН — СН = СН2;
дивинил
▶
изопрен
алкадиены с изолированными двойными связями
СН2 = СН — СН2 — СН = СН2.
9.
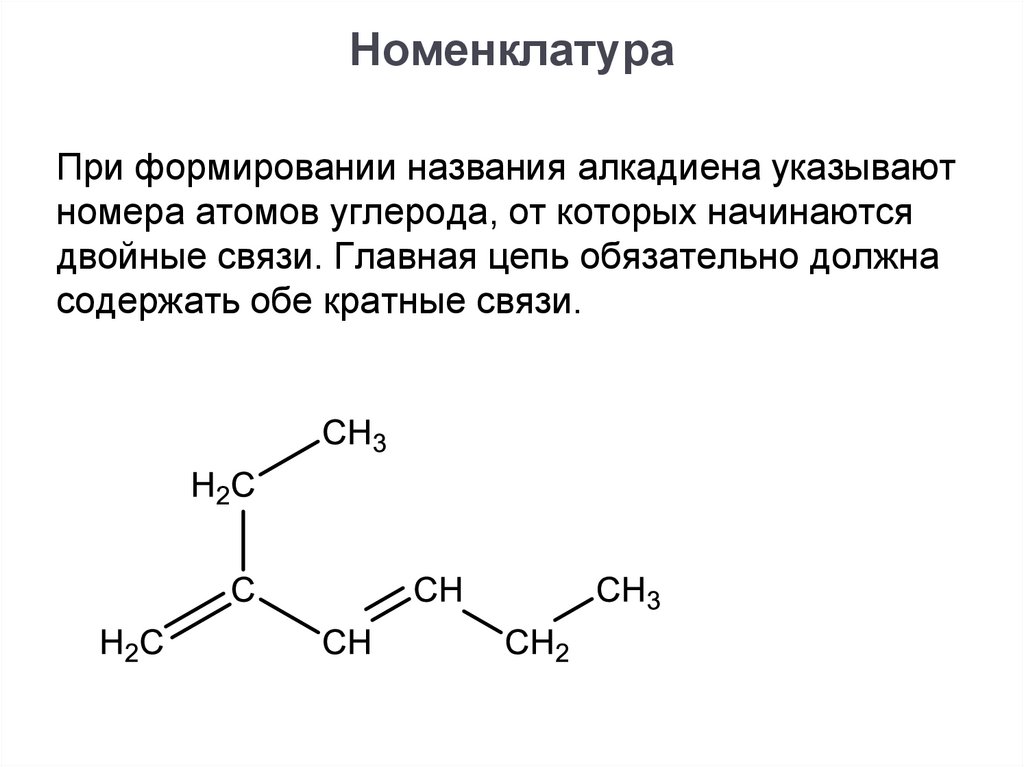
НоменклатураПри формировании названия алкадиена указывают
номера атомов углерода, от которых начинаются
двойные связи. Главная цепь обязательно должна
содержать обе кратные связи.
10.
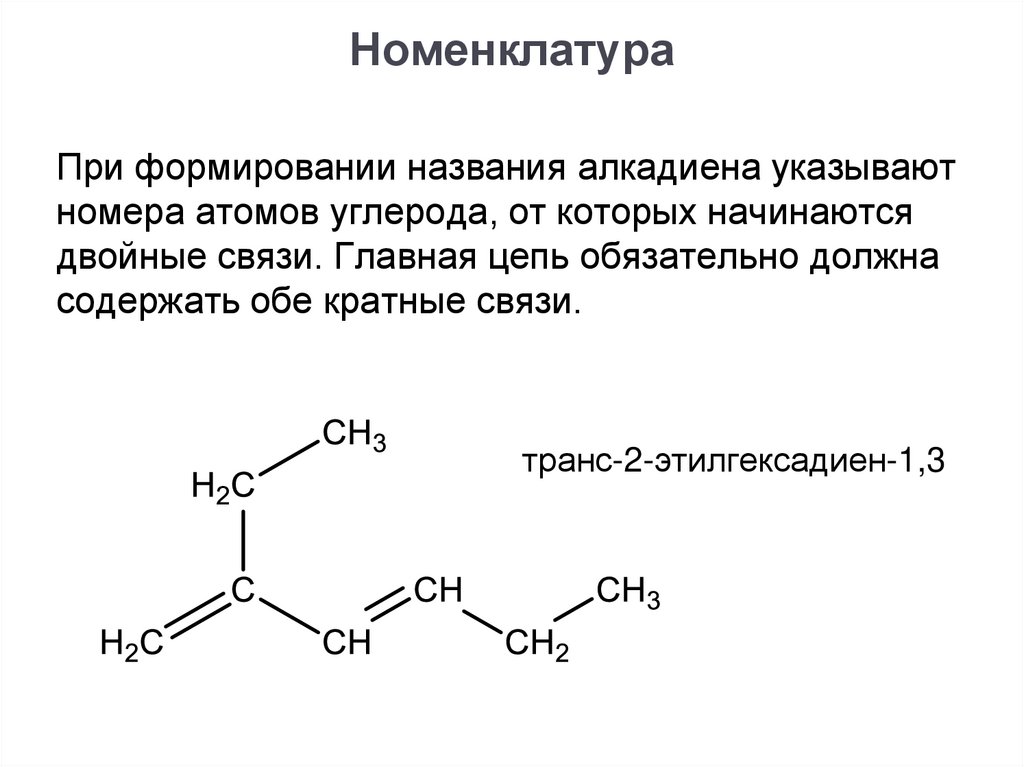
НоменклатураПри формировании названия алкадиена указывают
номера атомов углерода, от которых начинаются
двойные связи. Главная цепь обязательно должна
содержать обе кратные связи.
транс-2-этилгексадиен-1,3
11.
Физические свойстваПри нормальных условиях
пропадиен-1,2,
бутадиен-1,3 (дивинил) — газы
2-метилбутадиен-1,3 (изопрен) — летучая жидкость.
Алкадиены с изолированными двойными связями
(простейший из них — пентадиен-1,4) — жидкости.
Высшие диены — твёрдые вещества.
12.
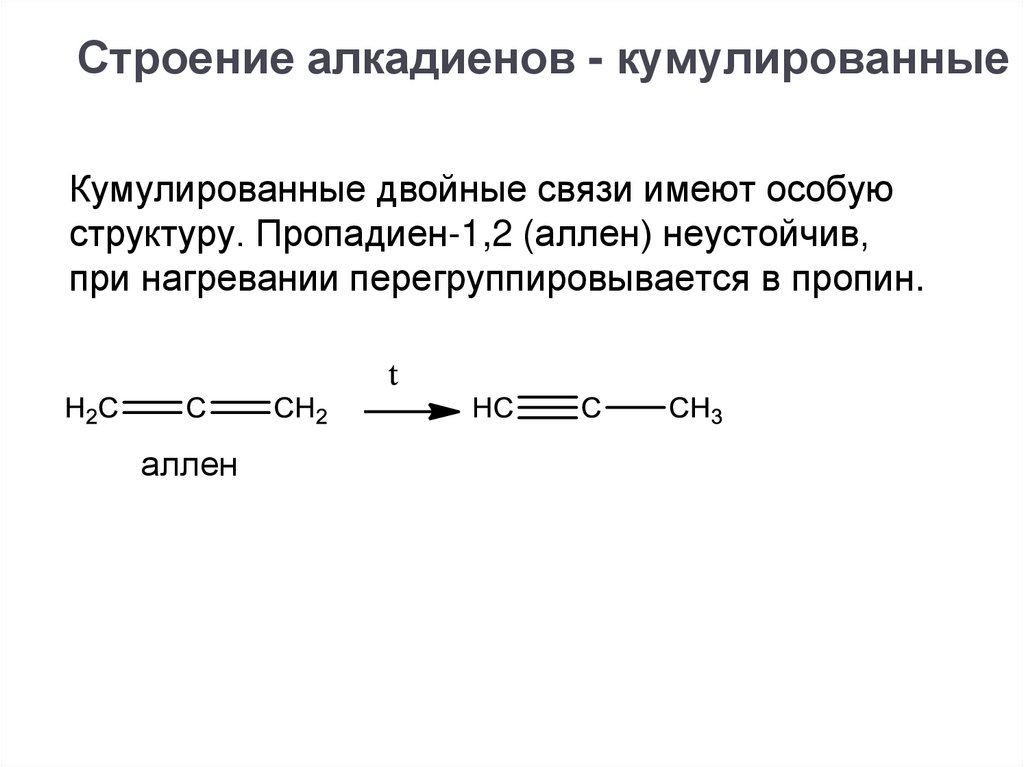
Строение алкадиенов - кумулированныеКумулированные двойные связи имеют особую
структуру. Пропадиен-1,2 (аллен) неустойчив,
при нагревании перегруппировывается в пропин.
аллен
13.
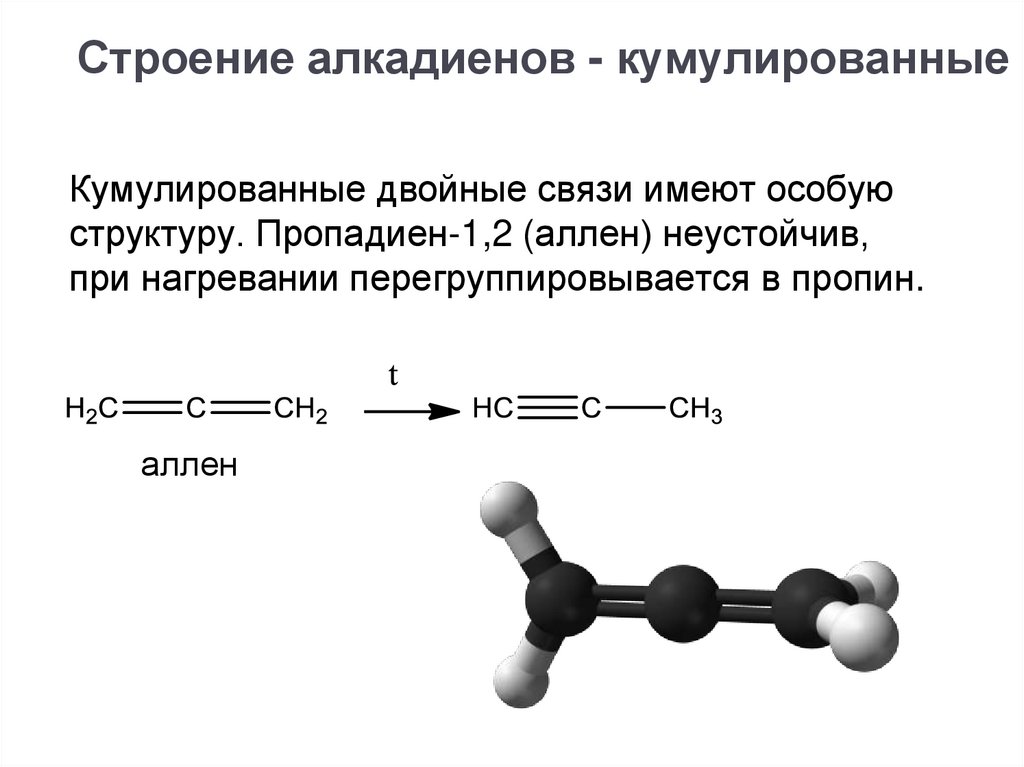
Строение алкадиенов - кумулированныеКумулированные двойные связи имеют особую
структуру. Пропадиен-1,2 (аллен) неустойчив,
при нагревании перегруппировывается в пропин.
аллен
14.
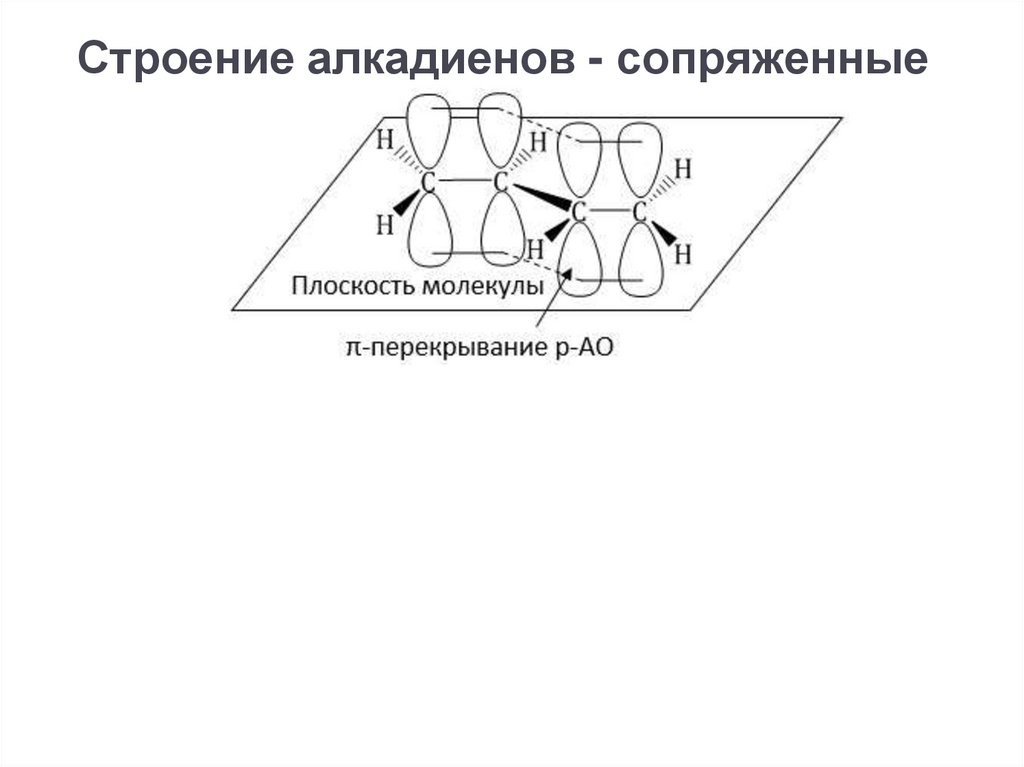
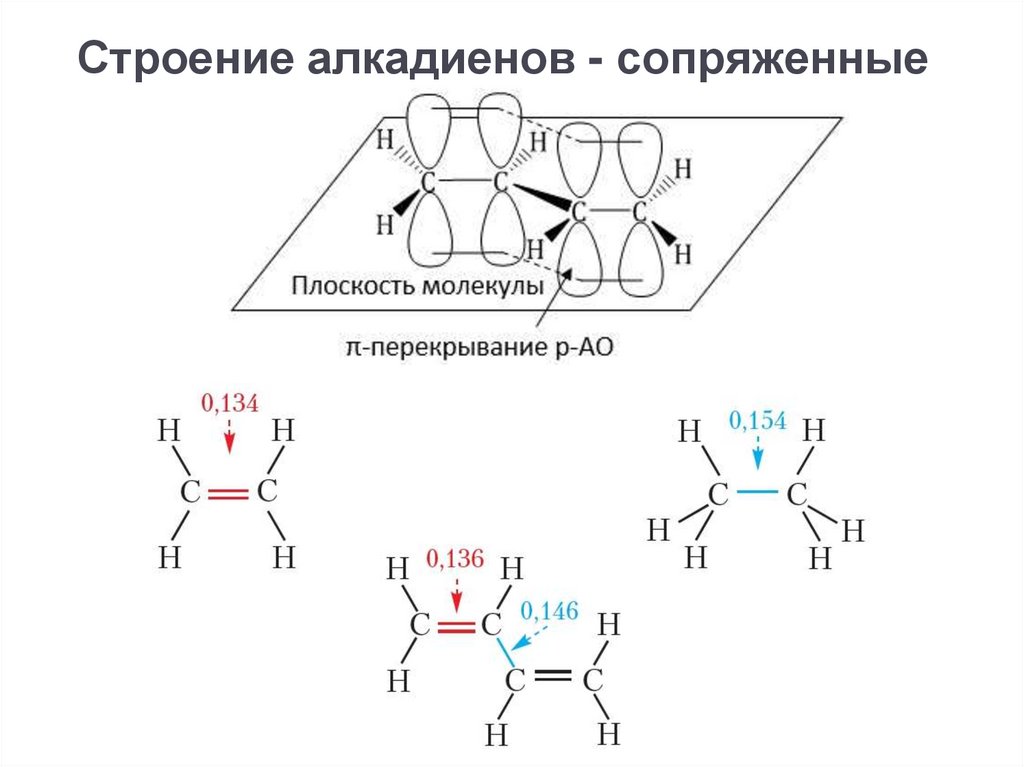
Строение алкадиенов - сопряженные15.
Строение алкадиенов - сопряженные16.
Химические свойства▶
кумулированные алкадиены = интересно,
но сложно - не проходим
СН2 = С = СН2;
▶
сопряжённые алкадиены = интересно, полезно и не
сложно - проходим
СН2 = СН — СН = СН2;
▶
изолированные алкадиены = алкены с двумя
двойными связями – уже прошли
СН2 = СН — СН2 — СН = СН2.
17.
Химические свойстваДля алкадиенов характерны реакции
электрофильного и радикального присоединения,
окисления и полимеризации.
AdE, AdR
18.
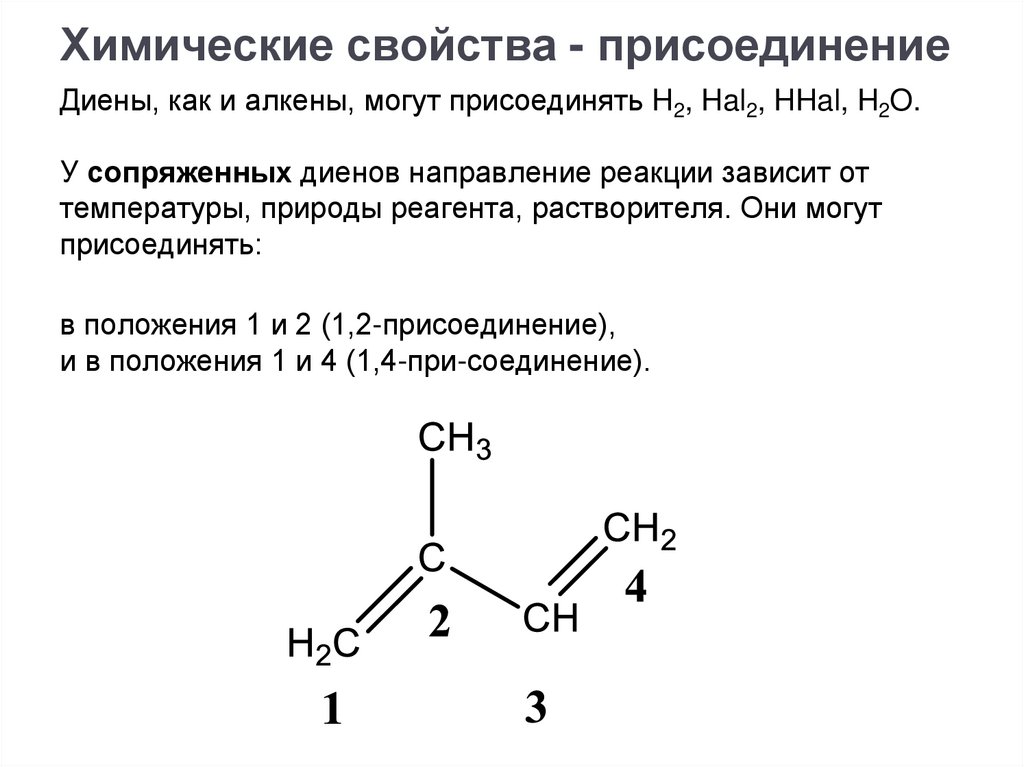
Химические свойства - присоединениеДиены, как и алкены, могут присоединять H2, Hal2, HHal, H2O.
У сопряженных диенов направление реакции зависит от
температуры, природы реагента, растворителя. Они могут
присоединять:
в положения 1 и 2 (1,2-присоединение),
и в положения 1 и 4 (1,4-при-соединение).
19.
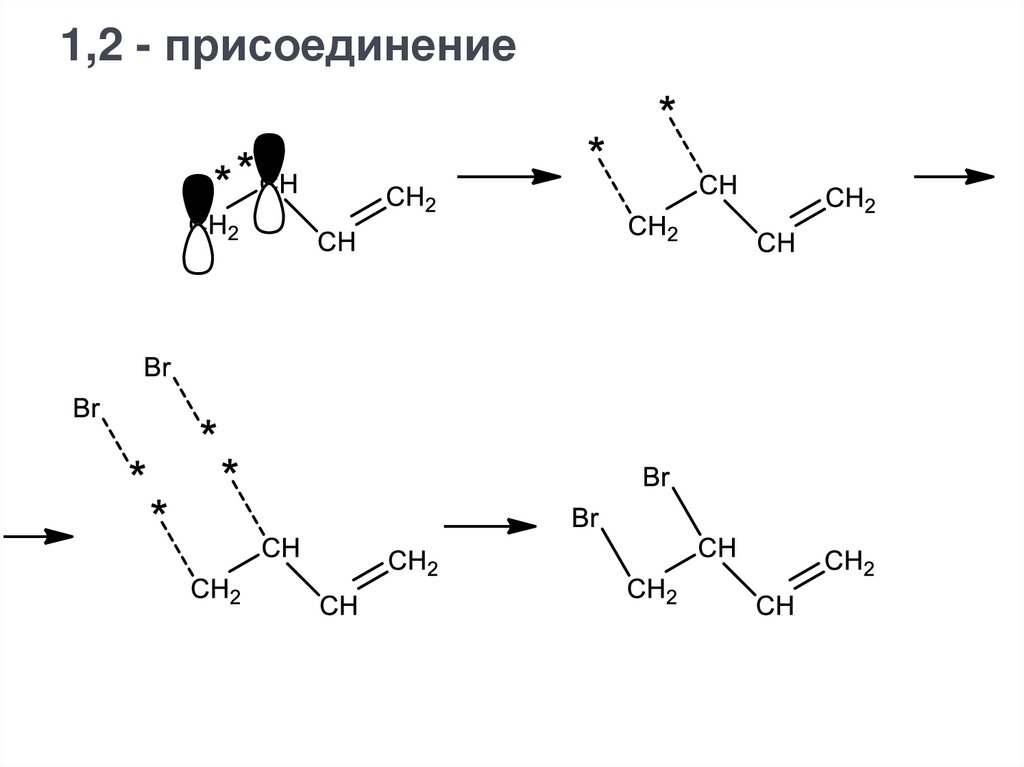
1,2 - присоединение20.
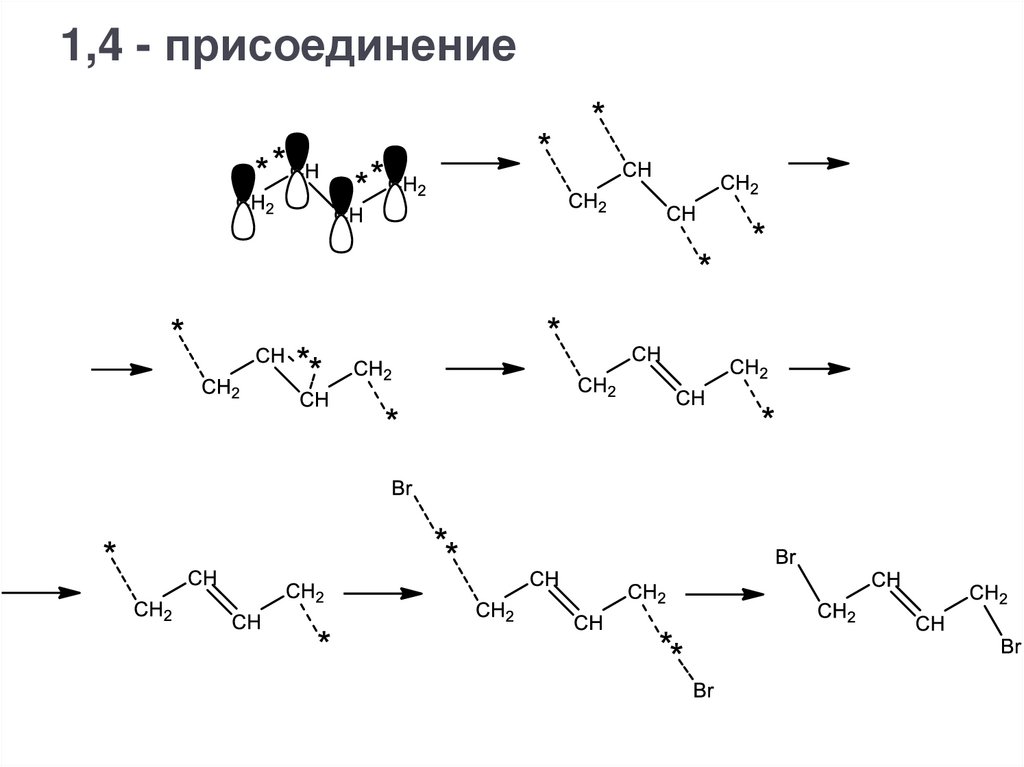
1,4 - присоединение21.
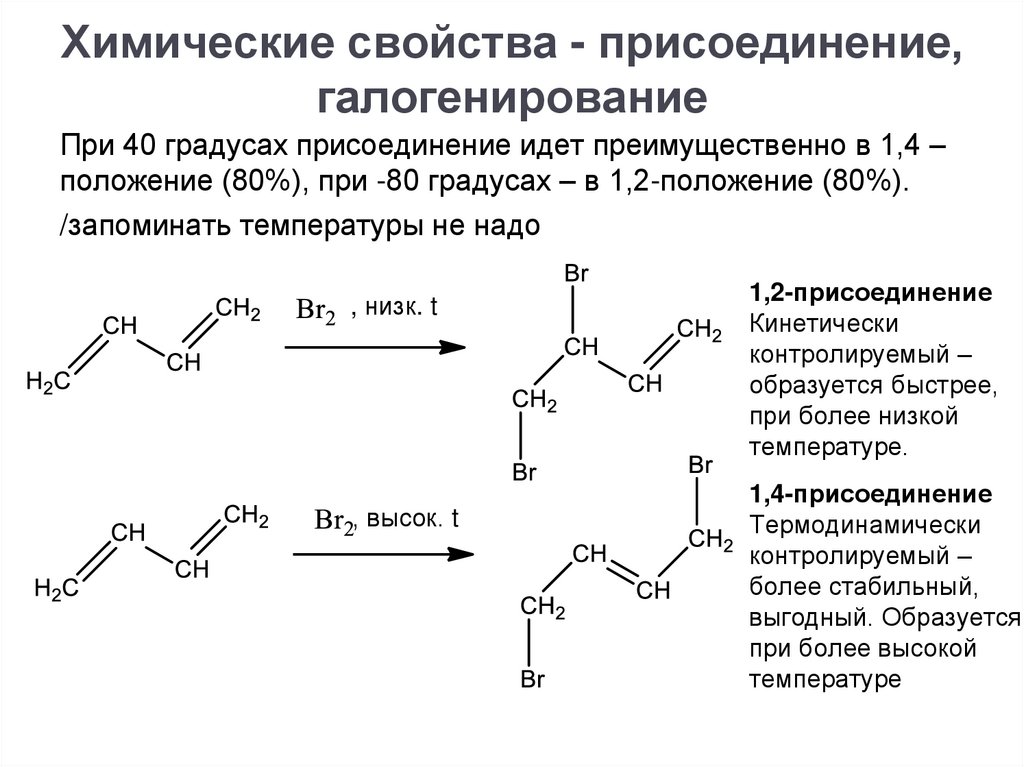
Химические свойства - присоединение,галогенирование
При 40 градусах присоединение идет преимущественно в 1,4 –
положение (80%), при -80 градусах – в 1,2-положение (80%).
/запоминать температуры не надо
, низк. t
, высок. t
1,2-присоединение
Кинетически
контролируемый –
образуется быстрее,
при более низкой
температуре.
1,4-присоединение
Термодинамически
контролируемый –
более стабильный,
выгодный. Образуется
при более высокой
температуре
22.
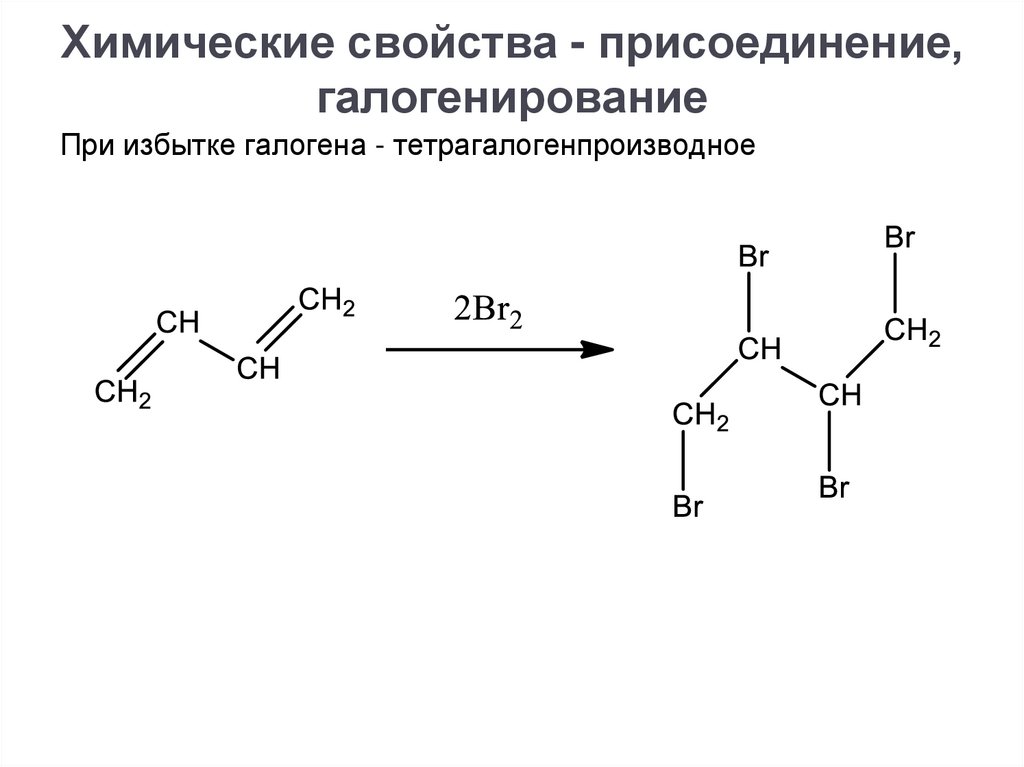
Химические свойства - присоединение,галогенирование
При избытке галогена - тетрагалогенпроизводное
23.
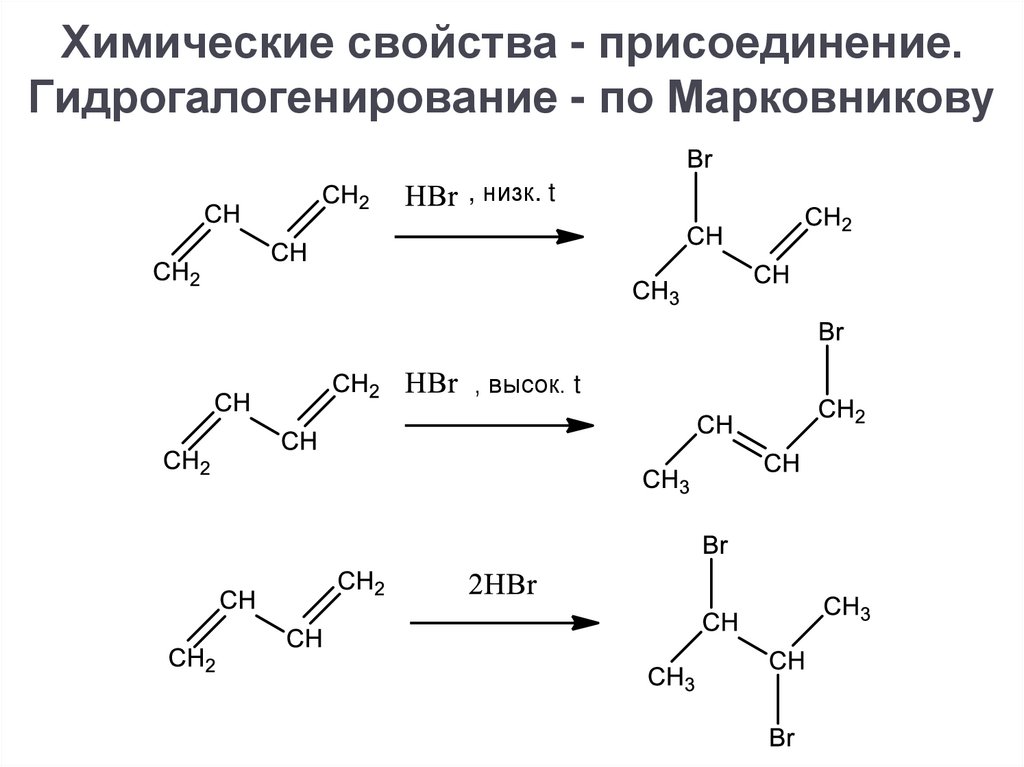
Химические свойства - присоединение.Гидрогалогенирование - по Марковникову
, низк. t
, высок. t
24.
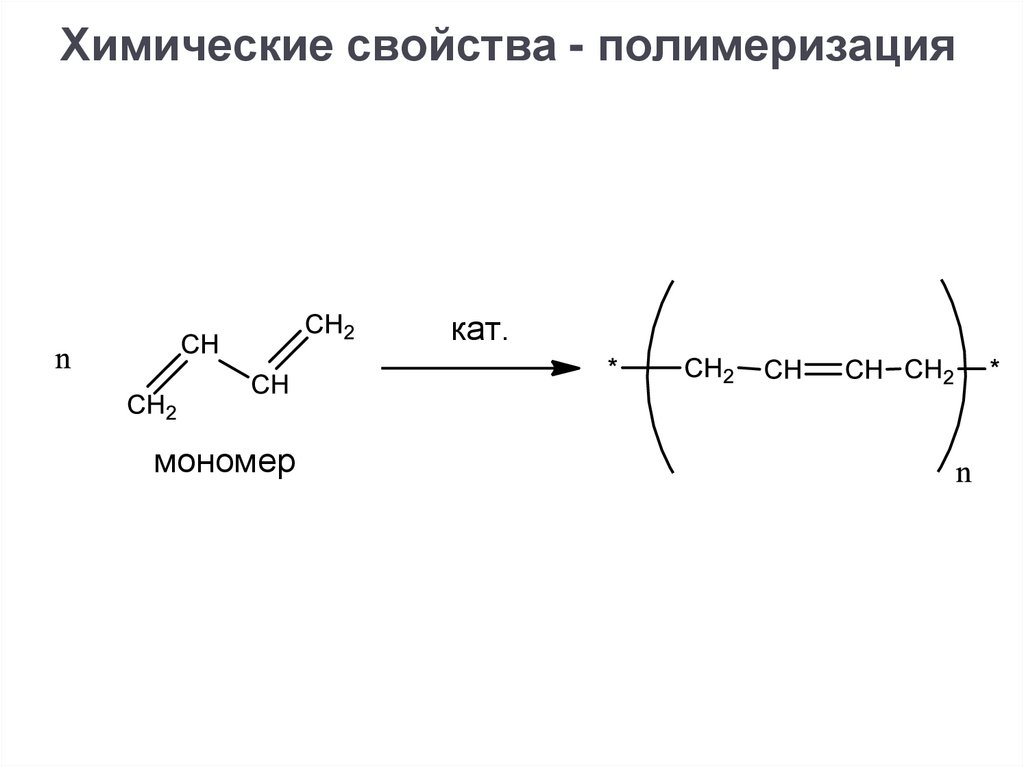
Химические свойства - полимеризациякат.
мономер
25.
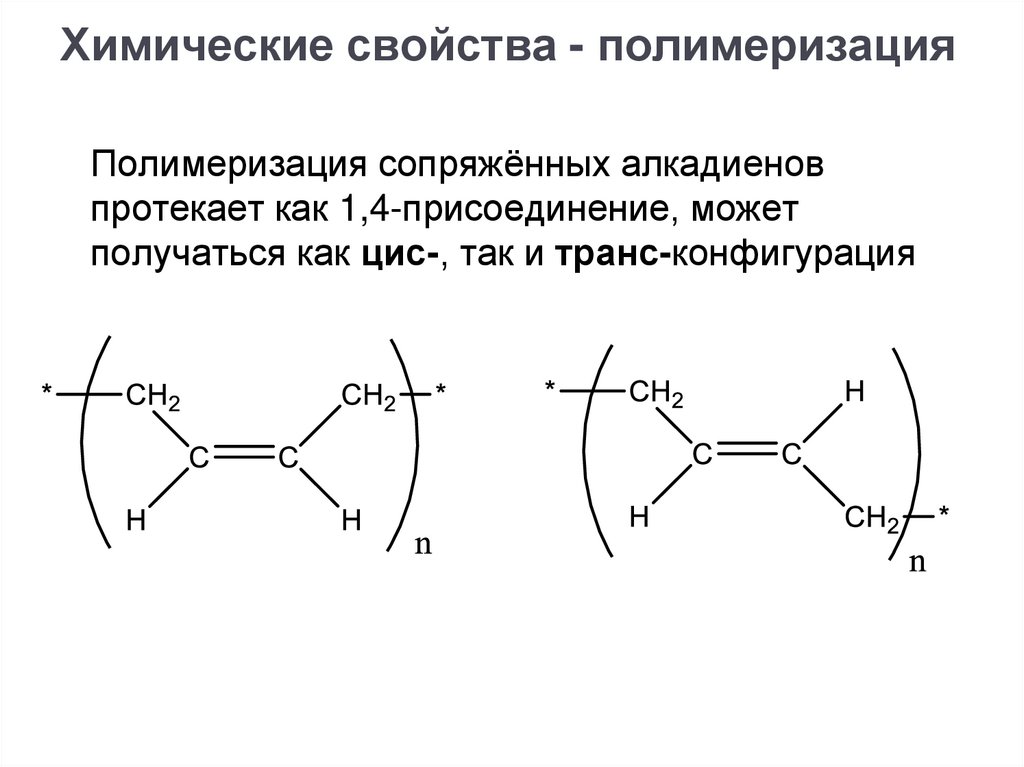
Химические свойства - полимеризацияПолимеризация сопряжённых алкадиенов
протекает как 1,4-присоединение, может
получаться как цис-, так и транс-конфигурация
26.
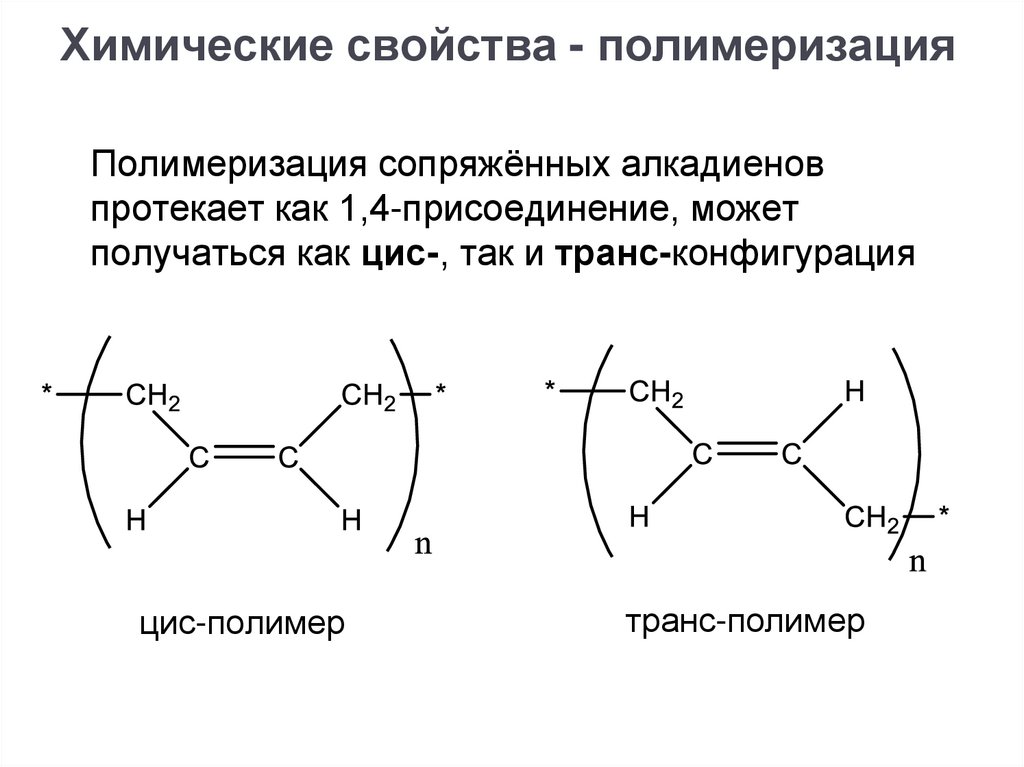
Химические свойства - полимеризацияПолимеризация сопряжённых алкадиенов
протекает как 1,4-присоединение, может
получаться как цис-, так и транс-конфигурация
цис-полимер
транс-полимер
27.
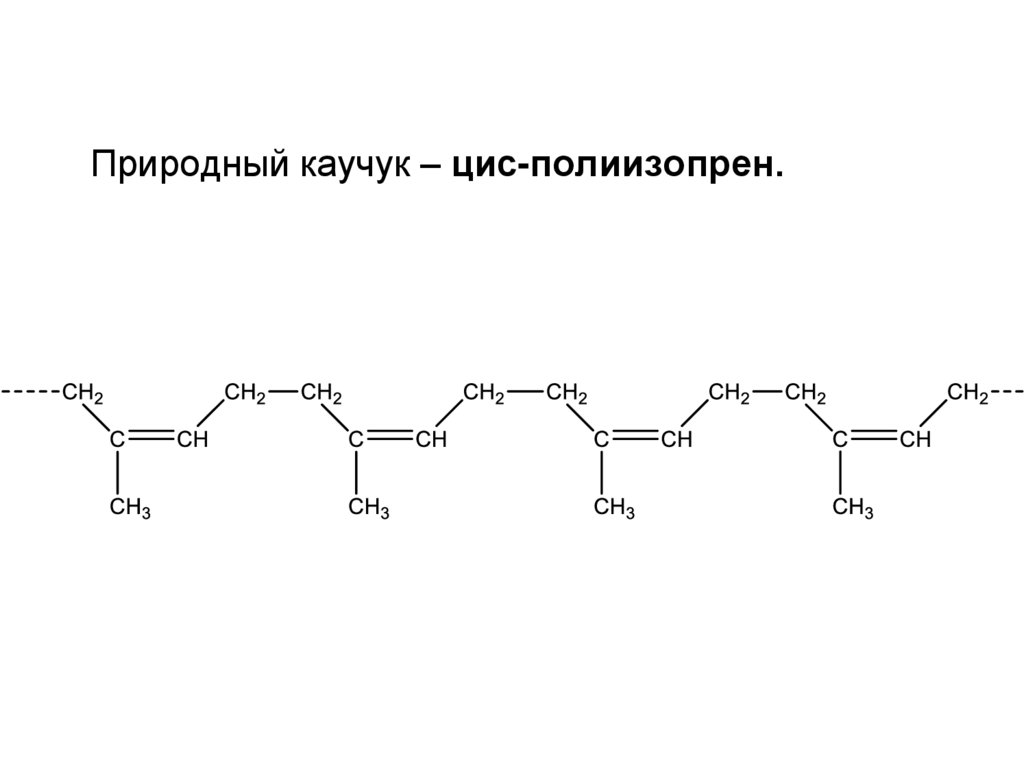
Природный каучук – цис-полиизопрен.28.
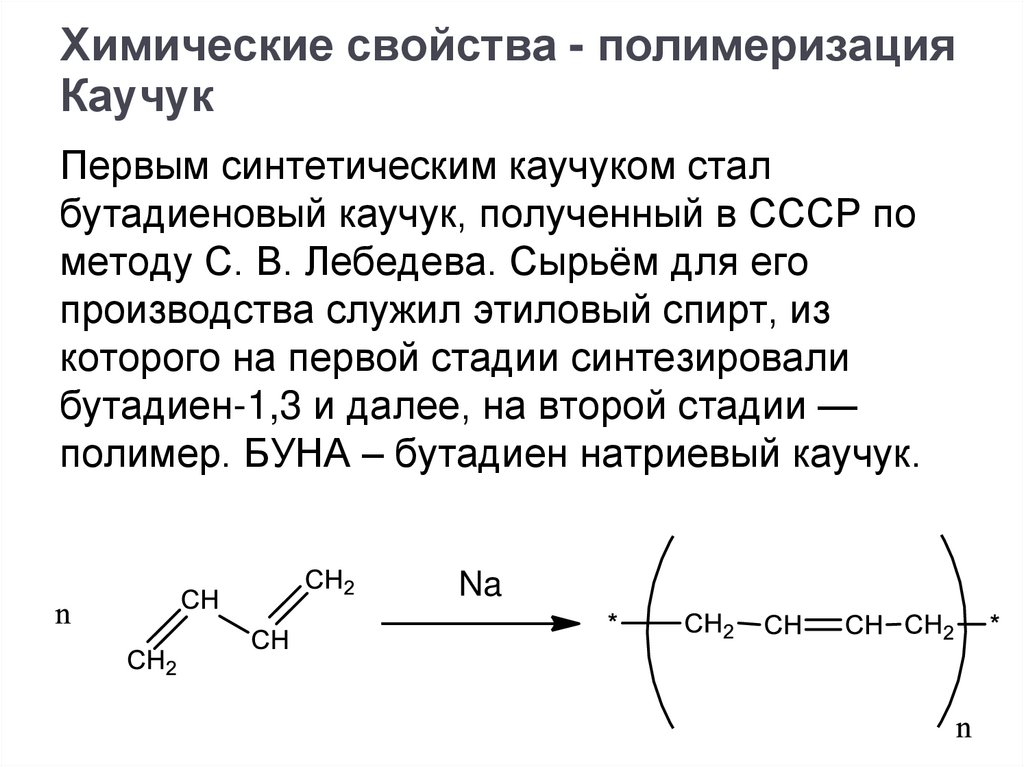
Химические свойства - полимеризацияКаучук
Первым синтетическим каучуком стал
бутадиеновый каучук, полученный в СССР по
методу С. В. Лебедева. Сырьём для его
производства служил этиловый спирт, из
которого на первой стадии синтезировали
бутадиен-1,3 и далее, на второй стадии —
полимер. БУНА – бутадиен натриевый каучук.
Na
29.
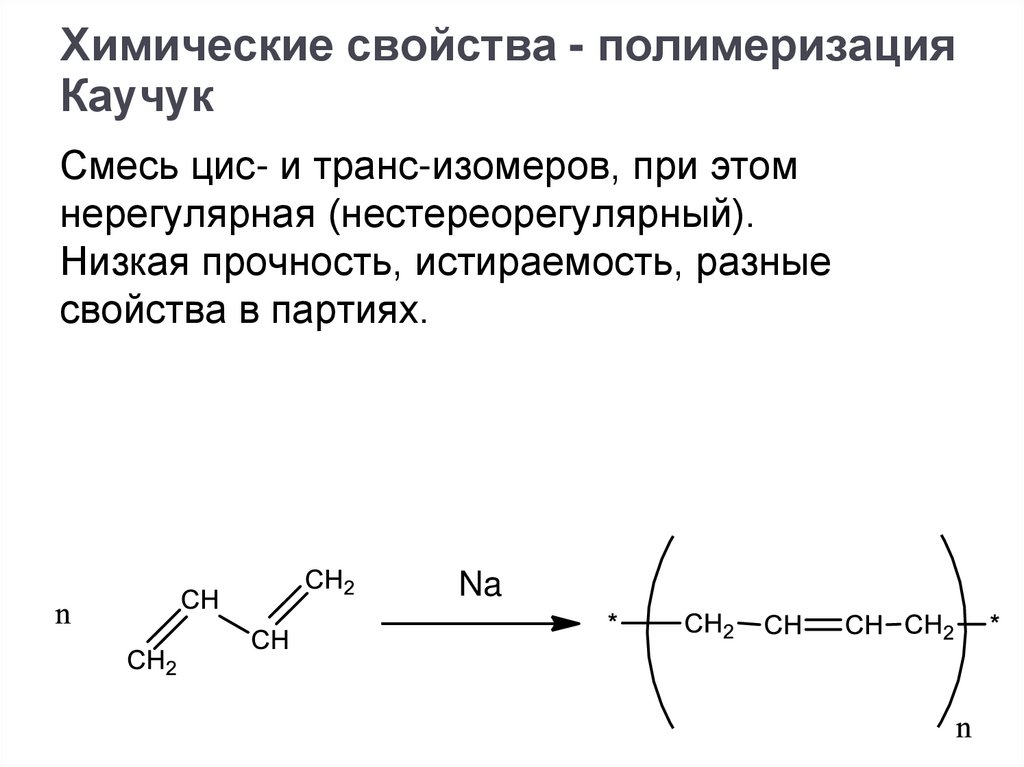
Химические свойства - полимеризацияКаучук
Смесь цис- и транс-изомеров, при этом
нерегулярная (нестереорегулярный).
Низкая прочность, истираемость, разные
свойства в партиях.
Na
30.
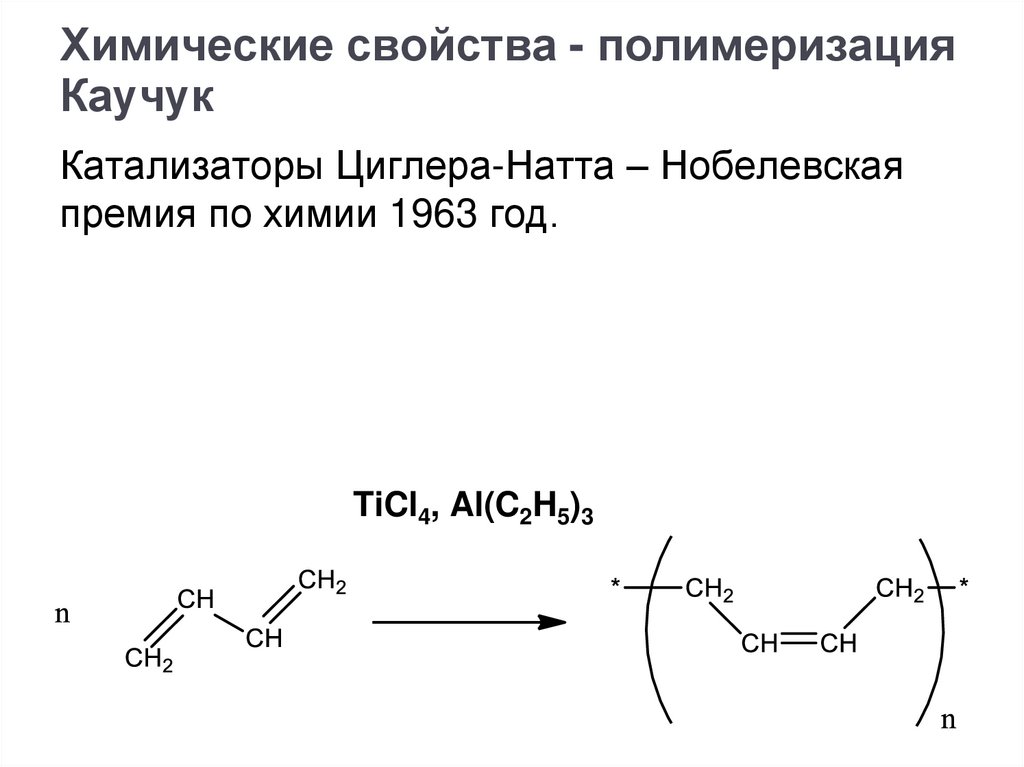
Химические свойства - полимеризацияКаучук
Катализаторы Циглера-Натта – Нобелевская
премия по химии 1963 год.
TiCl4, Al(C2H5)3
31.
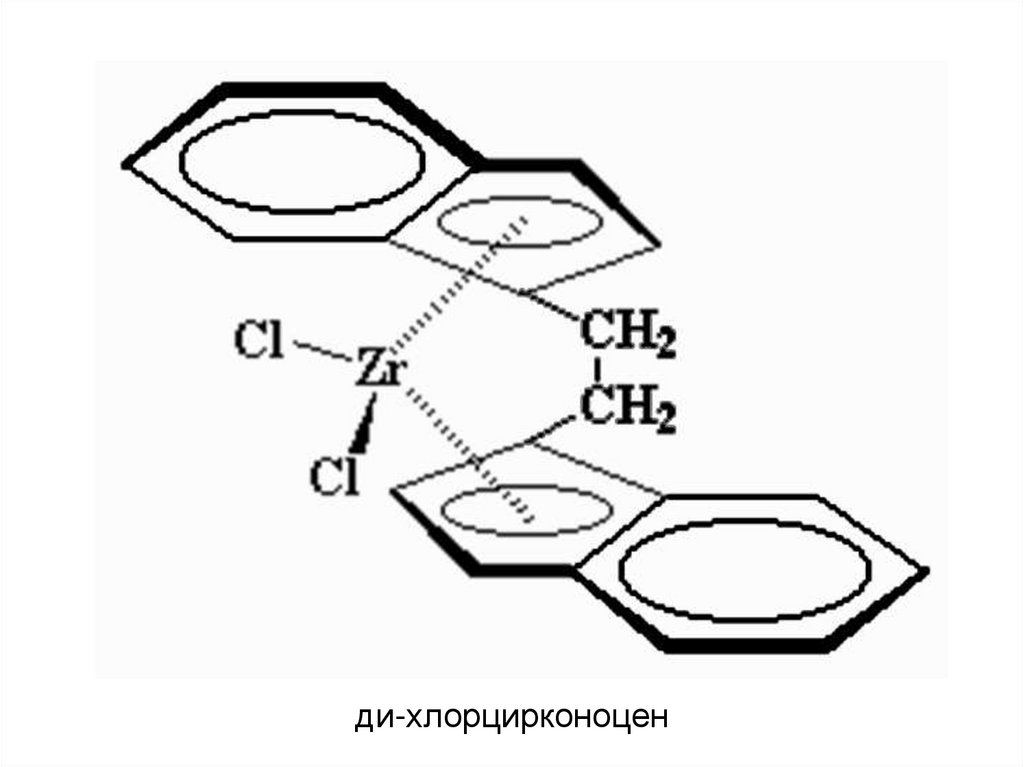
ди-хлорцирконоцен32.
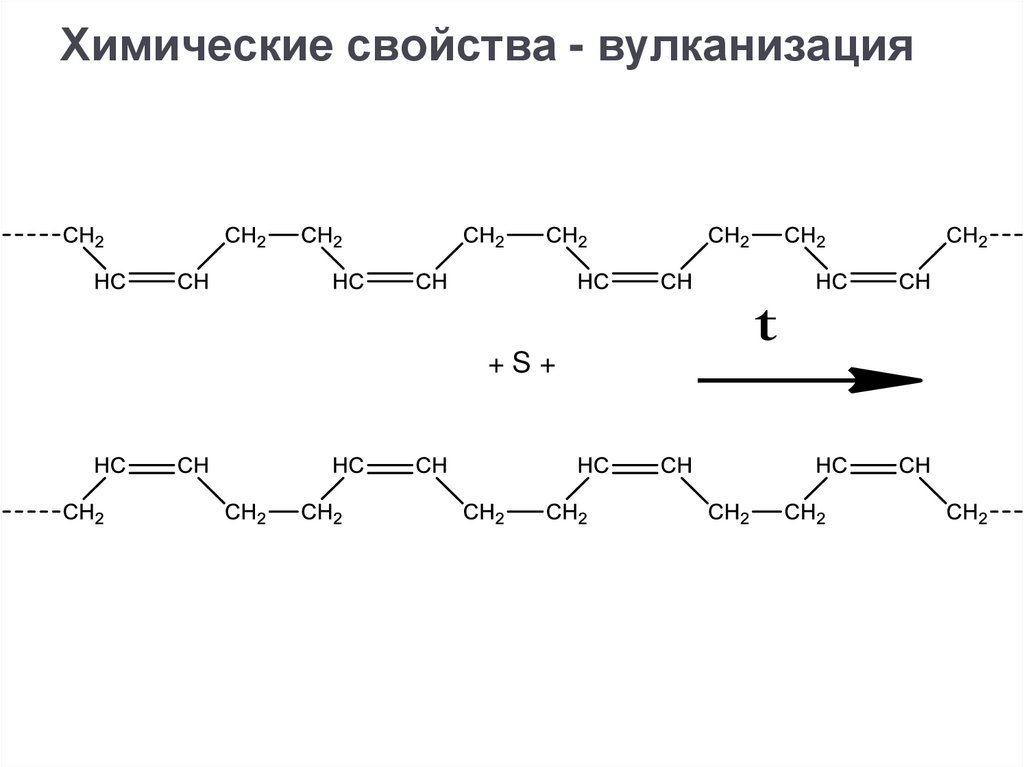
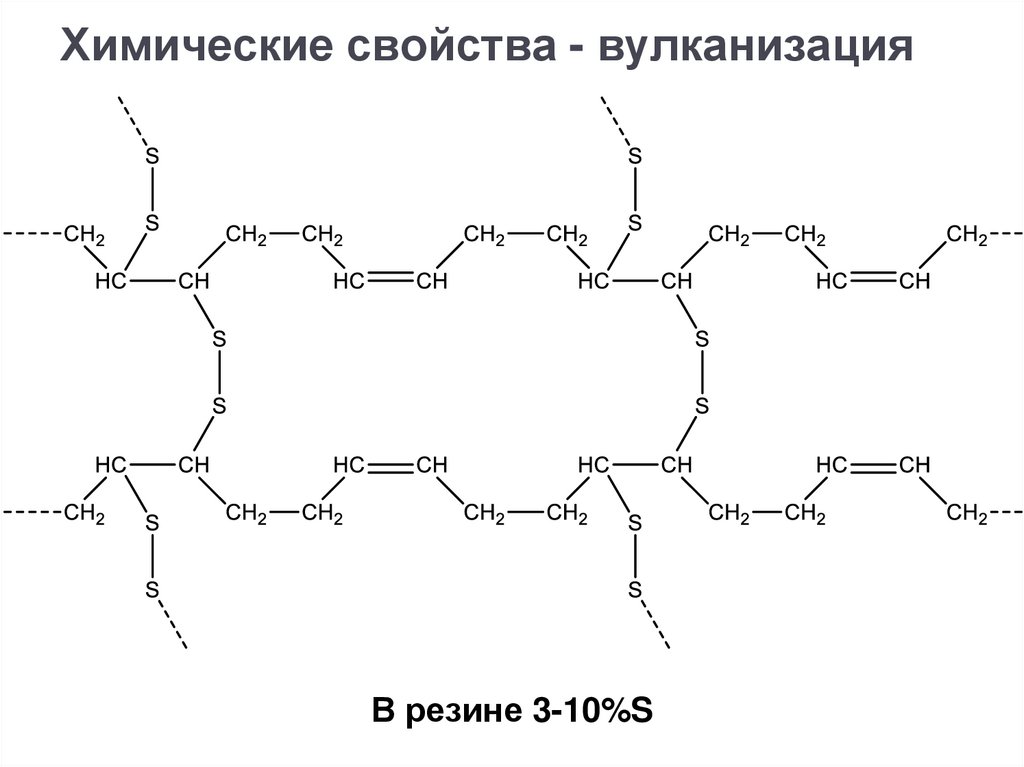
Химические свойства - вулканизация+S+
33.
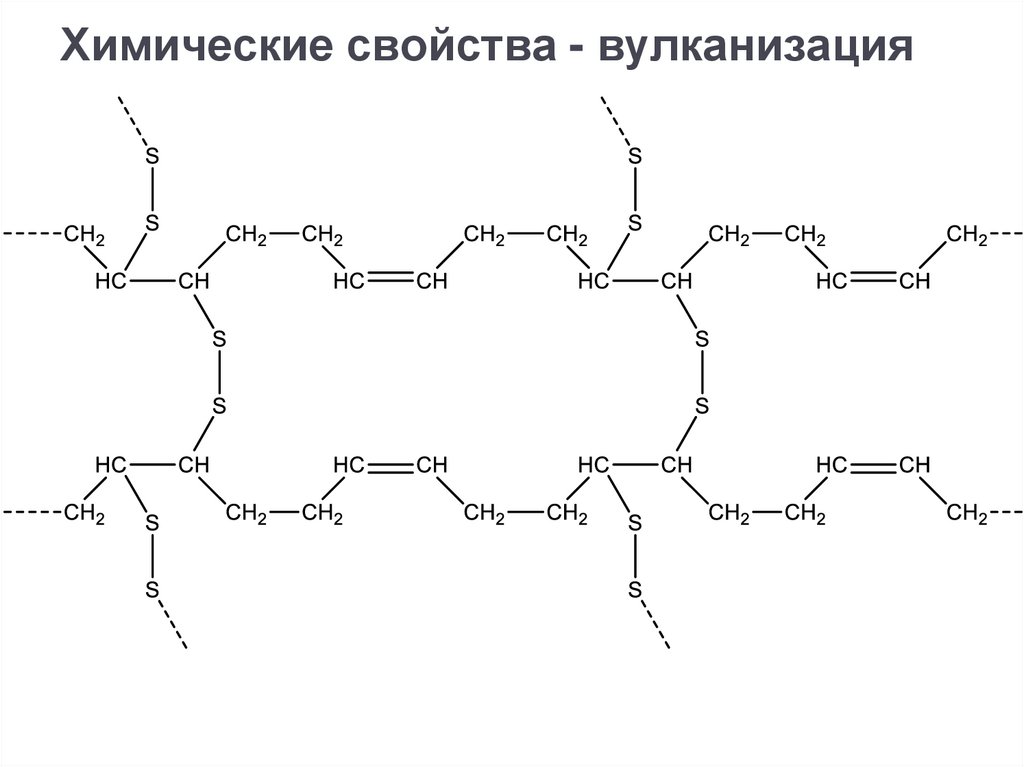
Химические свойства - вулканизация34.
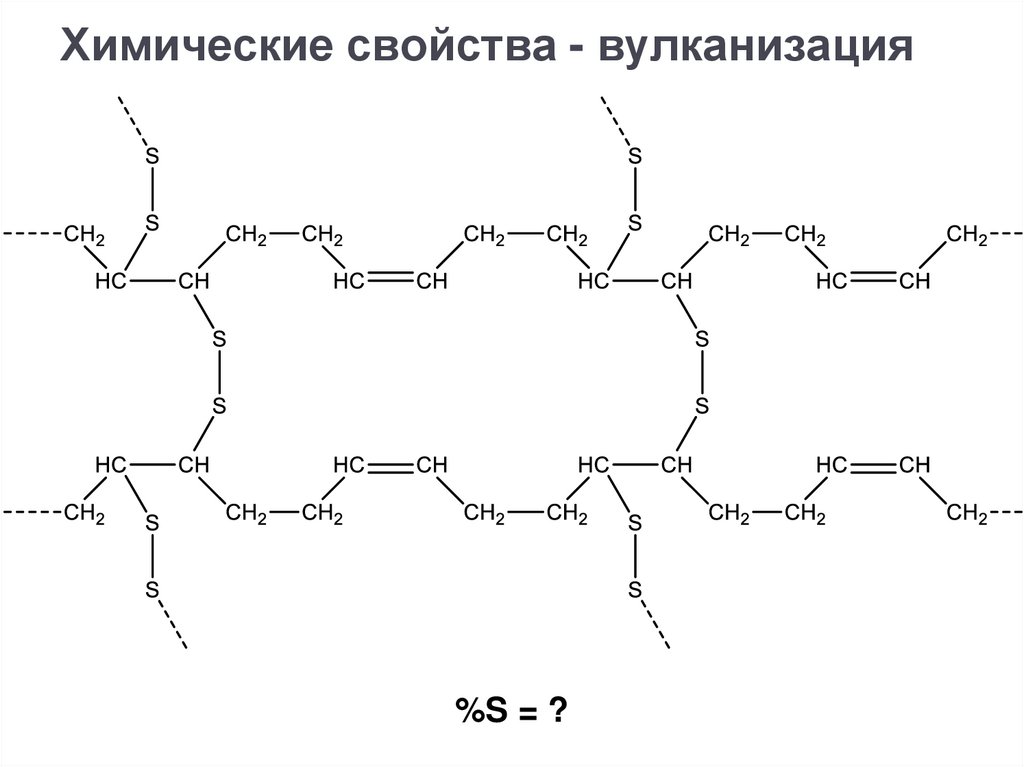
Химические свойства - вулканизация%S = ?
35.
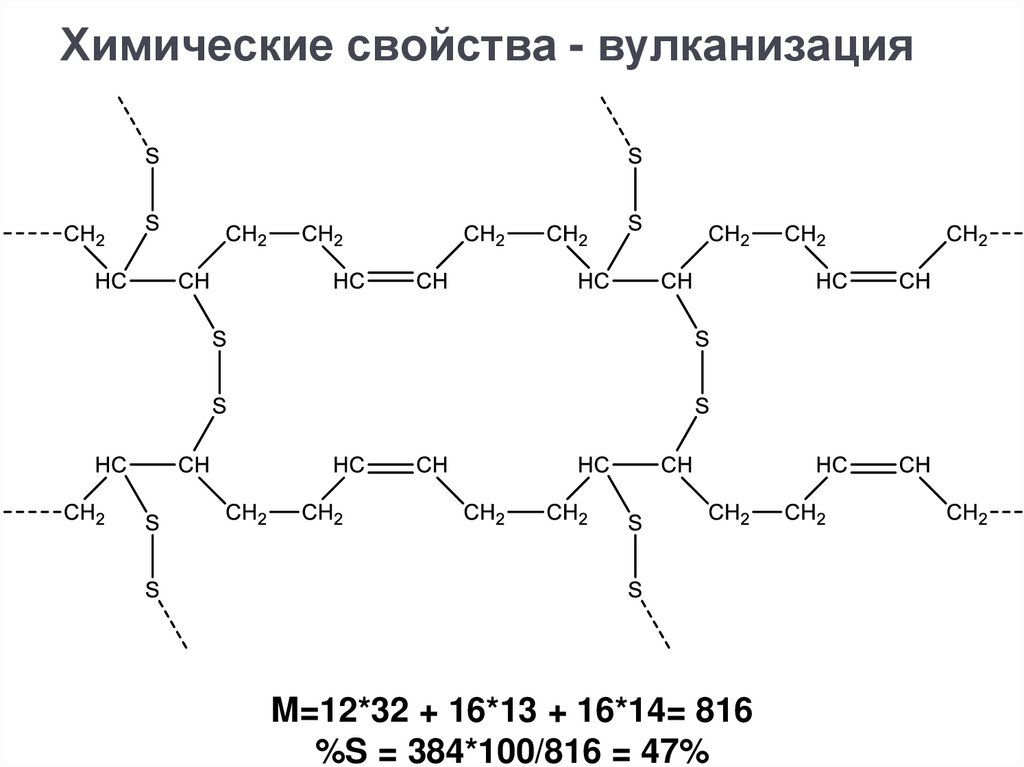
Химические свойства - вулканизацияM=12*32 + 16*13 + 16*14= 816
%S = 384*100/816 = 47%
36.
Химические свойства - вулканизацияВ резине 3-10%S
37.
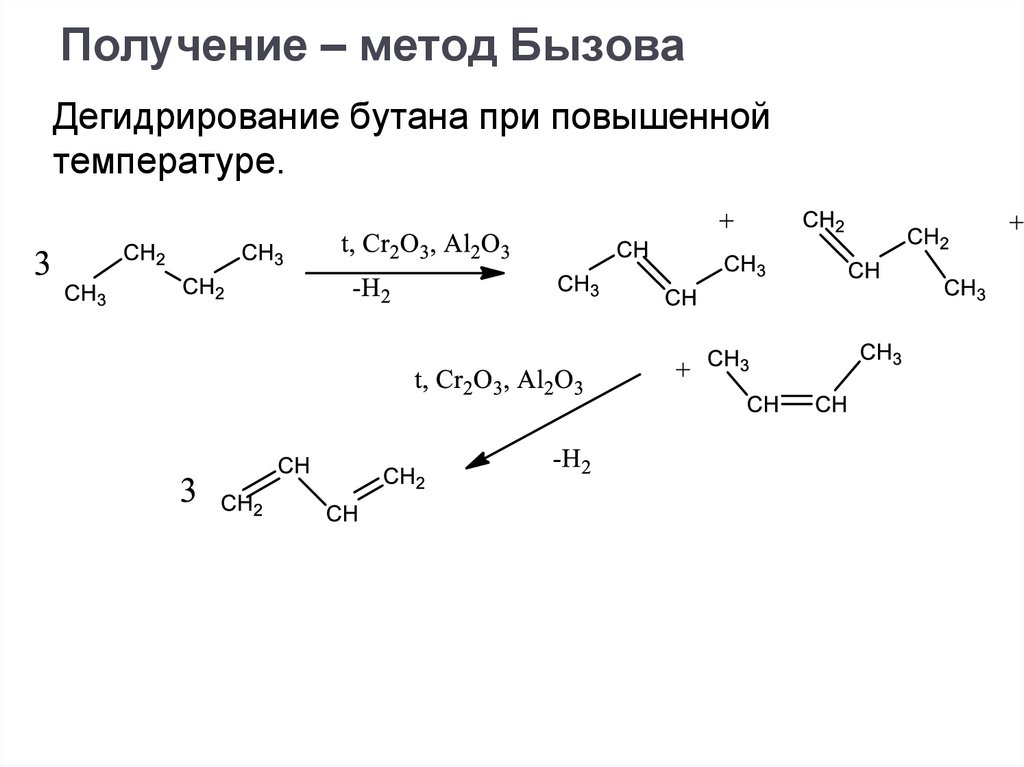
Получение – метод БызоваДегидрирование бутана при повышенной
температуре.
38.
39.
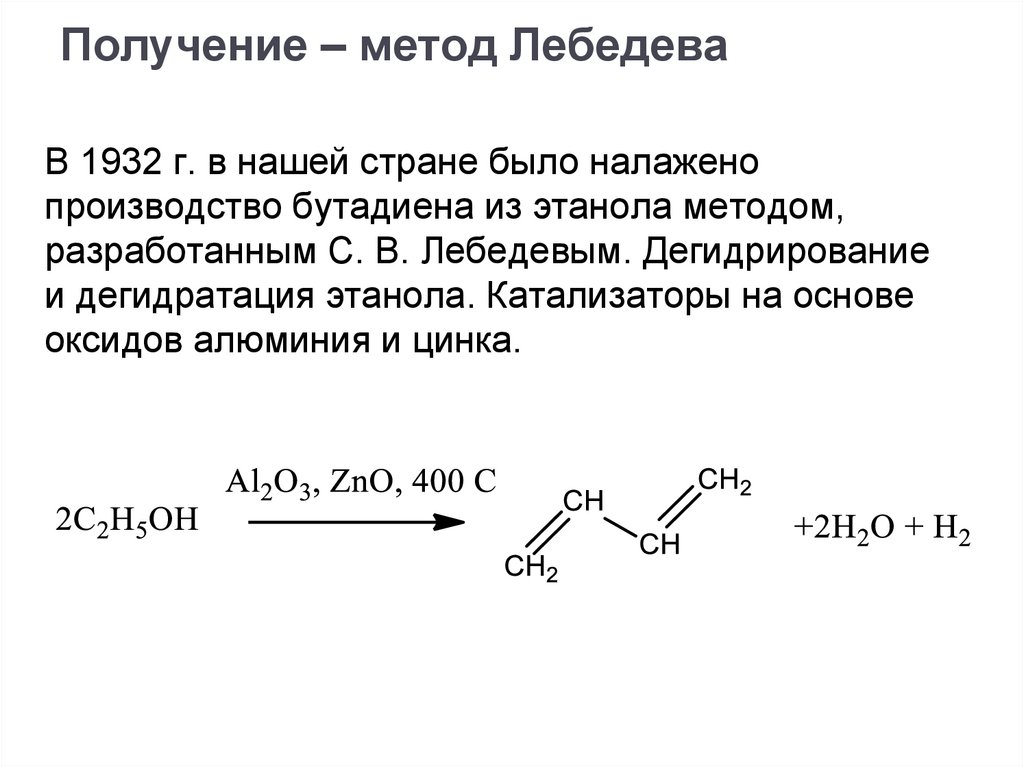
Получение – метод ЛебедеваВ 1932 г. в нашей стране было налажено
производство бутадиена из этанола методом,
разработанным С. В. Лебедевым. Дегидрирование
и дегидратация этанола. Катализаторы на основе
оксидов алюминия и цинка.
40.
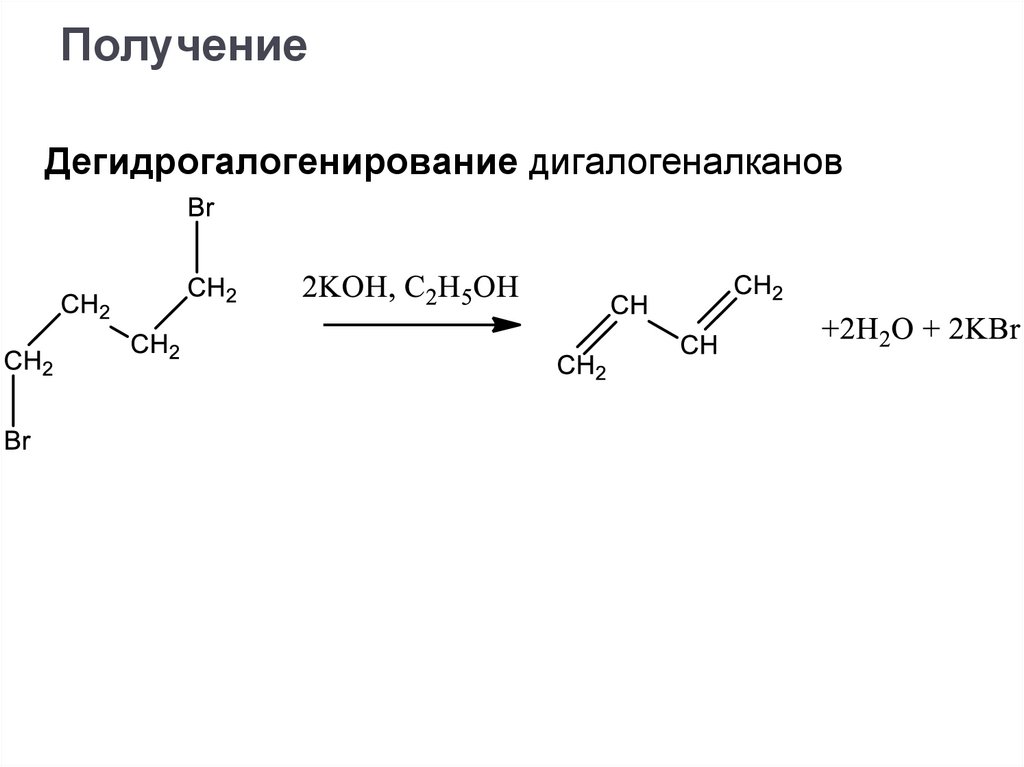
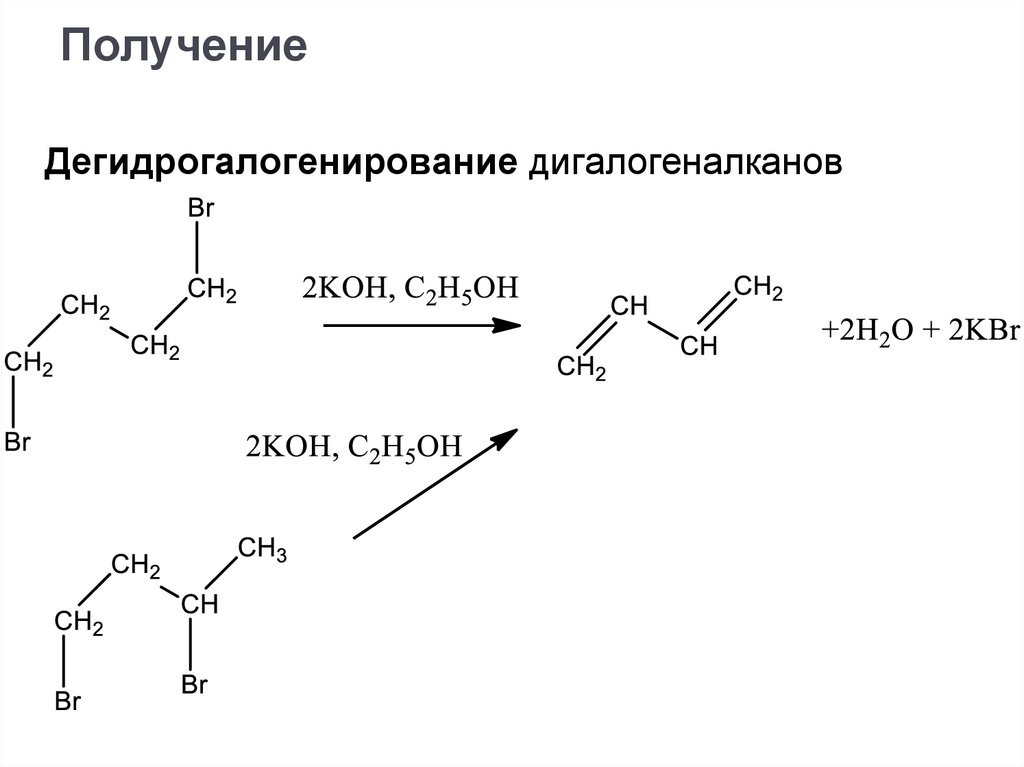
ПолучениеДегидрогалогенирование дигалогеналканов
41.
ПолучениеДегидрогалогенирование дигалогеналканов
42.
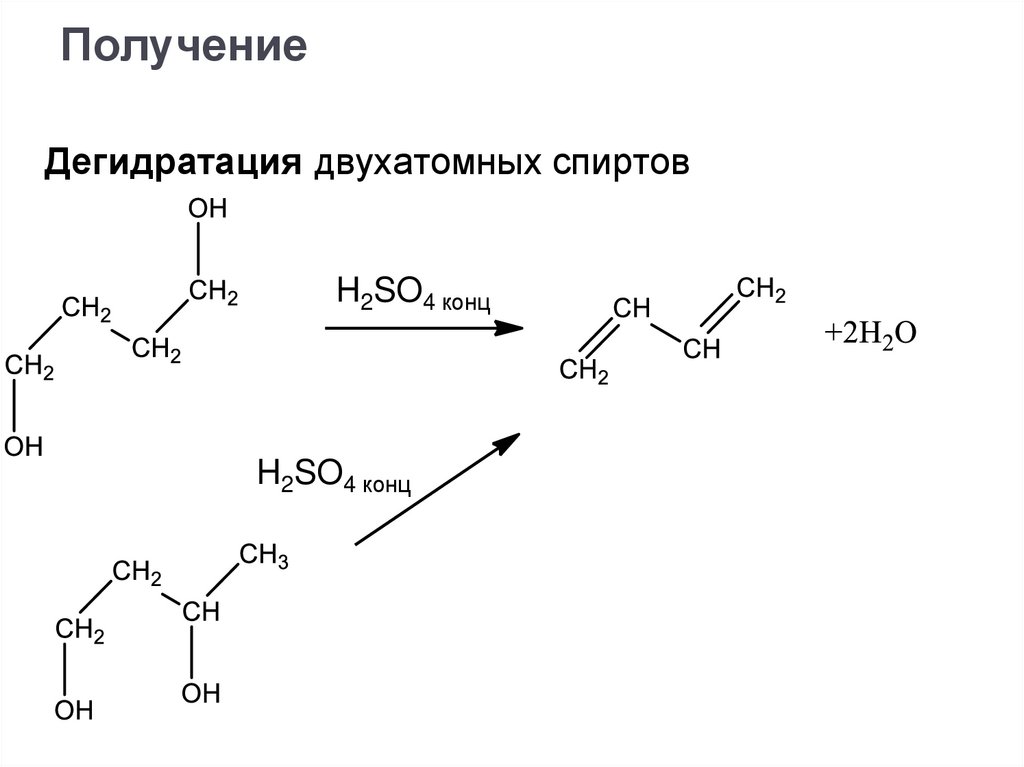
ПолучениеДегидратация двухатомных спиртов
H2SO4 конц
H2SO4 конц









 chemistry
chemistry








