Similar presentations:
Нітроген. Азот. Сполуки Нітрогена
1.
Нітроген. Азот. СполукиНітрогена.
2.
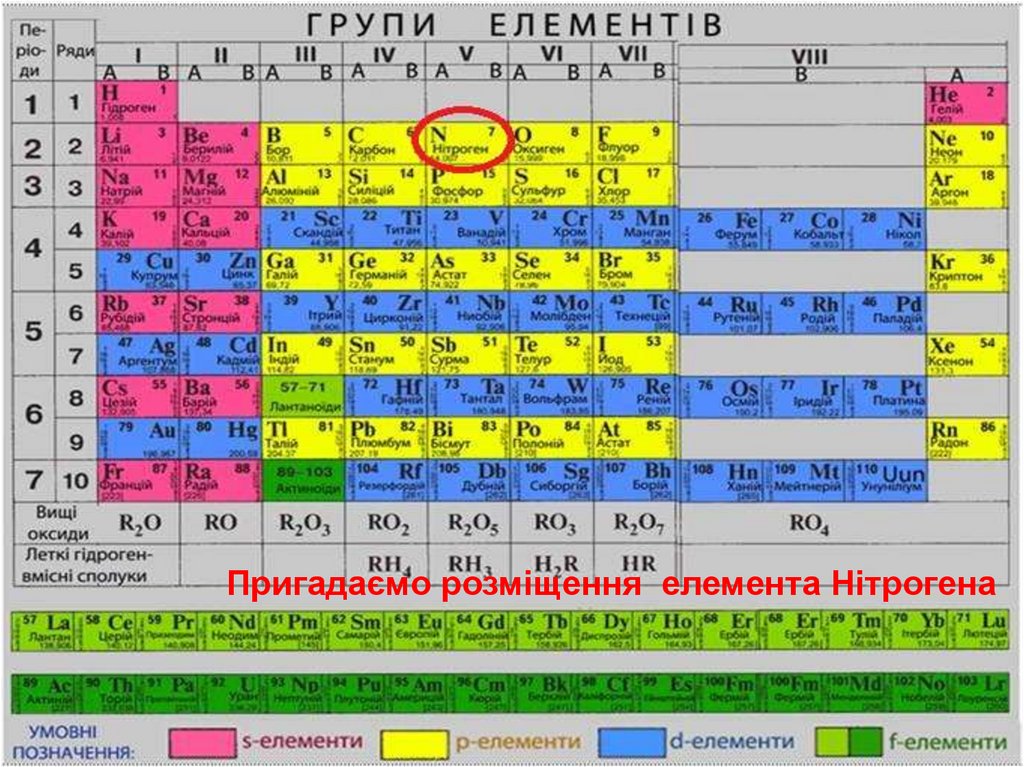
Пригадаємо розміщення елемента Нітрогена3.
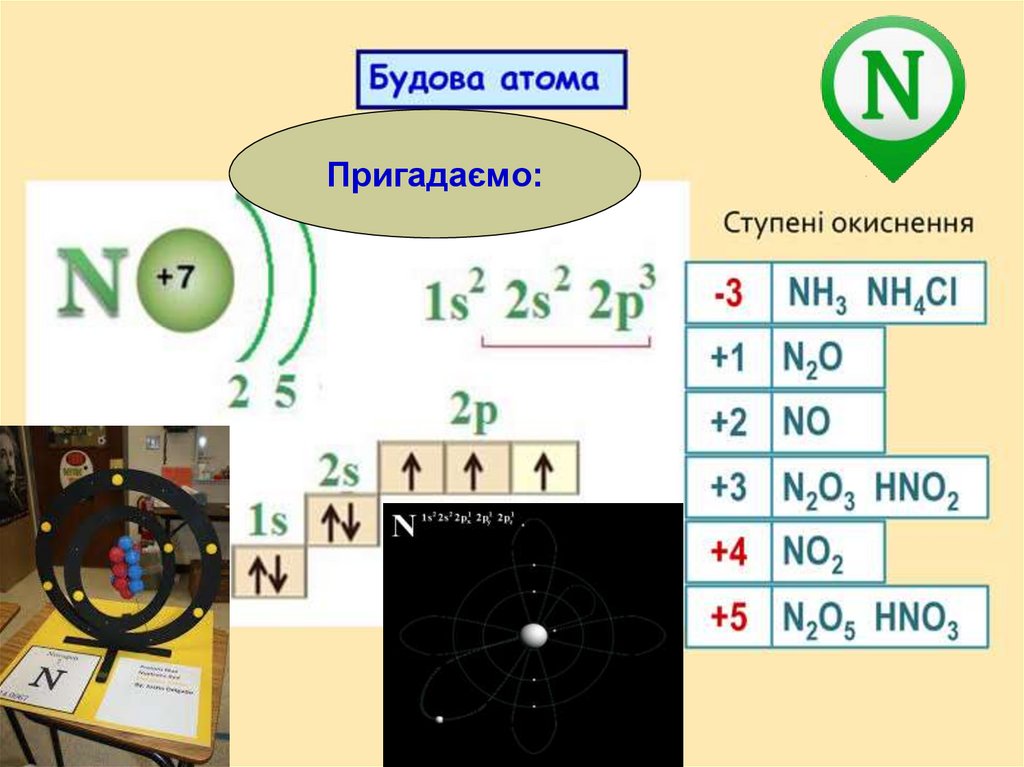
Пригадаємо:4.
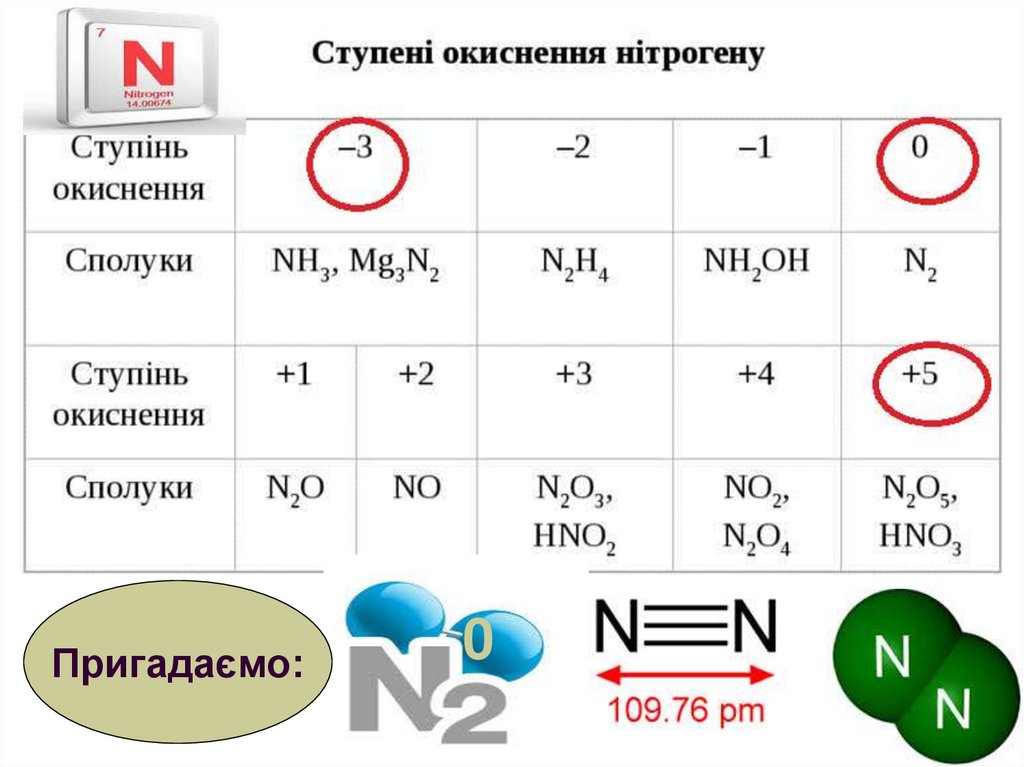
Пригадаємо:0
5.
Походження поняттяНітроген:
латинська: nitrum ,
грецька: нітрон та гени ;
самородна сода, що
утворює. Азот іноді
називали "обпаленим" або
"дефлогізованим"
повітрям. Французький хімік
Антуан Лоран Лавуазьє
назвав азот азоту, що
означає без життя.
Завдання.
Дати пояснення щодо
хімічної інертності простої
речовини азот.
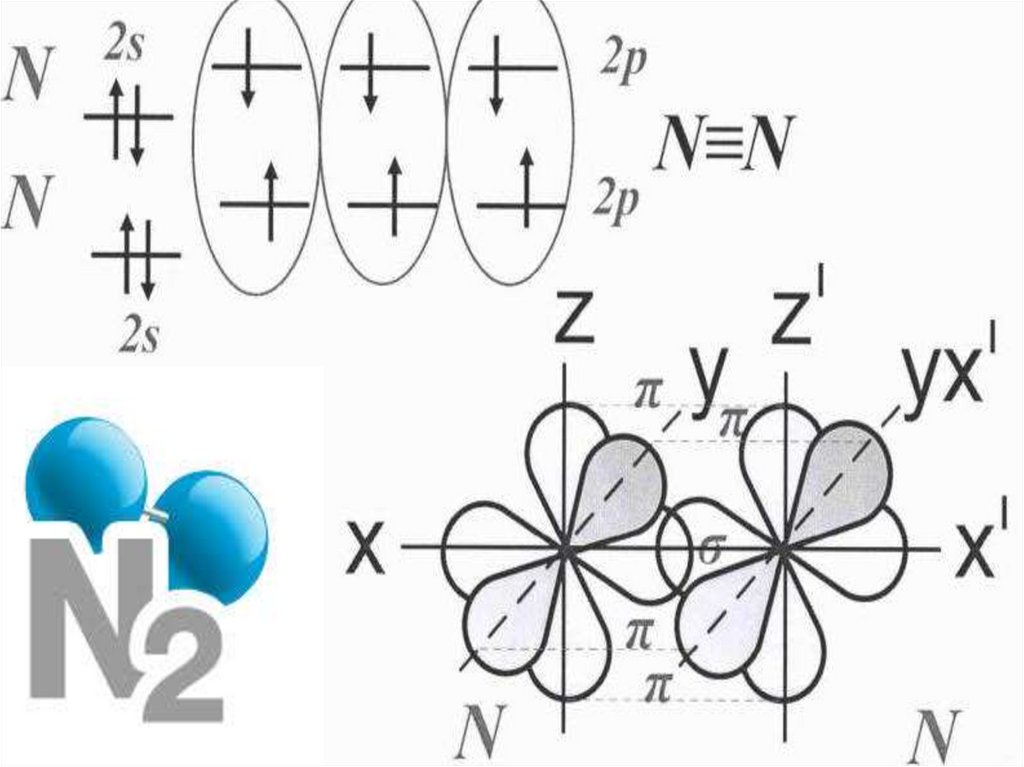
6. У молекулі N2 атоми зв’язані потрійним зв’язком. Велика енергія зв’язку зумовлює високу стійкість і малу хімічну активність N2.
..
:N∙ + ∙N:
˙
˙
:N
N:
7.
8.
9.
За звичайних умов азот реагує лише з літієм, зіншими металами – при нагріванні, утворюючи
нітриди. З воднем сполучається лише при
підвищених температурах і тиску, з киснем – при
температурах понад 3000oС. У реакціях з киснем
і фтором є відновником, в інших випадках –
окисником:
6Li+N2 = 2Li3N
3Mg+N2 = Mg3N2
3H2+N2 = 2NH3
N2+O2 = 2NO
N2+3F2 = 2NF3
10. Сполуки Нітрогену
*Для виробництва добрив, барвників, пластмас і ліків потрібні нітрогеновмісні
сполуки. Але на Землі Нітроген міститься переважно у вигляді простої речовини
N2 у складі повітря. Зв'язування атмосферного азоту в хімічні сполуки — вкрай
важливе завдання для людства. Його можна реалізувати кількома шляхами:
взаємодією азоту з киснем, воднем або металами.
Нітратна кислота
Амоніак
Солі амонію. Нітрати
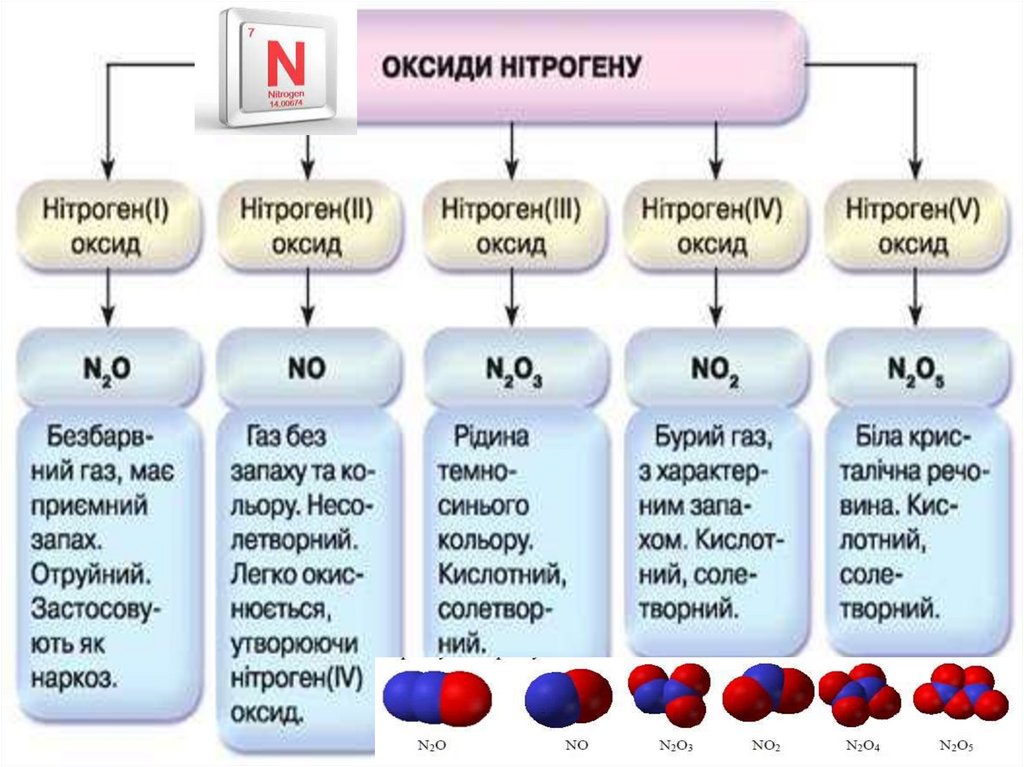
Оксиди
Нітрогену N2Oх
11.
12.
Нітроген входить до складу білків і, отже, зумовлюєіснування рослин, тварин, взагалі життя на 3eмлі.
У природі Нітроген зустрічається як у вільному стані,
так і у зв'язаному. У вільному стані Нітроген у вигляді
азоту входить до складу повітря (об'ємна частка N2
становить 78 %, масова — 75,6 %).
У вигляді неорганічних сполук Нітроген у невеликих
кількостях є в ґрунті.
13.
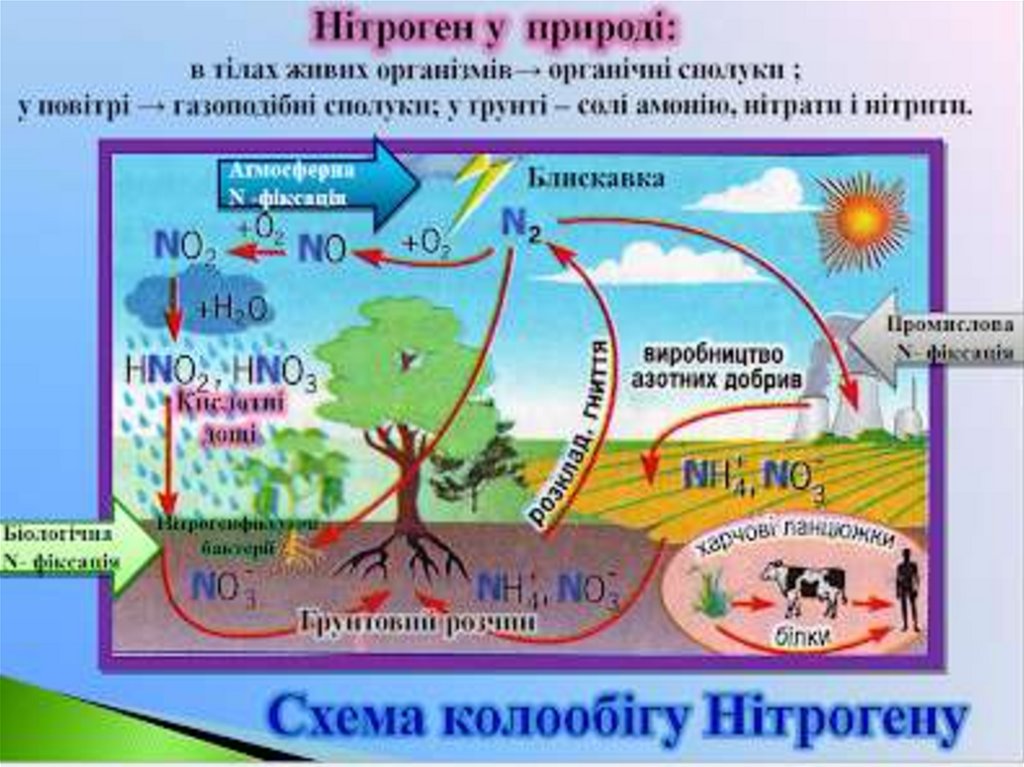
Під час грози атмосферний азот сполучається з киснем,утворюючи NО, що окиснюється киснем повітря до NО2 і
зрештою перетворюється на нітратну кислоту (кислі дощі),
яка потрапляє в ґрунт і там унаслідок взаємодії з
мінералами переходить у нітрати. N2 + O2 = 2NO ;
2NO + O2 = 2NO2 ;
Нітратний нітроген (NО3-) тільки після відновлення до
аміаку може бути використаний рослиною для синтетичного
процесу. 2NO2 + H2O = HNO3 + HNO2
Одночасно відбувається розкладання нітрогеновмісних
речовин і виділення вільного азоту в атмосферу (робота
спеціальних бактерій).
14.
Рослини засвоюють Нітроген неорганічних сполук,які у ґрунті, у вигляді йонів NH4 і NO3. У рослинах
здійснюється синтез білків. Рослини частково
поїдаються травоїдними тваринами, і білкові
речовини потрапляють до організму тварин. Під
час гниття залишків рослин і тварин під впливом
спеціальних бактерій відбуваються складні
біохімічні процеси, внаслідок яких органічні
сполуки, що містять Нітроген, перетворюються на
неорганічні сполуки Нітрогену, які повертаються в
ґрунт. Ці сполуки знову засвоюються рослинами, і
цикл перетворень замикається.
15.
16.
ЗАВДАННЯ.1. Розгляньте схему колообігу азоту в
природі.
2. Дайте відповіді на наступні питання:
а) у резуьтаті діяльності яких організмів в
атмосферу надходить найбільша кількість
азоту?
б) назвіть основні компоненти колообігу
азоту.
в) які зміни відбудуться у кругообігу азоту,
якщо раптом знакнуть азотфіксувальні
бактерії та водорості?
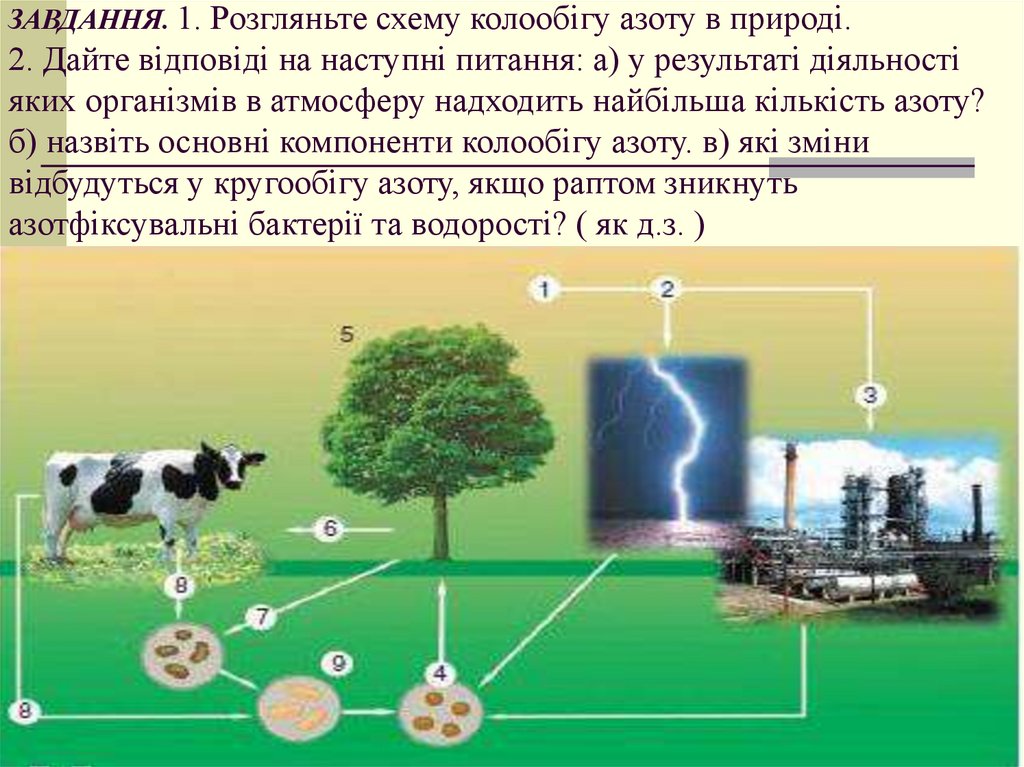
17. ЗАВДАННЯ. 1. Розгляньте схему колообігу азоту в природі. 2. Дайте відповіді на наступні питання: а) у результаті діяльності
яких організмів в атмосферу надходить найбільша кількість азоту?б) назвіть основні компоненти колообігу азоту. в) які зміни
відбудуться у кругообігу азоту, якщо раптом зникнуть
азотфіксувальні бактерії та водорості? ( як д.з. )
18.
Збираючи врожай, людина втручається у цейпроцес, Порушуючи природну рівновагу, збіднюючи
ґрунт Нітрогеном. Тому й треба постійно вносити
Нітроген у ґрунт у вигляді азотних добрив.
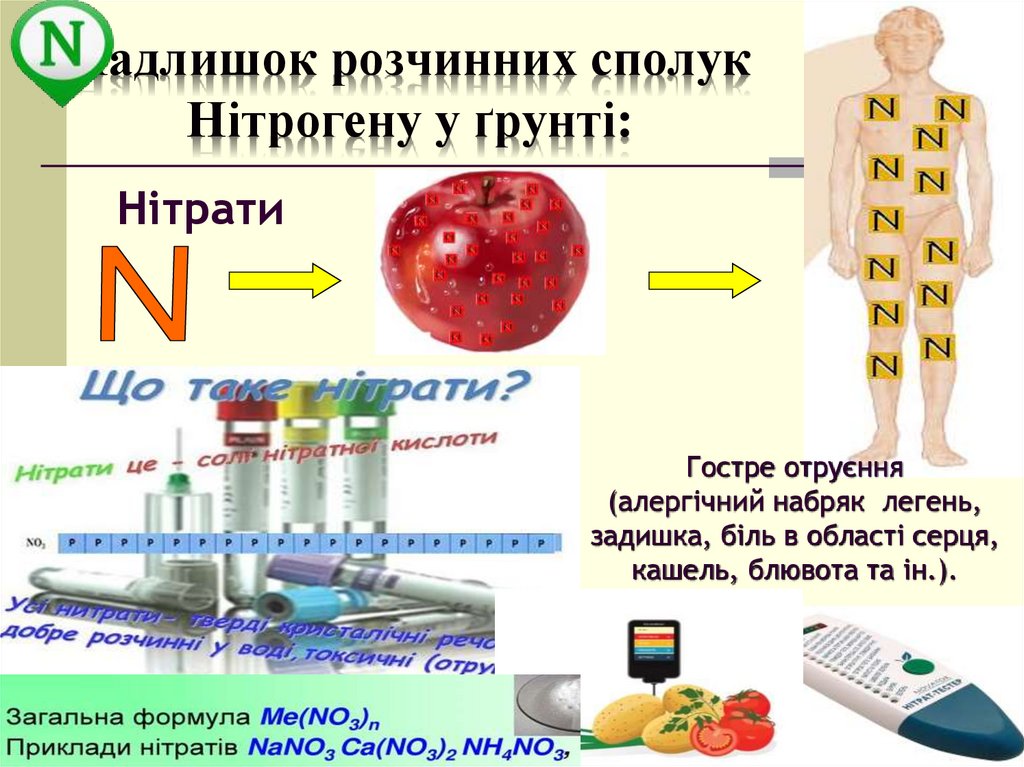
19. Надлишок розчинних сполук Нітрогену у ґрунті:
* Надлишок розчинних сполукНітрогену у ґрунті:
Нітрати
Гостре отруєння
(алергічний набряк легень,
задишка, біль в області серця,
кашель, блювота та ін.).
20.
21.
Нітроген. Сполуки Нітрогену. Використання.Сполуки Нітрогену містяться в продуктах
харчування, добривах, отрутах та вибухових
речовинах. Газовий азот використовується як
середовище для покриття під час виробництва
електронних компонентів. Азот також
використовується для відпалу нержавіючих сталей
та інших сталевих виробів. Рідкий азот
використовується як холодоагент. Хоча
газоподібний азот є досить інертним, ґрунтові
бактерії можуть "закріпити" азот у придатній для
використання формі, яку потім можуть
використовувати рослини та тварини. Нітроген є
складовою частиною всіх білків. Нітроген
відповідає за оранжево-червоний, синьо-зелений,
синьо-фіолетовий та насичено-фіолетовий кольори
полярного сяйва.
22. Цікаві факти про азот.
Першовідкривачем азоту є — шотландський хімікі фізик Даніель Резерфорд (1772 рік).
Слово «азот» з давньогрецької перекладається як
«неживий».
Азот — четвертий найпоширеніший елемент
Сонячної системи (після водню, гелію і кисню).
Атмосфера таких планет як Уран, Нептун, Плутон і
супутників — Титан, Тритон в основному
складається з азоту.
Азот входить до складу білків таких як: гемоглобін,
хлорофіл та ін. Температура кипіння азоту: 195,75
°C.
23. Цікаві факти про азот.
Азот, при швидкому зниженні тиску здатнийпривести до кесонної хвороби. Азот, при
температурі -209,86 °С переходить у твердий
стан (як сніг або кристал ) .
Харчова добавка Е941 — є азотом, що
використовується в харчовій промисловості як
газове середовище для пакування та зберігання.
1 літр рідкого азоту, при нагріванні до 20 °С,
створює близько 700 літрів газу.
Азотне пожежогасіння (на відміну від води,
порошку і піни) є найефективнішим способом
гасіння пожежі.
Тіло людини містить близько 3 % азоту.
24.
25. НАЗВІТЬ ЦІ ЕЛЕМЕНТИ
Оксиди цих елементіввикидаються в
атмосферу
внаслідок роботи
теплових
електростанцій,
автомобільних
двигунів, хімічних
підприємств.
Сполучаючись з
атмосферною
вологою, утворюють
дрібні крапельки
речовин,
які переносяться у
вигляді туману й
випадають на землю у
вигляді відомого всім
природного явища,
згубно впливаючи на
навколишнє
середовище.
26.
1. Елементи що утворюють ці оксиди займають сусіднєгоризонтальне положення в періодичній системі Д.І.
Менделєєва.
2. Вміст оксидів цих елементів у атмосфері
викликає кислотні дощі.
3. Обидва елементи утворюють отруйні оксиди.
4. Елементи можуть утворювати прості речовини
газоподібного та твердого агрегатного стану.
5. Один елемент утворює оксид, який називають “лисячим
хвостом”, а оксид другого елемента добувають
спалюванням газу, що пахне тухлими яйцями.




















 chemistry
chemistry








