Similar presentations:
Классификация химико-технологических процессов. Способы повышения скорости реакций
1. Классификация химико-технологических процессов. Способы повышения скорости реакций
Классификация химикотехнологических процессов.Способы повышения скорости
реакций
2. Химико-технологические процессы
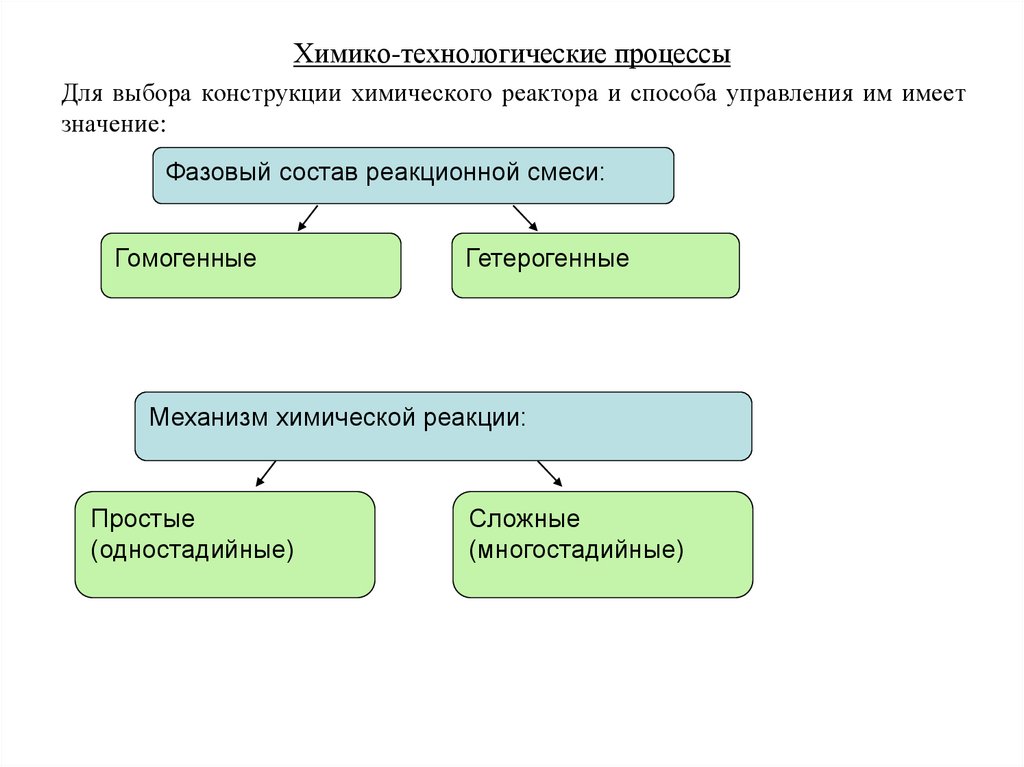
Для выбора конструкции химического реактора и способа управления им имеетзначение:
Фазовый состав реакционной смеси:
Гомогенные
Гетерогенные
Механизм химической реакции:
Простые
(одностадийные)
Сложные
(многостадийные)
3.
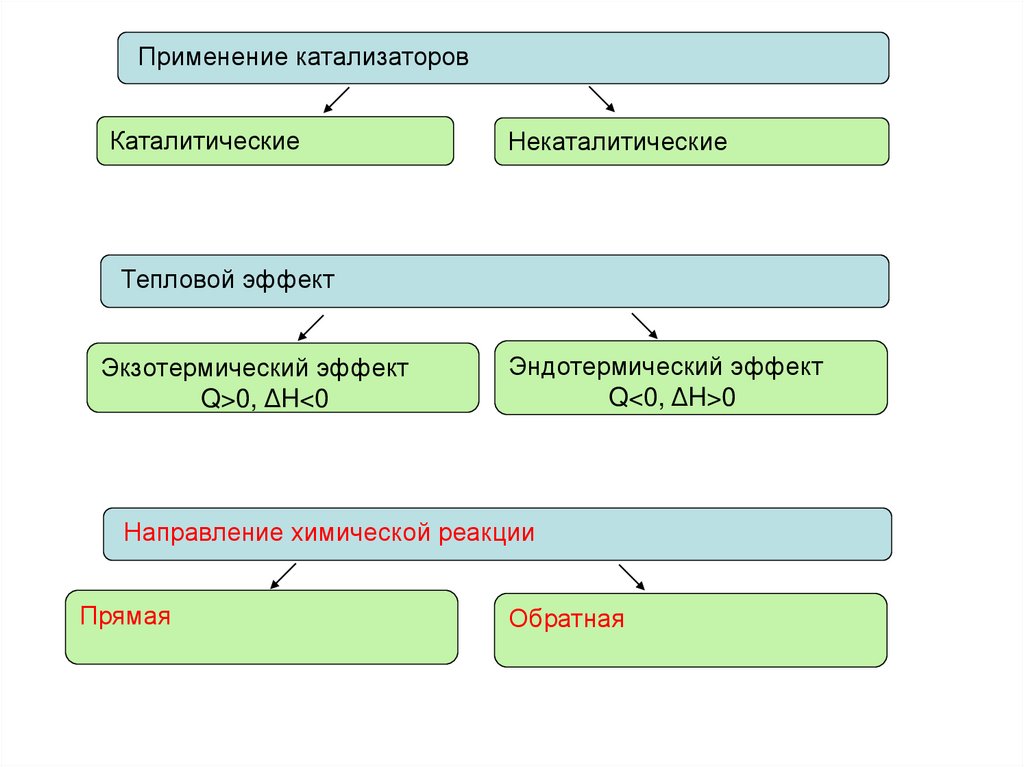
Применение катализаторовКаталитические
Некаталитические
Тепловой эффект
Экзотермический эффект
Q>0, ΔH<0
Эндотермический эффект
Q<0, ΔH>0
Направление химической реакции
Прямая
Обратная
4.
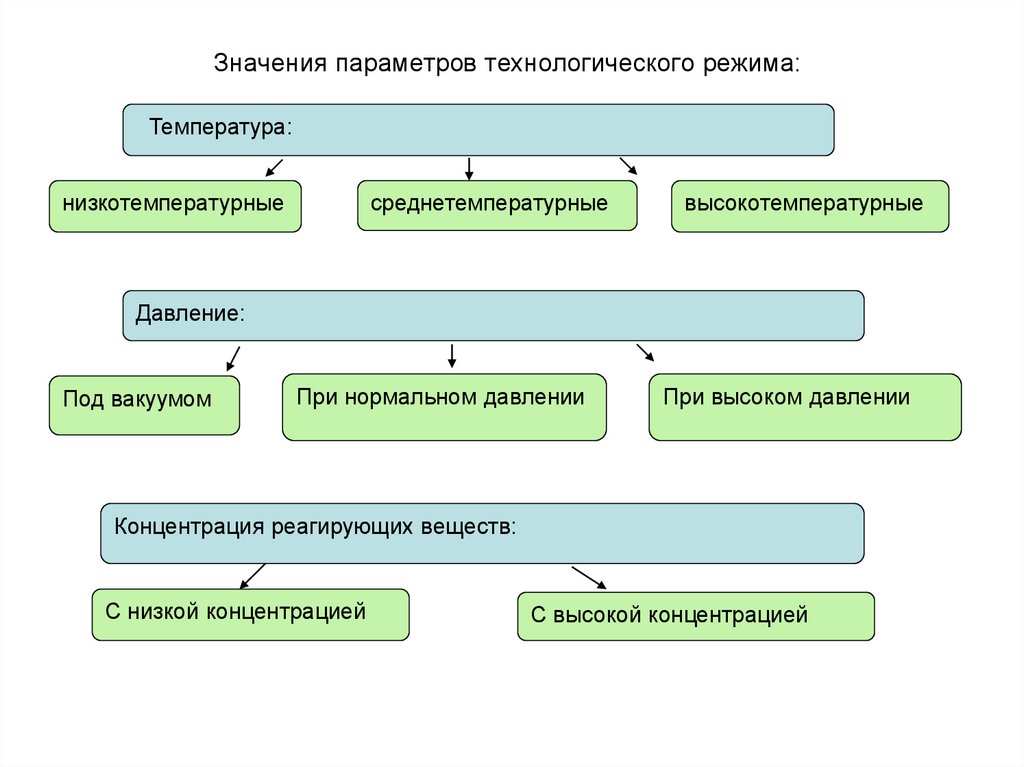
Значения параметров технологического режима:Температура:
среднетемпературные
низкотемпературные
высокотемпературные
Давление:
Под вакуумом
При нормальном давлении
При высоком давлении
Концентрация реагирующих веществ:
С низкой концентрацией
С высокой концентрацией
5. Основные формулы расчета скорости реакции
Cкорость процесса, выраженную нарастанием количества продукта во времениопределяют по формуле:
u=k*v*ΔC
При постоянстве реакционного объёма:
для гомогенных процессов u=k*ΔC
для гетерогенных процессов
Для режима смешения:
Т.к. ΔC ср = ΔC к
u=k*v* ΔC к
u=k* ΔC к
u=k*F*ΔC
6. Способы повышения скорости реакции: ( ΔC, k, F, v )
Увеличение движущей силы п роцесса ΔС может достигается:а) возрастанием концентраций взаимодействующих компонентов в исходных материалах (сырье);
б) повышением давления;
в) регулированием температуры процесса;
г) отводом продуктов реакции из реакционного объема с целью сдвига равновесия в сторону продукта.
Увеличение константы скорости процесса k может достигаться:
а) повышением температуры взаимодействующей системы;
б)применением катализаторов;
в) усилением перемешивания реагирующих масс (турбулизацией системы).
Увеличение поверхности соприкосновения фаз в гетерогенных системах достигается:
в зависимости от вида системы: Г— Ж , Г— Т, Ж — Т, Ж — Ж и Т— Т, а также от необходимого режима
процесса, т. е. применяемых давлений, температур, концентраций реагентов, катализаторов и т. п.
Способ создания поверхности соприкосновения определяет конструкцию аппарата для данной агрегатной
системы.
Во всех случаях стремятся увеличить поверхность более тяжелой (плотной) фазы — твердой в системах
Г— Т, Ж — Т и жидкой в системе Г— Ж ; более легкая фаза во всех типах аппаратов омывает поверхность
тяжелой фазы.



 chemistry
chemistry








