Similar presentations:
Медицинские растворы. Растворение как диффузионно-кинетический процесс. Способы разделения гетерогенных систем
1.
Медицинские растворы.Растворение как
диффузионнокинетический процесс.
Способы разделения
гетерогенных систем.
Технология водных
растворов.
Стандартизация.
2. ТЕОРИЯ РАСТВОРЕНИЯ
Растворимость – способность веществрастворяться
в
воде
или
других
растворителях.
Растворение –диффузионно-кинетический процесс, протекающий при соприкосновении
растворяемого
вещества
с
растворителем
и
сопровождаемый
выравниванием концентрации растворенного вещества во всем объеме вещества.
3. Стадии растворения:
1.Контакттвердого тела с растворителем,
сопровождающийся
смачиванием,
адсорбцией
и
проникновением
растворителя в микропоры.
2.Взаимодействие растворителя и вещества
на
поверхности
раздела
фаз,
сопровождающееся сольватацией молекул
или ионов и их отрывом.
3.Переход
сольватированных ионов и
молекул в жидкую фазу.
4.Выравнивание концентраций во всех слоях
растворителя.
4. Стадии растворения:
Смачивание зависит отполярности
растворителя
и
поверхности
пористости твердого тела, наличия
микротрещин
адсорбированного воздуха, влаги
добавление ПАВ ускоряет процесс
смачивания
5. Факторы, ускоряющие процесс растворения:
нагревание уменьшает вязкость растворителяи прочность
кристаллической решетки,
увеличивается скорость диффузии, что важно
для
неполярных
растворителей,
не
образующих сольватов
предварительное
измельчение
растворяемого вещества ускоряет растворение
за счет увеличения поверхности контакта
вещества с растворителем
перемешивание
облегчает
доступ
растворителя
к
веществу,
способствует
изменению концентрации раствора у его
поверхности
6. Растворение как химический процесс
Д.И.Менделеев:Растворение не только физический
процесс,
но
и
химическое
взаимодействие
растворителя
и
растворяемого
вещества.
Однородность растворов, выделение
или поглощение тепла, изменение
объема при растворении – близость
растворов к химическим соединениям.
7. Растворение как химический процесс
Контракцияуменьшение суммарного объема и
повышение
температуры
при
смешивании
этанола,
метанола,
глицерина и других спиртов с водой
Образование сольватов
обусловливается полярностью молекул
растворяемого
вещества,
благодаря
которой они притягивают полярные
молекулы растворителя.
8. Растворение как химический процесс
Гидраты (водные сольваты)неустойчивые соединения, но иногда
гидратная вода настолько прочно
связана
с
молекулами
растворяемого вещества, что при
выделении последнего из раствора
она входит в состав его кристаллов
(глюкоза,
терпингидрат,
магния
сульфат, квасцы).
9. Технологический процесс получения медицинских растворов
1.Санитарная обработка:-помещений
-оборудования
-персонала
2. Подготовка ЛВ и растворителя:
-отвешивание
-отмеривание по объему
-измельчение
-просеивание
-получение воды очищенной и этанола заданной
концентрации
10. Технологический процесс получения медицинских растворов
3. Растворение (введение ЛВ в растворитель)4. Очистка
-отстаивание
-фильтрование
-центрифугирование
5. Стандартизация
-органолептический контроль
-содержание действующих веществ
-определение плотности
-чистота
-концентрация этанола в спиртовых растворах
6. Фасовка и упаковка, оформление
-флаконы
-ампулы
-ангро
11. Растворители
Растворители - индивидуальные химическиесоединения или их смеси, способные растворять
различные вещества, т.е. образовывать с ними
однородные системы- растворы.
Растворители должны обладать:
хорошей растворяющей способностью
химической
и
фармакологической
индифферентностью
отсутствием неприятного вкуса и запаха
микробиологической стабильностью
огне-, пожаро-, взрывобезопасностью
экономичностью
12. Способы приготовления растворов в заводских условиях
1. Простое растворение лекарственного вещества врастворителе:
-Sol.Calcii chloridi 5% 200 ml.
2. Электрохимический способ - электролиз.
Основан
на
совокупности
процессов
электрохимического
окисления-восстановления,
происходящих на погруженных в электролит
электродах при прохождении электрического тока.
- Sol. Aluminii subacetatis 8%.
Анодное растворение алюминия в 8% растворе
уксусной кислоты (ванна – катод, Al - анод).
Процесс ведут до получения плотности раствора
1.040-1.046 при рН=4.0-4.7.
13. Способы приготовления растворов в заводских условиях
3. Химический способ.Sol. Aluminii subacetatis 8%.
Раствор
получают
при
химическом
взаимодействии веществ в две стадии.
а. Синтезируют Al(OH)3 из алюмокалиевых
квасцов и кальция карбоната.
2KAl(SO4)2
12H2O+3CaCO32Al(OH)3+2CaSO4+K2SO4+3CO2+21H2O
b. Al(OH)3 промывают от электролитов и
обрабатывают 30% уксусной кислотой.
Al(OH)3+CH3COOH---Al(OH)(CH3COOH)2+2H2O
4.
Разведение
концентрированных
растворов.
14. Номенклатура растворов
1. Водные растворы для внутреннегоприменения:
- Sol. Calcii chloridi 5%-200 ml
- Sol. Kalii chloridi 10%
2. Водные растворы для наружного
применения:
- Sol. Aluminii subacetatis 8% (liqor Burovi)
- Sol. Plumbus subacetatis
3. Водные растворы, получаемые разведением
концентрированных растворов:
- Perhydrolum с содержанием H2O2 27,5-31%
- Sol. Hydrogenii peroxidi diluta (2,7-3,3%)
- Sol. Ammonii caustici 10%
15. Номенклатура растворов
4. Масляные растворы для наружногоприменения:
- Oleum Mentholi 2% с вазелиновым маслом
- Sol. Camphorae oleosae 10% в подсолнечном
масле
5. Масляные растворы для внутреннего
применения:
- Ergocalciferoli oleosa (витамин D)
- Sol. Retinoli oleosa (витамин А)
16. Номенклатура растворов
6. Глицериновые растворы- Sol. Lugoli
7. Спиртовые растворы
- Sol. Camphore spirituosa 10% (70 ч. 96% этанола
+ 20 ч. Воды очищенной)
- Sol. Acidi salycilici spirituosa 1% (66 ч. 95%
этанола + 33 ч. Воды очищенной)
- Sol. Borici spirituosa 3% (66 ч. 95% этанола + 31 ч.
Воды очищенной)
- Sol. Methilenii coerulei spirituosa 1% (на 90%
этаноле)
- Sol. Iodi spirituosa (содержание этанола не менее
46%)
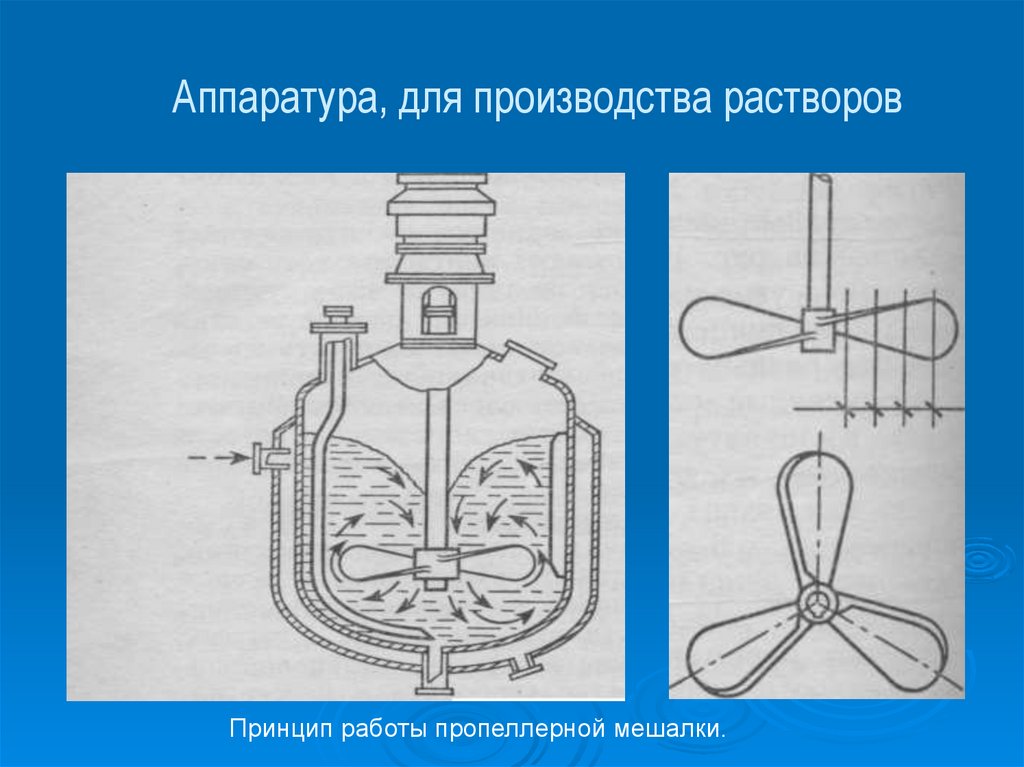
17. Аппаратура, для производства растворов
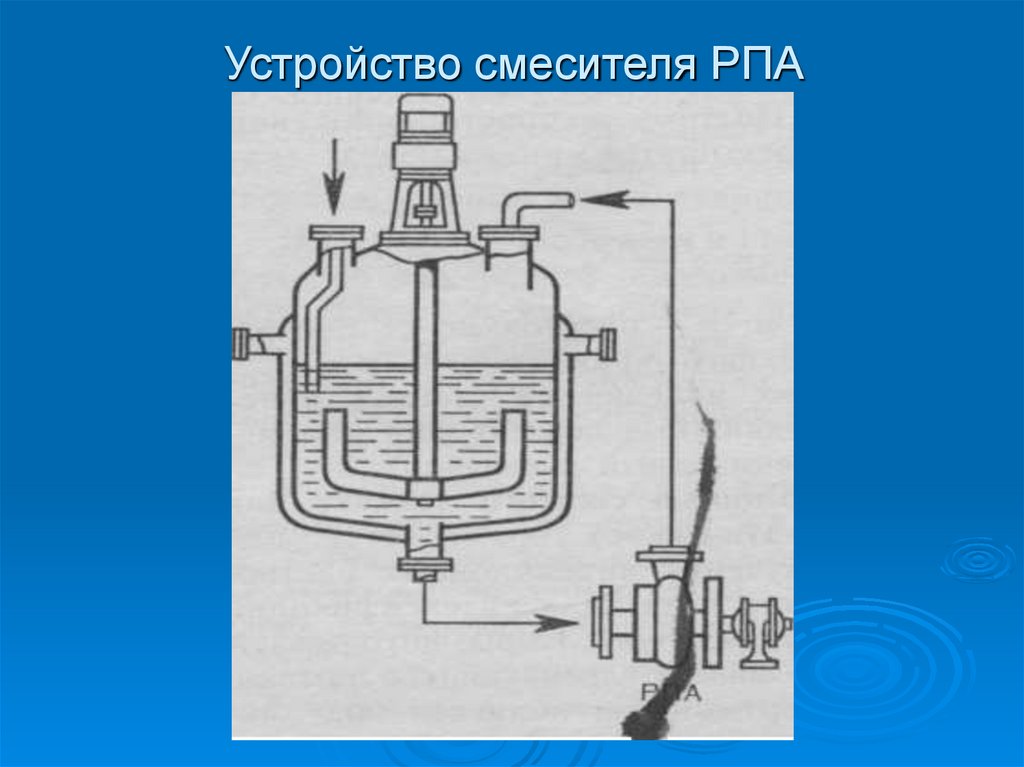
Принцип работы пропеллерной мешалки.18. Устройство смесителя РПА
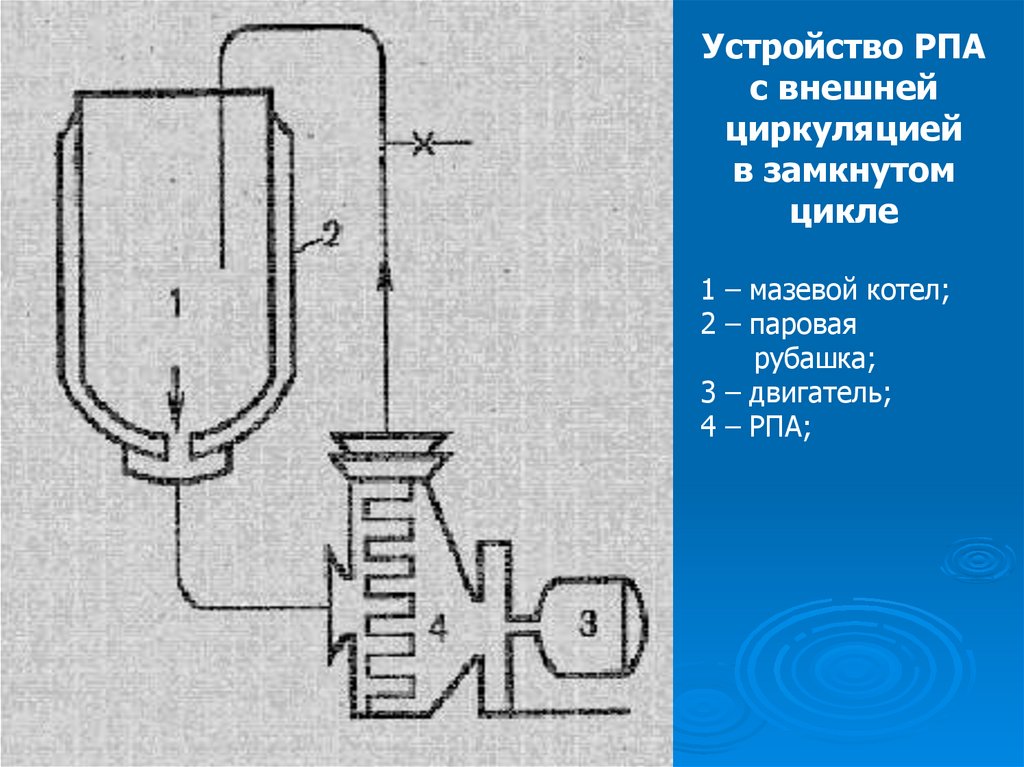
19.
Устройство РПАс внешней
циркуляцией
в замкнутом
цикле
1 – мазевой котел;
2 – паровая
рубашка;
3 – двигатель;
4 – РПА;
20. Пути интенсификации процесса растворения
1. Нагревание или охлаждение.2. Перемешивание :
-механическое с помощью мешалок;
-пневматическое- сжатым воздухом;
-гравитационное;
-перемешивание в трубопроводе;
-акустическое (ультразвуковым)
-циркуляционное (перекачиванием).
21. Очистка растворов
1. Отстаивание2. Фильтрование
Выбор способа и условий разделения связан со
свойствами исходных дисперсных систем
(удельная поверхность, вязкость, плотность
дисперсных сред, величина поверхностного
натяжения) свойства образующегося осадка:
полидисперсность, форма частиц, пористость,
возможность агрегации.
22. Отстаивание жидких гетерогенных систем
Отстаиваниежидких
гетерогенных
системразделение под действием сил тяжести.
Скорость оседания частиц V(м/сек) определяется
по уравнению Стокса:
V=2r(dф-dc) g/9n
r - радиус частиц, м
g - плотность фазы и среды, г/м
n - вязкость среды, пуаз
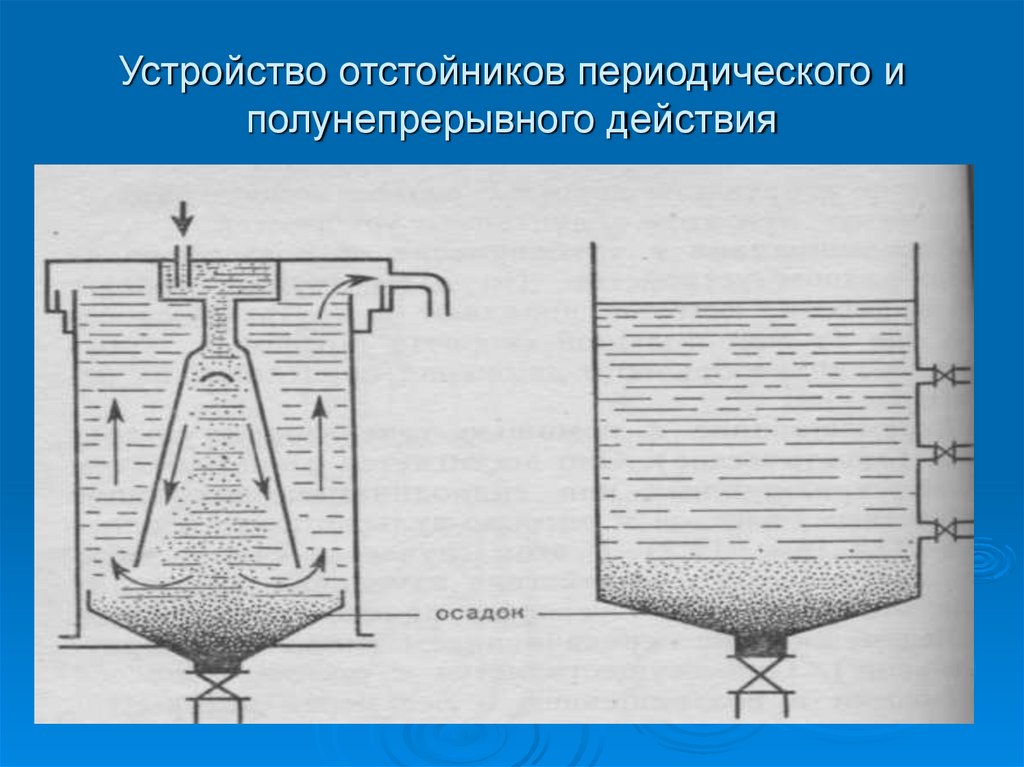
Отстаивание
проводят
в
отстойниках
или
седиментаторах
периодического,
полунепрерывного и непрерывного действия.
Недостаток
процессадлительность,
малая
производительность и неполное разделение(осадок
содержит до 70% жидкости)
23. Устройство отстойников периодического и полунепрерывного действия
24. Фильтрование растворов
Фильтрование – это процесс разделениянеоднородных систем: взвесей и аэрозолей с
помощью пористых перегородок (фильтров).
Фильтрование представляет собой освобождение
жидкой фазы от всех взвешенных частиц. Скорость
фильтрования зависит от давления, при котором
идет процесс, от величины пор фильтрующего
материала, от вязкости жидкости. Процесс
задерживания частиц может проходить как в толще
фильтрующего материала, так и на поверхности.
Фильтрующие перегородки :
- сжимающиеся (гибкие) – тканевые фильтры;
- несжимающиеся – фильтры в виде плит,
патронов, пластин.
25. Требования к фильтрующим материалам:
-должныобладать
определенной
прочностью
-иметь
структуру,
обеспечивающую
эффективное задержание частиц при
высокой проницаемости
-материал не должен выделять в раствор
волокна
или
частицы
и
взаимодействовать с лекарственными
веществами
-должен
выдерживать
стерилизацию,
регенерацию, давление
-должен быть доступным и дешевым.
26. Фильтрование растворов
При удержании частиц на поверхностиобразуется
дополнительный
фильтрующий слой. Для увеличения
поверхности
адсорбции
добавляют
вспомогательные вещества в количестве
от 0,1% до 0,5%(иногда до 2%). Это
кезельгур,
уголь
активированный,
порошок целлюлозы, перлит, белая глина.
27. Фильтрование растворов
Фильтрование может проходитьпри постоянном или переменном
давлении.
Фильтр,
работающий
под
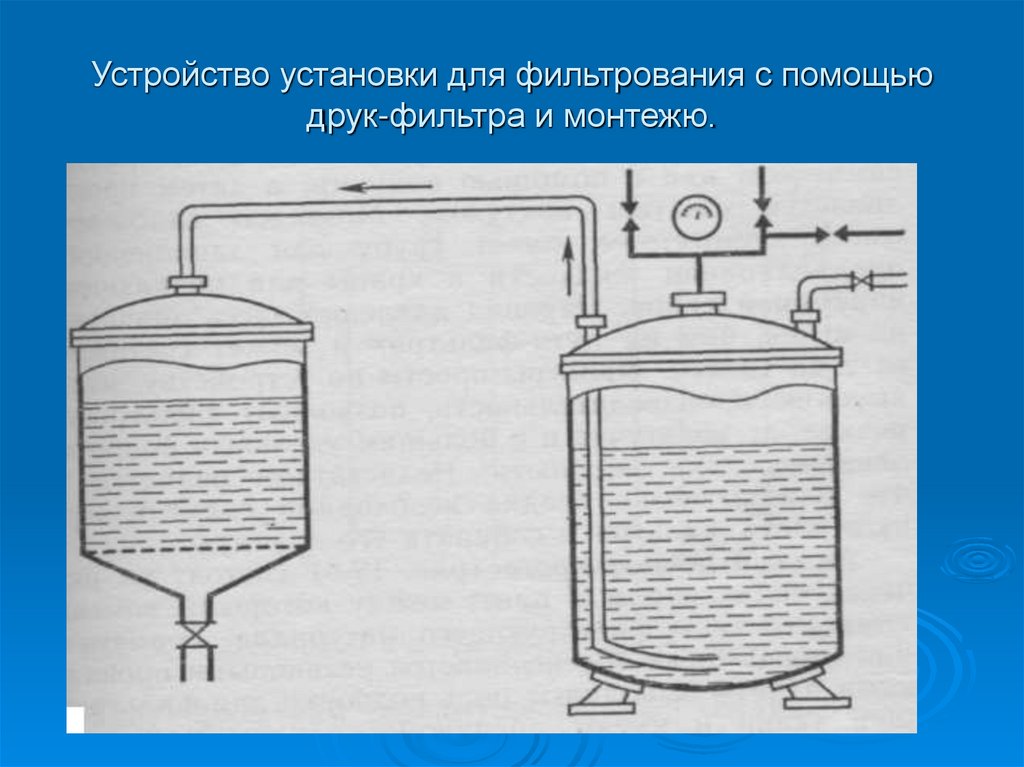
давлением, называется друк-фильтр.
Фильтры,
работающие
под
вакуумом называются нутч-фильтры.
Для фильтрования жидкостей с
небольшим
количеством
осадка
используются
рамные
фильтры,
которые легко регенерируются.
28. Устройство установки для фильтрования с помощью друк-фильтра и монтежю.
29. Установка для фильтрования с помощью нутч-фильтра
Нутч-фильтрРесивер
Вакуумный насос
30. Центрифугирование растворов
Центрифугирование - способ очисткирастворов, по существу представляющий собой
процесс отстаивания или фильтрования в поле
центробежных
сил.
Развиваемые
при
центрифугировании
центробежные
силы
оказывают на разделяемую жидкость более
сильное воздействие, чем сила тяжести и
давление.
Поэтому
центрифугирование
является более эффективным процессом
очистки.
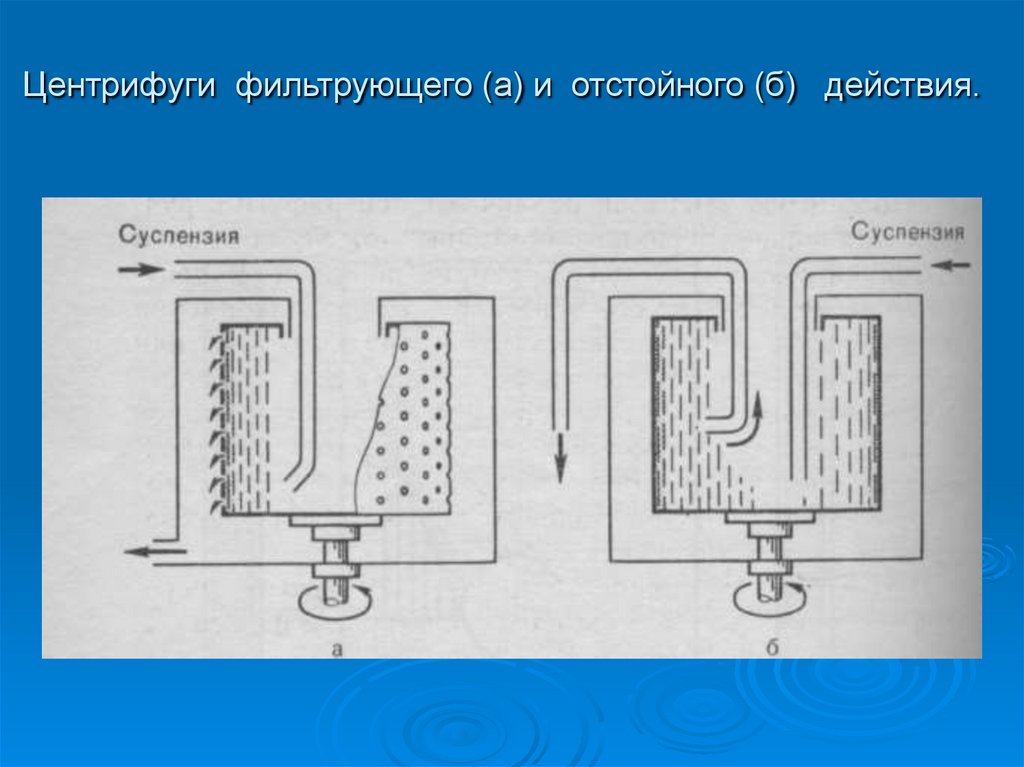
Центрифуги различают по конструкции и
скорости вращения на отстойнике, имеются т.н.
фильтрующие, отстойные и суперцентрифуги.
31. Центрифуги фильтрующего (а) и отстойного (б) действия.
32. Стандартизация растворов
- внешнийвид (цвет, запах, вкус,
отсутствие механических
мутность,
включений)
- содержание действующих веществ
(количественное
содержание
действующего вещества)
- плотность
- чистота (микробиологическая чистота
на наличие бактерий и дрожжевых и
плесневых грибов)
- концентрация этанола в спиртовых
растворах
33. Расчеты по растворам
При несоответствии концентраций раствора требуемойследует рассчитать необходимое количество
растворителя или концентрированного раствора:
1. Разведение по массе: X1=m a-b/b-c
X2=m a-c/b-c
a - концентрация укрепителя
b - концентрация требуемого раствора
с - концентрация разбавителя
m – масса раствора
2. Разведение по объему: X1=V a-b/b-c
X2=V a-c/b-c
a - концентрация укрепителя
b - концентрация требуемого раствора
с - концентрация разбавителя
V – объем раствора
34. Расчеты по растворам
3. Расчеты по плотности:плотность определяют пикнометром или
ареометром (денсиметром).
Денсиметр при температуре 20 град.
Показывает плотность с точностью до 0,01.
Точность
до
0,001
обеспечивается
применением пикнометра: взвешивают пустой
пикнометр (m), с очищенной водой (m1), и с
исследуемой
жидкостью
(m2);
вычисляют
плотность по формуле:
p= (m2-m) 0,99703/(m1-m) + 0,0012
0,99703 – плотность воды при t=20 град.
0,0012 – плотность воздуха при t=20 град.
35. Фасовка и упаковка растворов
- флаконы из стекла марки НС-1, НС-2- ампулы (стеклянные и полимерные)
- ангро (бутыли из стекла)
Хранение медицинских растворов
Факторы, влияющие на хранение:
- температура
- герметичность упаковки (воздействие
атмосферного воздуха, влажность)
- воздействие солнечного света
36. Примерные сроки хранения медицинских растворов
1. Растворы для наружного применения:водные – 3 года
масляные - 5 лет
2. Глазные капли – 2 года
3. Растворы для внутреннего применения:
- водные – 3 года
- масляные –3 года
4. Стерильные (ампулированные) – 3 года
5. Растворы, полученные разведением
концентрированных растворов – 2 года
6. Глицериновые –2 года
7. Спиртовые – 2 года






























 medicine
medicine








