Similar presentations:
Углеводы. Образовательные: совершенствовать знания о связи между строением и свойствами органических соединений
1. Урок химии в 10 классе на тему: «Углеводы»
Подготовила: учитель химииМБОУ «СОШ №50»
Сулейманова Ашура Каримовна
Махачкала 2019г.
2. Цель:
научиться делать выводы о природенеизвестного вещества на основании
теоретических знаний и проведенного
эксперимента.
3. Задачи:
1.Образовательные: совершенствовать знания о связи междустроением и свойствами органических соединений на примере
глюкозы, познакомиться с физическими свойствами углеводов,
изучить свойства и применение глюкозы.
2.Развивающие: продолжить развитие навыков исследовательской
деятельности через постановку проблемы, выдвижения гипотезы и
её проверке; создать условия для развития умений наблюдать и
объяснять химические явления, умений анализировать результаты
наблюдаемых опытов.
3.Воспитательные: совершенствовать интеллектуальные умения
(анализ, прогнозирование, умение устанавливать причинноследственные
связи),
соответствующие
возможностям,
способностям, потребностям обучающихся и ориентировать
учеников на их личностное развитие.
4. Эпиграф
«Химик не такой должен быть,который дальше дыму и пеплу ничего
не видит, а такой, который на
основании опытных данных может
делать теоретические выводы».
(М.В. Ломоносов)
5. Девиз
«Нет «актеров» и «зрителей» все –участники
Говорить так, чтобы тебя понимали.
Будь активным, стремись к успеху.
Критикуются идеи, а не личности.
Возражай»
6.
7.
8.
9. ОПРЕДЕЛЕНИЕ:
Углеводы – органические соединения,состоящие из углерода, водорода и
кислорода, причем водород и кислород
входят в соотношении (2 : 1) как в воде,
отсюда и название.
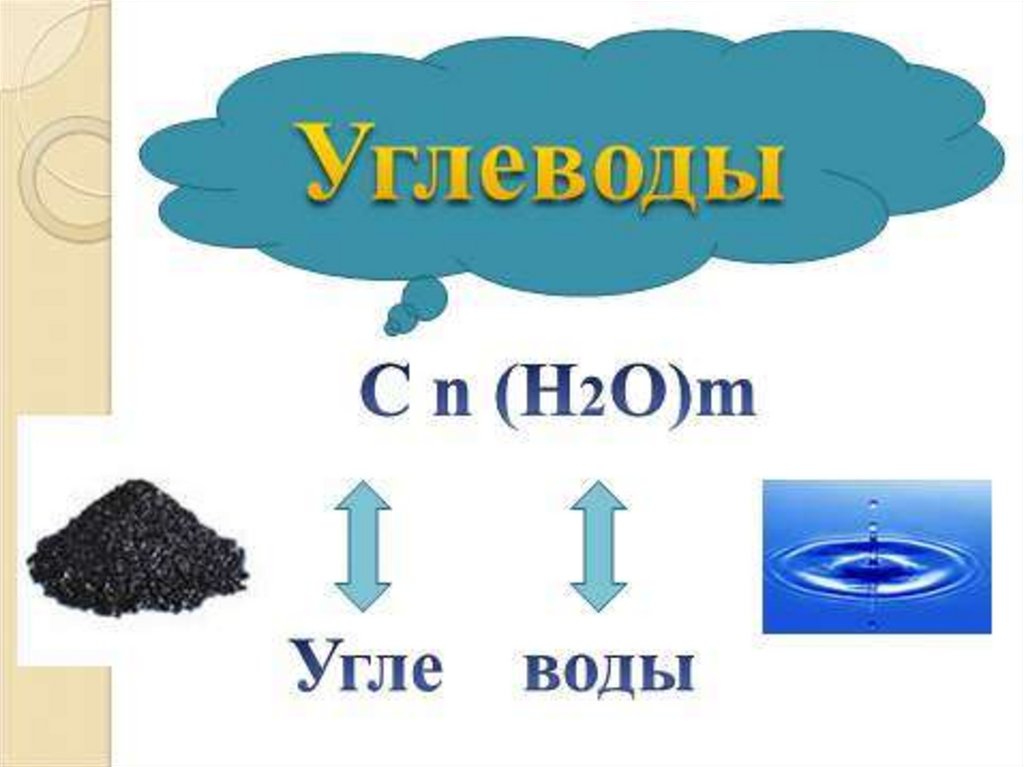
На основе этой аналогии русский химик
К. Шмидт в 1844 г. предложил термин
углевода (углерод и вода), а общая
формула углеводов Сn(Н2О)m
10. История названия
Первые представители класса посоставу отвечали общей формуле
Cn(H2O)m
то есть :
n C * m H2O
11. Немного из истории:
А. М. Бутлеров(1861г.) – автор первого
синтеза сахароподоб ного вещества.
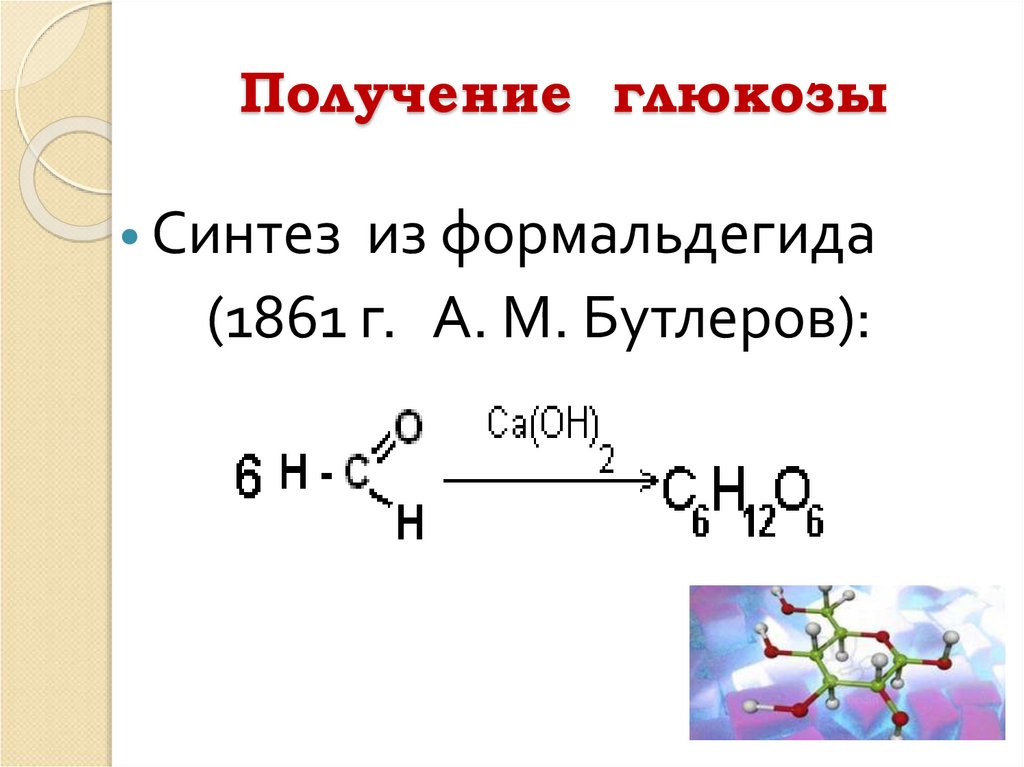
12. Получение глюкозы
• Синтез из формальдегида(1861 г. А. М. Бутлеров):
13.
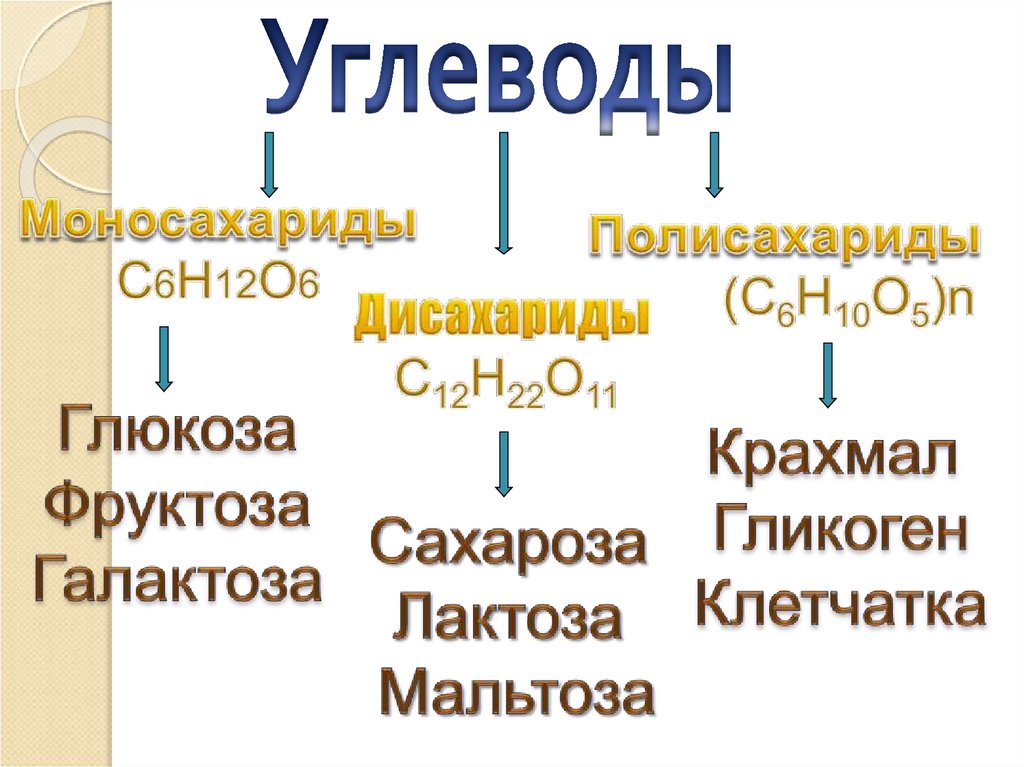
14. КЛАССИФИКАЦИЯ УГЛЕВОДОВ
МОНОСАХАРИДЫ— углеводы, которые
не гидролизуются. В зависимости от числа атомов
углерода подразделяются на триозы, тетрозы,
пентозы, гексозы.
ДИСАХАРИДЫ
– углеводы, которые
гидролизуются с образованием двух молекул
моносахаридов.
ПОЛИСАХАРИДЫ
—
высокомолекулярные соединения — углеводы,
которые гидролизуются с образованием множества
молекул моносахаридов.
15.
16. САМОСТОЯТЕЛЬНАЯ РАБОТА
Сравнить физические свойства углеводов разных классов,открыть учебник на странице
I группа – глюкоза – стр. 103-104
II группа – сахароза – стр. 110-111
III группа - крахмал – стр. 112-113
и заполнить таблицу.
17. Сравнение физических свойств углеводов разных классов
Признаки сравнения1. Формула
2. Группа
3. Агрегатное состояние
4. Цвет
5. Запах
6. Вкус
7. Растворимость в воде
Глюкоза
Сахароза
Крахмал
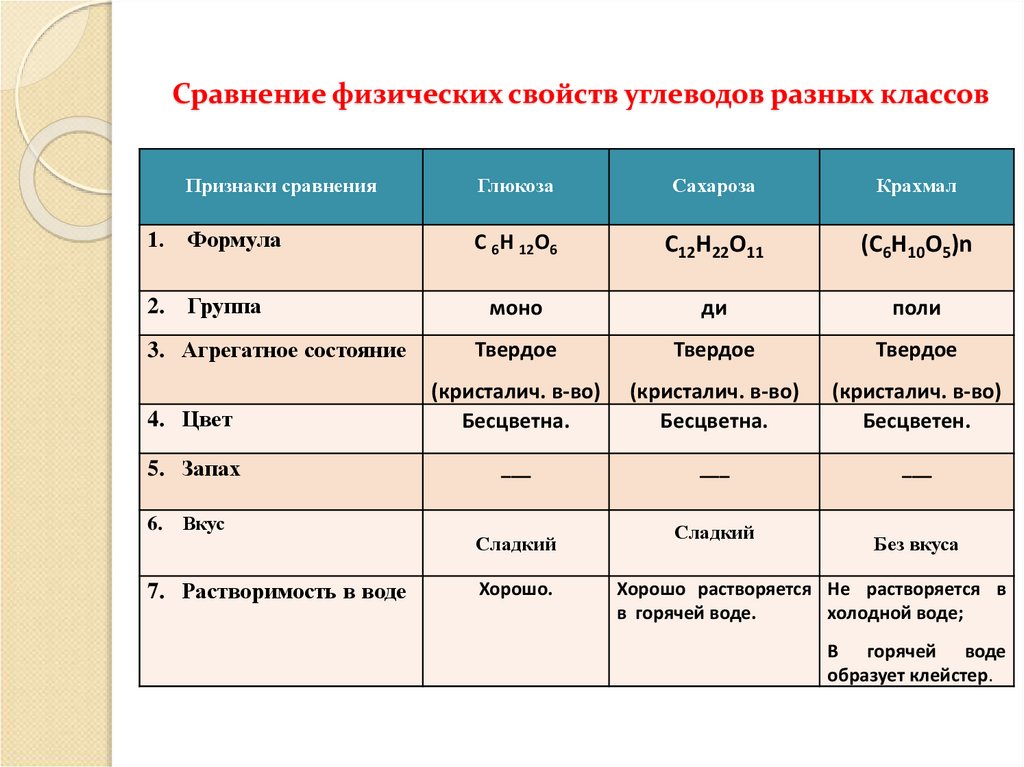
18. Сравнение физических свойств углеводов разных классов
Признаки сравненияГлюкоза
Сахароза
Крахмал
1. Формула
С 6Н 12О6
С12Н22О11
(С6Н10О5)n
2. Группа
моно
ди
поли
3. Агрегатное состояние
Твердое
Твердое
Твердое
4. Цвет
(кристалич. в-во)
Бесцветна.
(кристалич. в-во)
Бесцветна.
(кристалич. в-во)
Бесцветен.
5. Запах
___
___
___
6. Вкус
7. Растворимость в воде
Сладкий
Хорошо.
Сладкий
Без вкуса
Хорошо растворяется Не растворяется в
в горячей воде.
холодной воде;
В горячей воде
образует клейстер.
19. Сахароза
Сахароза, тростниковый или свекловичныйсахар, один из важнейших дисахаридов
20. Крахмал
главный резервныйполисахарид растений;
21. Целлюлоза в природе
Хлопок и нитиЛён и волокна из льна
22. Решить задачу:
Определитьмолекулярную
формулу вещества, если в его
состав входят 40% углерода, 6,7%
водорода, 53,3 % кислорода.
Относительная плотность по
воздуху = 6,21.
23.
24. Лабораторная работа
Цель:изучить свойства углеводов на примере
глюкозы. Научиться проводить качественные
реакции.
Задачи:
развить познавательный интерес к предмету;
дисциплинированность;
четко следовать инструкции;
соблюдать правила техники безопасности;
грамотно оформлять свои наблюдения и
выводы;
25. Опыт №1 Проверить наличие карбоксильной группы в глюкозе.
Опыт №2Проверить наличие гидроксильных
групп в глюкозе.
26. Опыт №3 Качественная реакция глюкозы с аммиачным раствором оксида серебра (I).
27. Уравнения реакций
1. Окисление гидроксидом меди (II)СH2OH(CHOH)4-COH + 2Cu(OH)2 t →
СH2OH(CHOH)4-COOH + Cu2O + 2H2O
2. Реакция «серебряного зеркала»:
СH2OH(CHOH)4-COH + 2[Ag(NH3)2]OH → СH2OH(CHOH)4-COOH + 2Ag↓+ 4NH3 + H2O
28. Глюкоза
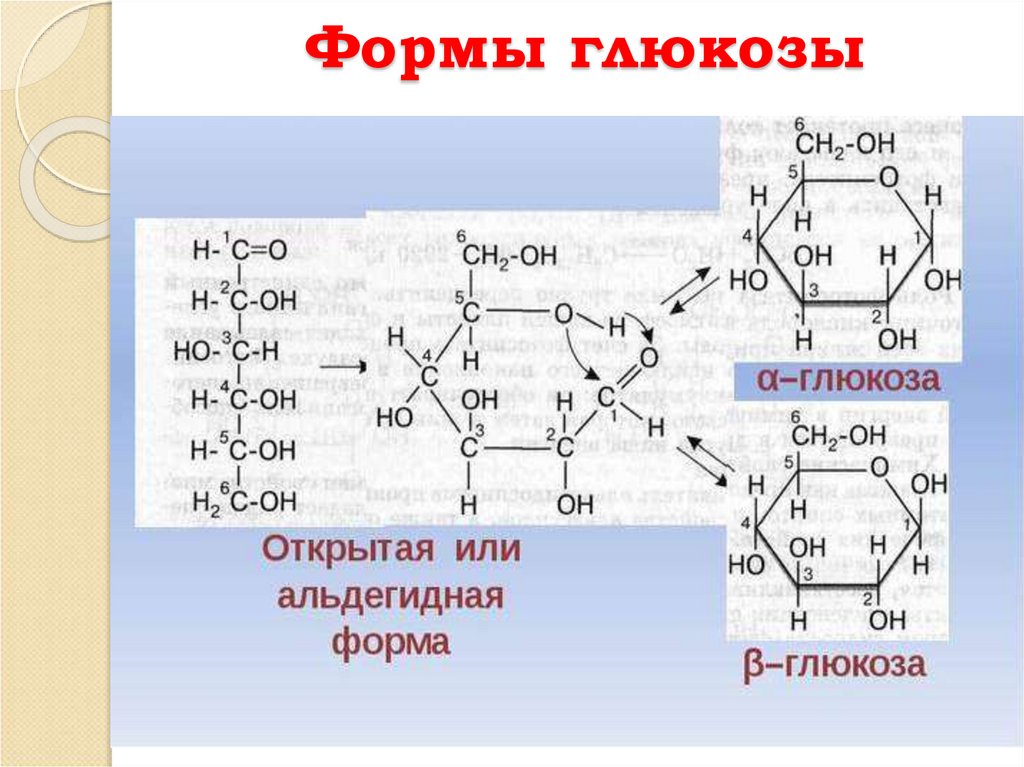
29. Формы глюкозы
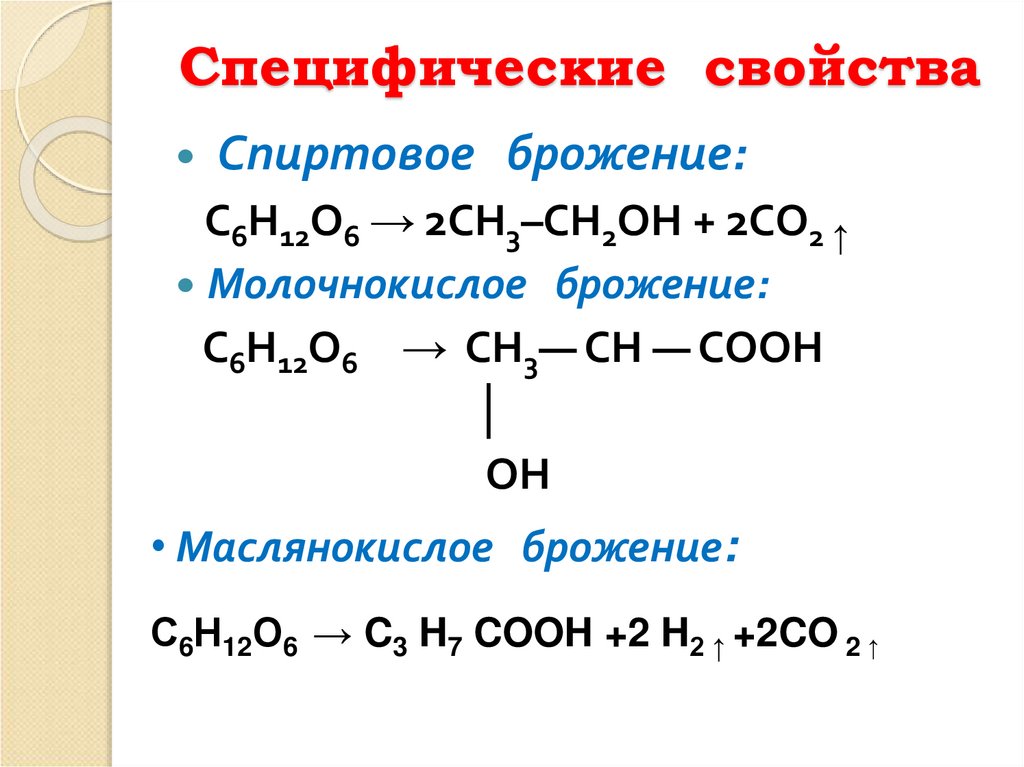
30. Специфические свойства
Спиртовоеброжение:
C6H12O6 → 2CH3–CH2OH + 2CO2 ↑
Молочнокислое брожение:
С6Н12О6 → СН3— СН — СООН
│
ОН
• Маслянокислое брожение:
С6Н12О6 → C3 H7 COOH +2 H2 ↑ +2CO 2 ↑
31. Основная роль углеводов в организме:
Углеводы – основной источникэнергии в организме
32. Рибоза и дезоксирибоза
в качестве структурногофрагмента входят в состав
нуклеиновых кислот – ДНК
и РНК, входят в структуру
гена.
33. Углеводы
Участвуют в синтезебелков, ферментов,
гормонов.
34. Применение углеводов
35. Глюкоза
В медицине.36. Углеводы
- источник питания37. Сахароза
Сахар - в качествепродукта питания.
38. Углеводы
Запасающая функция, резервпитательных веществ и
энергии
(в виде АТФ) в организме.
39. Крахмал
В пищевой промышленностикрахмал используется для получения
глюкозы и патоки,
в текстильной — для обработки
тканей.
40. Целлюлоза
Самая гигиеничная одежда - хлопок, лён.41. Целлюлоза и хитин
Строительный материал растительныхклеток (каркас для оболочек клеток).
Хитин образует наружный скелет
ракообразных, насекомых,
паукообразных.
42. Целлюлоза
Бумага, деньги, книги,газеты, фото- и
киноплёнка.
43. Целлюлоза
Деревянные дома, мебель.44.
45.
ТЕСТ НАТЕМУ:
«УГЛЕВОДЫ».
10 КЛАСС.
46. Рефлексия:
Мы сегодня с вами, говоря словами МихаилаВасильевича Ломоносова, пытались увидеть
«дальше дыму и пеплу»; делали выводы,
исследовали природу неизвестного вещества на
основании теоретических знаний и эксперимента.
1. Помогла ли она вам разобраться в
премудростях химии?
2. Возможно ли на ваш взгляд проведение
исследований без теоретической основы?
3. Достигли мы поставленных целей?


































 biology
biology