Similar presentations:
Респираторный дистресс-синдром
1.
федеральное государственное бюджетное образовательное учреждениевысшего образования «Тюменский государственный медицинский университет»
Министерства здравоохранения Российской Федерации
(ФГБОУ ВО Тюменский ГМУ Минздрава России)
Институт материнства и детства
Кафедра детских болезней и поликлинической педиатрии
Тема : «Респираторный дистресс-синдром»»
Подготовила: студентка 535 группы Алиева Элиза
Преподаватель: к.м.н., доцент кафедры
Гордийчук Светлана Николаевна
2.
Синдром дыхательных расстройств или «респираторный дистресс-синдром»(РДС) новорожденного представляет расстройство дыхания у детей в первые дни
жизни, обусловленное первичным дефицитом сурфактанта и незрелостью легких. В
соответствии с МКБ-10 эта нозология имеет код P22.0.
Этиология
РДС - наиболее частая причина возникновения дыхательной недостаточности в раннем
неонатальном периоде. Встречаемость его тем выше, чем меньше гестационный
возраст и масса тела ребенка при рождении. Проведение пренатальной профилактики
при угрозе преждевременных родов также влияет на частоту развития РДС.
• У детей, родившихся ранее 30 нед гестации и не получавших пренатальной
профилактики бетаметазоном или дексаметазоном, его частота составляет около
65%, при проведении профилактики - 35%;
• у детей, родившихся на сроке гестации 30-34 нед: без профилактики - 25%, при
проведении профилактики - 10%.
• У детей, родившихся с гестацией более 34 нед, частота развития РДС составляет
менее 5%.
3.
Факторы рискаПредрасполагающие факторы развития РДС, которые могут быть выявлены до рождения
ребенка или в первые минуты жизни:
1. Развитие РДС у сибсов;
2. Гестационный диабет и сахарный диабет 1-го типа у матери;
3. Гемолитическая болезнь плода;
4. Преждевременная отслойка плаценты;
5. Преждевременные роды;
6. Мужской пол плода при преждевременных родах;
7. Кесарево сечение до начала родовой деятельности;
8. Асфиксия новорожденного.
Основные причины развития РДС у новорожденных детей:
• Нарушение синтеза и экскреции сурфактанта альвеолоцитами 2-го типа, связанное с
функциональной и структурной незрелостью легочной ткани;
• Врожденный качественный дефект структуры сурфактанта (крайне редко).
4.
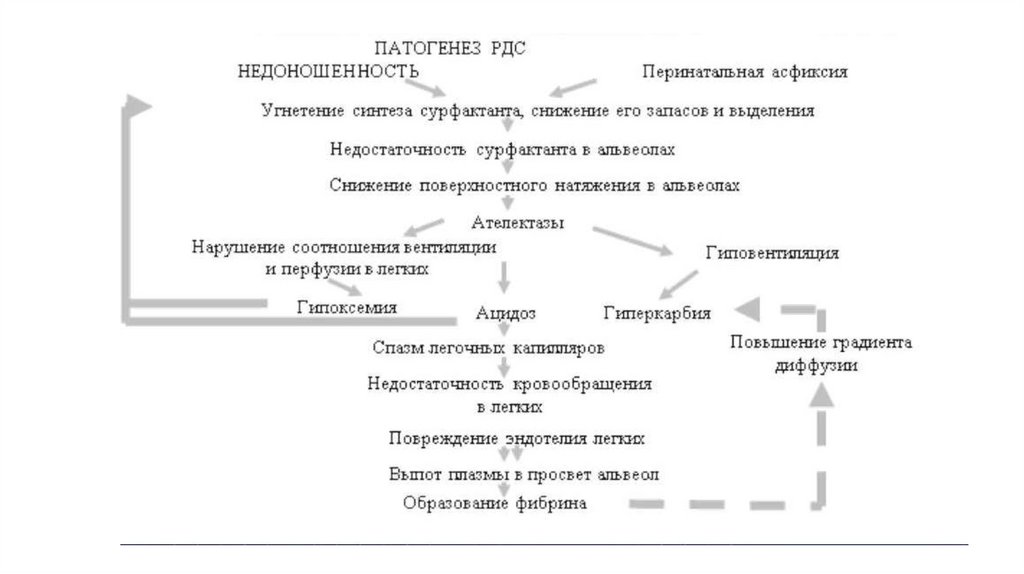
ПатогенезКлючевое звено патогенеза РДС - дефицит сурфактанта, возникающий вследствие
структурно-функциональной незрелости легких.
При дефиците (или сниженной активности) сурфактанта повышается проницаемость
альвеолярных и капиллярных мембран, развиваются застой крови в капиллярах,
диффузный интерстициальный отек и перерастяжение лимфатических сосудов;
происходит спадение альвеол и формирование ателектазов. Вследствие этого
уменьшаются функциональная остаточная емкость, дыхательный объем и жизненная
емкость легких. Как следствие, увеличивается работа дыхания, происходит
внутрилегочное шунтирование крови, нарастает гиповентиляция легких. Этот процесс
приводит к развитию гипоксемии, гиперкапнии и ацидоза.
На фоне прогрессирующей дыхательной недостаточности возникают нарушения
функции сердечно-сосудистой системы: вторичная легочная гипертензия с право-левым
шунтом крови через функционирующие фетальные коммуникации; транзиторная
дисфункция миокарда правого и/или левого желудочков, системная гипотензия.
5.
6.
Клиническая картинаОдышка, возникающая в первые минуты – первые часы жизни;
Экспираторные
шумы
(«стонущее
дыхание»),
обусловленные
развитием
компенсаторного спазма голосовой щели на выдохе;
Западение грудной клетки на вдохе (втягивание мечевидного отростка грудины,
подложечной области, межреберий, надключичных ямок) с одновременным
возникновением напряжения крыльев носа, раздувания щек (дыхание «трубача»);
парадоксальное дыхание (западение передней брюшной стенки на вдохе), пена у рта (у
половины больных), отек кистей и стоп. Типична плоская грудная клетка (в виде
«спичечного коробка»)
Цианоз при дыхании воздухом;
Ослабление дыхания в легких, крепитирующие хрипы при аускультации;
Нарастающая потребность в дополнительной оксигенации после рождения.
7.
Клиническая оценка тяжести дыхательных расстройствКлиническая
оценка
степени
тяжести
дыхательных нарушений проводится по шкале
Сильверман (Silverman) у недоношенных и по
шкале
Доунс
(Downes)
у
доношенных
новорожденных не столько с диагностической
целью, сколько для оценки эффективности
проводимой респираторной терапии или в
качестве показания для ее начала.
10 баллов – крайне тяжелый СДР
6-9 баллов – тяжелый
5 баллов – средней тяжести
менее 5 баллов – начинающийся СДР
8.
9.
Степени тяжести РДС• 1 СТЕПЕНЬ – наблюдается у более зрелых детей с состоянием средней тяжести при рождении.
Клинические признаки появляются в первые часы жизни. Признаки дыхательной недостаточности
скрытые, появляются при функциональной нагрузке: кормлении, перемене положения тела,
проведении манипуляций. ЧД не более 72 в минуту. Газовый состав крови соответствует возрасту. В
течение 3-4 дней состояние ребенка быстро улучшается. Прогноз благоприятный.
• 2 СТЕПЕНЬ (средне-тяжелая) – состояние при рождении тяжелое, около 50% детей нуждаются в
проведении реанимационных мероприятий. Первые признаки заболевания появляются сразу после
рождения или через 1-2 часа. Длительность СДР от 5 до 10 суток. С 7-8 дня дети начинают дышать без
дотации кислорода. Нередко присоединяются инфекционно-воспалительные заболевания.
• 3 СТЕПЕНЬ (тяжелая форма) – развивается у детей с наиболее значительной степенью незрелости
(до 34 недели гестации, родившихся в крайне тяжелом состоянии). Первые признаки с момента
рождения: резкое угнетение ЦНС (гипоксия, арефлексия, стон, нарушение терморегуляции), большой
диапазон частоты дыхания (от 60 до 140 в минуту), повторные приступы апное, асфиксии и цианоза,
сероватый оттенок кожи. Дыхание ослабленное, хрипов в первые сутки мало, укорочение
перкуторного звука, местами с тимпаническим оттенком. Резкая тахи- или брадикардия, глухость
сердечных тонов, гипоксия миокарда на ЭКГ.
9
10.
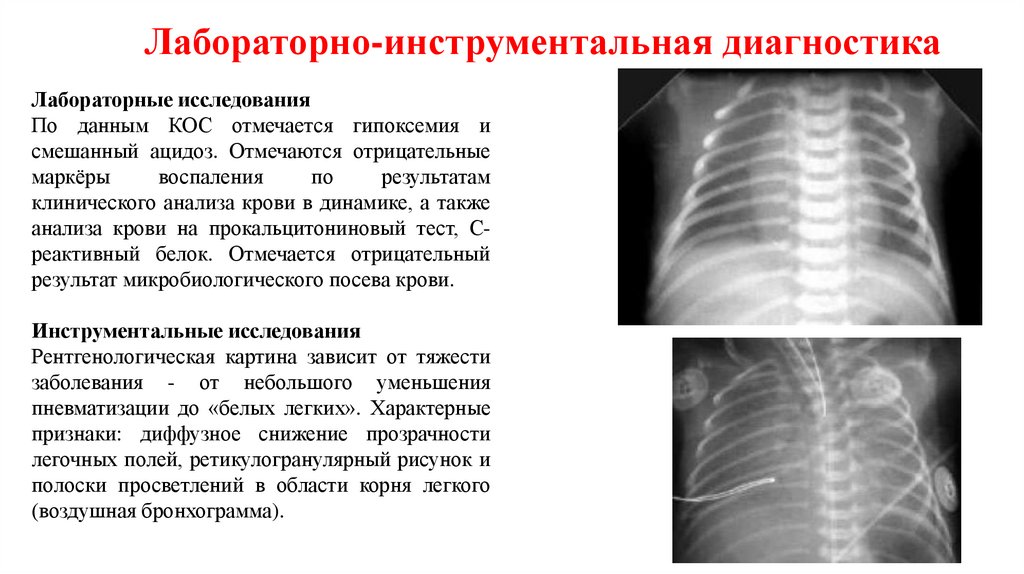
Лабораторно-инструментальная диагностикаЛабораторные исследования
По данным КОС отмечается гипоксемия и
смешанный ацидоз. Отмечаются отрицательные
маркёры
воспаления
по
результатам
клинического анализа крови в динамике, а также
анализа крови на прокальцитониновый тест, Среактивный белок. Отмечается отрицательный
результат микробиологического посева крови.
Инструментальные исследования
Рентгенологическая картина зависит от тяжести
заболевания - от небольшого уменьшения
пневматизации до «белых легких». Характерные
признаки: диффузное снижение прозрачности
легочных полей, ретикулогранулярный рисунок и
полоски просветлений в области корня легкого
(воздушная бронхограмма).
11.
ЛечениеЦель терапии в реанимационном отделении поддержание легочного газообмена, восстановление
альвеолярного объема и создание условий для
внеутробного созревания ребенка.
Респираторная терапия
Задачи респираторной терапии у новорожденных с РДС:
поддержание артериального РaО2 на уровне 50-70 мм
рт.ст. (SpO2 - 91-95%), раСО2 - 45-60 мм рт.ст., рН 7,257,4.
Показания к поддержке спонтанного дыхания с
помощью назального CPAP у новорожденных с РДС
следующие.
• Профилактически в родильном зале у недоношенных
детей с гестационным возрастом 27-32 нед.
• При оценке по шкале Сильвермана/Доунс более 2
баллов у детей старше 32 нед с самостоятельным
дыханием.
К противопоказаниям относят шок, судороги, легочное
кровотечение, синдром утечки воздуха.
12.
Неинвазивная ИВЛНеинвазивная назальная ИВЛ имеет преимущество перед СРАР в качестве стартовой
респираторной терапии у детей с экстремально низкой массой тела.
Показания
• В качестве стартовой респираторная терапия после профилактического введения
сурфактанта без интубации.
• В качестве респираторной терапии у недоношенных после экстубации (в том числе и
после метода INSURE).
• Апноэ, резистентные к терапии СРАР и кофеином.
• Нарастание дыхательных нарушений более 3 баллов по шкале Сильвермана и/или
возрастание потребности в FiO2 >0,4 у детей на СРАР.
Противопоказания
• Шок, судороги, легочное кровотечение, синдром утечки воздуха, срок гестации более
35 нед.
13.
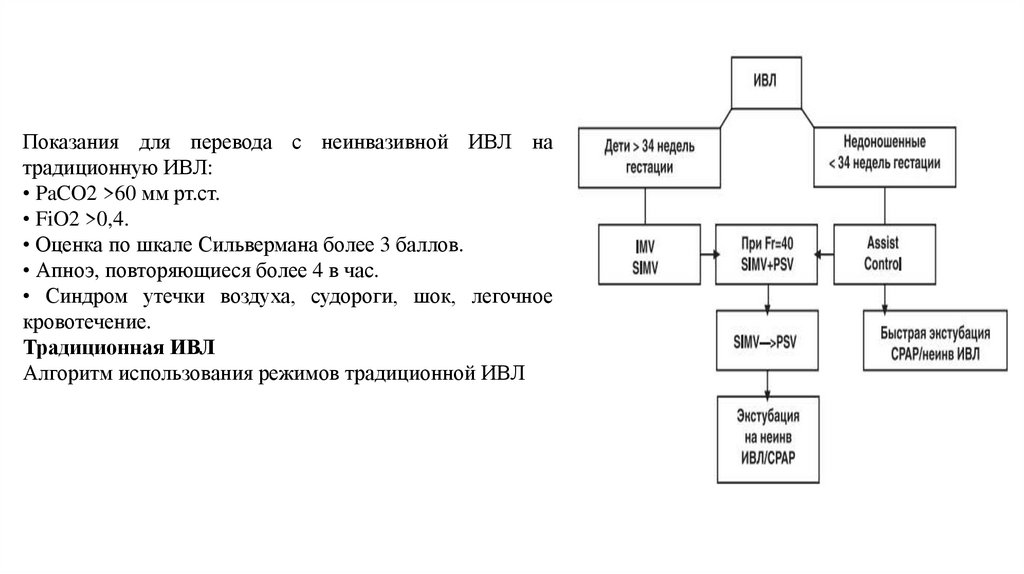
Показания для перевода с неинвазивной ИВЛ натрадиционную ИВЛ:
• PaCO2 >60 мм рт.ст.
• FiO2 >0,4.
• Оценка по шкале Сильвермана более 3 баллов.
• Апноэ, повторяющиеся более 4 в час.
• Синдром утечки воздуха, судороги, шок, легочное
кровотечение.
Традиционная ИВЛ
Алгоритм использования режимов традиционной ИВЛ
14.
Инфузионная терапияНачало через 30-40 мин после рождения (коррекция нарушений гемодинамики, питание)
1-е сутки – 60-80 мл/кг 5-10% глюкоза,
Объем и характер инфузионной терапии определяется:
ОЦК, интенсивностью мозгового кровотока;
диурезом;
динамикой массы тела;
состоянием ССС, периферической циркуляцией;
КОС, ионограммой крови;
условиями выхаживания
15.
Сурфактантная терапияПоказания к введению сурфактанта с профилактической целью:
детям, родившимся ранее 27 недели гестации
родившимся на 27-29 неделе гестации, если женщине не проводилась антенатальная
профилактика стероидными препаратами
детям, родившимся на 30-31 неделе гестации, если в родовом зале потребовалась интубация
трахеи для ИВЛ в связи с неэффективным самостоятельным дыханием
Препарат в разовой дозе (200 мг/кг) вводят в первые 15 мин после рождения ребенка,
вторую дозу препарата вводят через 6-12 ч. при необходимости.
Применение сурфактанта с лечебной целью:
Введение сурфактанта недоношенным новорожденным на СРАР следует осуществлять при
первых признаках неэффективности СРАР - возрастании оценки по шкале Сильвермана
более 3 баллов, увеличении концентрации кислорода во вдыхаемой газовой смеси более 3540%.
16.
Введение сурфактанта следует осуществлять быстро, болюсно. Введение препаратаможет проводиться через катетер, обрезанный таким образом, чтобы конец катетера не
выходил за пределы интубационной трубки, или с помощью специальной
двухпросветной интубационной трубки. Голова новорожденного должна располагаться
при введении сурфактанта по средней линии.
Куросурф - готовая суспензия для эндотрахеального введения. Рекомендуемая начальная
дозировка не менее 200 мг/кг. Данная дозировка является более эффективной, чем 100
мг/кг, и приводит к наилучшим результатам лечения недоношенных с РДС. Повторная
дозировка Куросурфа составляет не менее 100 мг/кг.
Альвеофакт - лиофилизат для приготовления суспензии для эндотрахеального
введения. Рекомендуемая производителем дозировка препарата 50 мг/кг.
17.
В первые часы после введения необходимо постоянно контролировать газовый составкрови, показатели вентиляции и легочной механики, чтобы своевременно уменьшить
PIP и FiO2.
При проведении нереспираторной терапии РДС ребенок должен быть уложен в
«гнездо» и помещен в кювез или открытую реанимационную систему. Положение на
боку или животе предпочтительнее, чем на спине.
Обязателен мониторный контроль основных функций (АД, ЧСС, ЧДД, температура
тела, SpO2).
В начальном периоде стабилизации лучше соблюдать тактику «минимальных
прикосновений». Важно поддерживать нейтральный температурный режим и
уменьшить потери жидкости через кожу.
Антибактериальную терапию назначают всем детям с РДС. Посев крови проводят до
назначения антибиотиков. Препаратами первого ряда могут быть ампициллин и
гентамицин.
18.
ПрофилактикаДля профилактики заболевания у новорожденных всем беременным со
сроком 24-34 нед при угрозе преждевременных родов рекомендуют
назначать один курс глюкокортикоидов в течение 7 дней. Повторные курсы
дексаметазона
увеличивают
риск
развития
перивентрикулярной
лейкомаляции (ПВЛ) и тяжелых нервно-психических нарушений.
В качестве альтернативных могут использоваться две схемы пренатальной
профилактики РДС:
• бетаметазон - 12 мг внутримышечно, через 24 ч, всего 2 дозы на курс;
• дексаметазон - 6 мг, внутримышечно, через 12 ч, всего 4 дозы на курс.
19.
Список литературы1. Володин, Н. Н. Неонатология : национальное руководство : краткое издание / под ред.
Н. Н. Володина. - Москва : ГЭОТАР-Медиа, 2019. - 896 с. - ISBN 978-5-9704-4877-9. Текст : электронный // ЭБС "Консультант студента"
2. Шабалов, Н. П. Неонатология : в 2 т. Т. 1. : учебное пособие / Н. П. Шабалов и др. - 7е изд. , перераб. и доп. - Москва : ГЭОТАР-Медиа, 2020. - 720 с. - ISBN 978-5-97045770-2. - Текст : электронный // ЭБС "Консультант студента"
3. КЛИНИЧЕСКИЕ РЕКОМЕНДАЦИИ под редакцией академика РАН Н.Н. Володина
«Ведение новорожденных с респираторным дистресс-синдромом»

















 medicine
medicine








