Similar presentations:
Валентность химического элемента. Определение валентности по химической формуле
1.
"Валентность химическогоэлемента.
Определение валентности по
химической формуле".
2. Пояснительная к дистанционному уроку.
• 1. Изучите презентацию• 2 Изучите параграф 16
• 3. Сделайте конспект по презентации
• 4 Выполните задания из презентации
• 5 Выполните упр. 2-5 и тестовые задания на
стр 58
3.
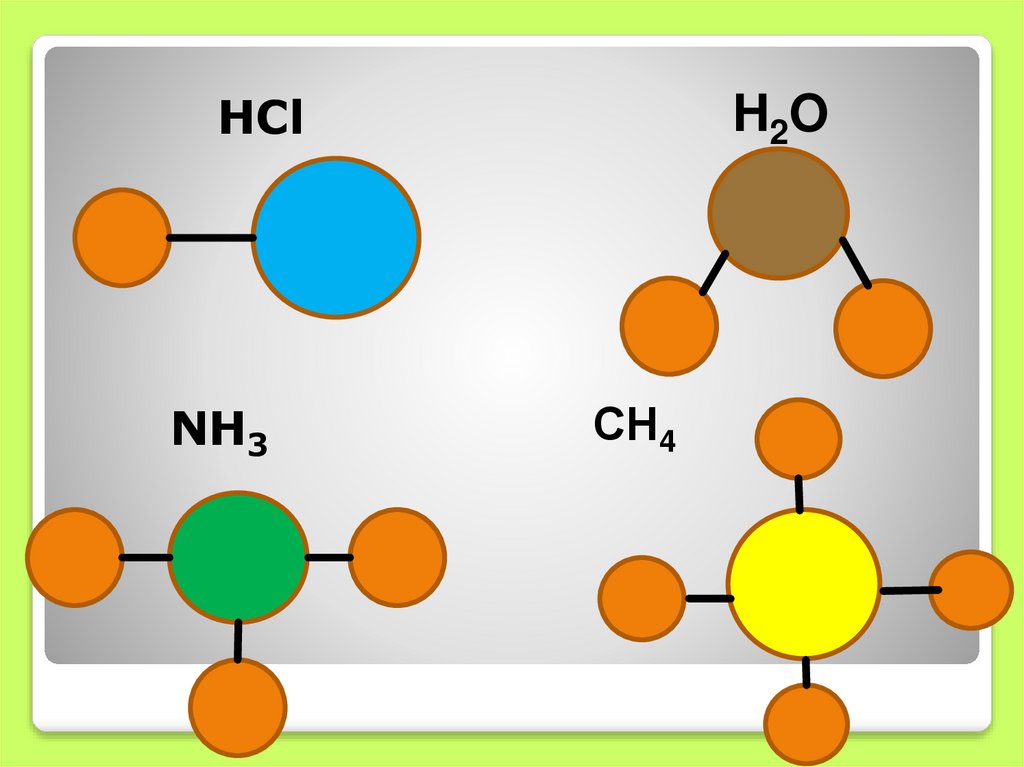
Задание(устно): сравнитекачественный и
количественный состав в
молекулах:
HCl , H2O, NH3, CH4.
4.
ВАЛЕНТНОСТЬ(от латинского valentia – «сила»).
- это способность атомов
соединяться друг с другом.
5.
Валентность – это свойство атомовудерживать определённое число других
атомов в соединении.
Валентность обозначается римскими цифрами.
Валентность атома водорода принята за
единицу, а у кислорода – II.
I
II
II I
HCl H2O
III I
H3N
IV
H4C
6.
НСlNН3
H2O
СН4
7.
« в бинарном соединении суммарнаявалентность одного элемента равна
суммарной валентности другого»
IV
II
С
О2
4∙1 = 2∙2
4=4
8.
Алгоритм определения валентностиПример
1. Запишите формулу вещества: H2S
2. Обозначьте известную валентность элемента
I
H2 S
3. Найдите число единиц валентности атомов известного элемента, умножив
валентность элемента на количество его атомов
2
I
H2 S
4. Поделите число единиц валентности атомов на количество атомов другого
элемента. Полученный ответ и является искомой валентностью
2
I II
H2 S
5. Сделайте проверку, то есть подсчитайте число единиц валентностей
каждого элемента
I II
H2 S
(2=2)
9.
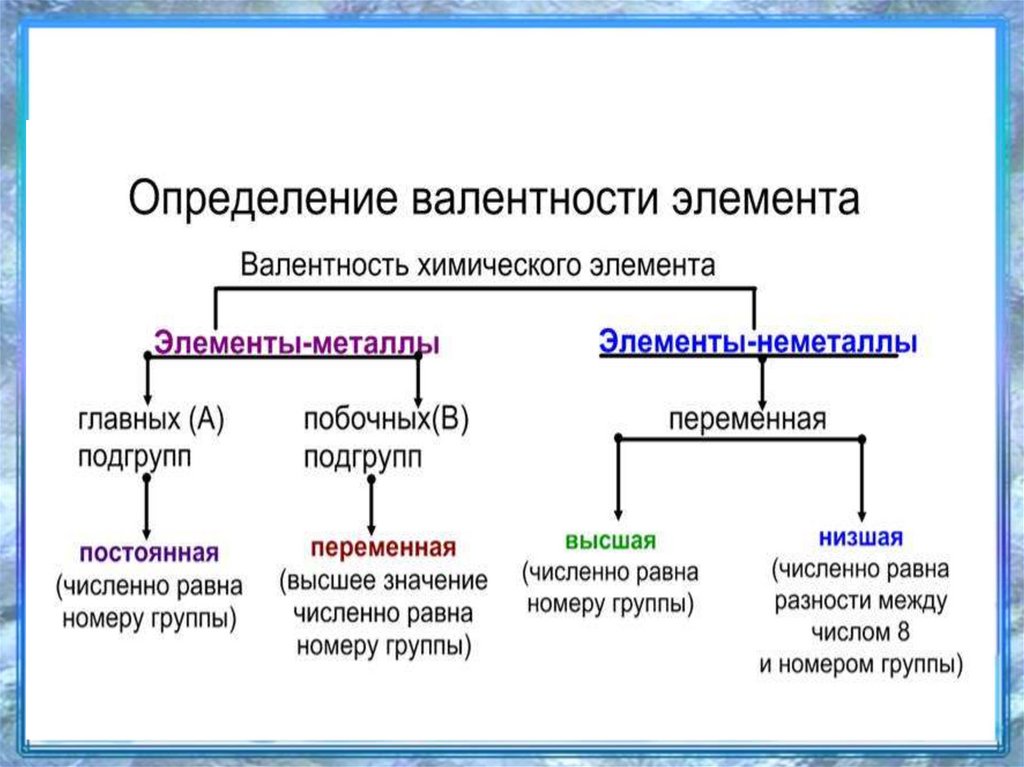
Валентность определяемая по номеругруппы –высшая
I гр. – валентность I (Na, K, Li)
II группа – валентность II (Ca, Mg,
Ba)
III группа – валентность III (Al, B)
10.
Валентность, найденнуюпо разности
8 — N группы
назовём низшей
11.
Определите низшую валентность серыи валентности элементов с ней
связанных, в ряду соединений:
I II IVII
Na2 S, C S2,
III II II II
Al2 S3, Fe S
12.
ЗАПОМНИ!!!Знак элемента с низшей
валентностью ставят на второе
место.
VI II
I II
S О3 ,
Nа2S .
13.
14.
15.
16. ВЫВОДЫ
• Валентность- свойство атомов присоединятьопределенное число других атомов
• В зависимости от строения атомов элементы
проявляют постоянную или переменную валентность
• Металлы главных подгрупп проявляют постоянную
валентность, равную номеру группы
• Валентность кислорода и водорода постоянна.
• В случаях переменной валентности высшее ее
значение равно номеру группы
• Для определения значения низшей валентности
элементов-неметаллов следует из числа 8 вычесть
номер группы
17.
Задание 1 сделать письменно: определитьвалентность элементов в веществах(переписать
формулы и проставить валентность)
SiH4, CrO3, H2S, CO2, CO, SO3, SO2, Fe2O3, FeO, HCl,
HBr, Cl2O5, Cl2O7, РН3, K2O, Al2O3, P2O5, NO2, N2O5,
Cr2O3, SiO2, B2O3, Mn2O7, MnO, CuO, N2O3.
18.
Задание 2 (сделать письменно):№1 Определите валентность атомов химических
элементов по формулам соединений: NH3,
Au2O3, SiH4, CuO.
• №2 Из приведённого ряда выпишите только те
формулы, в которых атомы металлов
двухвалентны: MnO, Fe2O3 , CrO3, CuO, K2O,
СаH2.
• №3 Найдите закономерность в
последовательности формул: N2O, NO, N2O3 и
проставьте валентности над каждым элементом.
19.
задание:§ 16, стр. 55-58, упр.2-5 на
стр. 58.
Тест стр.58

















 chemistry
chemistry








