Similar presentations:
Биофизика мембранных процессов. Мембранный транспорт
1.
ФГОУ ВПО ЮФУ каф. биохимии и микробиологии2. Виды мембранного транспорта (МТ)
Мембранный транспорт (МТ)1.Пассивный транспорт
нейтральная
1.1.Простая диффузия
ионная
1.1.1. Осмос
1.1.2. Через поры
1.1.3. Через липидный бислой
1.2.Фильтрация
1.3. Облегченная диффузия
2.Активный транспорт
2.1.Первичный активный транспорт
2.2. Вторичный активный транспорт
ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
2
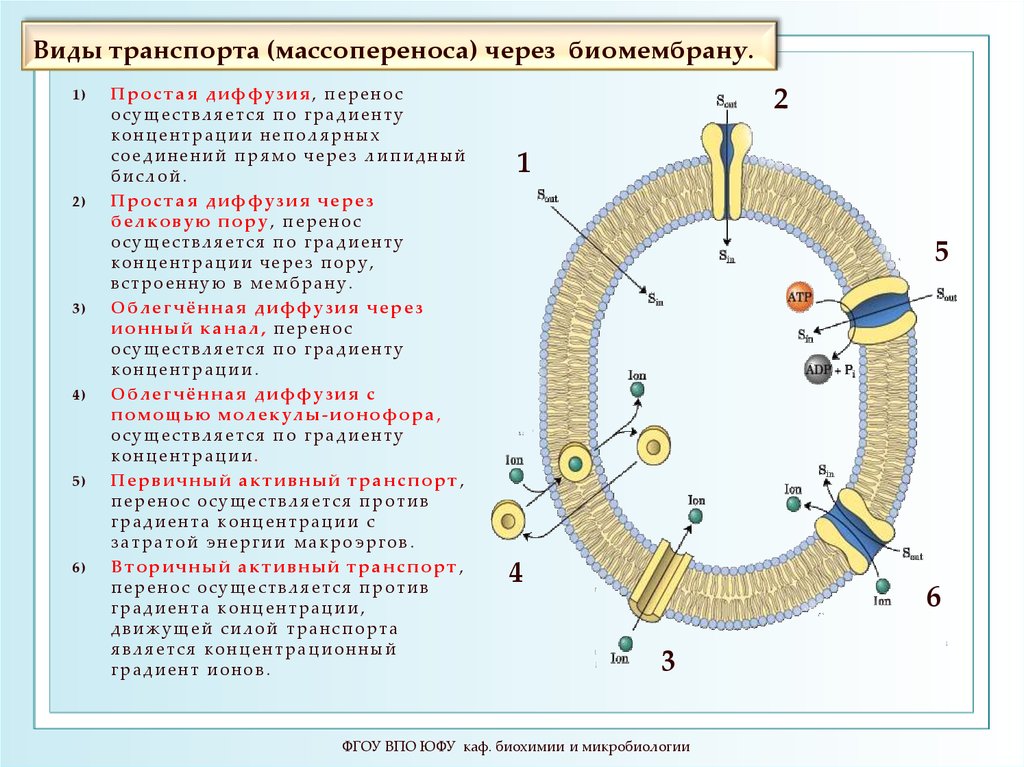
3. Виды транспорта (массопереноса) через биомембрану.
1)2)
3)
4)
5)
6)
Простая диффузия, перенос
осуществляется по градиенту
концентрации неполярных
соединений прямо через липидный
бислой.
Простая диффузия через
белковую пору, перенос
осуществляется по градиенту
концентрации через пору,
встроенную в мембрану.
Облегчённая диффузия через
ионный канал, перенос
осуществляется по градиенту
концентрации.
Облегчённая диффузия с
помощью молекулы-ионофора,
осуществляется по градиенту
концентрации.
Первичный активный транспорт ,
перенос осуществляется против
градиента концентрации с
затратой энергии макроэргов.
Вторичный активный транспорт ,
перенос осуществляется против
градиента концентрации,
движущей силой транспорта
является концентрационный
градиент ионов.
2
1
5
4
6
3
ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
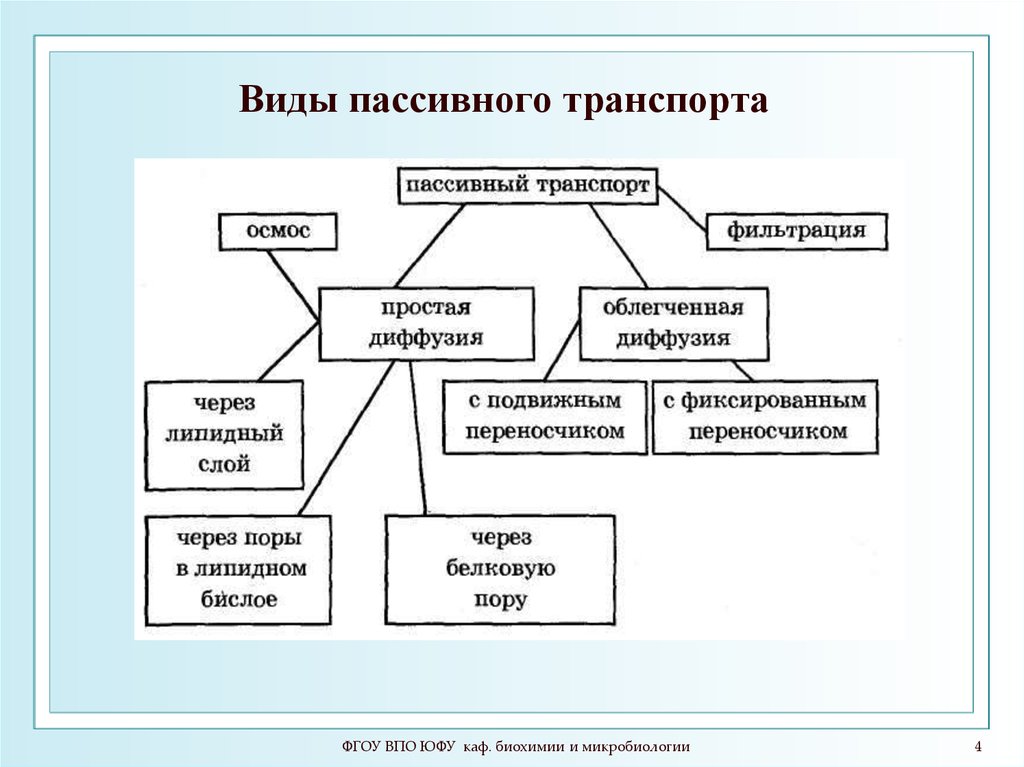
4. Виды пассивного транспорта
ФГОУ ВПО ЮФУ каф. биохимии и микробиологии4
5. Энергия пассивного транспорта создается различными градиентами:
концентрационным
осмотическим
электрическим
градиентом гидростатического давления
жидкости
электрохимическим (совокупность
концентрационного и электрического)
6. Виды пассивного транспорта
1.2.
3.
4.
Диффузия
Осмос
Фильтрация
Облегченная диффузия
ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
6
7.
Диффузия –это самопроизвольный процесс
проникновения вещества из
области большей в область
меньшей его концентрации в
результате теплового
хаотического движения молекул.
8. Простая диффузия описывается уравнением Фика : скорость диффузии dm/dt прямо пропорциональна градиенту концентрации dc/dx, площади S, через кот
Простаядиффузия
описывается
уравнением Фика : скорость диффузии
dm/dt
прямо
пропорциональна
градиенту
концентрации
dc/dx,
площади
S,
через
которую
осуществляется
диффузия,
и
коэффициенту диффузии D.
9.
dmdc
= DS
dt
dx
1. Скорость диффузии - это количество вещества,
диффундирующего в единицу времени через
данную площадь.
2. Градиент концентрации - это изменение
концентрации вещества, приходящееся на
единицу длины, в направлении диффузии.
3. Знак «-» показывает, что диффузия идет из
области большей в область меньшей
концентрации.
4. D - коэффициент диффузии.
10. Осмос - движение молекулы воды через полупроницаемые мембраны из места с меньшей концентрацией растворенного вещества в места с большей к
Осмос - движение молекулы воды черезполупроницаемые мембраны из места с
меньшей концентрацией растворенного
вещества в места с большей концентрацией.
Осмос - это простая диффузия воды из мест с ее
большей концентрацией в места с меньшей
концентрацией воды. Это явление
обуславливает гемолиз эритроцитов в
гипотонических растворах.
11. Уравнение, описывающее осмотический перенос воды.
dmk S P1 P2
dt
где
dm
dt
- количество воды, проходящей через
мембрану площадью S за единицу времени;
Р1 и Р2 – осмотическое давление растворов по обе
стороны мембраны;
k – коэффициент проницаемости.
12. Фильтрация – это движение раствора через поры в мембране под действием градиента гидростатического давления. Явление фильтрации играет в
Фильтрация –это движение раствора через поры в
мембране под действием градиента
гидростатического давления.
Явление фильтрации играет важную
роль в процессе переноса воды через
стенки кровеносных сосудов.
13. Фильтрация – движение жидкости через поры какой-либо перегородки под действием гидростатического давления.
dV
dt
πr
P
P
1
2
4
8ηl
где
r – радиус поры
l – длина поры
η – вязкость жидкости
Р1-Р2 – разность давления
между началом и концом
поры
V – объем фильтрованной
жидкости
14. Уравнение Коллендера-Бернульда описывает транспорт веществ через липидный бислой
dmP S C1 C 2
dt
где
С1 и С2 – концентрации
вещества по разные стороны
мембраны
Р – коэффициент проницаемости
мембраны
S – площадь, через которую
идет перенос
Р = DK/L (С1 - С2)
D – коэффициент диффузии
К – коэффициент
распределения
вещества между мембраной и
средой
L – толщина мембраны
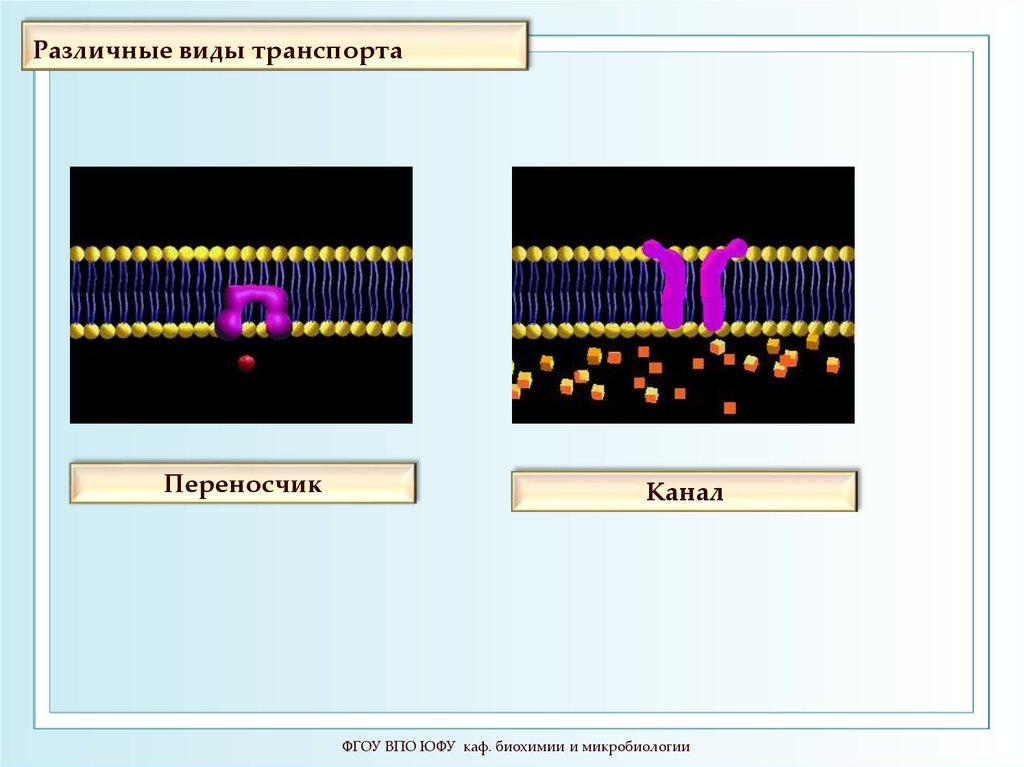
15. Различные виды транспорта
ПереносчикКанал
ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
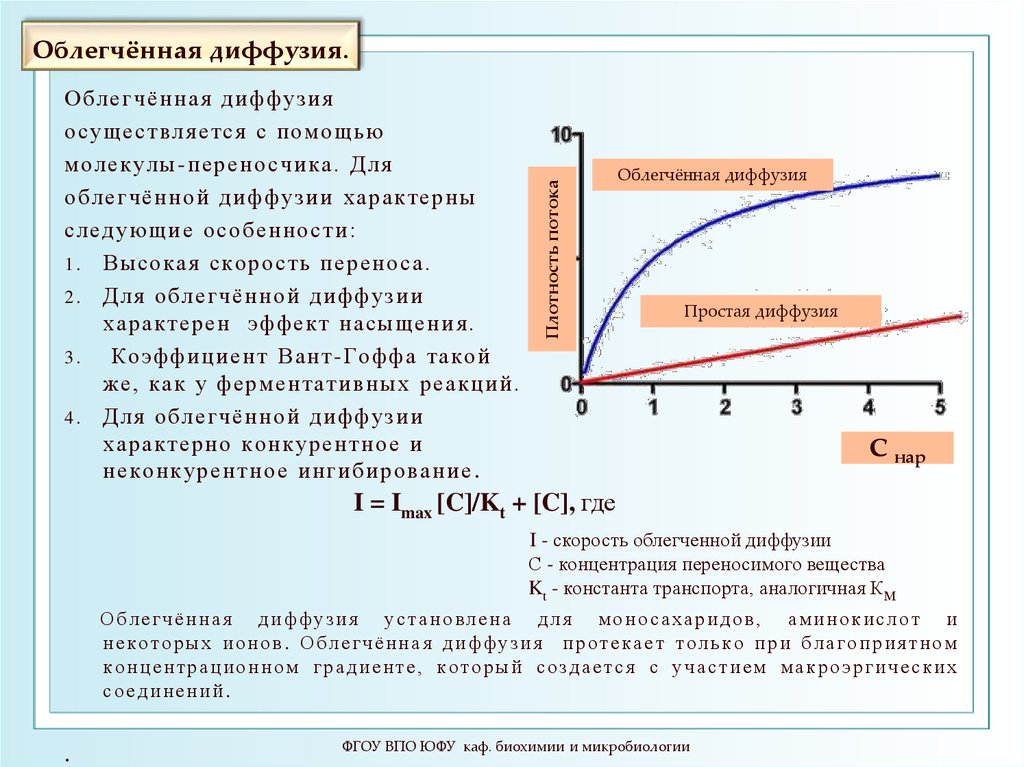
16. Облегчённая диффузия.
Облегчённая диффузияосуществл яется с помощью
молекулы -пер ено счика. Для
облегчённо й диффуз ии характер ны
следующи е особенно сти :
1 . Высокая скорость перено са.
2 . Для облегчённо й диффуз ии
характерен эффект насыщени я.
3.
Коэффици ент Вант-Го ффа такой
же, как у ферментативных реакций.
4 . Для облегчённо й диффуз ии
характерно конкурентно е и
неконкур ентно е ингибирован ие .
Плотность потока
Облегчённая диффузия.
Облегчённая диффузия
Простая диффузия
С нар
I = Imax [C]/Kt + [C], где
I - скорость облегченной диффузии
С - концентрация переносимого вещества
Kt - константа транспорта, аналогичная КМ
Об ле г ч ё н н а я д и ф ф узи я ус т а н о вл е н а д л я м о н о с а х а р и д ов , а м и н о к и с ло т и
н е к о т о р ы х и о н ов . Об ле г ч ё н н а я д и ф ф узи я п р о т е к а е т т о л ьк о п р и б ла г о п р и я тн ом
к о н ц е н тр а ц и о н н о м г р а д и е н т е , к о то р ы й с о зд а е тс я с уч а с ти е м м а к р о эр г и ч е с к и х
соединений.
.
ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
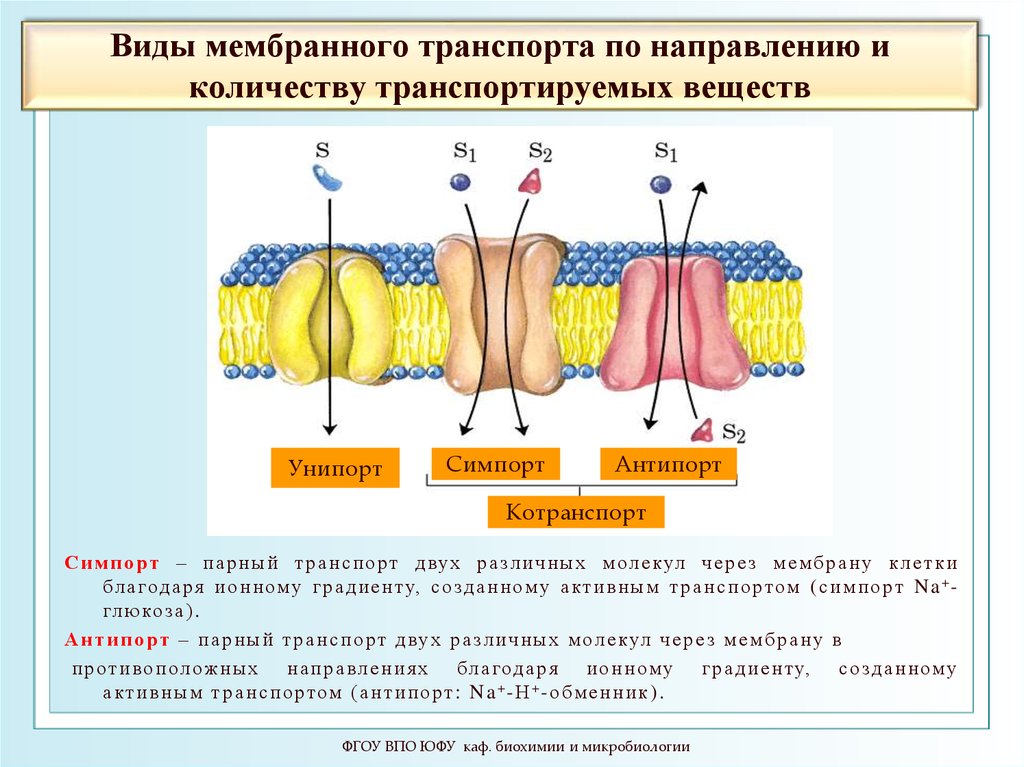
17. Виды мембранного транспорта по направлению и количеству транспортируемых веществ
УнипортСимпорт
Антипорт
Котранспорт
С и м по рт – п а р н ы й т р а н с п о рт д вух р а з ли ч н ых м ол е кул ч е р е з м е м б р а н у к ле тк и
бла год а р я и о н н ом у г р а д и е н ту, с о зд а н н ом у а кт и в н ы м т р а н с п о ртом ( с и мп о рт N a + гл ю ко за ) .
А н т и п о рт – п а р н ы й т р а н с п о рт д вух р а з л и ч н ы х м ол е кул ч е р е з м е м б р а н у в
п р оти во п олож н ы х н ап р а вл е н и я х бл а год а р я и о н н ом у г р а д и е н ту, с о зд а н н ом у
а кт и в н ы м т р а н с п о ртом ( а н т и п о рт : N a + - Н + - о бм е н н и к ) .
ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
18. Активный транспорт. Виды активного транспорта.
П е р в и ч н ый а к т и в н ы й т р а н с п о рт – т р а н с м е м б р а н н ы й п е р е н о с в е щ е с т в п р от и вг р а д и е н т а ко н ц е н т р а ц и и с з ат р ато й э н е р г и и м а к р о э р г и ч е с к и х с о ед и н е н и й .
Первичный активный
транспорт
Вторичный активный
транспорт
В т о р и ч н ый а к т и в н ый т р а н с п о р т – т р а н с м е м б р а н н ый п е р е н о с в е щ е с т ва п р о т и в
э л е к т р о х и м и ч е с к о г о г р а д и е н т а , с о п р я ж е н н ы й с п о т о к о м д р у г о г о в е щ е с т ва ,
которое первоначально было закачано с помощью первичного активного
т р а н с п о р та . И о н н ы е г р а д и е н т ы с н а б ж а ют э н е р г и е й в т о р и ч н ый а к т и в н ый
т р а н с п о р т.
ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
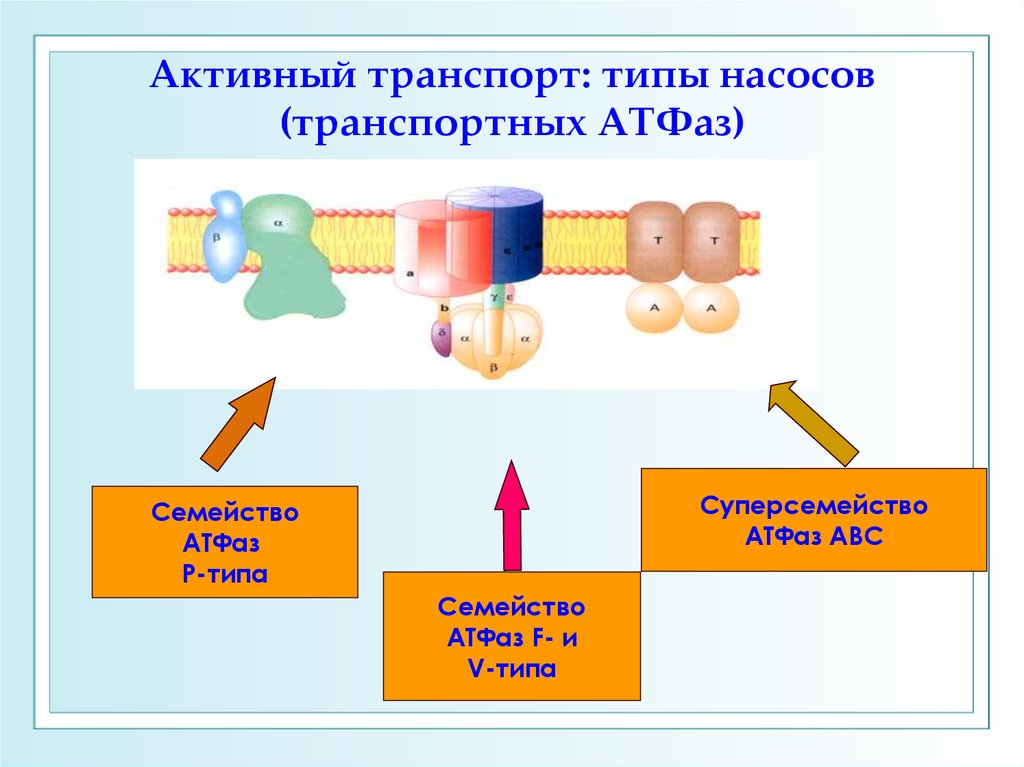
19. Активный транспорт: типы насосов (транспортных АТФаз)
СуперсемействоАТФаз АВС
Семейство
АТФаз
Р-типа
Семейство
АТФаз F- и
V-типа
20.
Типы насосов (транспортных АТФ-аз)1. АТФ-азы Р-типа – переносчики ионов, которые обратимо
фосфорилируются с помощью АТФ по аспартату, что инициирует
конформационный переход при транспорте иона (Na+,K+- АТФ-аза,
Са+- АТФ-аза).
2. АТФ-азы F- типа – это обратимы АТФ-зависимые протонные насосы,
катализируют трансмембранный перенос протонов против градиента
за счет гидролиза АТФ («F- тип» происходит из определения этих
АТФ-аз как энергосопрягающих факторов) (Н-АТФ-аза/АТФ-синтаза).
3. АТФ-азы V-типа - протон-транспортирующие АТФ-азы,
обеспечивающие закисление вакуолей, лизосом, эндосом, комплекса
Гольджи (сходны с АТФ-азами F-типа).
4. АВС-транспортеры – используют АТФ для запуска активного
транспорта множества субстратов (выкачивают аминокислоты,
пептиды, белки, ионы металлов, липиды, желчные кислоты, лекарства
и др. из клетки против градиента концентрации) (Р-гликопротеин –
мультилекарственный транспортер отвечает за устойчивость опухолей
к протовоопухолевым препаратам).
ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
21.
АВС-транспортер, «выкачивающий»липофильные вещества из клетки
ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
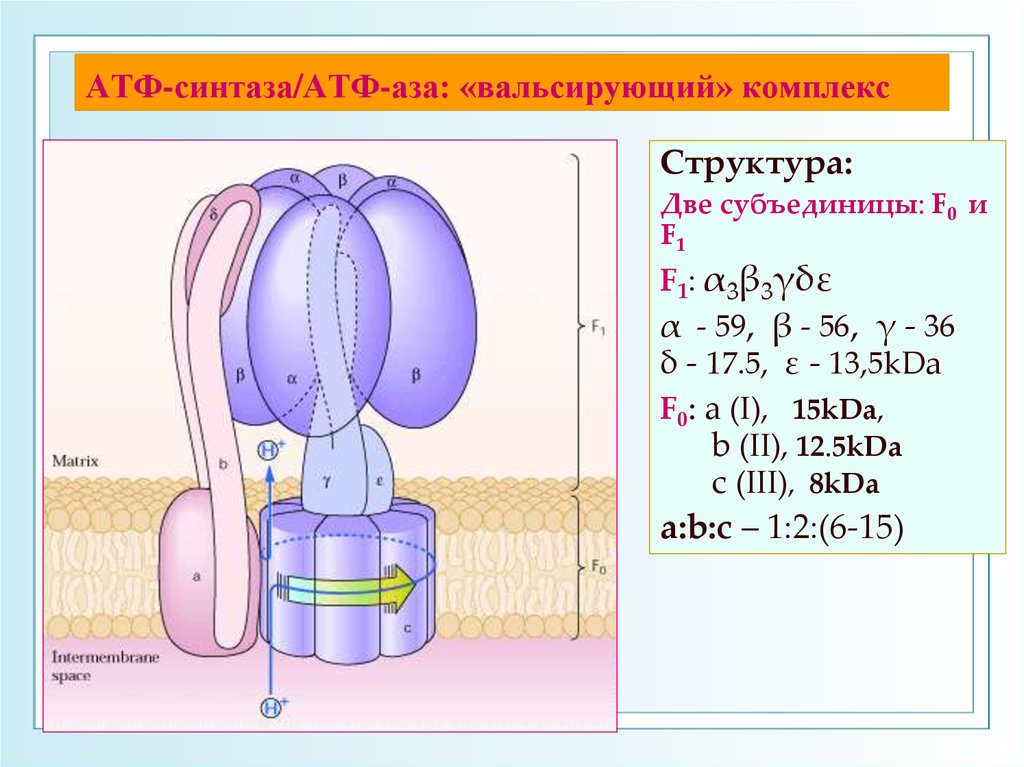
22. АТФ-синтаза/АТФ-аза: «вальсирующий» комплекс
Структура:Две субъединицы: F0 и
F1
F1: α3β3γδε
α - 59, β - 56, γ - 36
δ - 17.5, ε - 13,5kDa
F0: а (I), 15kDa,
b (II), 12.5kDa
c (III), 8kDa
а:b:с – 1:2:(6-15)
23.
Механизм действия Р-гликопротеина (P-gp)ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
23
24.
ФГОУ ВПО ЮФУ каф. биохимии и микробиологии25. Роль онкотического и гидростатического давления в транспорте воды через мембрану
ФГОУ ВПО ЮФУ каф. биохимии и микробиологии25
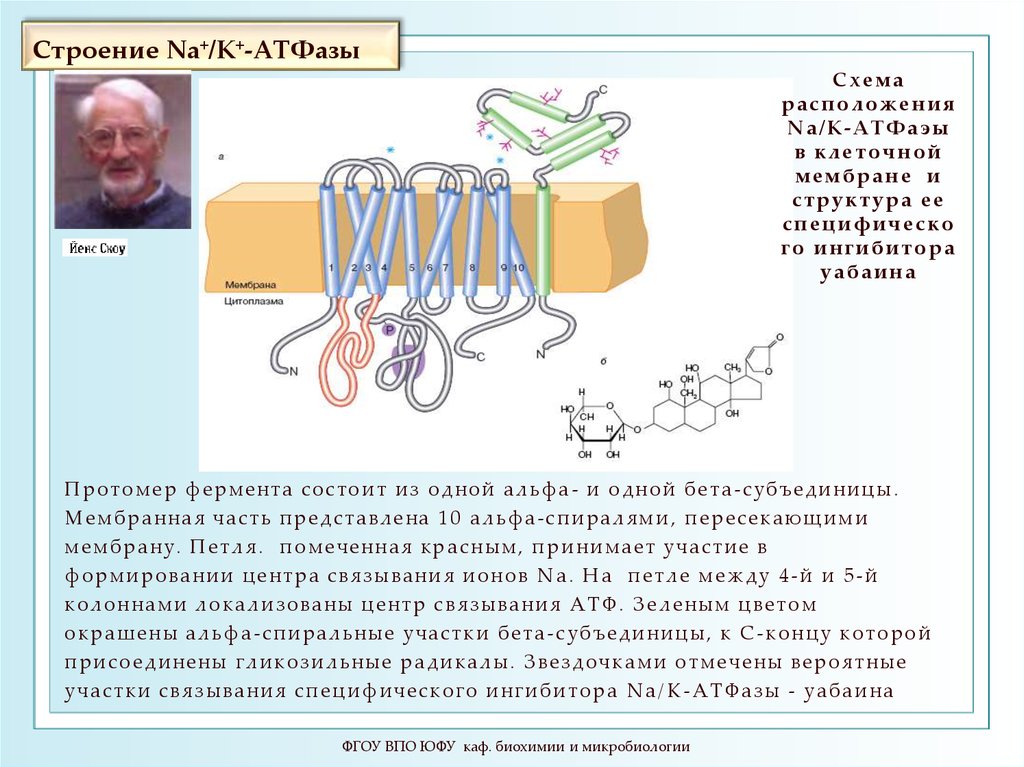
26. Строение Na+/K+-ATФазы
Схемарасположения
Na/K-АТФаэы
в клеточной
мембране и
структура ее
специфическо
го ингибитора
уабаина
П р о т о м е р ф е р м е нт а с о с т о и т и з о д н о й а л ь фа - и о д н о й б е т а - с у б ъ е д и н и цы .
М е м б р а нна я ч а с т ь п р е д с т а в ле на 1 0 а л ь фа - с пи ра ля м и , п е р е с е к а ю щ и м и
м е м б р а ну . П е т л я . п о м е ч е нн а я к p a c н ы м , п р и н и м а е т у ч а с т и е в
ф о р м и ро в а ни и ц е н т р а с в я з ы в а ни я и о н о в N а . Н а п е т л е м е ж д у 4 - й и 5 - й
к о л о н н а м и л о к а л и з о в а ны ц е н т р с в я з ы в а ни я А Т Ф . З е л е н ы м ц в е т о м
о к р а ш е н ы а л ь фа - с пи ра ль ны е у ч а с т к и б е т а - с у б ъ е д и ни цы , к С - к о н цу к о т о р о й
п р и с о е д и не ны г л и к о з и ль ны е р а д и к а лы . З в е з д о ч к а м и о т м е ч е ны в е р о я т ны е
у ч а с т к и с в я з ы ва н и я с п е ц и ф и ч е с к о г о и н г и б и то р а N a / K - А Т Ф а з ы - у а б а и н а
ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
27. Реакционный цикл Na+/K+-ATФазы
Шесть основных последовательньх реакций включают:1.) Связынание ионов натрия Е1- конформером, его взаимодействие с АТР и образование
фосфорилированного интермедиата.
2.) Окклюзия ионов натрия конформацией Е1Р.
3.) Активируемый ионом и магния переход Е1Р – Е2Р, приводящий к высвобождению ионов
Na во внешнюю среду и связывание с ионным центром K.
4.) Окклюдирование ионов K.
5.) Дефосфорилирование фермента, приводящее к высвобождению ионов калия во
внутриклеточное пространство.
6.) Переход конформации E2 в E1
ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
28. Связывание ионов Na+ и K+ в ионных центрах Na+/K+-ATФазы
а - к р и с т а лли ч е с к а я р е ш е т к а с о з д а в а е м а я 1 2к и с л о р о д ны м и а т о м а м и д и к а р б о н о в ы к
а м и но к и с ло т в к о н ф о р м а ц и и
с о о т в е т с т в у ю щ е й с в я з ы в а ни ю т р е х и о н о в
н а т р и я ( Е1 и л и д в у х и о н о в к а л и я Е 2 )
b— петля между 2-й и 3-й пептидной цепи
а л ь фа - с у б ъ е д и н и ц ы , у ч а с тв у ю щ а я в
ф о р м и ро в а ни и и о н н о г о ц е н т р а ( к р а с ны м и
т о ч к а м и у к а з а на л о к а л и з а ци я д и к а р б о но в ы к
а м и но к и с ло т ) .
В д в и г а ни е п е т л и м е ж д у к о л о н н а м и 2 и 3 п р и
к о н ф о р м а ц и о н но м п е р е х о д е ф е р м е нт а
о б е с п е ч и в а е т и з м е н е ни е д о с т у п но с ти
и о н н о г о ц е н т р а с н а р у жно й и л и в н у т р е нне й
с т о р о н ы м е м б ра н ы .
ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
29.
Все морские птицы (например, альбатрос) имеют ряд специальныхприспособлений к круглогодичной жизни на морской воде - мощные
солевые железы, через ноздри выводящие излишки соли из
организма. При активном функционировании желез с клюва птиц
регулярно стекают капли солевого секрета.
ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
30.
ФГОУ ВПО ЮФУ каф. биохимии и микробиологии31. Генерация и распространение биоэлектрических потенциалов - важнейшее физическое явление в живых клетках и тканях, которое лежит в основе:
Генерация и распространениебиоэлектрических потенциалов важнейшее физическое явление в живых
клетках и тканях, которое лежит в основе:
- возбудимости клеток,
- регуляции внутриклеточных процессов
- работы нервной системы,
- регуляции мышечного сокращения.
32. Для возникновения биопотенциалов решающее значение имеют потенциалы, обусловленные асимметричным, неравномерным распределением ионов.
33.
ДиффузионныйЭлектродный
Потенциалы
Фазовый
Мембранный
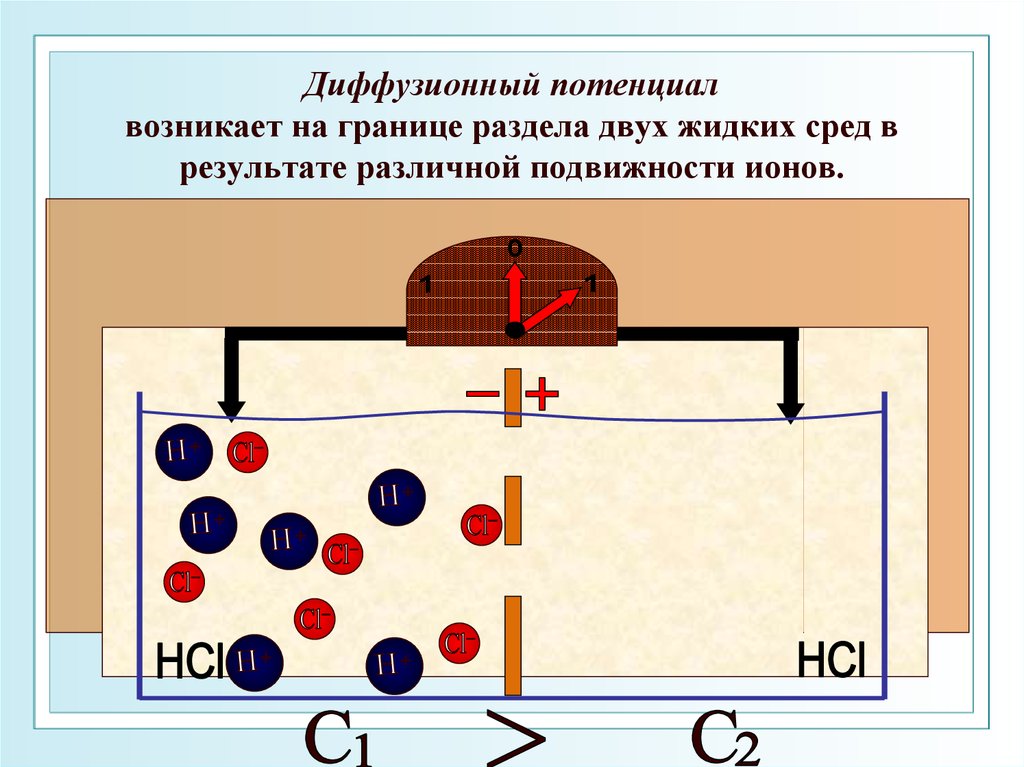
34. Диффузионный потенциал возникает на границе раздела двух жидких сред в результате различной подвижности ионов.
35. Диффузионный потенциал определяется из уравнения Гендерсона
U V RTa1
Ε
ln
U V nF
a2
Где
U – подвижность катионов
V – подвижность анионов
R – универсальная газовая постоянная
Т – абсолютная температура
n – валентность
F – число Фарадея
а1 – активность ионов в области, откуда идет диффузия
а2 – активность ионов в области, куда идет диффузия
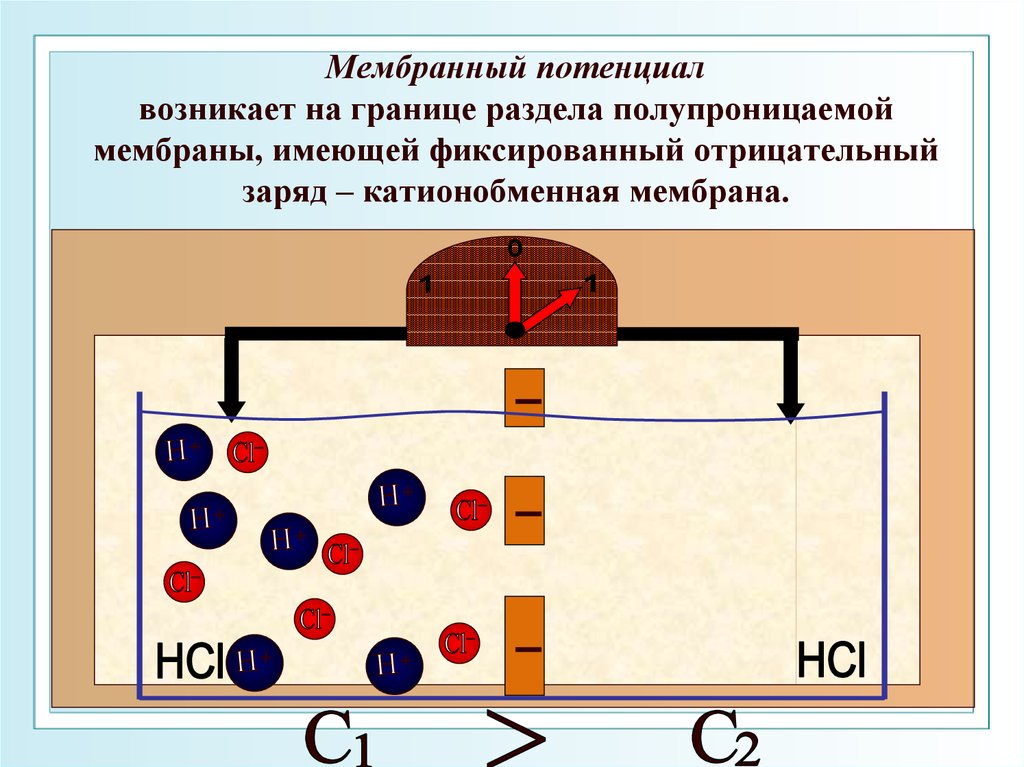
36. Мембранный потенциал возникает на границе раздела полупроницаемой мембраны, имеющей фиксированный отрицательный заряд – катионобменная
мембрана.▬
▬
▬
37. Мембранный потенциал определяют из уравнения Нернста
RTa1
Ε
ln
nF
a2
Где
R – универсальная газовая постоянная
Т – абсолютная температура
n – валентность
F – число Фарадея
а1 – активность ионов в области, откуда идет диффузия
а2 – активность ионов в области, куда идет диффузия
38. Фазовые потенциалы возникают на границе раздела двух несмешивающихся фаз.
39. Электродный потенциал возникает в результате диффузии ионов из электрода в раствор электролита.
40. В 1902 году Бернштейном была выдвинута мембранная теория биопотенциалов. В 50-60-х годах теория была развита и экспериментально доказана А. Ход
В 1902 году Бернштейном былавыдвинута мембранная теория
биопотенциалов.
В 50-60-х годах теория была
развита и экспериментально
доказана А. Ходжкиным и
А. Ф. Хаксли.
41. Сущность мембранной теории биопотенциалов
Потенциал покоя и потенциал действияявляется по своей природе мембранными
потенциалами, обусловленными
1)полупроницаемыми свойствами клеточной
мембраны и
2)неравномерным распределением ионов между
клеткой и средой, которое поддерживается
механизмами активного транспорта,
локализованными в самой мембране.
42. Мембранным потенциалом называется разность потенциалов между внутренней и наружной поверхностями мембраны.
Мембранный потенциалПотенциал покоя
Потенциал действия
43. Потенциал покоя – стационарная разность электрических потенциалов, регистрируемых между внутренней и наружной поверхностями мембраны в
Потенциал покоя – стационарнаяразность электрических потенциалов,
регистрируемых между внутренней и
наружной поверхностями мембраны в
невозбужденном состоянии.
44. Потенциал покоя.
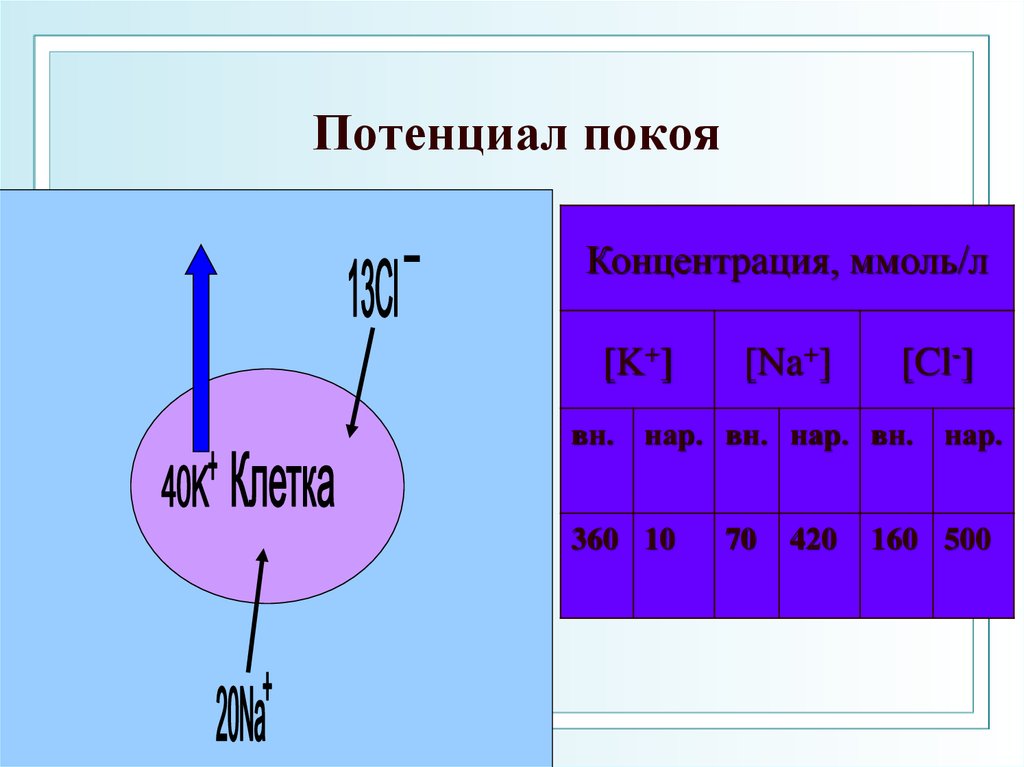
ФГОУ ВПО ЮФУ каф. биохимии и микробиологии45. Потенциал покоя
Концентрация, ммоль/л[K+]
[Na+]
[Cl-]
вн. нар. вн. нар. вн. нар.
360 10
70
420
160 500
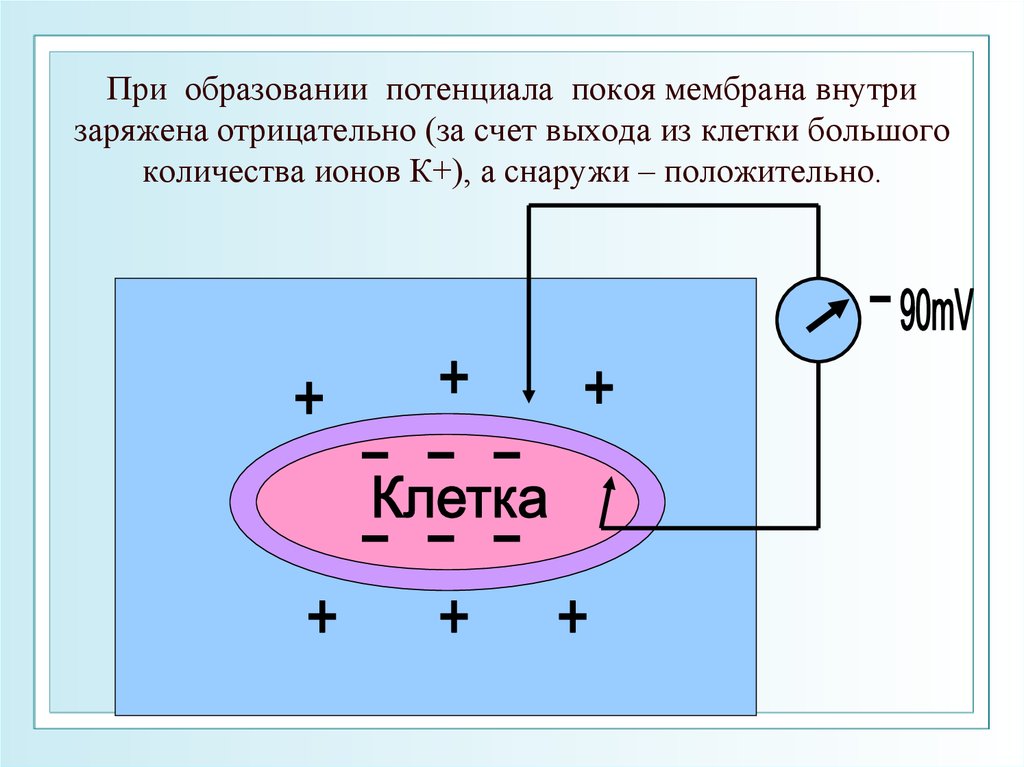
46. При образовании потенциала покоя мембрана внутри заряжена отрицательно (за счет выхода из клетки большого количества ионов К+), а снаружи
При образовании потенциала покоя мембрана внутризаряжена отрицательно (за счет выхода из клетки большого
количества ионов К+), а снаружи – положительно.
47.
Потенциал покоя. В мембране открыты калиевые ионныеканалы постоянного тока, закрыты натриевые каналы,
работает насос-обменник (Na+/K+-АТФаза).
ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
48.
Нервная клетка и потенциал действияСхема распределения зарядов по разные стороны мембраны
возбудимой клетки в спокойном состоянии (A) и при возникновении
потенциала действия - деполяризация (B).
ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
49.
Причины отрицательности мембранного потенциалапокоя:
• Покоящаяся клеточная мембрана более
проницаема для ионов К+, чем для других ионов.
Поскольку концентрация К+ внутри клетки намного
выше, чем снаружи, К+ через калиевые каналы
выходит из клетки и создает избыток отрицательного
заряда на цитоплазматической стороне клеточной
мембраны. Это основной вклад: -60 мВ
• Электорогенный Na/К- насос в мембране
покоящейся клетки остается активен и также
участвует в создании отрицательного заряда
внутренней поверхности мембраны.
Его вклад: -10 мВ. В сумме это дает -70мВ.
ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
50. Уравнение Нернста для потенциала покоя
Εп.п.K
RT вн.
ln
F
K
снар.
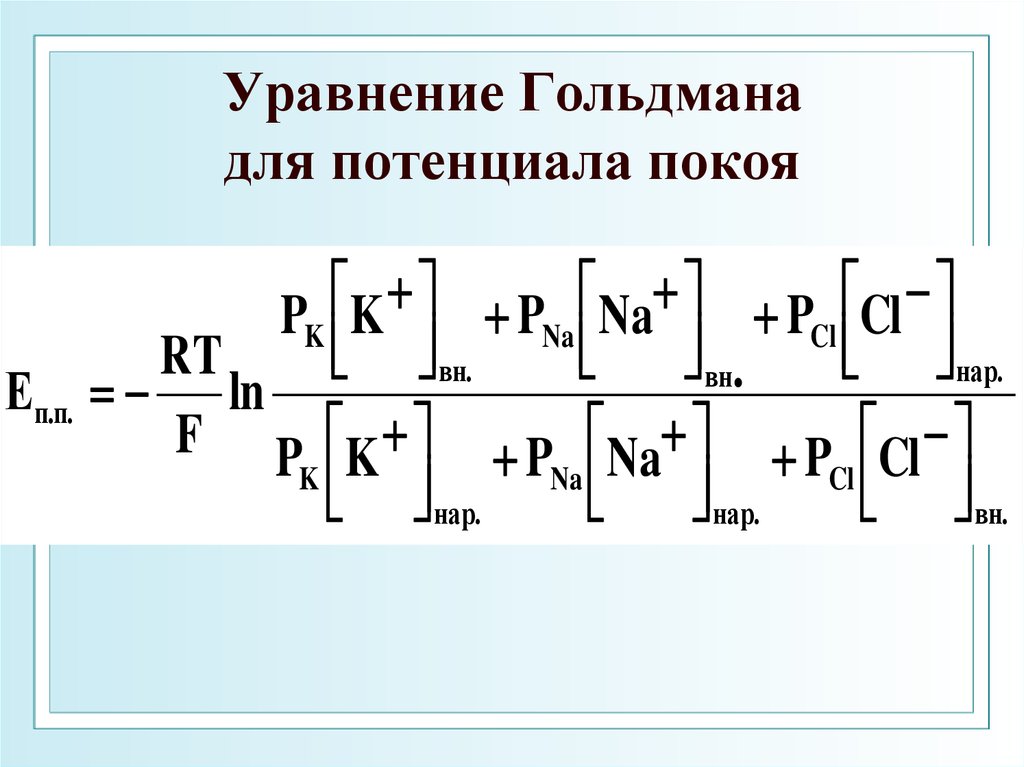
51. Уравнение Гольдмана для потенциала покоя
Εп.п.PK K
PNa Na
PCl Cl
вн.
вн.
нар.
RT
ln
F P K P Na P Cl
K
нар. Na
нар. Cl вн.
52. Отношение коэффициентов проницаемости для состояния покоя
PК : РNa : PCl = 1 : 0,04 : 0,4553. С учетом работы электрогенных ионных насосов для мембранного потенциала было получено уравнение Томаса (1972 г.)
mPK KPNa Na
вн.
вн.
RT
Ε
ln
п.п.
F
mPK K
PNa Na
нар.
нар.
Где m =3/2 - отношение количества ионов натрия к количеству
ионов калия, перекачиваемых Na+ - K+-насосом.
54.
Потенциал покоя и потенциал действияФГОУ ВПО ЮФУ каф. биохимии и микробиологии
55.
Потенциал действия (ПД) – этопоследовательность изменений,
мембранного потенциала, которая
запускается в ответ на воздействие
надпороговых стимулов и приводит к
возбуждению клетки.
56. Потенциалом действия называется электрический импульс, обусловленный изменением ионной проницаемости мембраны и связанный с распростра
Потенциалом действия называетсяэлектрический импульс,
обусловленный изменением ионной
проницаемости мембраны и
связанный с распространением по
нервам и мышцам волны
возбуждения.
57. Потенциал действия
58. При генерации потенциала действия происходит перезарядка мембраны: внутри она становится зараженной положительно (за счет входа ионов Na+
При генерации потенциала действия происходит перезарядкамембраны: внутри она становится зараженной положительно (за
счет входа ионов Na+ в клетку), а снаружи – отрицательно.
59. Возбудимость – это способность клеток к быстрому ответу на раздражение, проявляющемуся через совокупность физических, физико-химических
Возбудимость – это способностьклеток к быстрому ответу на
раздражение, проявляющемуся через
совокупность физических, физикохимических процессов и
функциональных изменений.
Обязательным признаком
возбуждения является изменение
электрического состояния клеточной
мембраны.
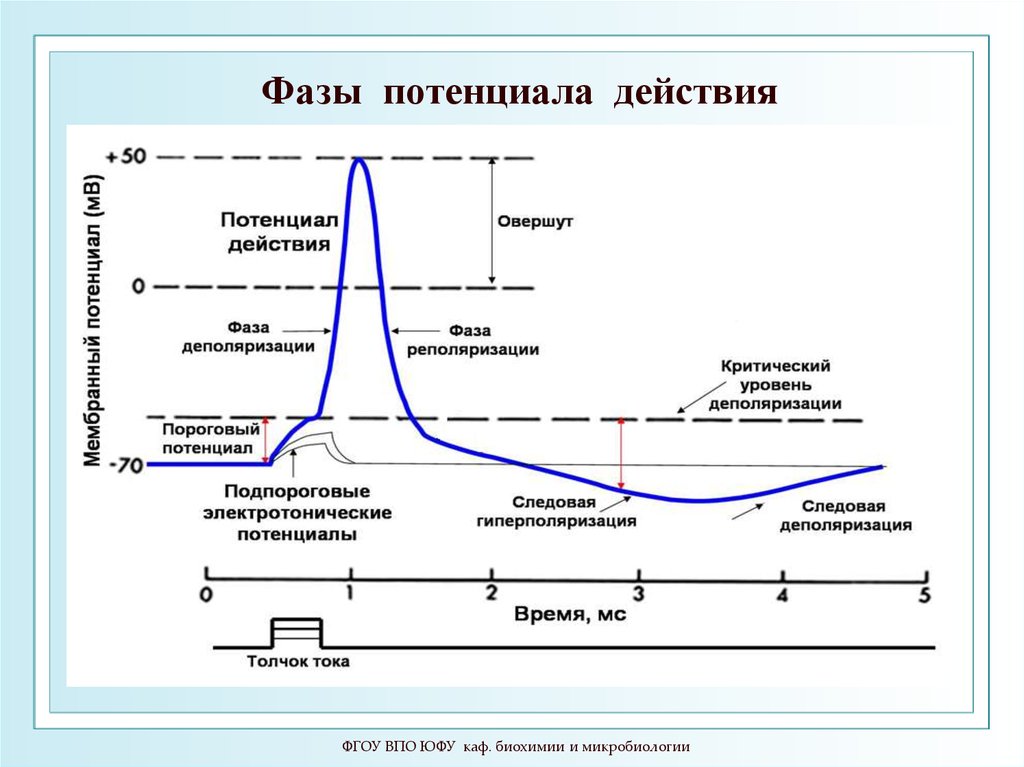
60.
Фазы потенциала действияФГОУ ВПО ЮФУ каф. биохимии и микробиологии
61.
Стимуляция нервной клетки достигает порогавозбудимости, необходимого для
возникновения потенциала действия.
• Начальное изменение мембранного
потенциала приводит к конформационным
изменениям Na+ - канала, который из
состояния покоя переходит в активное
состояние, что приводит к проникновению Na+
в клетку по электрохимическому градиенту.
Это вызывает дальнейшую деполяризацию
клетки. Потенциал действия развивается по
закону все или ничего и реализует свою
программу полностью независимо от других
изменений в клетке.
62.
Поскольку деполяризация в клетке продолжается,открывается больше потенциал-зависимых К+каналов, и К+ начинает по электрохимическому
градиенту выходить из клетки. В то же время
длительная деполяризация вызывает инактивацию
Na+- каналов. Благодаря замедлению потока Na+
и выходу положительно заряженных ионов К+
начинается реполяризация клетки и возвращение
мембранного потенциала к исходному уровню
покоя.
• После восстановления исходного уровня
мембранного потенциала Na+ и К+ каналы
возвращаются в состояние покоя.
63.
Изменение проницаемости мембраны для ионовнатрия и калия при генерации ПД
ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
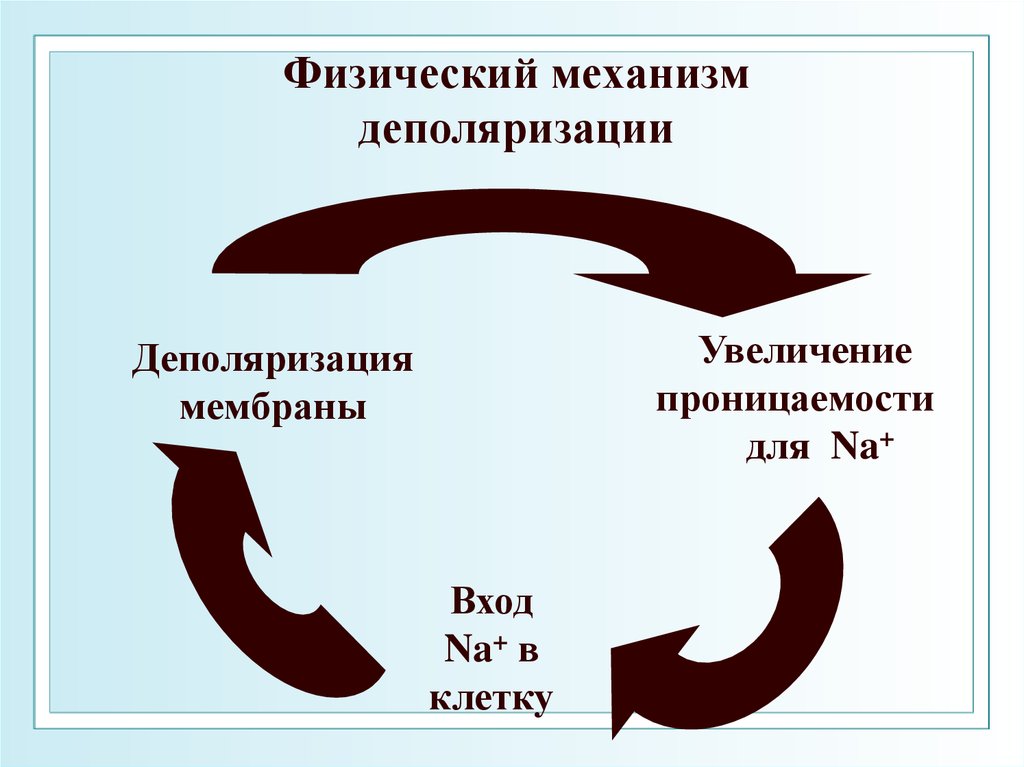
64. Физический механизм деполяризации
Увеличениепроницаемости
для Na+
Деполяризация
мембраны
Вход
Na+ в
клетку
65. Отношение коэффициентов проницаемости ионов для фазы деполяризации
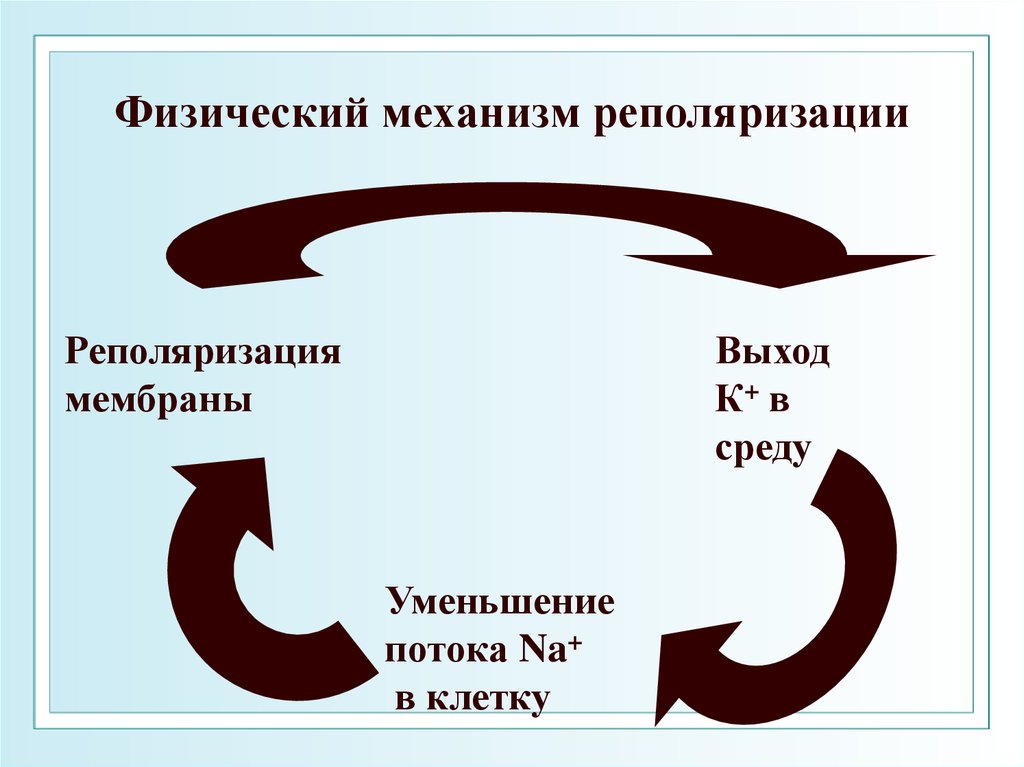
PК : РNa : PCl = 1 : 20 : 0,4566. Физический механизм реполяризации
Реполяризациямембраны
Выход
К+ в
среду
Уменьшение
потока Na+
в клетку
67. Формирование потенциала действия обусловлено двумя ионными потоками через мембрану: поток ионов натрия внутрь клетки приводит к перезаря
Формирование потенциала действияобусловлено двумя ионными
потоками через мембрану: поток
ионов натрия внутрь клетки
приводит к перезарядке мембраны, а
противоположно направленный
поток ионов калия обуславливает
восстановление исходного
потенциала покоя.
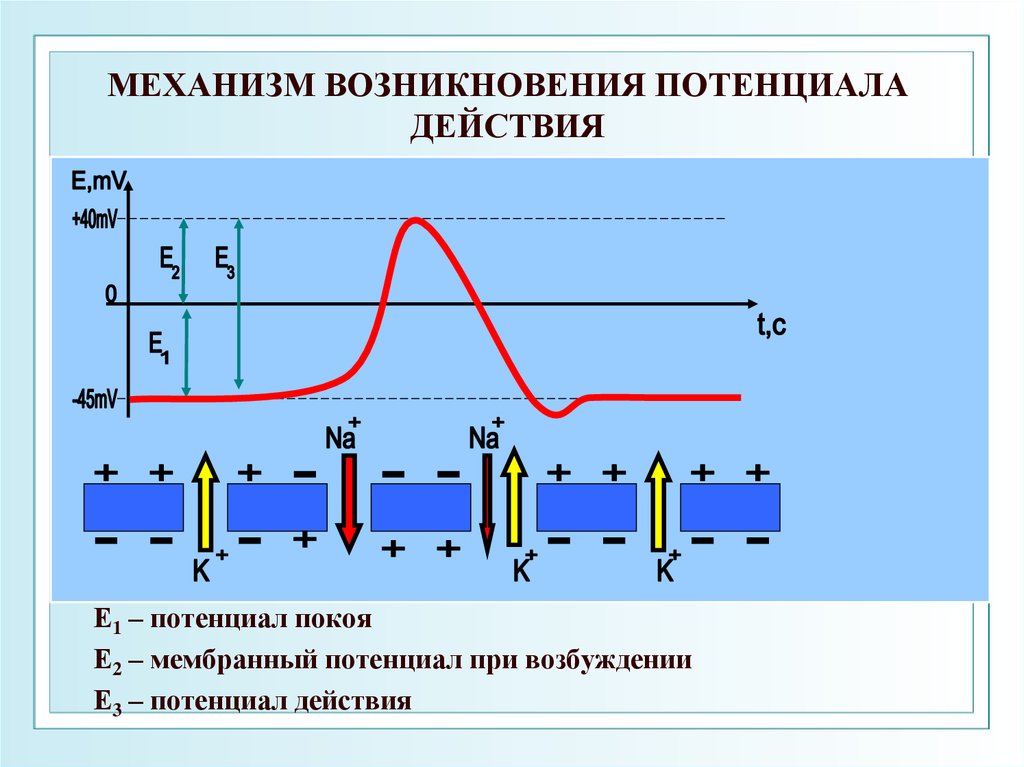
68. МЕХАНИЗМ ВОЗНИКНОВЕНИЯ ПОТЕНЦИАЛА ДЕЙСТВИЯ
Е1 – потенциал покояЕ2 – мембранный потенциал при возбуждении
Е3 – потенциал действия
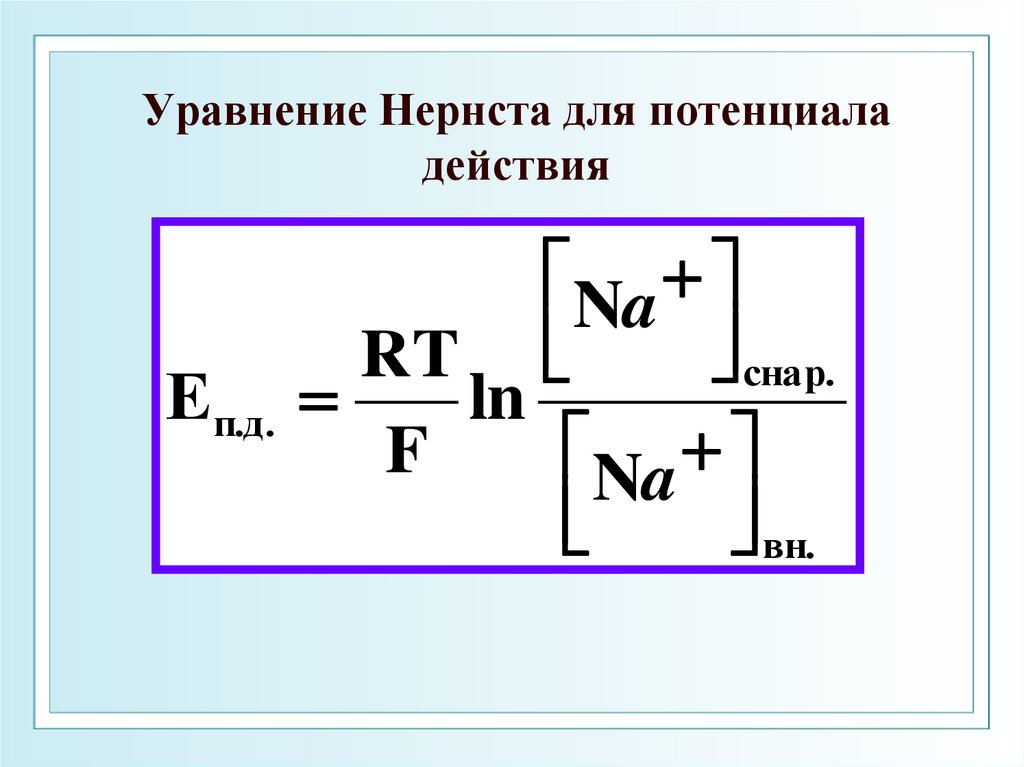
69. Уравнение Нернста для потенциала действия
Εп.д.Na
снар.
RT
ln
F
Na
вн.
70. Уравнение Ходжкина-Хаксли, описывающее мембранный потенциал, который складывается из потенциала покоя и потенциала действия
NaK
RT
вн.
снар.
Е
ln
ln
м.п. F
K
Na
вн.
снар.
71.
ФГОУ ВПО ЮФУ каф. биохимии и микробиологии72. Ионный канал.
ФГОУ ВПО ЮФУ каф. биохимии и микробиологии73. Ионный транспорт
Затраты энергии, необходимые для проникновения иона внеполярную фазу, оценивают по формуле Борна. Энергия,
затрачиваемая на перемещение иона из воды в мембрану, зависит
от:
1)радиуса иона
2)диэлектрических проницаемостей воды и мембраны.
Где
z - валентность иона
e - элементарный заряд
r - радиус иона
εM - диэлектрическая проницаемость мембраны
εв - диэлектрическая проницаемость воды
ФГОУ ВПО ЮФУ каф. биохимии и
микробиологии
74.
Вероятность перехода иона из воды в липидную фазу:Непосредственный перенос ионов через липидный
бислой за счет диффузии маловероятен:
ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
74
75. Изменение энергии при переходе гидрофильного вещества через липидный бислой мембраны
ФГОУ ВПО ЮФУ каф. биохимии и микробиологии76. Свойства ионных каналов
1. Селективность2. Независимость работы отдельных
каналов
3. Дискретный характер проводимости
4. Зависимость параметров каналов от
мембранного потенциала
77. Свойства ионных каналов
1.Селективность – способность пропускать ионы одного типа.• ИК обладают абсолютной селективностью по отношению к
катионам или анионам;
• Через катион-селективные каналы проходят различные ионы,
но проводимость для основного иона максимальна;
• Способность ионного канала пропускать различные ионы
называется относительной селективностью и
характеризуется рядом селективности. Это соотношение
проводимости канала для различных ионов, взятых при одной
концентрации. Для основного иона селективность
принимается за 1 (для Na-канала ряд селективности:
• Na+ : K+ = 1 : 0,05).
ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
78. 2.Независимость работы отдельных каналов
Прохождение тока через отдельный ионныйканал не зависит от того, идет ли ток ионов
через другие каналы.
Например, К+-каналы могут быть включены
или выключены, но ток через Na+-каналы не
меняется. Изменение проницаемости ионных
каналов меняет мембранный потенциал.
79. 3.Дискретный характер проводимости
Проводимость ионного канала дискретна, ион может находится в двух состояниях:
открытом и закрытом. Переходы между этими
состояниями происходят в случайные моменты
времени и подчиняются статистическим
закономерностям. Сдвиг мембранного
потенциала выше порогового значения
увеличивает вероятность открытия каналов,
т.е. идет процесс их активации.
80. 4.Зависимость параметров каналов от мембранного потенциала
Ионные каналы нервных волокон чувствительны кмембранному потенциалу, например К+-каналы и Na+каналы. Это проявляется в том, что после начала
деполяризации мембраны соответствующие токи
начинают изменяться с той или иной кинетикой. Ионселективный канал имеет сенсор, чувствительный к
действию электрического поля.
81.
В 2003 году Нобелевская премияпо химии была присуждена
американскому учёному Родерику
Маккиннону за открытие структуры
ионного канала. В 1998 году ему удалось
кристаллографическими
методами получить трёхмерную
молекулярную структуру калиевого
канала бактерии Streptomyces lividans.
Изображение белка появилось
на обложке журнала «Science»,
редакция которого посчитала открытие
Маккиннона одним из десяти самых
выдающихся научных достижений года.
Этот белок состоит из 4 субъединиц,
имеющих α-спиральное строение. Через
полость в центре и переносится катион
калия.
ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
82.
Строение потенциал-чувствительногокалиевого канала
ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
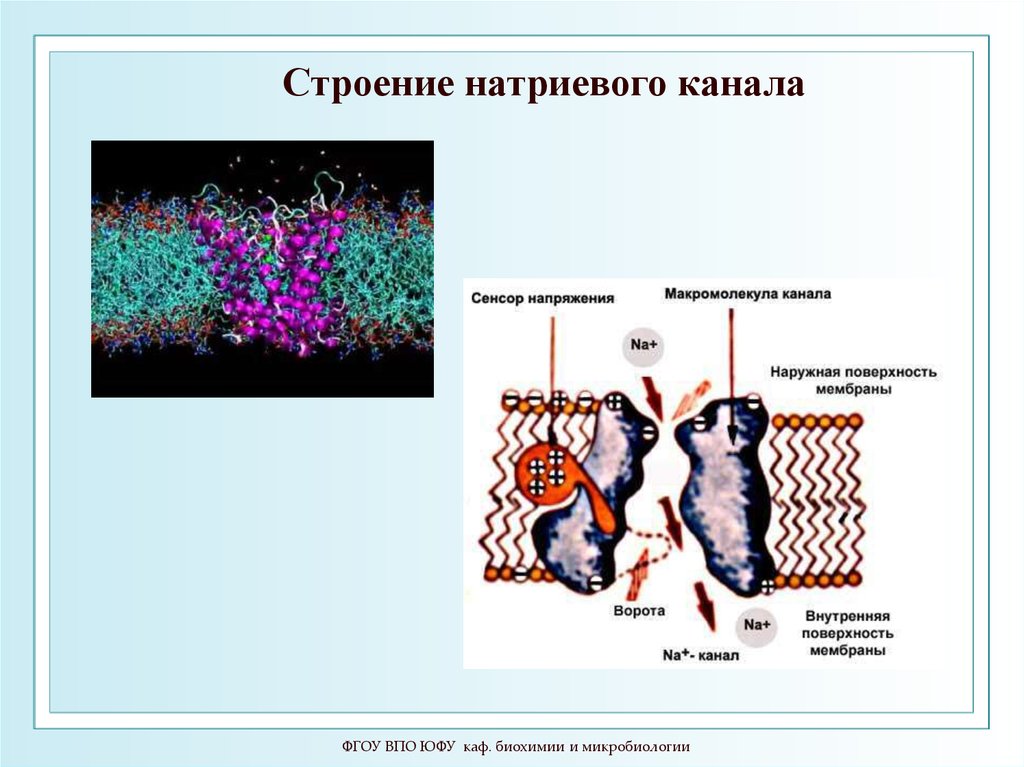
83.
Строение натриевого каналаФГОУ ВПО ЮФУ каф. биохимии и микробиологии
84. Потенциал-чувствительный натриевый канал
Канал состоит из четырёх похожих фрагментов-повторов (а), обозначенных I–IV. Каждый фрагментсодержит шесть трансмембранных α-спиралей. Четыре спирали (S1–S4) формируют потенциалчувствительный домен. Общий для канала поровый домен образован восемью спиралями, по две (S5 и S6)
от каждого повтора. Четвёртая спираль в каждом потенциал-чувствительном домене положительно заряжена. Она
выполняет роль сенсора потенциала. На рисунке показаны места, с которыми связываются α- и β-токсины
скорпионов. В пространстве повторы структуры потенциал-чувствительного натриевого канала располагаются
вокруг общей оси (б). Центральный поровый домен канала образован восемью спиралями, а потенциалчувствительные домены расположены на периферии. Участок между спиралями S5 и S6 содержит «селективный
фильтр» (в), обеспечивающий избирательное пропускание ионов Na+
ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
85. Сравнение параметров ионных каналов
Na+- каналК+ - канал
1. Сечение поры
0,31х 0,51 нм
0,45 х 0,45 нм
2. Энергетический профиль
Энергетический барьер в центре канала
Энергетические барьеры при входе и
выходе из канала
3. Анионный центр
СООН-гр.+5 атомов О+ мол. Н2О
СООН-гр.+4 атома О
Na+ сохраняет в гидратной оболочке 1- Диаметр иона К+
соответствует
3 мол. Н2О
диаметру поры
4. Вольтамперная характеристика
5. Селективность
Более селективен – проходит только К+
Менее селективен
Na : К = 1: 0,05
6. Блокаторы
Тетродотоксин
ФГОУ ВПО ЮФУ
Тетраэтиламмоний
каф. биохимии и микробиологии
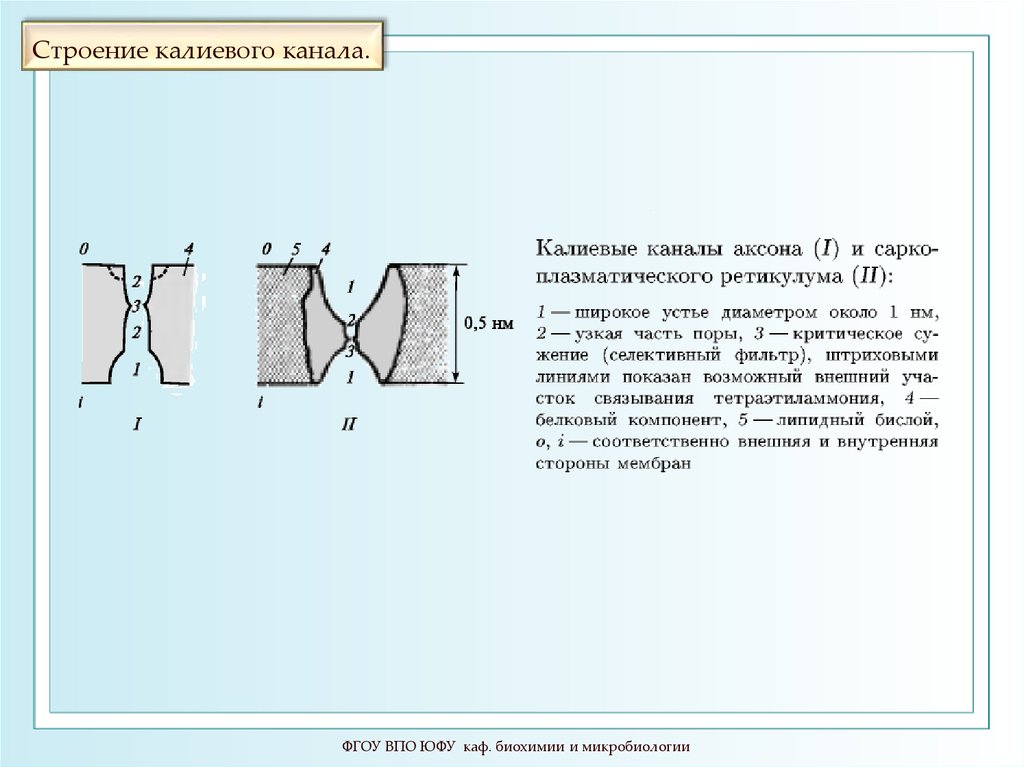
86. Строение калиевого канала.
ФГОУ ВПО ЮФУ каф. биохимии и микробиологии87. Энергетические профили ионных каналов.
Входящий и выходящий потоки Na+ в К+-канале независимы; этот факт соответствуетэнергетическому профилю с высоким центральным барьером (кривая 1). Однако такая
форма энергетического профиля не согласуется с данными о существовании в селективном
центре N а -канала фиксированной анионной группы, которое доказывается зависимостью
проводимости К+-каналов от рН среды. Протонирование кислотной группы (рК 5,2)
приводит к блокированию Na+-канала. При физиологических значениях рН состоянию
канала с депротонированной кислотной группой больше соответствует профиль, в котором
центральный энергетический барьер расщеплен на два (кривая 2). В таком канале
фиксированный анионный центр, притягивая катионы, облегчает их вход в канал.
ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
88.
Блокатор натриевых каналов тетродотоксинРыба фугу — японский деликатес, популярный у любителей острых ощущений. «Хочешь
есть фугу — напиши завещание», «Кто ест фугу, тот глуп, и кто не ест, тоже глуп»... Фугу
делают из нескольких видов рыб семейства иглобрюхих (Tetraodontidae).
ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
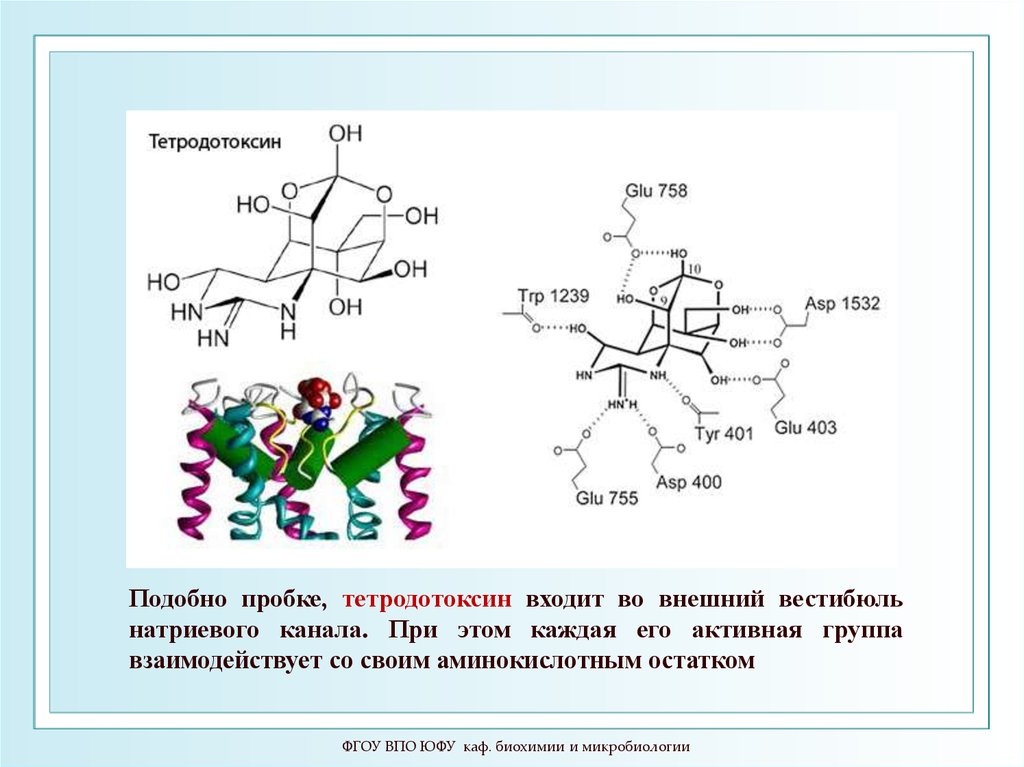
89.
Подобно пробке, тетродотоксин входит во внешний вестибюльнатриевого канала. При этом каждая его активная группа
взаимодействует со своим аминокислотным остатком
ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
90.
Хищныйбрюхоногий
моллюск
Conus
textile
и
структура
конотоксина. Справа — конотоксин в канале; в отличие от тетродотоксина,
он прикрывает канал сверху. Конотоксины — пептиды с несколькими
цистеиновыми S-S-мостиками.
ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
91.
Молекула батрахотоксина сидит вканале и не дает ему закрыться,
пропуская ионы
натрия. Стрелкой показан ток
ионов
Третий класс соединений, воздействующих на потенциал-зависимые натриевые
каналы, представляет батрахотоксин южноамериканских лягушек листолазов
(Phyllobates). Они канал не блокируют. Наоборот, связывание этих токсинов приводит к
тому, что канал удерживается в открытом состоянии и непрерывно пропускает ионы.
Но хотя механизм действия абсолютно противоположный, биологический эффект тот
же — плачевный для жертвы.
ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
92.
Местные анестетикиМестные анестетики блокируют быстрый вход Na+, возникновение и проведение
возбуждения. Большинство местных анестетиков являются
амфифильными молекулами.
ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
92
93. Действие местных анестетиков.
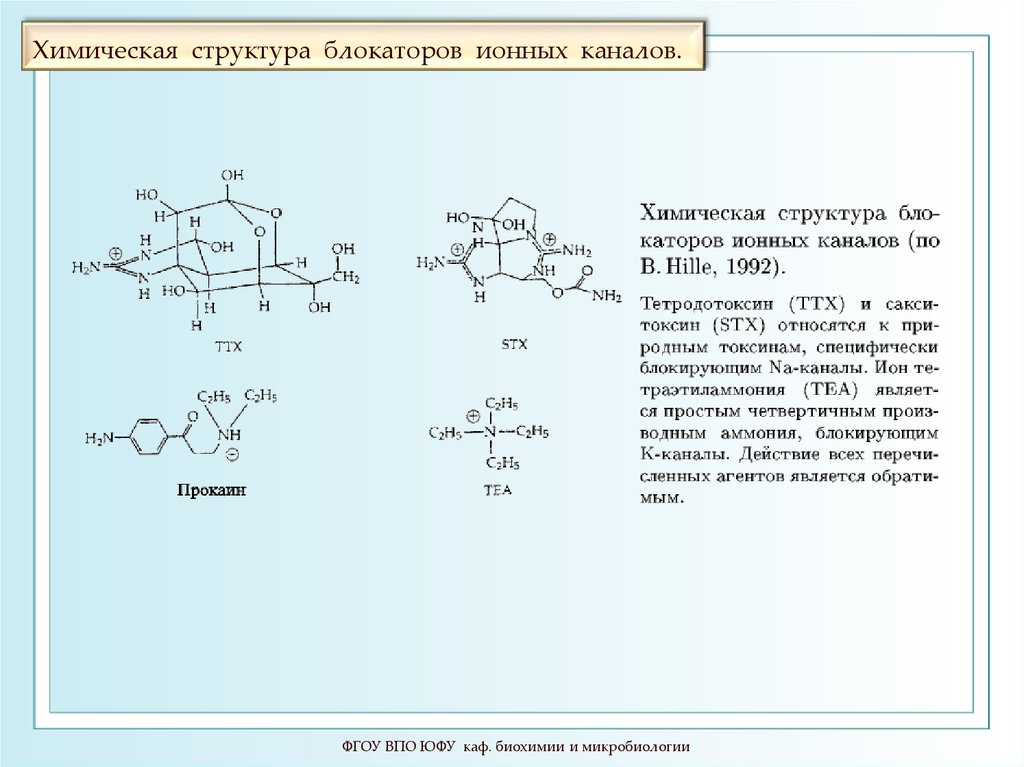
ФГОУ ВПО ЮФУ каф. биохимии и микробиологии94. Химическая структура блокаторов ионных каналов.
ФГОУ ВПО ЮФУ каф. биохимии и микробиологии95. Метод пэтч-кламп, разработанный Неером и Закманом, позволяет изучать отдельные ионные каналы
ФГОУ ВПО ЮФУ каф. биохимии и микробиологии96.
Нобелевская премия по химии 2003 г. былавручена «за открытия, касающиеся каналов
в клеточных мембранах» - Питеру Эгру
«за открытие водных каналов»
Выступление П.Эгра в МГУ в 2013 г.
Открытие, сделанное профессором
Эгром, — яркий пример роли
счастливого случая в науке. Недаром
сам нобелевский лауреат любит
повторять на своих лекциях: «Всегда
относитесь к научной деятельности
как к приключению… Мы не знаем,
что ждет нас за поворотом, и в этом
смысле я, скорее, Гекльберри Финн,
чем Альберт Эйнштейн».
ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
97. Аквапорины образуют гидрофильные трансмембранные каналы для переноса воды
ФГОУ ВПО ЮФУ каф. биохимии и микробиологии98.
Индуцированный ионный транспортосуществляется ионофорами, которые
делятся на 2 группы:
1. Подвижные переносчики
2. Каналообразующие агенты
(каналоформеры)
98
99.
1. Подвижные переносчики.Перенос иона через мембрану с участием подвижного переносчика
включает 4 стадии:
1. Образование комплекса иона с ионофором на одной стороне
мембраны.
2. Перемещение комплекса через мембрану.
3. Освобождение иона на другой стороне.
4. Возвращение ионофора.
Возможны 2 схемы работы переносчика:
1. Малая "карусель", когда ионофор не выходит из мембраны.
2. Большая "карусель", когда ионофор проходит мембрану насквозь, а
образование и распад комплекса происходит вне мембраны.
Так, для заряженного комплекса радиусом 1 нм свободная энергия
перехода из воды в мембрану составляет около 15 кДж/моль в отличие
от энергии свободного иона - 250-300 кДж/моль
ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
99
100.
Подвижные переносчики. Валиномицин.Антибиотик валиномицин впервые был выделен из
экстракта штамма бактерий Streptomyces
fulvissimus австрийским исследователем Г. Брокманом в
1954–1955 годах. А в 1963 году в лаборатории акад.
М. М. Шемякина установили химическую
структуру этого соединени.
Валиномицин - макроциклическое соединение, состоящее
из шести α-аминокислот и шести α-гидроксикислот,
соединённых друг с другом попеременно амидными и
сложноэфирными связями.
В 1978 году Ю. А. Овчинников и член-корреспондент АН
СССР В.Т. Иванов были удостоены Ленинской премии за
исследование ионофоров.
ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
101. Ионофоры. Валиномицин.
1.2.
3.
Молекула валиномицина (а) напоминает своей
конфигурацией браслет, является полярным
соединением, причем отрицательные полюса
образованных им диполей сосредоточены у
карбонильных групп.
Взаимодействуя между собой в слабо полярной
среде, они отталкиваются друг от друга и
потому повернуты наружу, что придает всей
молекуле гидрофильность. В липидную
мембрану она внедриться не может и находится
в примембранном водном растворе (б).
Если же в воде растворена калиевая соль, то К+
входит во внутреннюю полость браслета (в).
Внедрение катиона в антибиотик вызывает
разворот
карбонильных
групп
валиномицина
за
счет
ион-дипольного
взаимодействия.
Карбонильные
группы
смещаются
во
внутреннюю
полость
валиномицина, а снаружи его оказываются
углеводородные
цепочки,
создающие
гидрофобный чехол на молекулярно-ионном
комплексе. Поэтому комплекс валиномицина с
калием хорошо растворяется в липидах, легко
внедряется в липидный бислой мембраны и
диффундирует в нем как жирорастворимое
вещество.
ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
102.
Кристаллическая структура ионофора - комплексаК+-валиномицин
ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
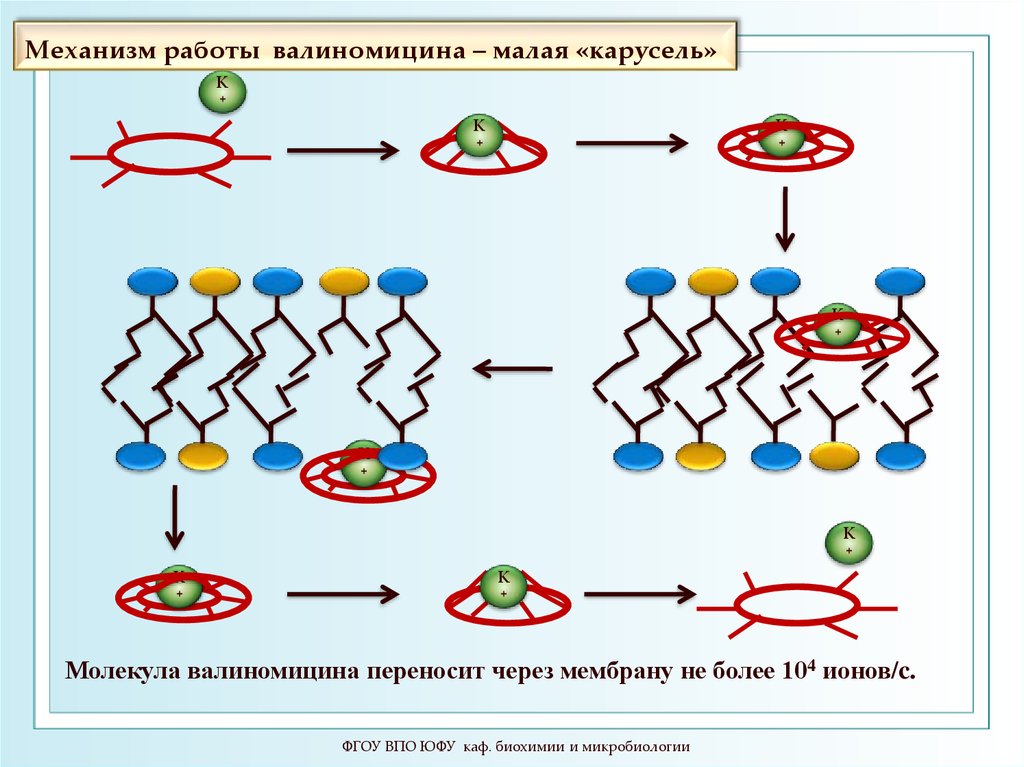
103. Механизм работы валиномицина – малая «карусель»
К+
К
К
+
+
К
+
К
+
К
+
К
К
+
+
Молекула валиномицина переносит через мембрану не более 104 ионов/c.
ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
104.
Скульптурная композиция комплексаК+-валиномицин перед входом в институт биоорганической
химии им. М.М.Шемякина и Ю.А.Овчинникова
ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
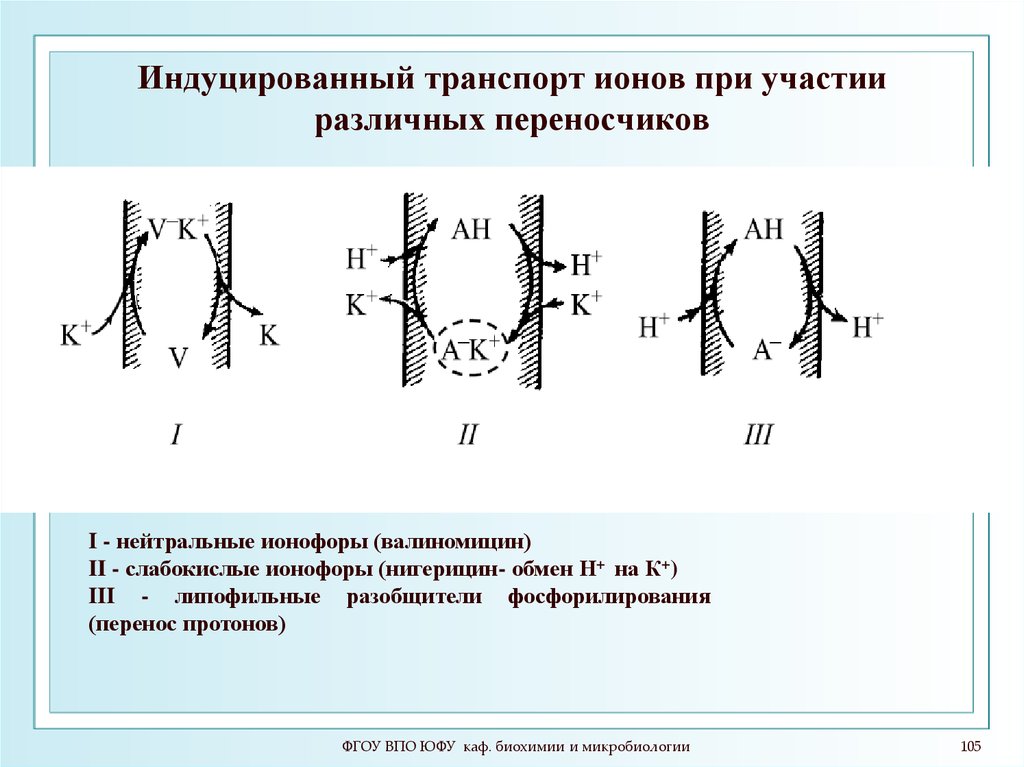
105. Индуцированный транспорт ионов при участии различных переносчиков
I - нейтральные ионофоры (валиномицин)
II - слабокислые ионофоры (нигерицин- обмен Н+ на
К+)
III - липофильные разобщители фосфорилирования
(перенос протонов)
I - нейтральные ионофоры (валиномицин)
II - слабокислые ионофоры (нигерицин- обмен Н+ на К+)
III - липофильные разобщители фосфорилирования
(перенос протонов)
ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
105
106. Грамицидин – каналообразующий антибиотик
1) Грамицидин сформирован 15 гидрофобнымиаминокислотами, на N-конце - формильная группа
(голова), на С-конце – этаноламин (хвост). Канал образован
димером — парой молекул грамицидина, расположенных
«голова к голове». Формильные концы соединяются
межмолекулярными водородными связями.
2) Молекула грамицидина имеет форму спирали. Такая же
форма присуща и димеру. Внутренность спирали
гидрофильна и заполнена 5—6 молекулами воды. Катион,
движущийся по каналу, проталкивает их подобно поршню.
3) Грамицидиновый канал проводит преимущественно
одновалентные катионы, причем проницаемость
мембраны для них растет по мере уменьшения гидратного
ионного радиуса. Почти не транспортируются анионы,
так как внутрь поры «смотрят» отрицательно заряженные
группы.
5) Скорость переноса 107 ионов калия за 1 с.
6) Грамицидиновый канал может пребывать либо в
открытом, либо в закрытом состоянии, что обусловлено
тепловым движением молекул грамицидина. За счет
теплового движения концы димера то погружаются в
липидную основу, то выходят на обе ее поверхности.
ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
107. Структура амфипатической α-спирали и расположение спиралей в мембране при формировании гидрофильного канала
108. Аламетицин – каналообразующий антибиотик
1.Аламетицин, пептидный антибиотик с молекулярной массой около 2 кДа.
2.
Аламетициновый канал собирается из молекул этого антибиотика как бочонок из
дощечек, причем встраивание дополнительного мономера («дощечки»)
увеличивает периметр поры примерно на 0,66 нм.
3.
Важной особенностью аламетициновых каналов является их зависимость от
внешнего электрического поля.
4.
В отсутствие разности потенциалов на липидной мембране молекулы
антибиотика распластаны на ее поверхности и не образуют каналов. Создание
трансмембранной разности потенциалов приводит к тому, что положительный
полюс аламетициновой молекулы оказывается на одной стороне мембраны, а
отрицательный (глутаминовый остаток) — на другой.
ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
109.
Проведение потенциала действия в безмиелиновых (А)и миелиновых (Б) нервных волокнах
ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
110.
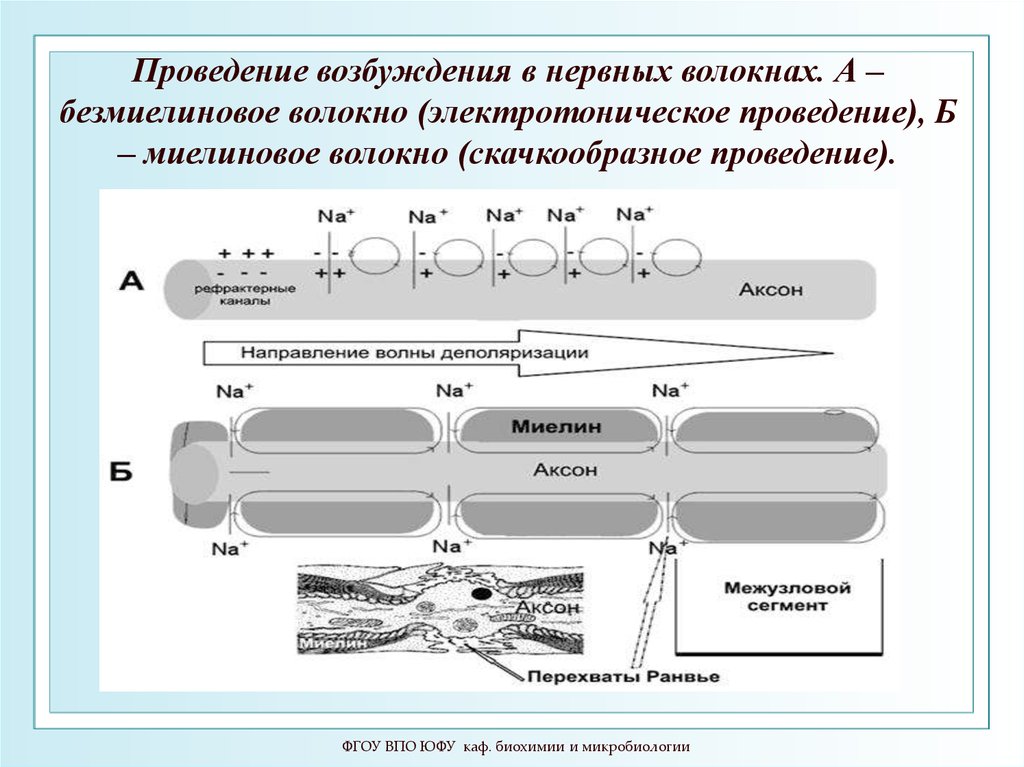
Проведение возбуждения в нервных волокнах. А –безмиелиновое волокно (электротоническое проведение), Б
– миелиновое волокно (скачкообразное проведение).
ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
111. Передача нервного импульса
Выделяют 2 способа повышения скорости передачи нервногоимпульса :
1. Увеличение диаметра нервных волокон (уменьшение
сопротивления)
2.Уменьшения емкости аксолеммы за счет появления миелиновых
волокон. Проведение идет скачками от одного перехвата Ранвье
до другого и называется сальтаторным.
Обеспечивает экономию энергии:
- Скорость проведения больше (25-140 м/c), чем при непрерывном
проведении (0,5-0,7 м/c)
- Потребление кислорода в 200 раз меньше, чем при непрерывном
проведении
- Скорость проведения в миелиновом волокне прямо
пропорциональна его диаметру, а в безмиелиновом - √ из
величины диаметра.
ФГОУ ВПО ЮФУ каф. биохимии и микробиологии





















































































 physics
physics








