Similar presentations:
Классы неорганических соединений
1.
Урок 8 класса.Химические свойства основания
2.
Классы неорганических соединенийСложные
неорганические
вещества
Оксиды
Основания
Кислоты
Соли
Основания – это сложные вещества, в состав которых входит
атомы металлов, соединенные с одной или несколькими
группами атомов ОН.
3.
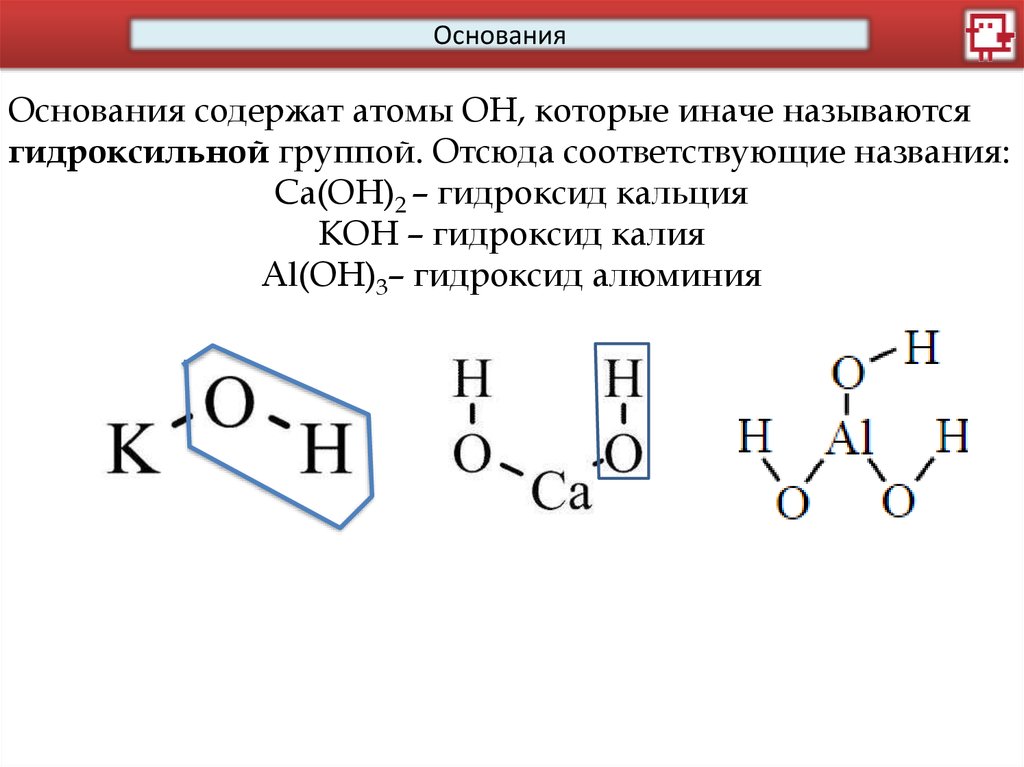
ОснованияОснования содержат атомы ОН, которые иначе называются
гидроксильной группой. Отсюда соответствующие названия:
Са(ОН)2 – гидроксид кальция
KOH – гидроксид калия
Al(OН)3– гидроксид алюминия
4.
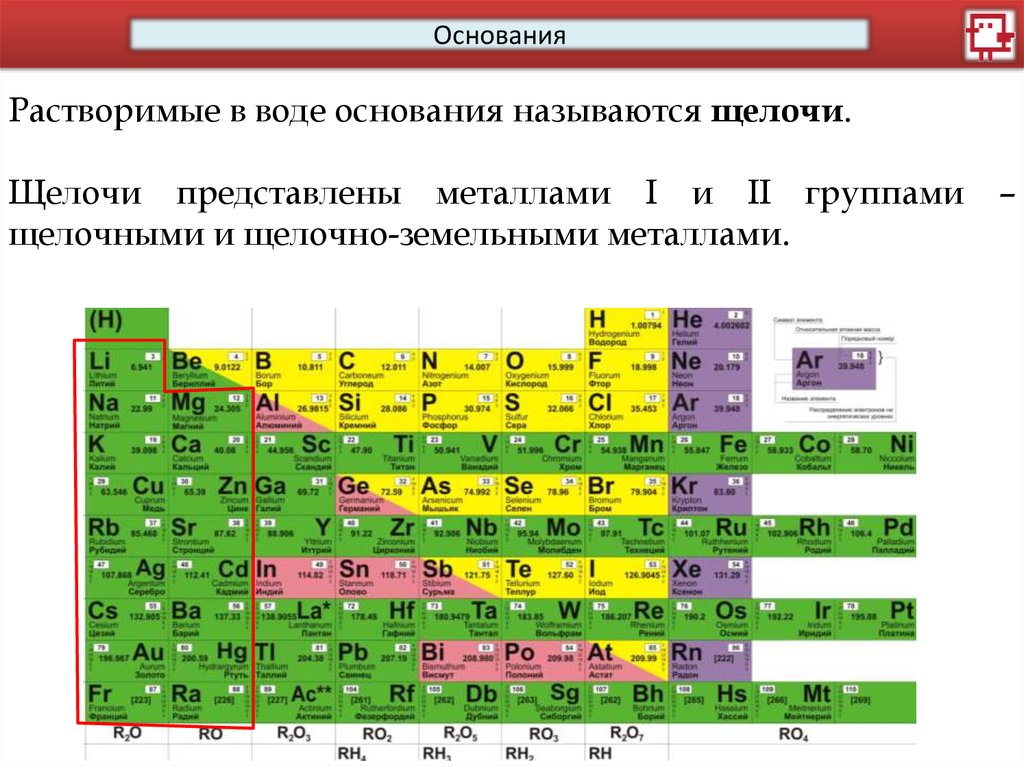
ОснованияРастворимые в воде основания называются щелочи.
Щелочи представлены металлами I и II группами
щелочными и щелочно-земельными металлами.
–
5.
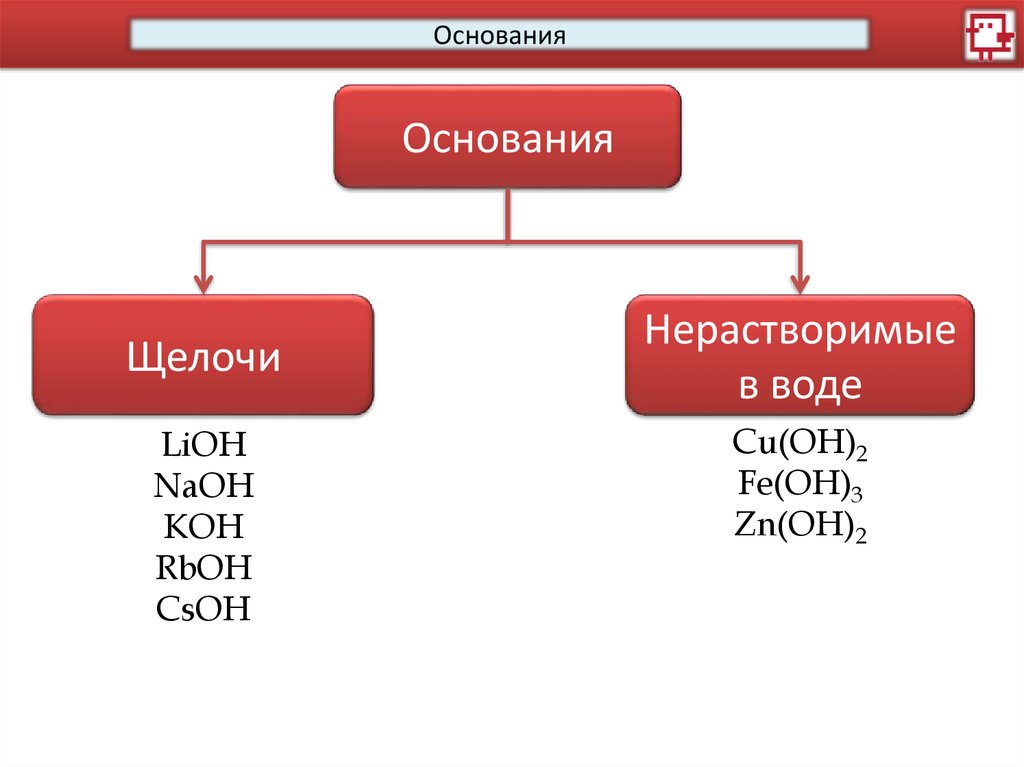
ОснованияОснования
Щелочи
LiOH
NaOH
KOH
RbOH
CsOH
Нерастворимые
в воде
Cu(OH)2
Fe(OH)3
Zn(OH)2
6.
ОснованияПолучение оснований:
• Щелочи можно получить при взаимодействии активных
металлов и их оксидов с водой.
СаО + Н2О = Са(ОН)2
Са + Н2О = Са(ОН)2 + Н2
Металлы, образующие не растворимые щелочи с водой не
реагируют.
Сu + H2O
CuO + H2O
Как же получить гидроксид меди?
7.
ОснованияКак же получить гидроксид меди?
CuCl2 + 2NaOH Cu(OH)2 + 2NaCl
Также и с другими:
FeCl3 + 3NaOH Fe(OH)3 + 2NaCl
8.
ОснованияНо бывают и исключения из этого правила.
Как получить гидроксид серебра?
9.
ОснованияНо бывают и исключения из этого правила.
Как получить гидроксид серебра?
Путём обменной реакции:
2AgNO3 + 2KOH Ag2O + H2O + 2KNO3
10.
ОснованияХимические свойства:
1) Нерастворимые в воде основания при нагревании
разлагаются с образованием
оксидов:
t
2Fe(OH)3 Fe2O3 + 3H2O
t
Ca(OH)2 CaO + H2O
11.
ОснованияХимические свойства:
2) Взаимодействие с кислотами – в такие реакции вступают
ВСЕ основания
Сu(OH)2 + H2SO4 CuSO4 + 2H2O
NaOH + HNO3 = NaNO3 + H2O
12.
ОснованияХимические свойства:
3) Основания могут вступать в реакцию с кислыми оксидами:
Сa(OH)2 + CO2 CaCO3 + H2O







 chemistry
chemistry








