Similar presentations:
Информационные макромолекулы
1. Информационные макромолекулы
Белки, структура и функции2.
Молекуля́рная биоло́гия —комплекс биологических наук,
изучающих механизмы хранения,
передачи и реализации генетической информации, строение и
функции нерегулярных биополимеров (белков и нуклеиновых
кислот).
3.
Геномика — это раздел м.б. , изучающий геномы.Основу геномики составляет расшифровка генома человека, что
является большим достижением биологии.
Геномика заложила основы клинической генетики на многие годы;
она дала теоретическое обоснование и конкретные методические
приемы, в том числе и автоматизированные, для поиска мутаций в
отдельных генах (моногенная патология), которые являются
этиологическими факторами врожденных нарушений метаболизма,
формирующих фено-типические проявления — клинические
симптомы.
Геномика выявляет возможные дефекты на пре- и трансляционном
уровне, которые предшествуют передаче генетической информации с
ДНК на РНК, синтезу матричной РНК (мРНК).
4.
Протеомика — наука, основнымпредметом изучения которой
являются белки, их функции и
взаимодействия в живых организмах, в том числе — в человеческом.
Основная задача протеомики —
количественный анализ экспрессии белков в клетках в зависимости от их типа, состояния или
влияния внешних условий.
Протеомика осуществляет сравнительный анализ больших
групп белков — от всех белков,
вовлеченных в тот или иной
биологический процесс до
полного протеома.
Метаболомика — это научное изучение
химических процессов, в которые
вовлечены метаболиты.
Транскриптомика - научное
направление, занимающееся
изучением транскриптома разных
видов организмов. Транскриптом
– это совокупность
всех транскриптов, синтезируемых
одной клеткой или группой клеток,
включая мРНК и не-кодирующие
РНК. Транскрипт — молекула
РНК, образующаяся в результате
транскрипции
5. Информационные макромолекулы
Живые организмы существуют в разнообразных условияхобитания благодаря своим основным свойствам
размножение
изменчивость
наследственность
рост и развитие
движение
Обмен веществ
реализуются в организме благодаря
высокомолекулярным соединениям, главными из которых являются
белки и нуклеиновые кислоты
6.
во временипространстве
в
обеспечивая, тем самым
существование вида
разнообразие видов
7. Белки и нуклеиновые кислоты
–это органические вещества - биополимеры,
высокомолекулярные соединения , состоящие из повторяющихся частей мономеров.
Процесс синтеза биополимеров называется
полимеризацией.
Ферменты
. каталитирующие процесс полимеразами
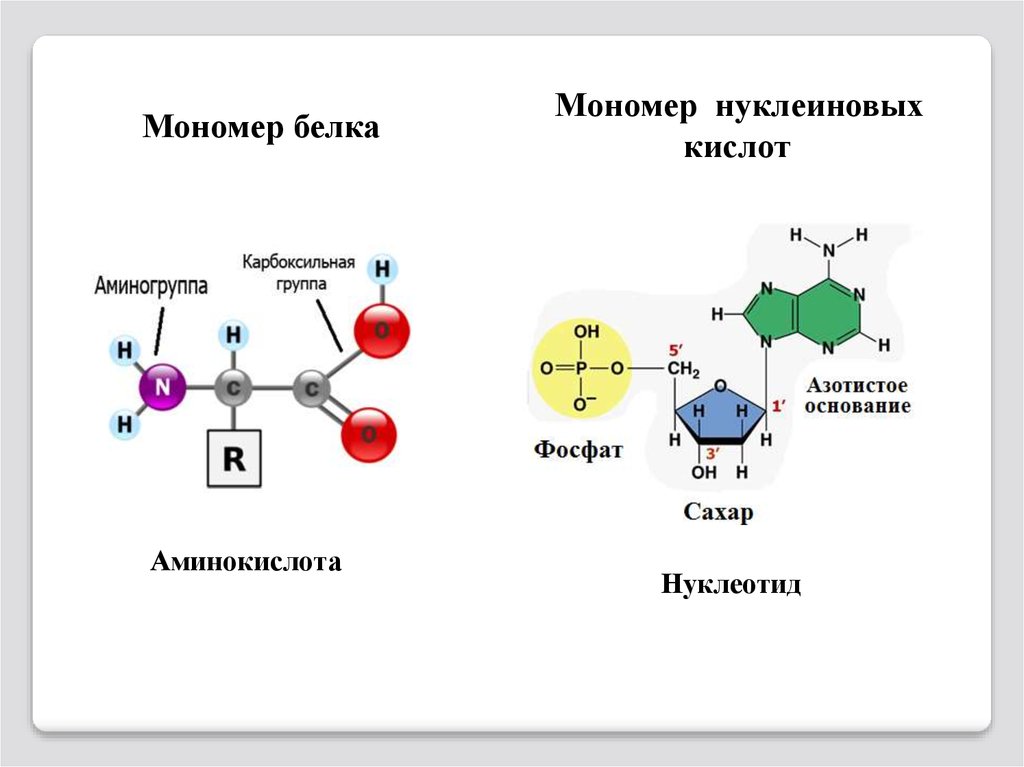
8.
Мономер белкаАминокислота
Мономер нуклеиновых
кислот
Нуклеотид
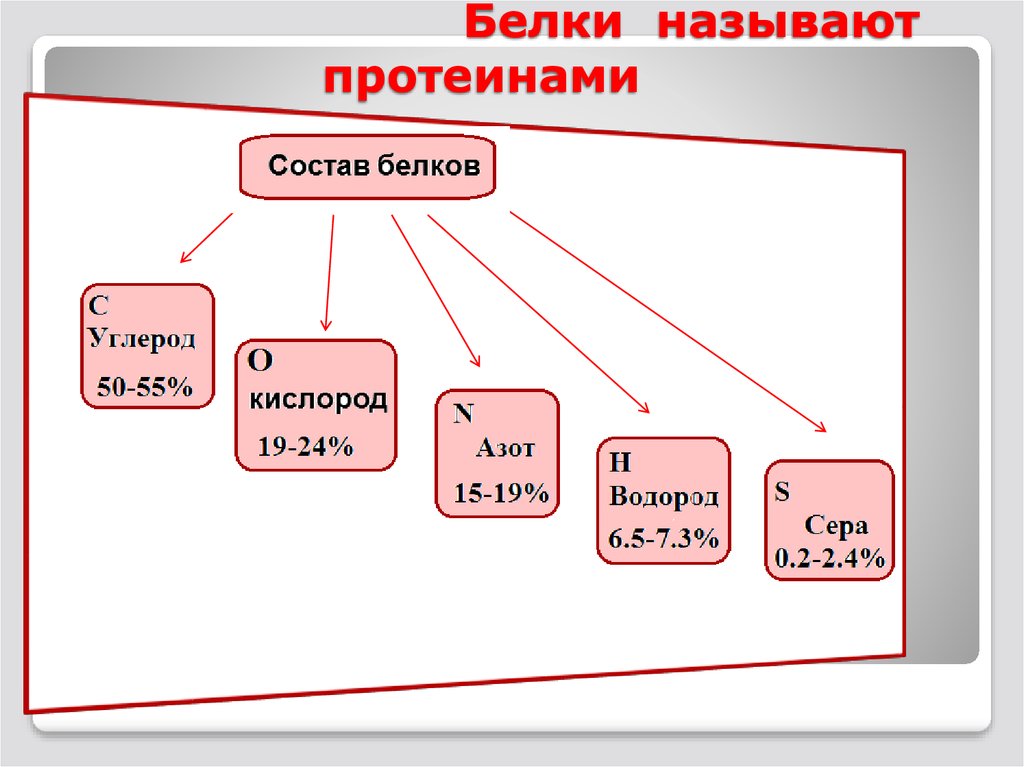
9. Белки называют протеинами
10.
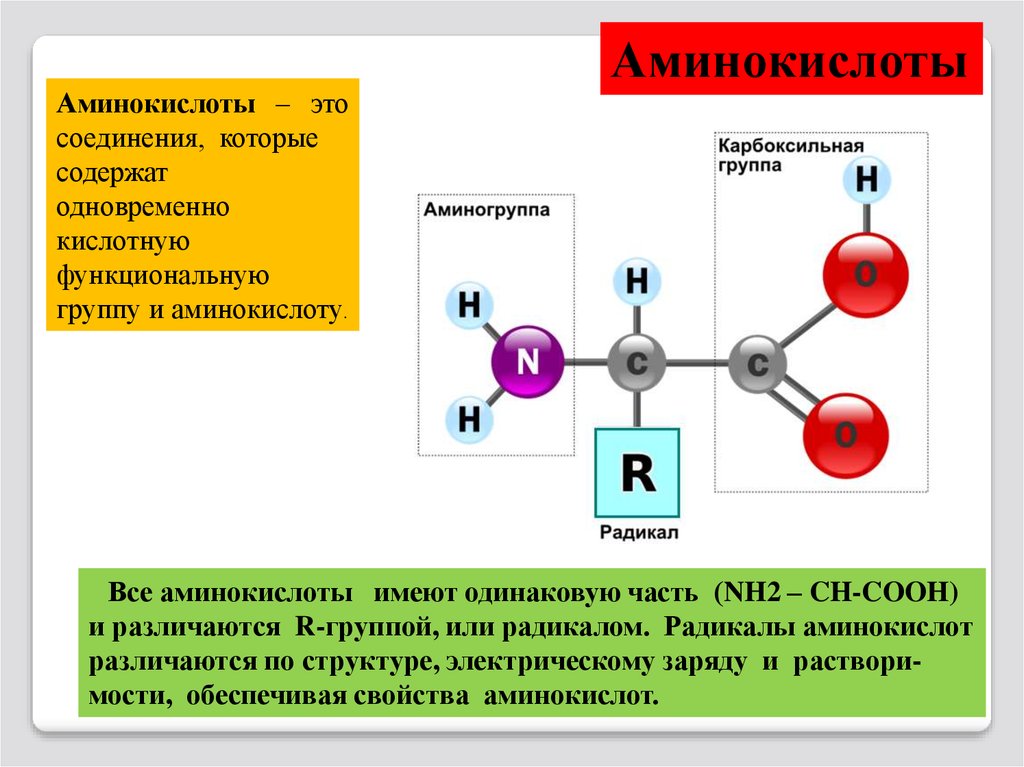
Аминокислоты – этосоединения, которые
содержат
одновременно
кислотную
функциональную
группу и аминокислоту.
Аминокислоты
Все аминокислоты имеют одинаковую часть (NH2 – CH-COOH)
и различаются R-группой, или радикалом. Радикалы аминокислот
различаются по структуре, электрическому заряду и растворимости, обеспечивая свойства аминокислот.
11.
АминокислотыОбщее число аминокислот - 300; из них в
состав белков входит
только 20.
Их называют протеиновыми или белковыми. В зависимости от
способности
растворятся в воде, аминокислоты делятся на:
неполярные(гидрофобн
ые)
и
полярные
(гидрофильные)
12.
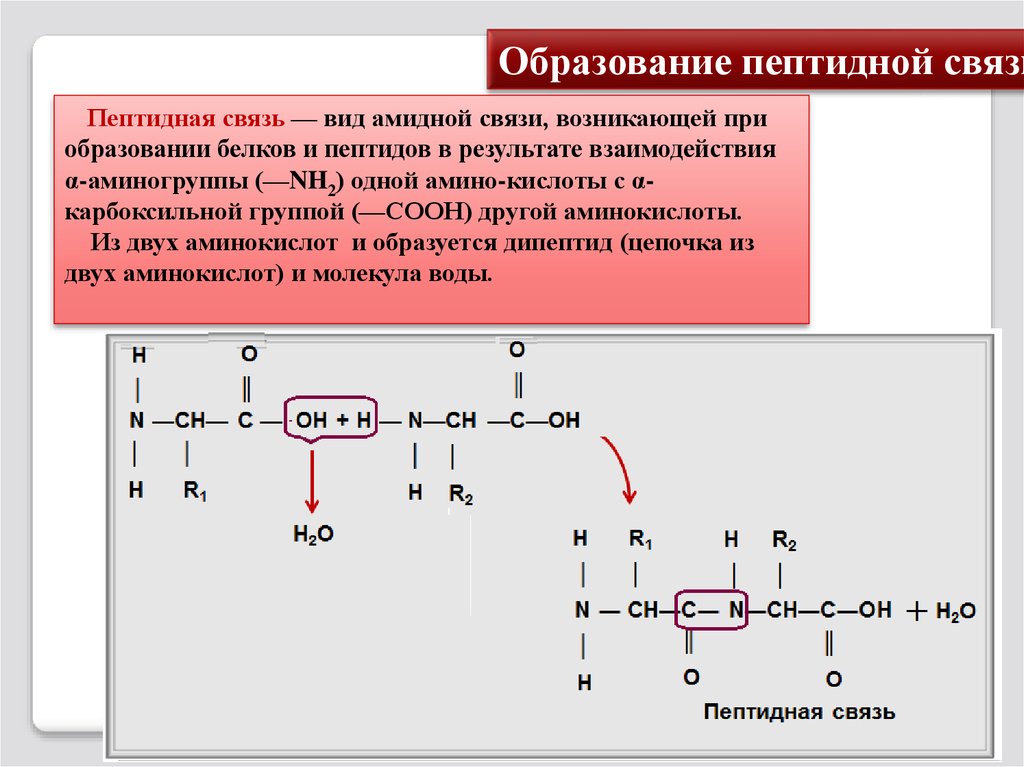
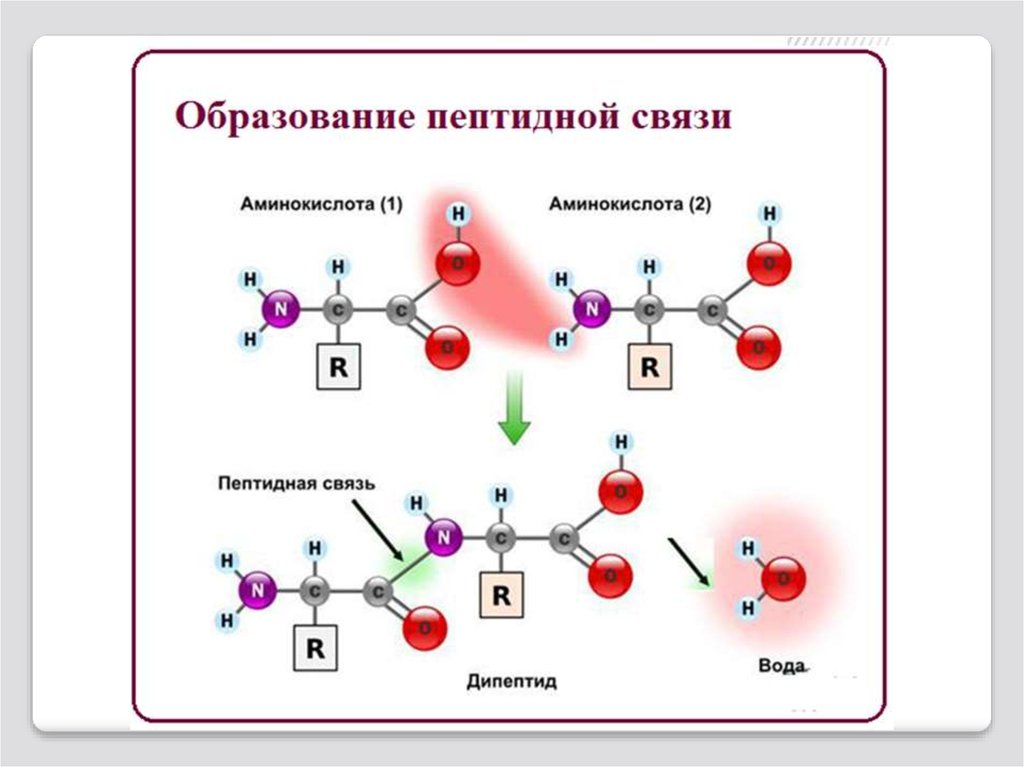
Образование пептидной связиПептидная связь — вид амидной связи, возникающей при
образовании белков и пептидов в результате взаимодействия
α-аминогруппы (—NH2) одной амино-кислоты с αкарбоксильной группой (—СООН) другой аминокислоты.
Из двух аминокислот и образуется дипептид (цепочка из
двух аминокислот) и молекула воды.
13.
14.
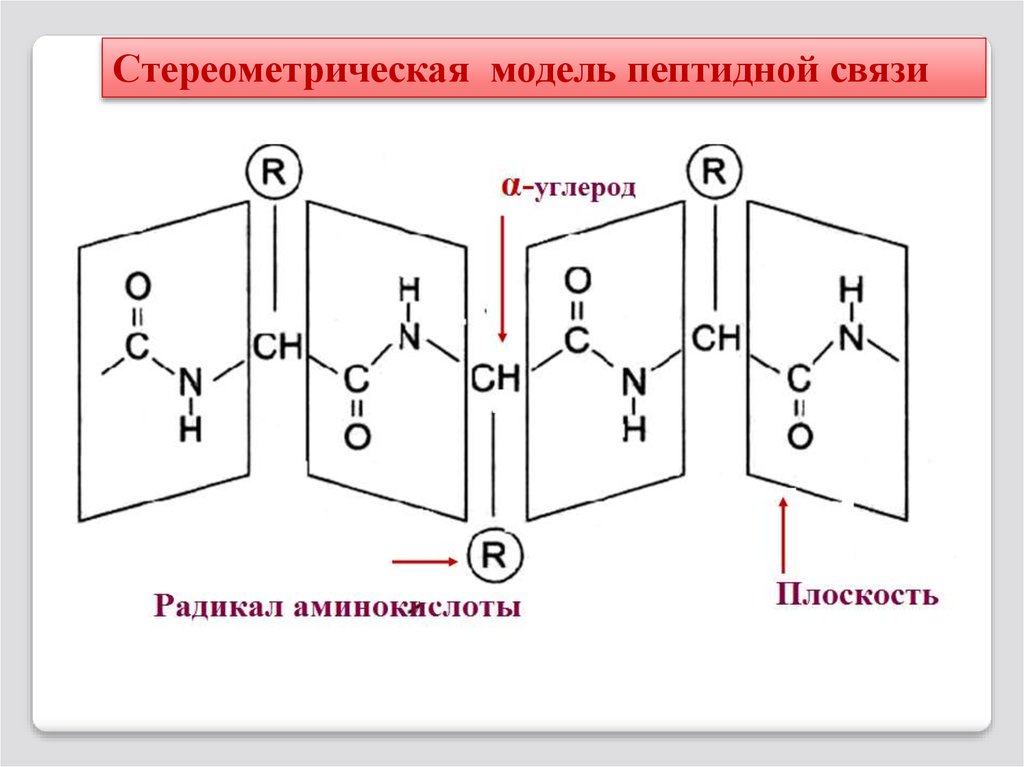
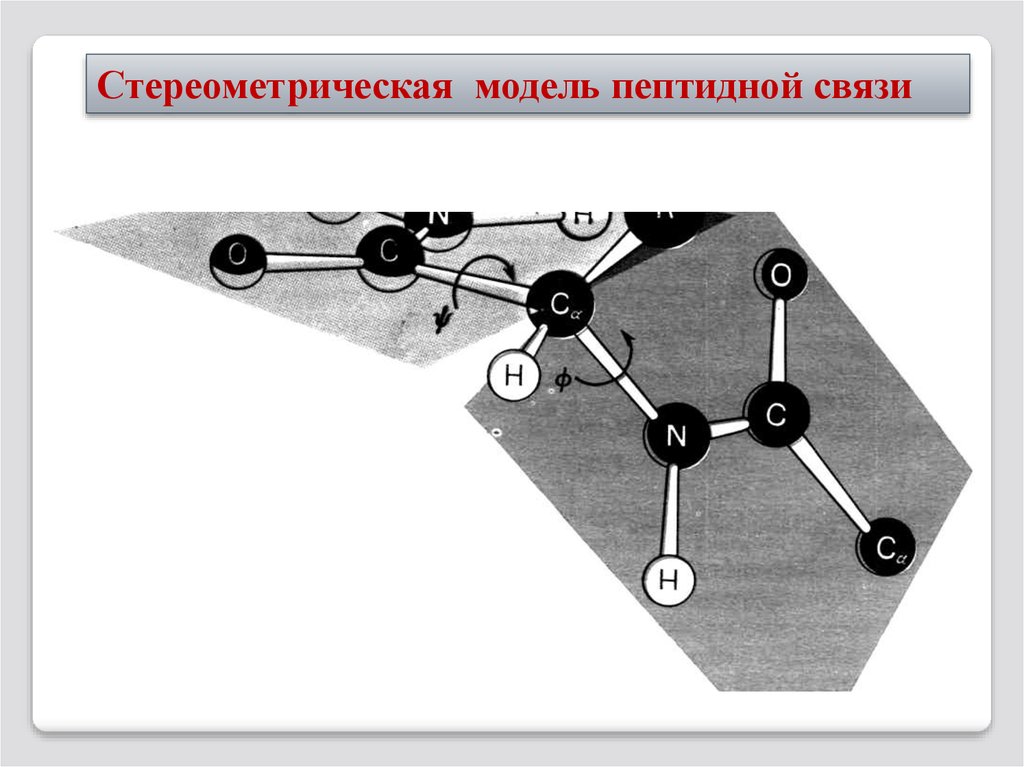
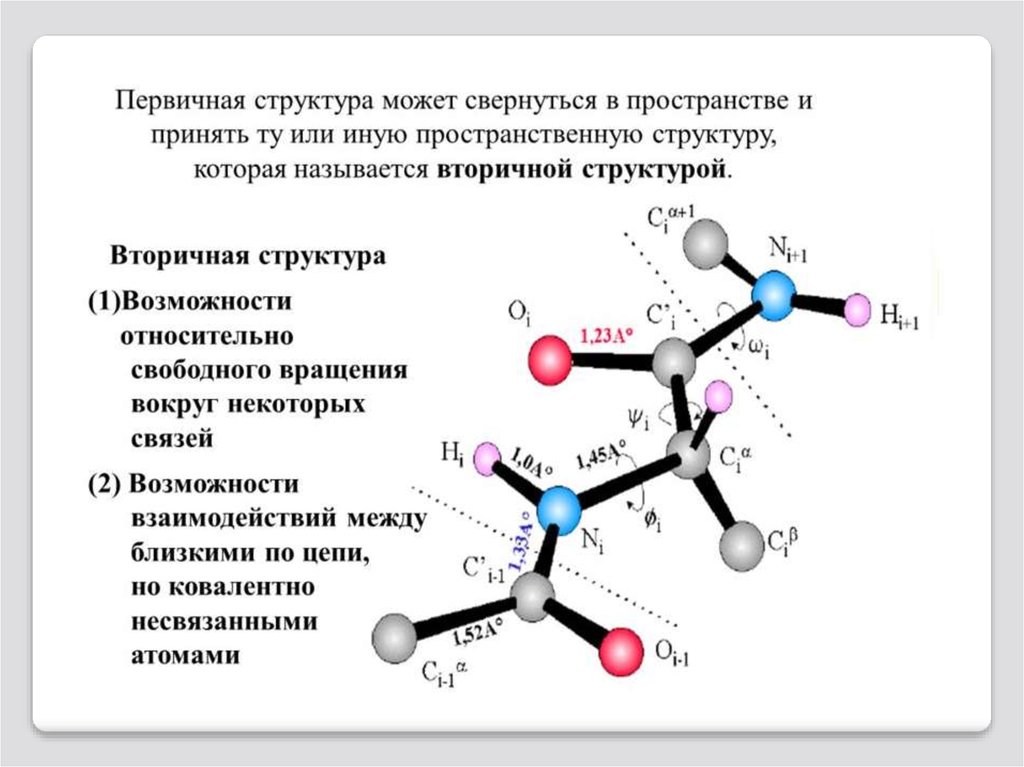
Пептидная связь характеризуется следующимисвойствами:
1. 4 атома пептидной связи лежат в одной
плоскости (рис.7а);
2. Атомы -О- и -Н- пептидной связи
имеют трансориентацию;
3. Длина С-N-связи имеет частично
двойной характер, поэтому она короче, чем
другие связи пептидной цепи и малоподвижна.
Вращение вокруг оси С-N практически
невозможно, что связано с особенностями электронного строения связи.
15.
Стереометрическая модель пептидной связи16.
Стереометрическая модель пептидной связи17.
Соединения, в которых аминокислотысоединены пептидными связями, называется пептидами:
олигопептиды (содержат до 10
аминокислот),
полипептиды (до 10 аминокислот)
белки (свыше 100 аминокислот).
Пептиды
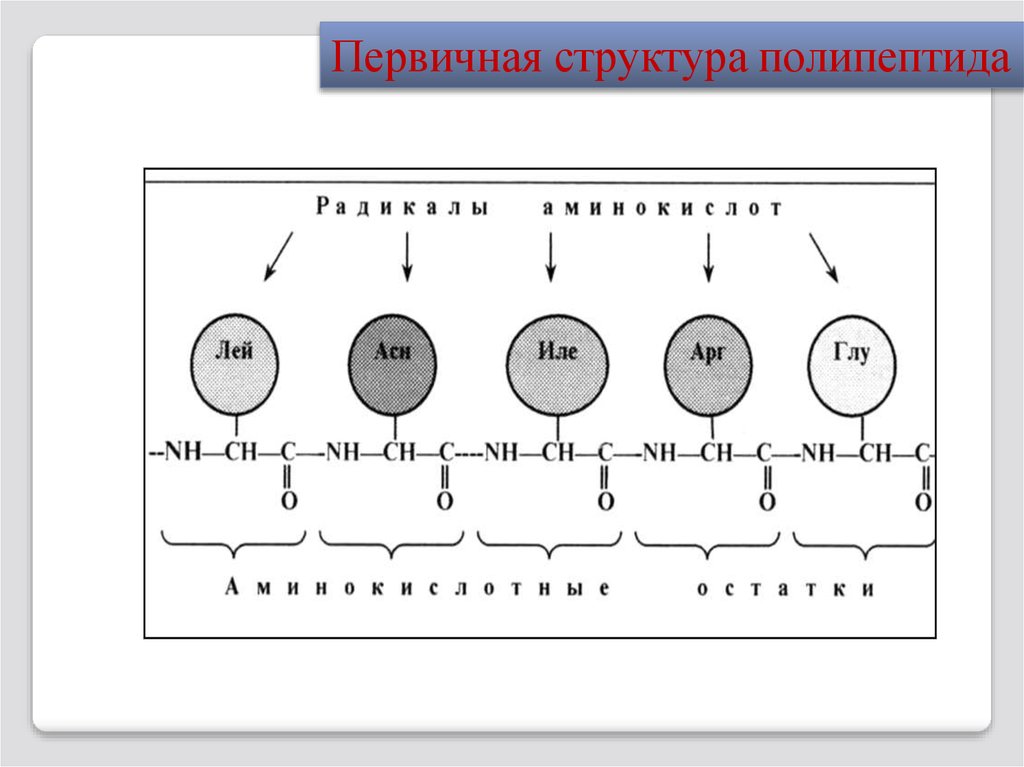
Мономеры полипептида называют
аминокислотными остатками.
18.
ПептидыВ каждом полипептиде на одном
конце имеется аминокислотный остаток со
свобод-ной аминогруппой (-NH2) и
называется N-концевым, а на другом – со
свободной кар-боксильной группой (СООН) и называется C-концевым.
Пептиды пишутся, читаются и
нумеруются с N-конца; аминокислотные остатки обозначаются символами. Например:
Аla-Tyr-Ley-Ser-……….-Cys
19.
20.
Первичная структура полипептида21.
22.
23.
24.
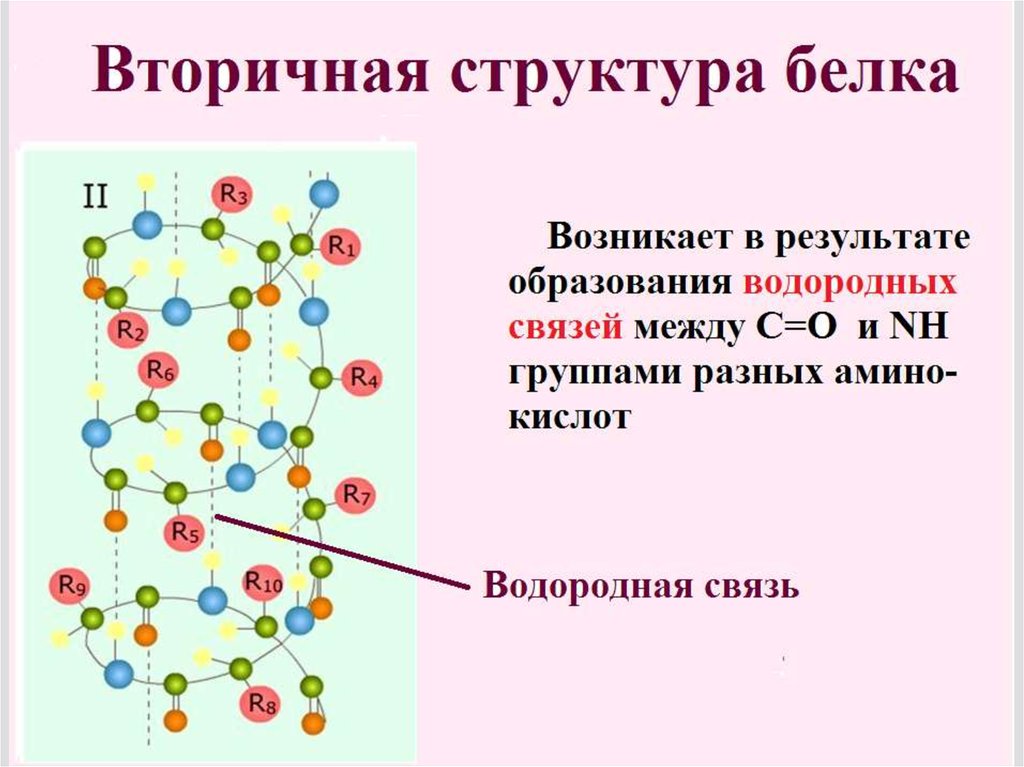
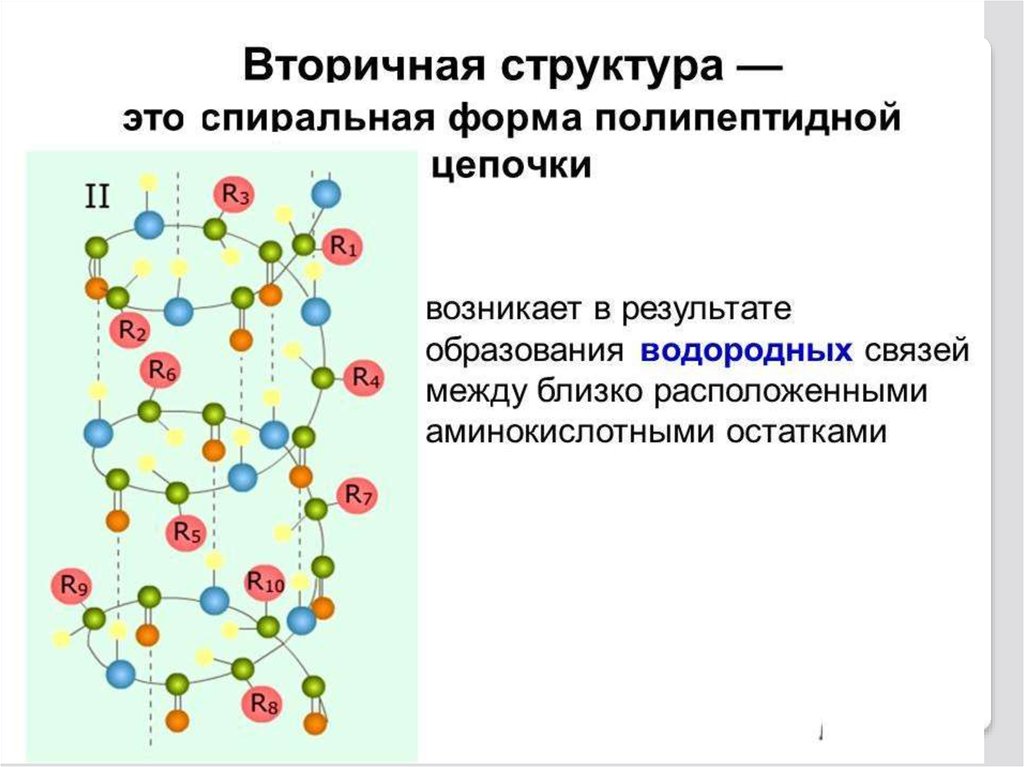
Α-спираль вторичной структурыполипептида
В α-спирали NH-группа одного
остатка аминокислоты соединяется водородной связью с СОгруппой пятого от нее остатка .
В итоге образуется спираль,
где на 1 виток приходится в среднем 3,6 аминокислотных остатков, шаг спирали равен 0,54мм,
диаметр спирали - 0,5мм.
Водородные связи ориентированы вдоль оси спирали
25.
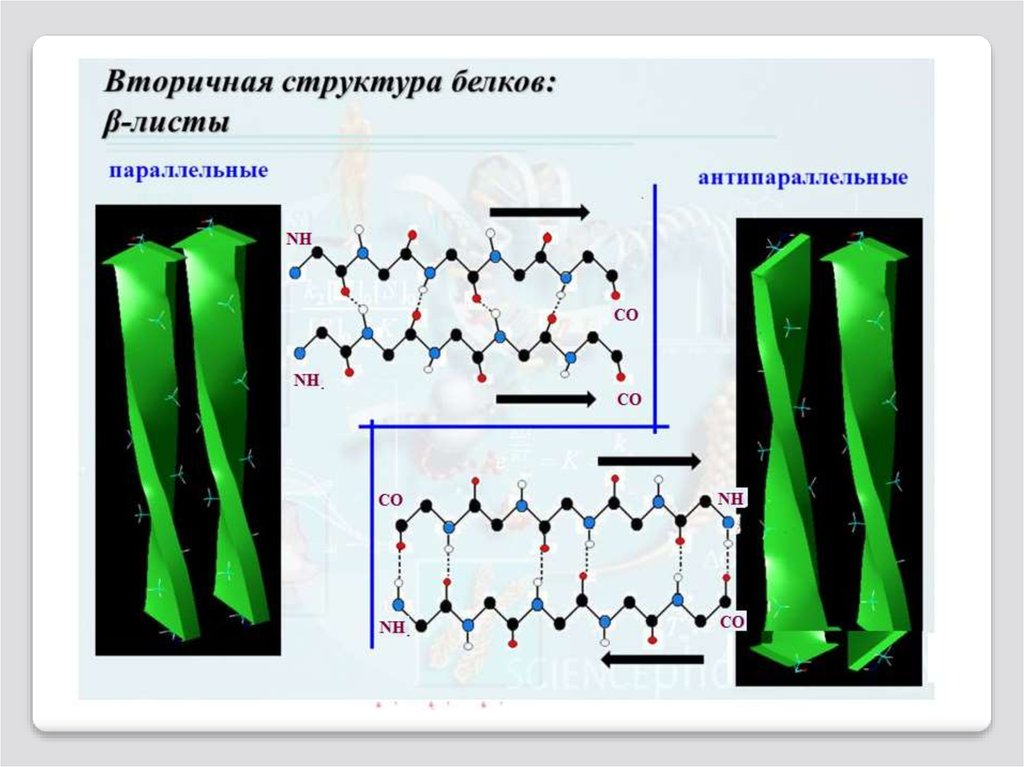
β-складчатый слой вторичной структурыполипептида
В случае β-структуры, или структуры складчатого
листа, полипептидные цепи растянуты, уложены параллельно друг
другу и связаны
между собой водородными связями.
Остов цепи не лежит в одной плоскости, а
вследствие небольших изгибов при αуглеродных атомах образует слегка волнистый слой. Боковые группы располагаются перпендикулярно плоскости слоя.
26.
27.
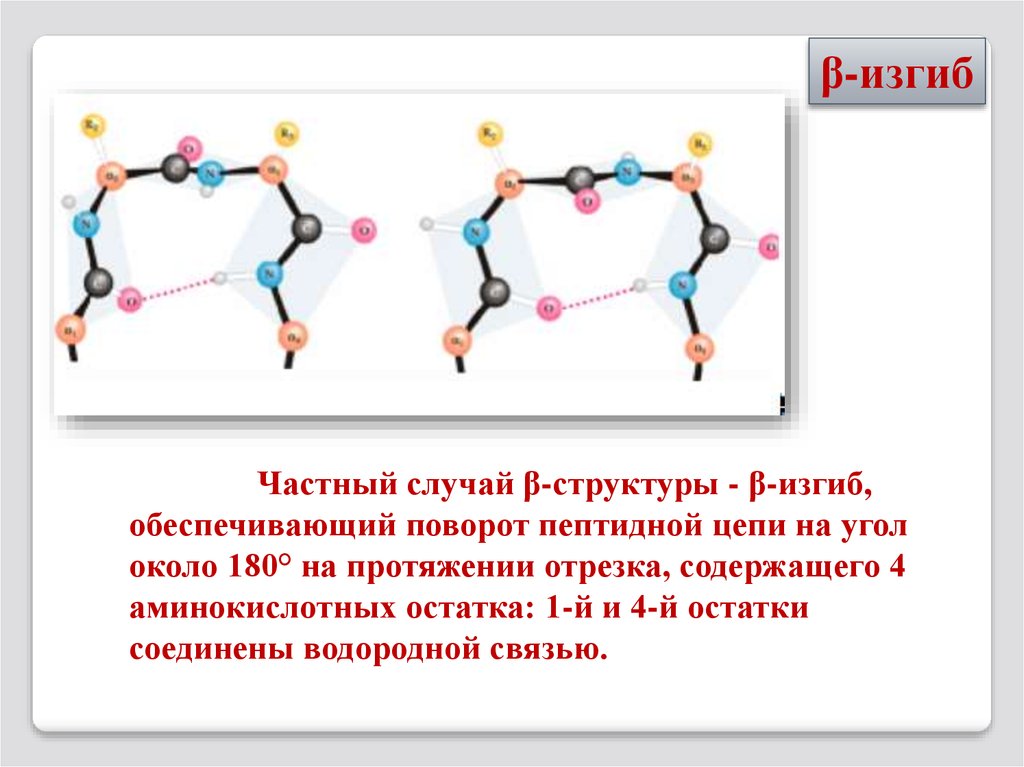
β-изгибЧастный случай β-структуры - β-изгиб,
обеспечивающий поворот пептидной цепи на угол
около 180° на протяжении отрезка, содержащего 4
аминокислотных остатка: 1-й и 4-й остатки
соединены водородной связью.
28.
Супервторичная структура белПространственная структура каждого
белка индивидуальна и определяется его
первичной структурой.
Однако сравнение конформаций разных по структуре и функциям белков
выявило наличие у них похожих сочетаний элементов вторичной структуры.
Такой специфический порядок формирования вторичных структур называют супервторичной структурой белков.
Супервторичная структура формируется
за счёт межрадикальных взаимодействий.
Супервторичная структура в виде α/βбочонка. А - триозофосфатизомераза; Б домен пируваткиназы.
29.
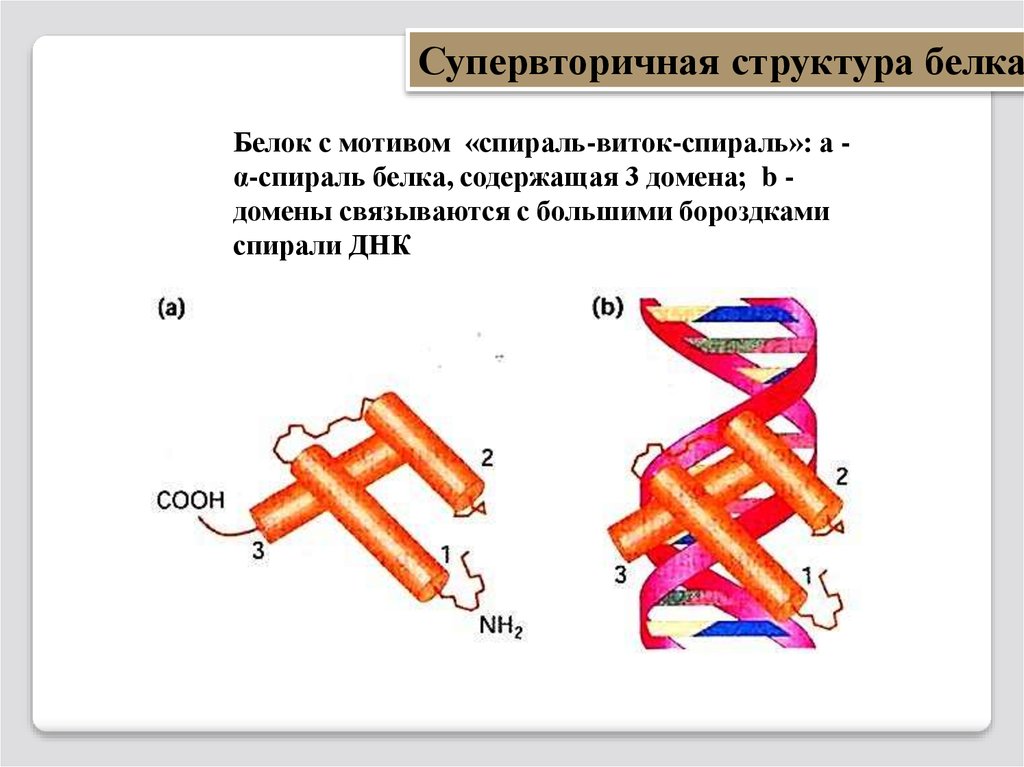
Супервторичная структура белкаБелок с мотивом «спираль-виток-спираль»: а α-спираль белка, содержащая 3 домена; b домены связываются с большими бороздками
спирали ДНК
30.
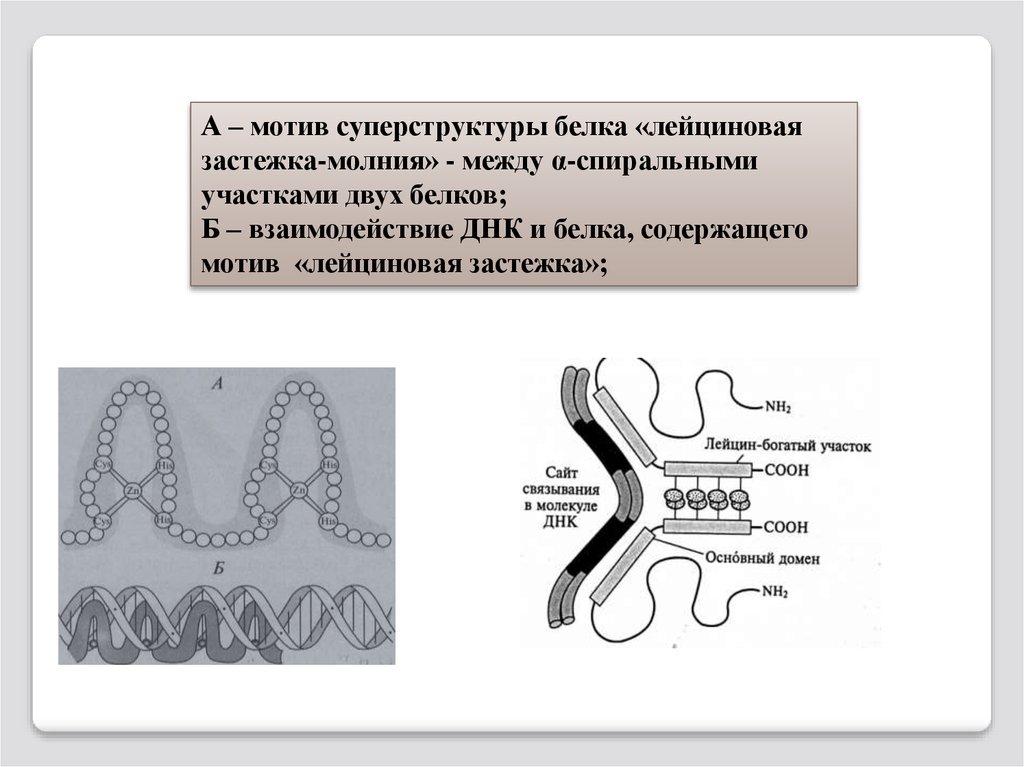
А – мотив суперструктуры белка «лейциноваязастежка-молния» - между α-спиральными
участками двух белков;
Б – взаимодействие ДНК и белка, содержащего
мотив «лейциновая застежка»;
31.
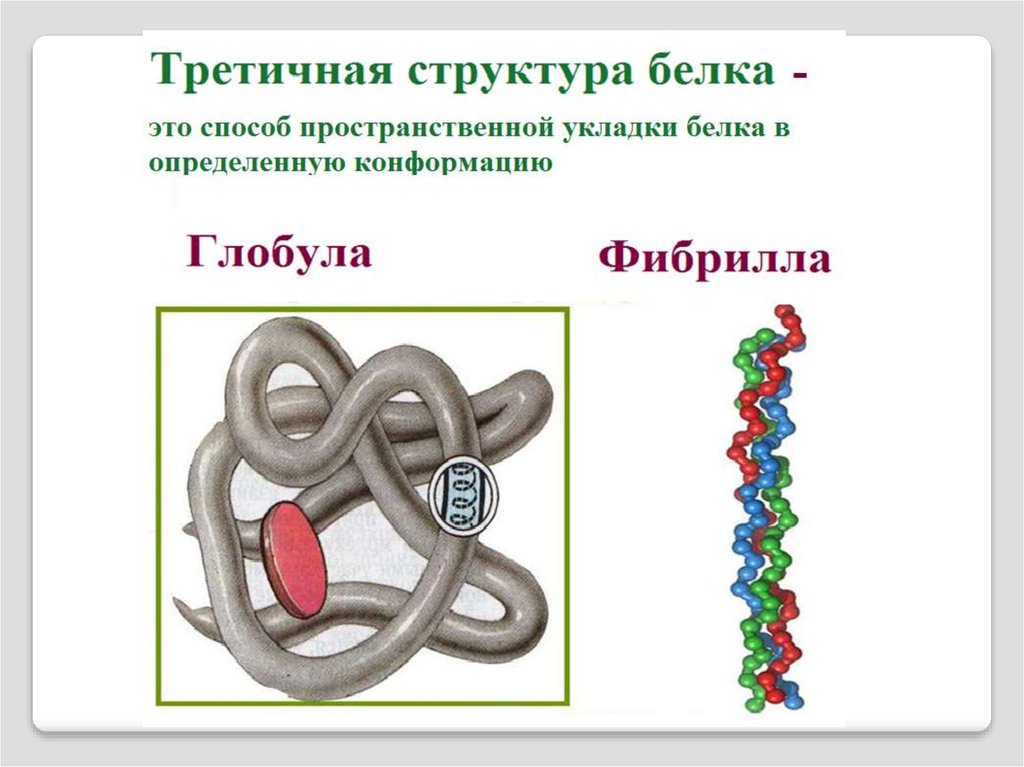
Третичная структура белкаТретичная структура белка – это
трех-мерная пространственная
структура, образующаяся за счет
взаимодействия между радикалами
аминокислот, наход-щимися на
значительном расстоянии друг от друга.
При укладке полипептидная цепь стремиться
при-нять энергетически наиболее выгодную
форму
полипептид в конформации либо α-спирали,
либо β-структуры или бесструктурного клубка,
укладывается в пространстве, образуя конформацию белковой глобулы.
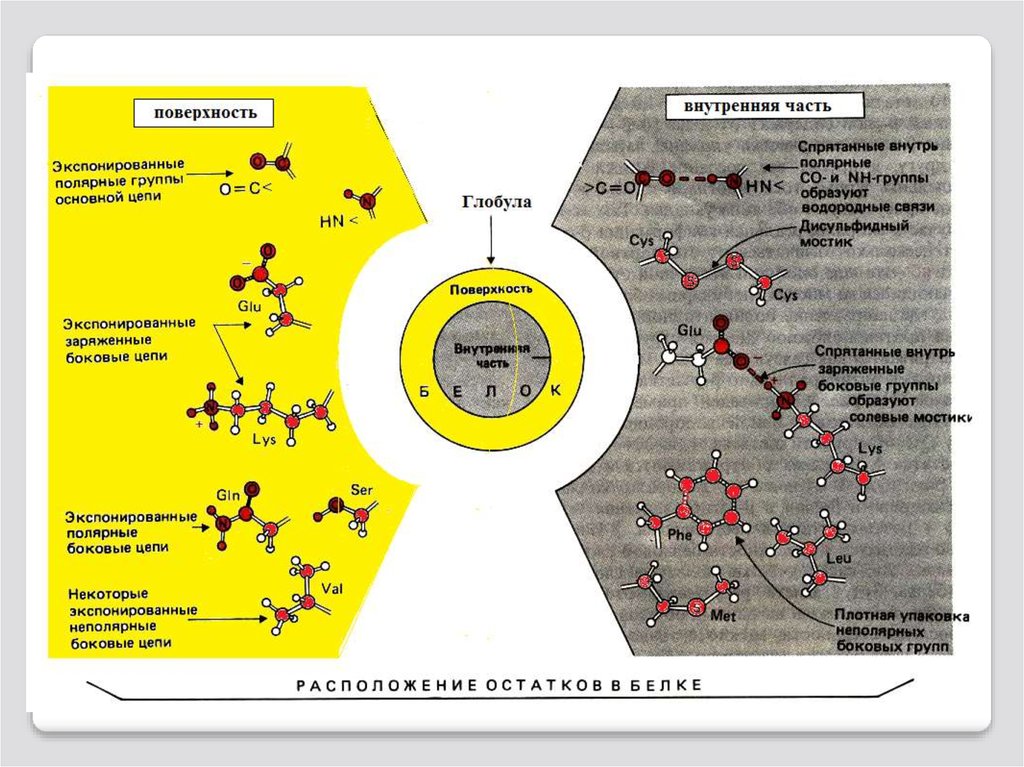
При этом гидрофобные радикалы аминокислот
стремятся к объединению внутри глобулы у бел-ков
растворимых в воде; между ними возникают
гидрофобные и вандерваальсовые взаимодейс-твия.
В результате внутри глобулы образуется гидрофобное
ядро.
32.
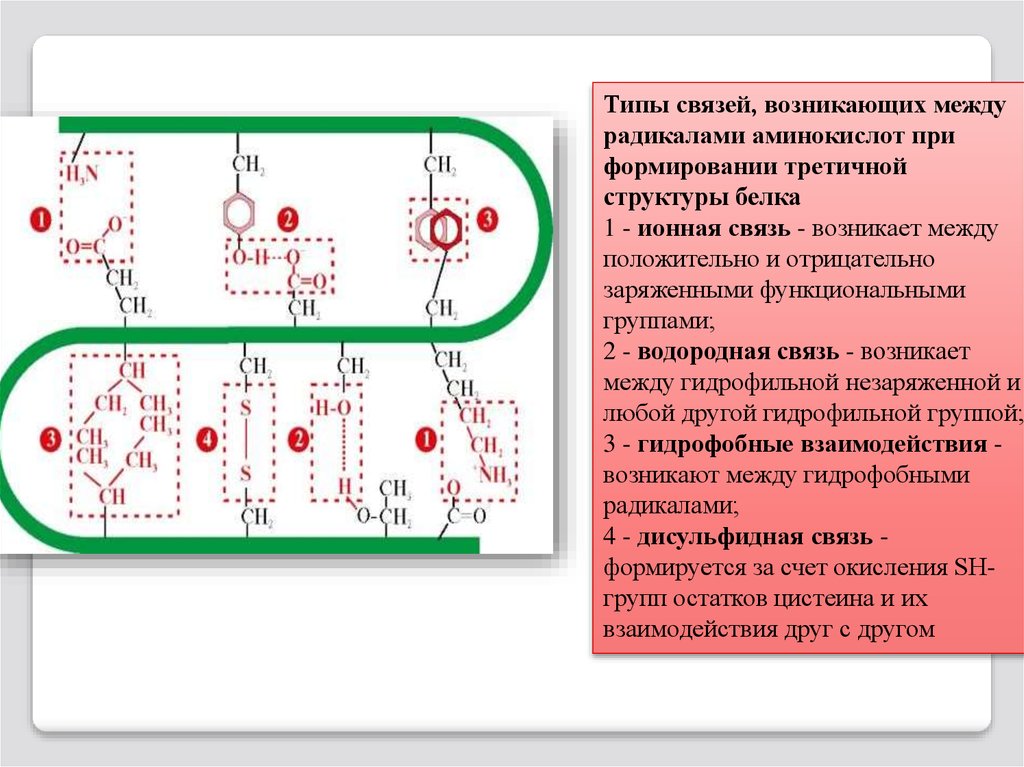
Типы связей, возникающих междурадикалами аминокислот при
формировании третичной
структуры белка
1 - ионная связь - возникает между
положительно и отрицательно
заряженными функциональными
группами;
2 - водородная связь - возникает
между гидрофильной незаряженной и
любой другой гидрофильной группой;
3 - гидрофобные взаимодействия возникают между гидрофобными
радикалами;
4 - дисульфидная связь формируется за счет окисления SHгрупп остатков цистеина и их
взаимодействия друг с другом
33.
34.
35.
Доме́н белка́ — элементтретичной структуры белка,
представляющий собой достаточно стабильную и независимую подструктуру белка, чей фолдинг проходит
независимо от остальных частей. В состав домена обычно
входит несколько элементов
вторичной структуры.
Доме́н
36.
Для выполнения белком его специфических функций ипридания ему активности необходимым условием является
присоединение к нему другого вещества лиганда.
Лигандами могут быть как низкомолекулярные
вещества, так и макромолекулы, в том числе и белок.
Взаимодействие белка с лигандом специфично и определяется
участком белковой молекулы, называемым активным центром
или центром связывания белка с лигандом.
Лигандами могут быть
неорганические (часто
ионы металлов) и органические низкомолекулярные и высокомолекулярные вещества.
Лиганды
37.
Активный центр – это участок молекулы белка, имеющийформу щели или узкого углубления – кармана;
сформирован радикалами аминокислот, собранными на
определенном пространстве в процессе фолдинга третичной
структуры данного белка и способных комплиментарно связываться с лигандом.
Свойства активного центра зависят от химических
свойств аминокислотных остатков в его составе и их точной
взаимной ориентации в пространстве. Поэтому малейшие
изменения в структуре белка приводят к изменению химических и физических свойств радикалов, нарушают структуру
активного центра и связывание белка с лигандом.
Подобное наблюдается при денатурации, когда активный
центр разрушается и утрачивается функциональная
активность белка.
38.
Связывание белка с лигандом высокоспецифично иобеспечивается комплиментарностью структуры активного
центра белка структуре лиганда .
Комплементарность - это пространственное и химическое
соответствие взаимодействующих молекул. Лиганд должен
пространственно совпадать с конформацией активного
центра, затем между лигандом и радикалами активного
центра возникают химические связи, удерживающие лиганд в
активном центре.
39.
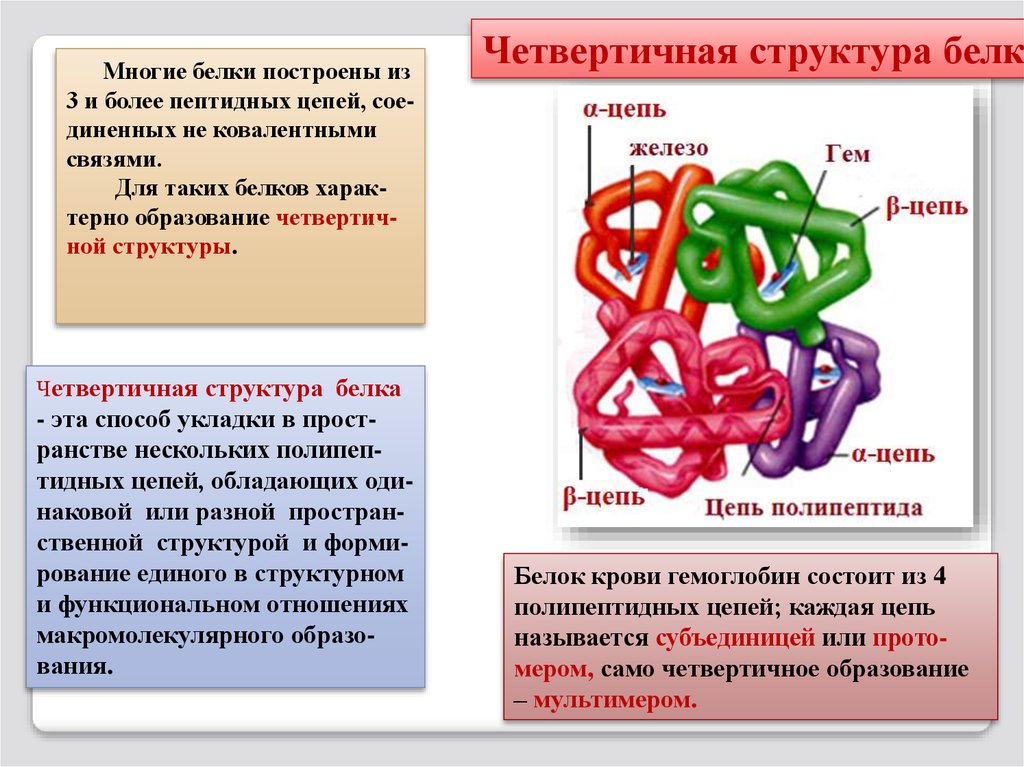
Многие белки построены из3 и более пептидных цепей, соединенных не ковалентными
связями.
Для таких белков характерно образование четвертичной структуры.
Четвертичная структура белка
Четвертичная структура белка
- эта способ укладки в пространстве нескольких полипептидных цепей, обладающих одинаковой или разной пространственной структурой и формирование единого в структурном
и функциональном отношениях
макромолекулярного образования.
Белок крови гемоглобин состоит из 4
полипептидных цепей; каждая цепь
называется субъединицей или протомером, само четвертичное образование
– мультимером.
40.
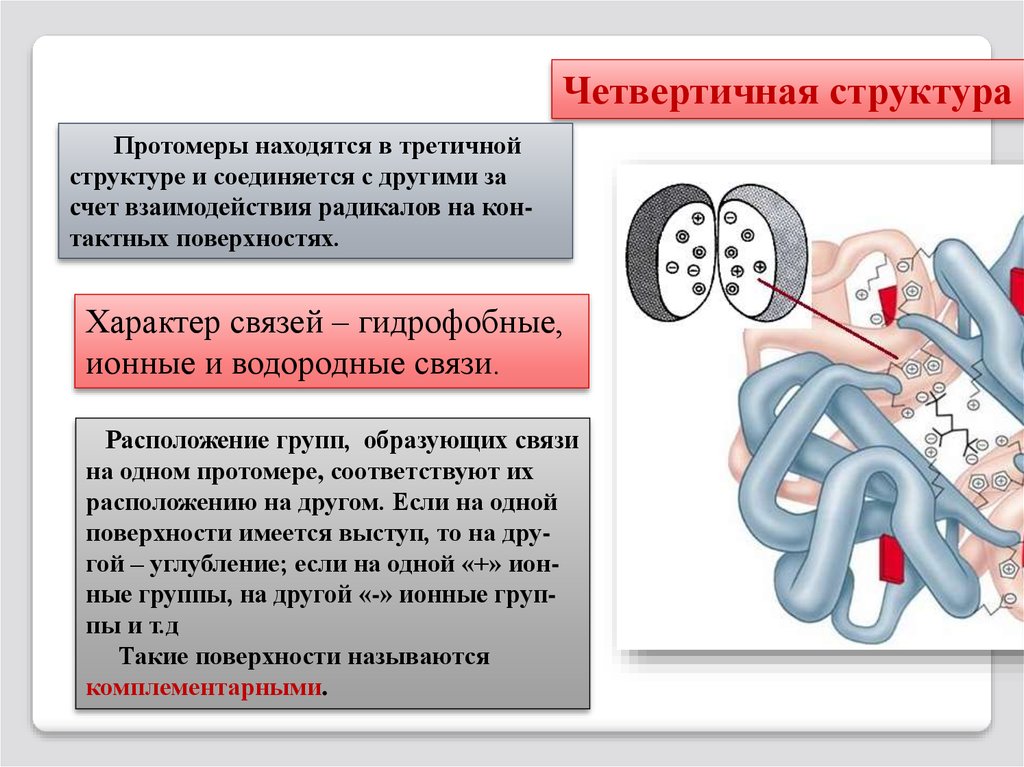
Четвертичная структура бПротомеры находятся в третичной
структуре и соединяется с другими за
счет взаимодействия радикалов на контактных поверхностях.
Характер связей – гидрофобные,
ионные и водородные связи.
Расположение групп, образующих связи
на одном протомере, соответствуют их
расположению на другом. Если на одной
поверхности имеется выступ, то на другой – углубление; если на одной «+» ионные группы, на другой «-» ионные группы и т.д
Такие поверхности называются
комплементарными.
41.
Четвертичная структура белкБелок в четвертичной структуре является комплексом, который является
единым целым и выполняет биологическую функцию, несвойственную отдельно
взятым протомерам.
Белки, состоящие из нескольких полипептидных цепей, называются олигомерными белками. Количество протомеров
колеблется от 2 до 10, редко больше
(ферритин – 24 протомера).
Субъединичная структура глутаматсинтетазы: а – протомер, б – мультимер
белка
42.
43.
44.
Фолдинг белПервичная структура белка
формируется в результате трансляции
белка.
Пептидная цепь претерпевает
пространственные изменения, приводящие к ее сворачиванию в правильную трехмерную структуру.
Этот процесс
называется
фолдингом.
Фолдинг включает процессы
образования вторичной, третичной и
четвертичной структур белка.
45.
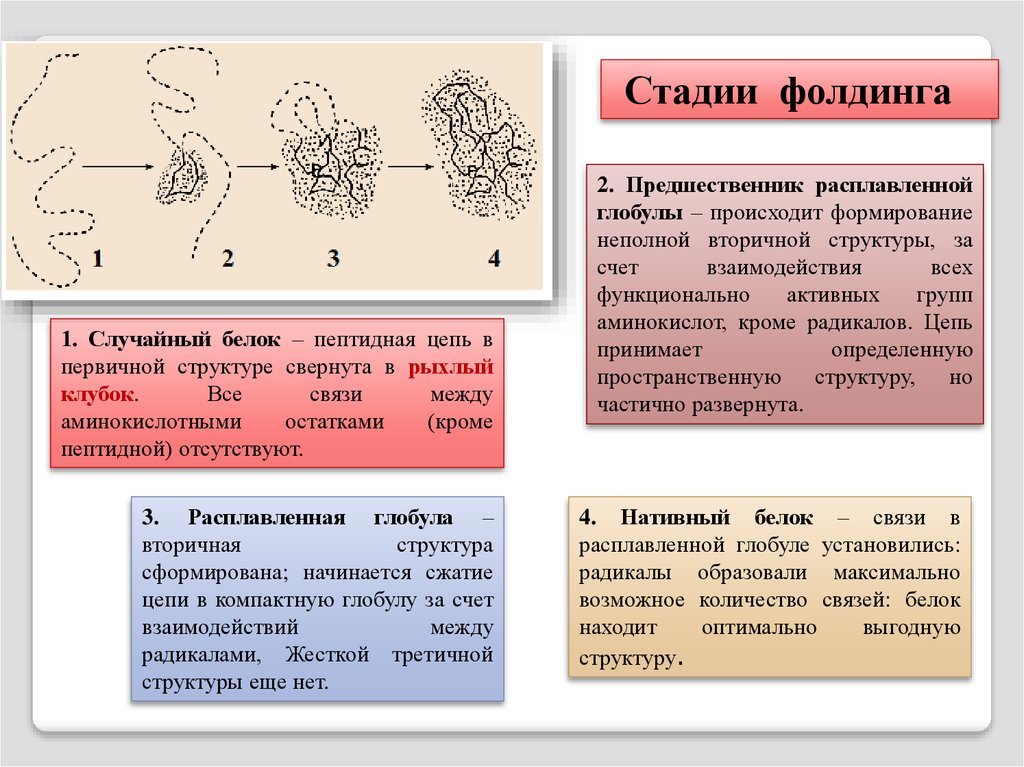
Стадии фолдинга1. Случайный белок – пептидная цепь в
первичной структуре свернута в рыхлый
клубок.
Все
связи
между
аминокислотными
остатками
(кроме
пептидной) отсутствуют.
3. Расплавленная глобула –
вторичная
структура
сформирована; начинается сжатие
цепи в компактную глобулу за счет
взаимодействий
между
радикалами, Жесткой третичной
структуры еще нет.
2. Предшественник расплавленной
глобулы – происходит формирование
неполной вторичной структуры, за
счет
взаимодействия
всех
функционально
активных
групп
аминокислот, кроме радикалов. Цепь
принимает
определенную
пространственную структуру, но
частично развернута.
4. Нативный белок – связи в
расплавленной глобуле установились:
радикалы образовали максимально
возможное количество связей: белок
находит
оптимально
выгодную
структуру.
46.
Крупные молекулы белков с большим молекулярнымвесом и сложной структурой в процессе фолдинга в
условиях высокой концентрации белков в клетке могут
взаимодействовать друг с другом, за счет своих
реакционноспособных радикалов. Гидрофобные радикалы
на поверхности молекул склонны к объединению
(агрегации), что нарушает ход их правильного фолдинга.
Поэтому на время фолдинга реакционноспособные
аминокислотные остатки одних белков должны быть
отделены от аминокислотных остатков других белков. Эту
функцию выполняют вспомогательные белки. Они
связываются с белками, находящимися в неустойчивом,
склонном к агрегации, состоянии, стабилизируют их
конформацию и обеспечивают их «правильный» фолдинг.
Такие белки называются факторами фолдинга и
делятся на две группы: фолдазы и шапероны.
47.
Фолдазы или ферменты фолдинга – это белки скаталитической функцией и требуются в
концентрациях значительно меньших, чем
катализируемые ими белки. Известно два вида фолдаз:
ПДИ и ППИ.
ПДИ (протеиндисульфидизомераза) каталитирует
перемещение (раз- рыв одних и образование других)
дисульфидных связей белка. Без этого фермента
любая, образующаяся -Ѕ-Ѕ- связь, фиксировалась бы
случайно, что с большой долей вероятности, проводило
бы к образованию непра- вильных конформаций.
ППИ (пептидилпролилизомераза) обеспечивает
«правильный» фолдинг белка, содержащего пролин.
48.
49.
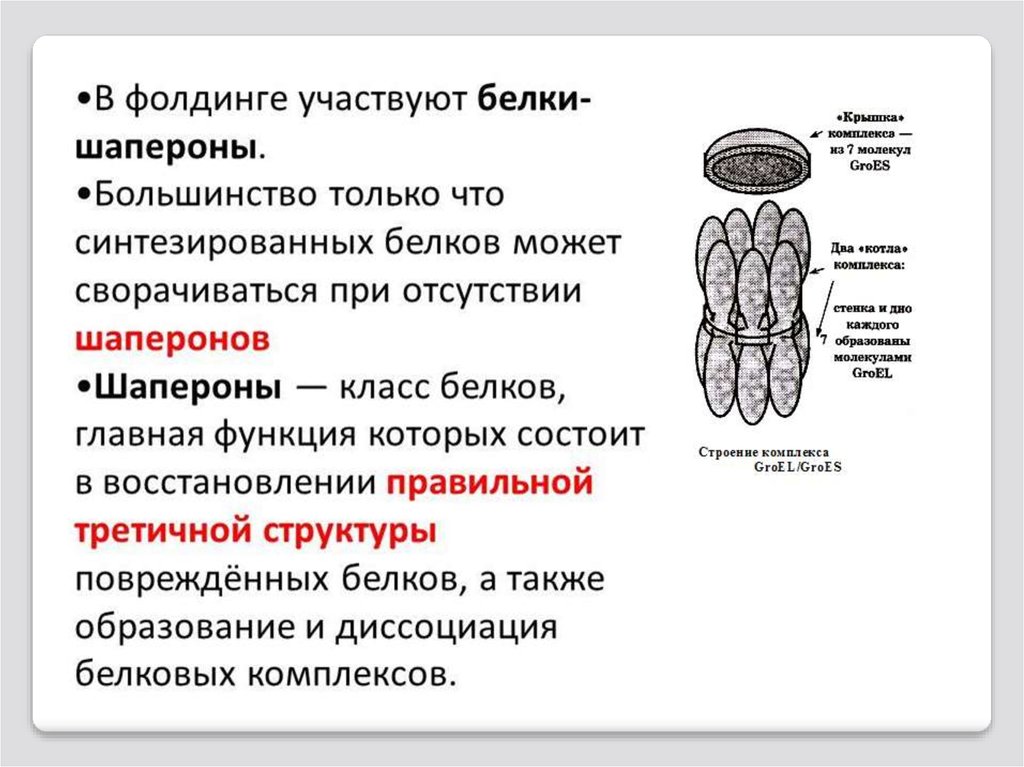
Шапероны (от франц. shaperon - няня) – это белки сразными механизмами действия; они требуется в колиествах, близких к количеству белков, фолдинг которых они
обеспечивают. Кроме того, шапероны не входят в состав
конечных продуктов фолдинга. В соответствии с молекулярной массой шапероны делятся на 6 групп:
Высокомолекулярные шапероны от 100 до 110
кДа;
Ш-90 - молекулярная масса от 83-90 кДа;
Ш-70 - молекулярная масса от 66-70кДа;
Ш-60 - молекулярная масса от 60 кДа;
Ш-40 - молекулярная масса от 40 кДа;
Низкомолекулярные шапероны от 15 до 30 кДа.
50.
Шапероны делятся на:Конститутивные - синтез
таких шаперонов не зависит от стрессовых воздействий на организм;
Индуцибельные - их синтез
в обычных условиях идет с
низкой скоростью; при наличии стрессовых условий резко увеличивается.
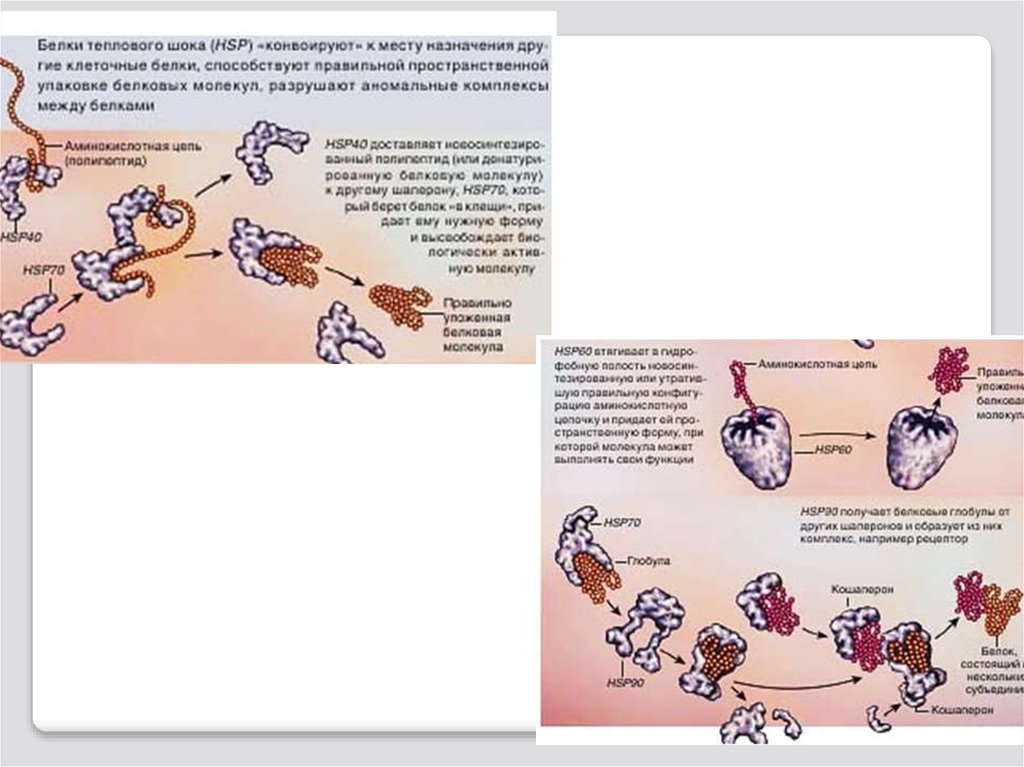
Индуцибельные шапероны относят к «белкам
теплового шока»; их синтез резко возрастает
практически во всех клетках при любых
стрессовых влияниях. Название «белки теплового
шока» возникло в результате того, что впервые эти
были обнаружены в клетках микроорганизмов при
воздействии высокими температурами.
51.
52.
53.
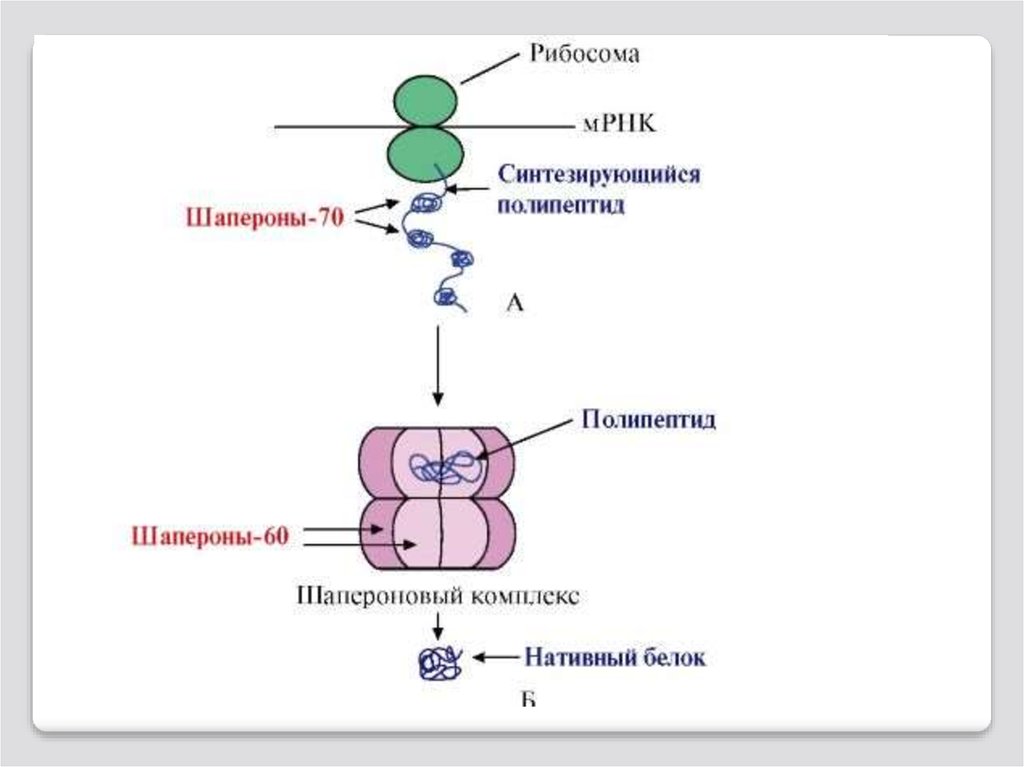
Функции и механизм действия шапероновІ. Контроль за обеспечением «правильного»
фолдинга новообразованных молекул белка
ІІ. Вторая функция шаперонов – контроль за
рефолдингом
ІІІ. Шапероны участвуют в некоторых видах внутриклеточного транспорта белков: транспорт новосинтеризованных белков в лизосомы, митохондрии и другие
органоиды, а также транспорт старых, отслуживших
белков, не поддающиеся рефолдингу в лизосомы.
ІV. Шапероны участвуют в поддержании ряда
белков в состоянии определенной
конформации, как бы незавершенном
фолдинге.
54.
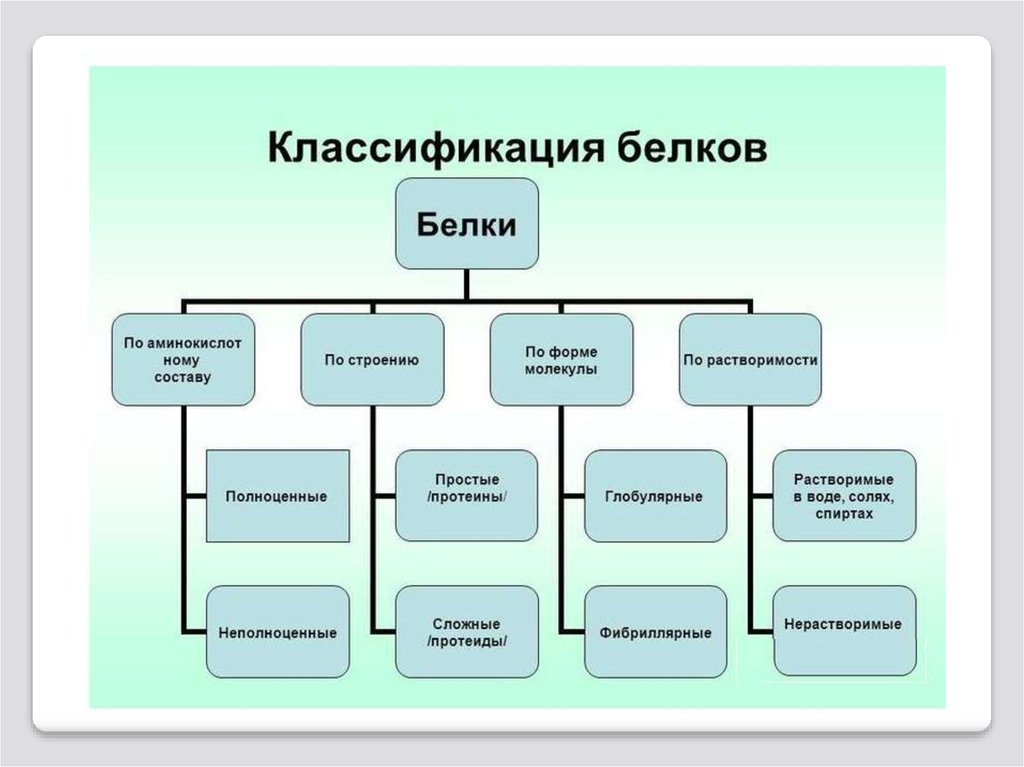
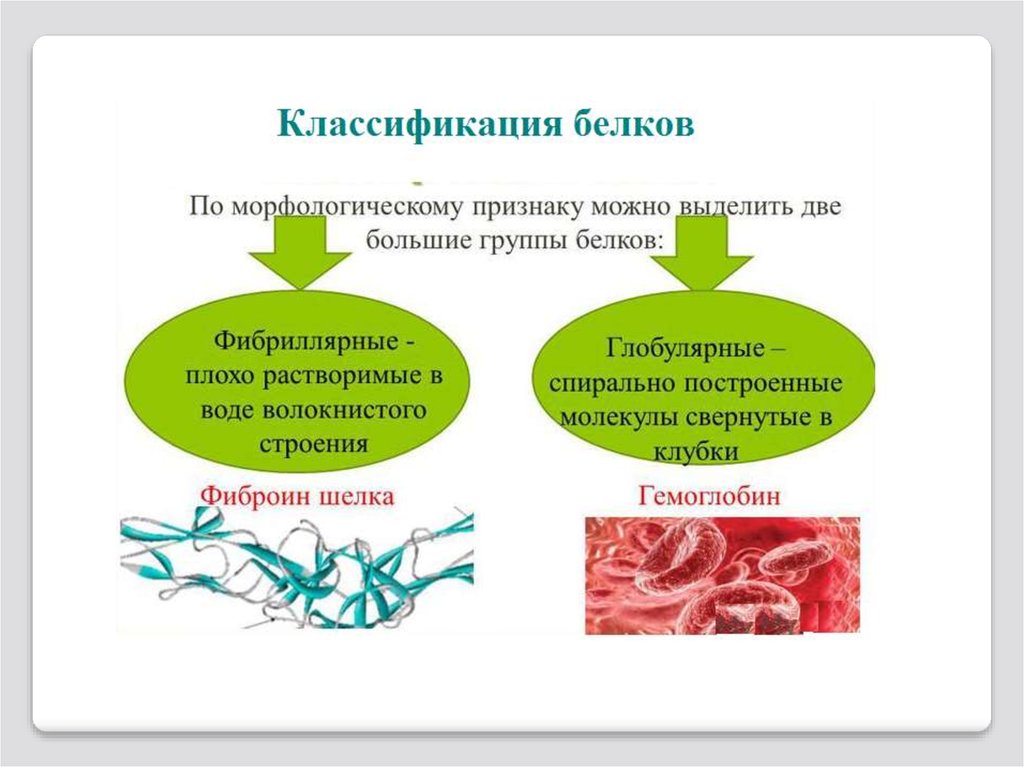
55. Классификация белков
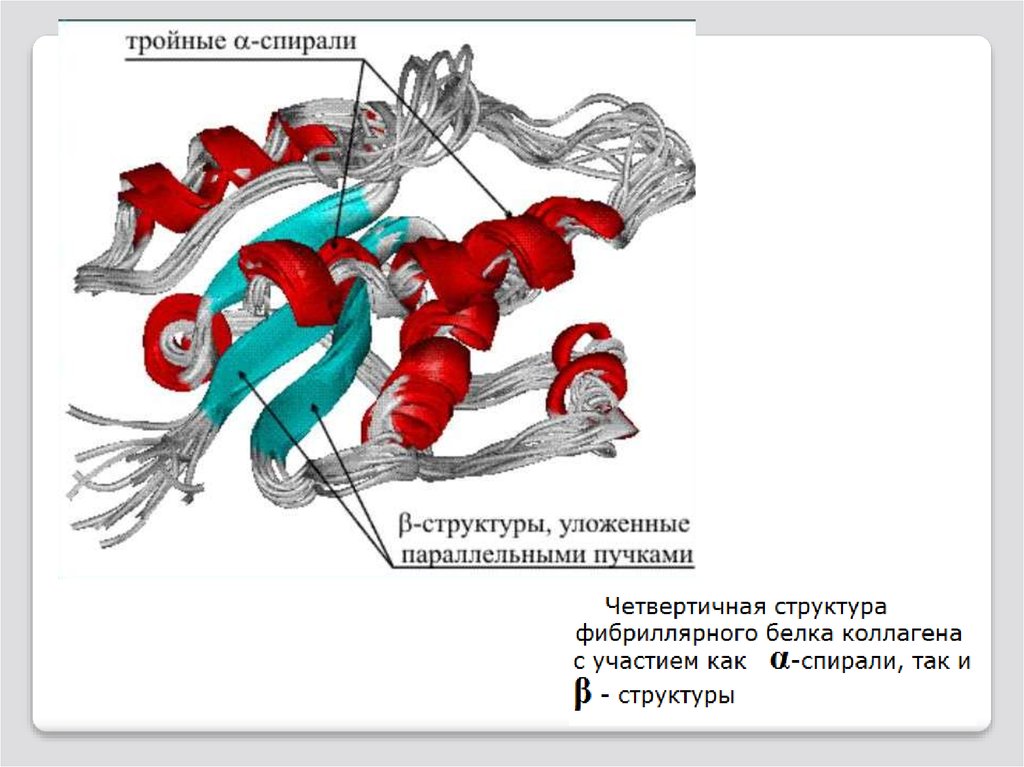
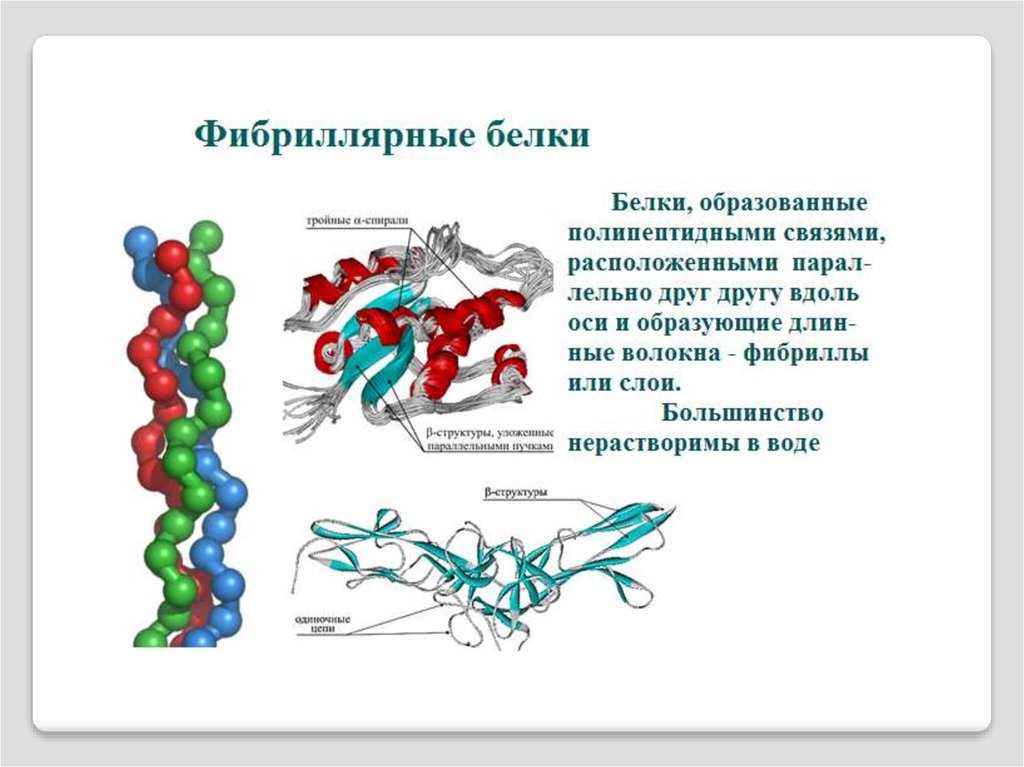
Белки можно классифицировать:по форме (глобулярные и фибриллярные),
по молекулярной массе (низко-, высокомолекулярные и др.);
по химическому строению (отсутствие или наличию небелковой
части): простые и сложные;
по функциям и локализации в клетке (ядерные,
цитоплазматические, лизосомальные, митохондриальные и др.),
по возможности регулировать синтез белков (конститутивные,
синтез которых идет с постоянной скоростью и индуцибельные,
синтез которых возрастает при воздействии факторов среды),
по продолжительности жизни в клетке (очень быстро
обновляющиеся, менее чем через час и медленно обновляющиеся в
течении недель и месяцев),
по схожим участкам первичной структуры и родственным
функциям (семейства белков): гемоглобины, иммуноглобулины,
гистоны, серины.
Классификация белков
56.
57.
58.
59.
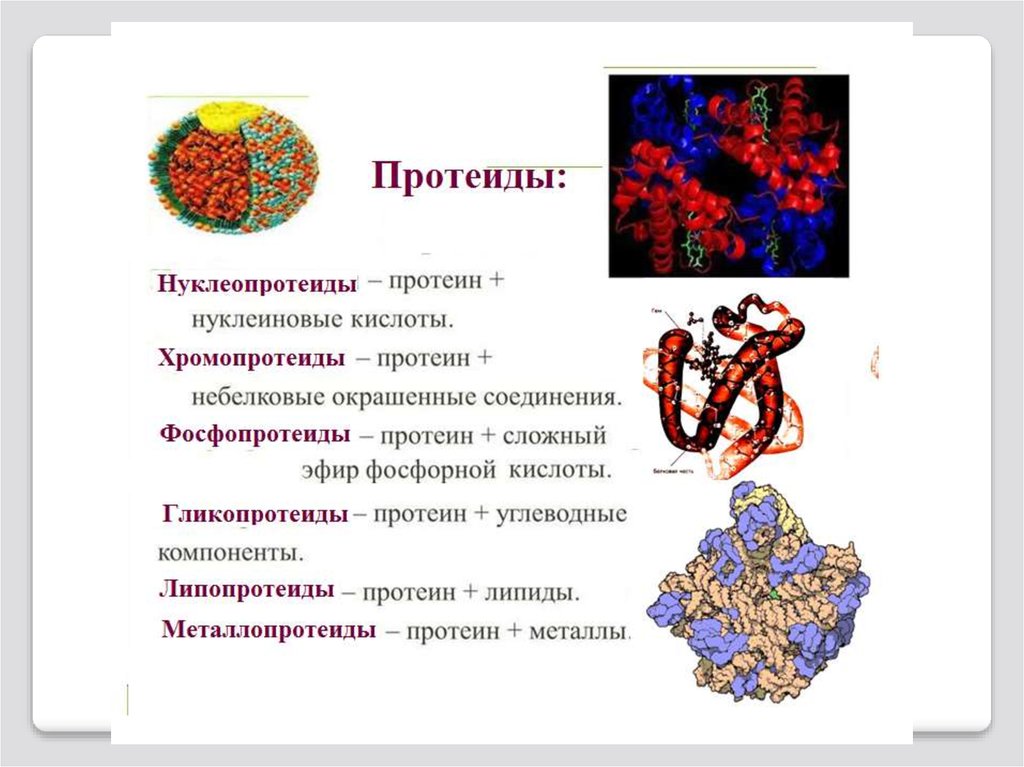
Некоторые сложные белкиБелки
Металлопротеины
Фосфопротеины
Гемопротеины
Флавопротеины
Гликопротеины
Протеогликаны
Липопротеины
Нуклеопротеины
Рибонуклеопротеины
(рибосомы и др.)
Дезоксирибонуклеопротеин
ы
(хроматин)
Простетическая группа
Ионы металлов
Н3РО4
Гем (ферропротопорфирин)
Флавиннуклеотиды
(прозводственные
рибофлавина В12)
Моносахариды
и
олигосахариды
Гликозаминглюканы
(мукополисахариды)
Триглицериды и сложные
липиды
РНК
ДНК
60.
61.
62.
Глобулярные белкиГлобулярные белки — белки, в молекулах
которых полипептидные цепи плотно свёрнуты
в глобулы (компактные шарообразные третичные структуры).
Глобулярная структура белков обусловлена
гидрофобно-гидрофильными взаимодействями: снаружи гидрофильные (имеющие
водородные соединения с окружающей средой), а внутри гидрофобные (отталкивающие
воду).
К глобулярным белкам относятся ферменты, иммуноглобулины,некоторые гормоны бел
ковой природы (например,инсулин) а также
другие белки, выполняющие транспортные,
регуляторные и вспомогательные функции.
63.
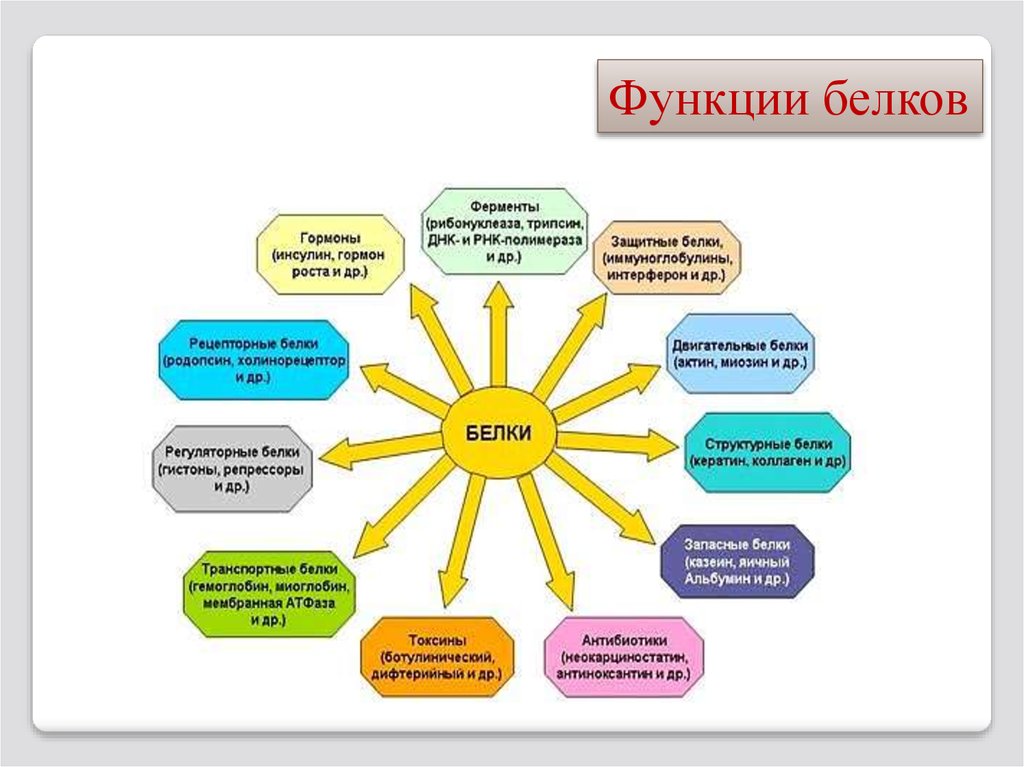
Функции белков64.
Денатурация белков (лат. denaturatus— лишённый природных свойств;
— изменение нативной конформации
белковой молекулы под действием
различных дестабилизирующих
факторов.
А) высокая или низкая температура;
Б) механическое воздействие;
В) облучение;
Г) действие спирта;
Д) действие солей тяжелых металлов
65. Информационные макромолекулы
Нуклеиновые кислоты66.
Нуклеиновые кислоты – этовысокомолекулярные
биополимеры ,
распадающиеся при
гидролизе на азотистые
основания (А, Г, Т, Ц, У),
пентозу (рибоза или
дезоксирибоза) и
фосфорную кислоту.
67.
Открытие НКНуклеиновые кислоты были
открыты в 1868 г. швейцарским
врачом Ф.Мишером
Впервые обнаружены в ядре
(«нуклеус» - ядро)
68.
1953Открыта
структура ДНК
Дата рождения
молекулярной
биологии
69.
Нобелевская премия 196270.
ДНК – самая большая молекула в клетке.Она намного больше белков и РНК
Каждая хромосома = одна молекула
ДНК
23 хромосомы человека = 23
молекулы ДНК
ДНК – это молекула-текст. В последовательности ее нуклеотидов записана вся наследственная программа организма
71.
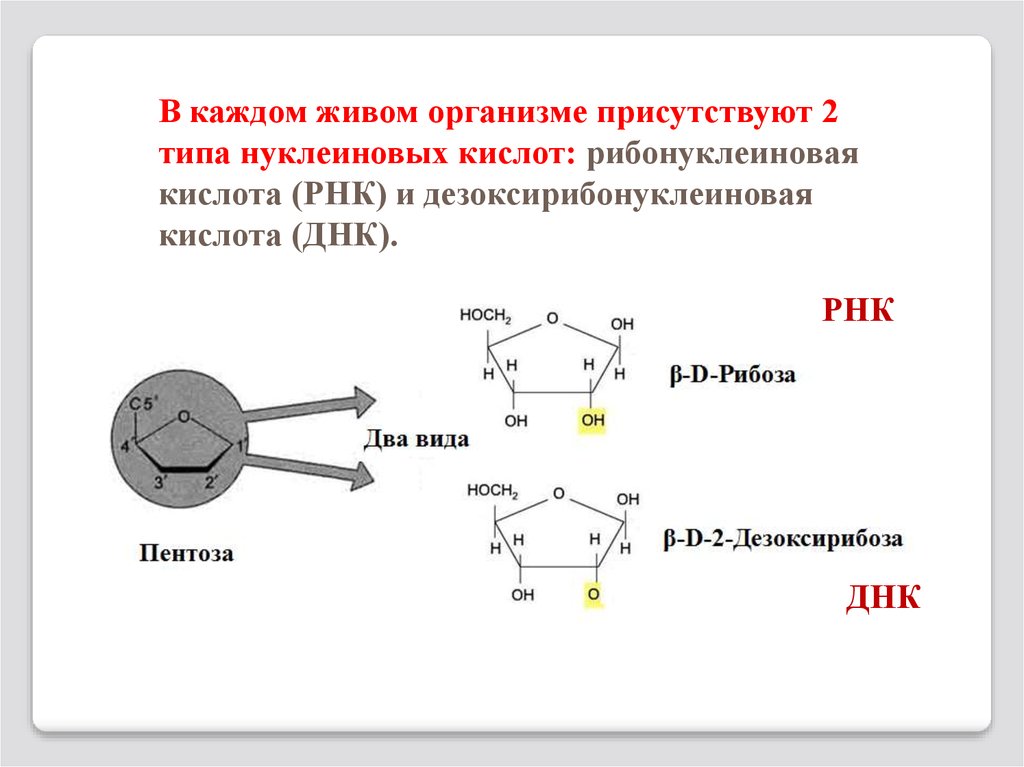
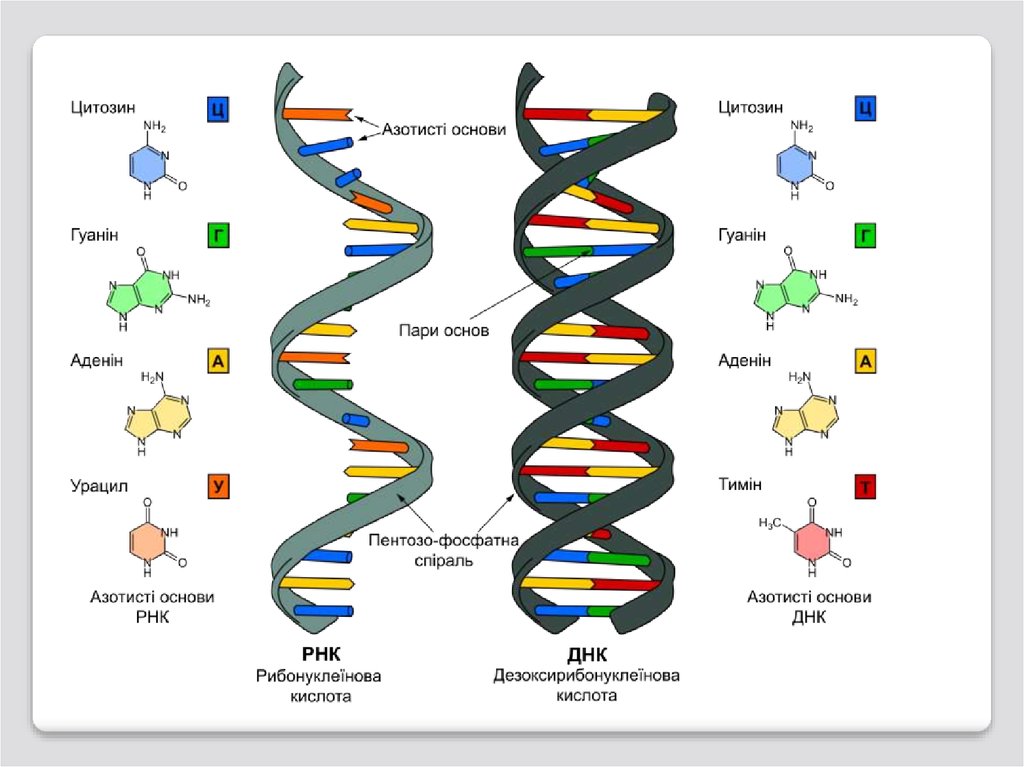
В каждом живом организме присутствуют 2типа нуклеиновых кислот: рибонуклеиновая
кислота (РНК) и дезоксирибонуклеиновая
кислота (ДНК).
РНК
ДНК
72.
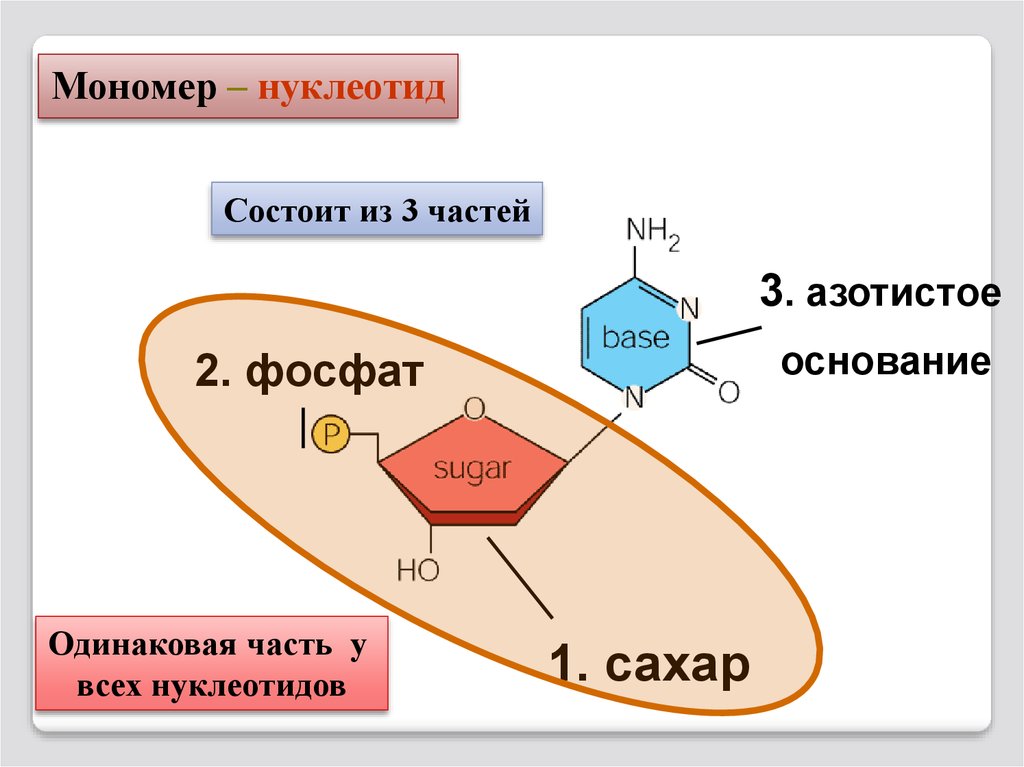
Мономер – нуклеотидСостоит из 3 частей
3. азотистое
основание
2. фосфат
Одинаковая часть у
всех нуклеотидов
1. сахар
73.
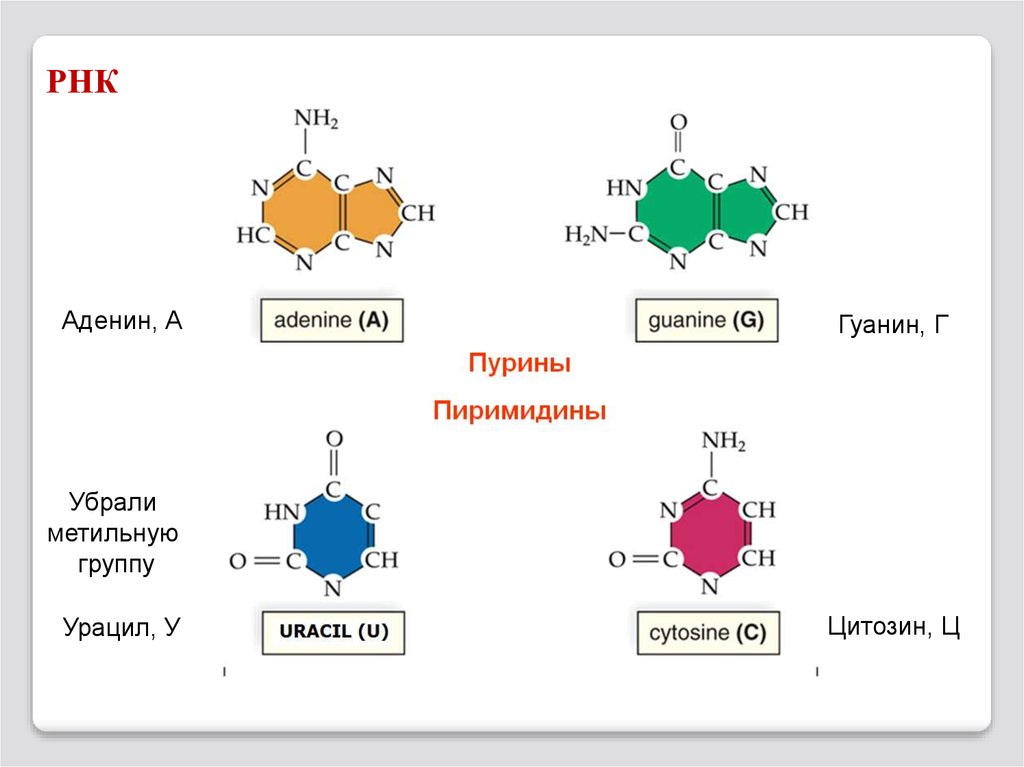
РНКАденин, А
Гуанин, Г
Убрали
метильную
группу
Урацил, У
Цитозин, Ц
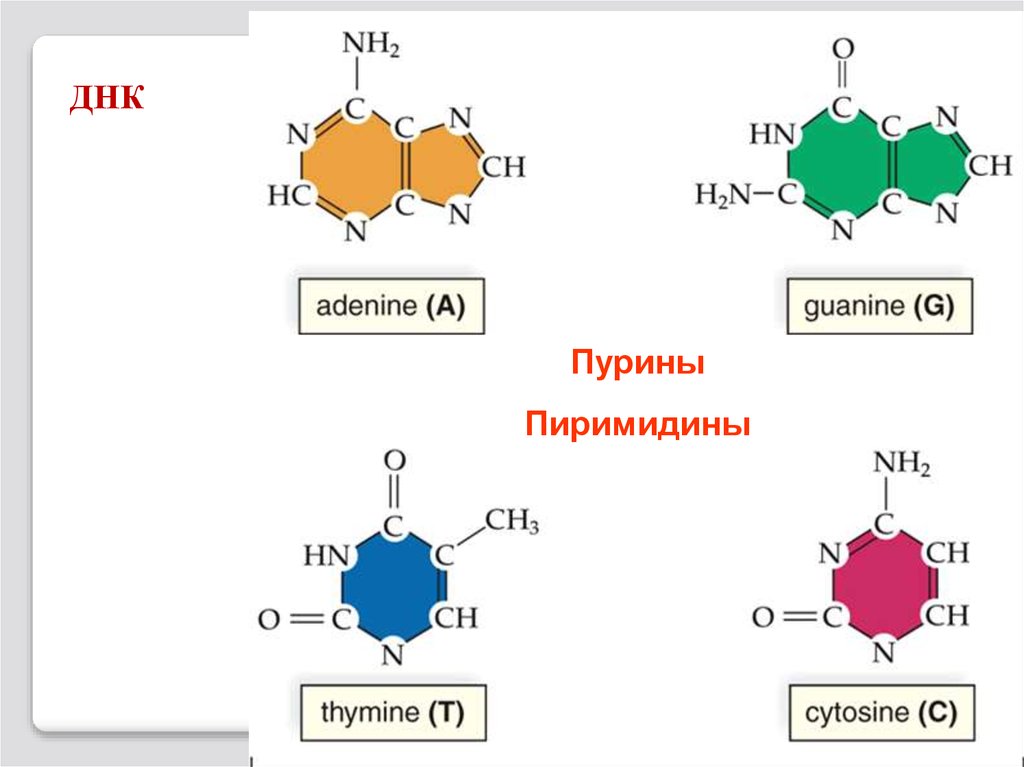
74.
ДНКПурины
Пиримидины
75.
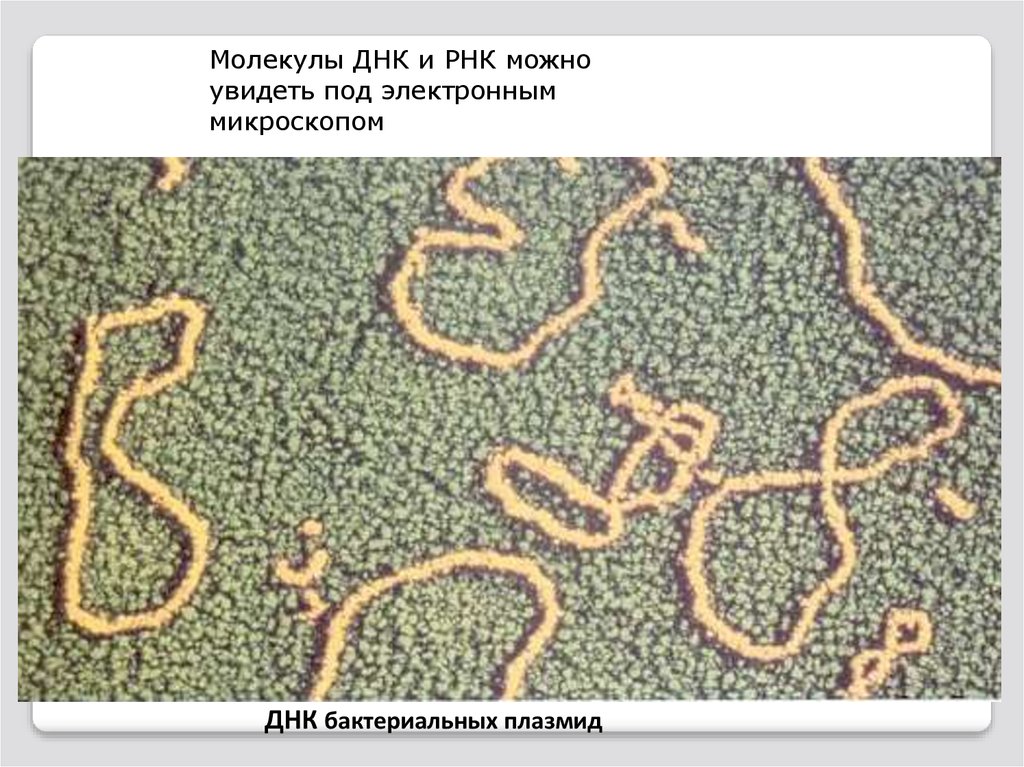
Молекулы ДНК и РНК можноувидеть под электронным
микроскопом
ДНК бактериальных плазмид
76.
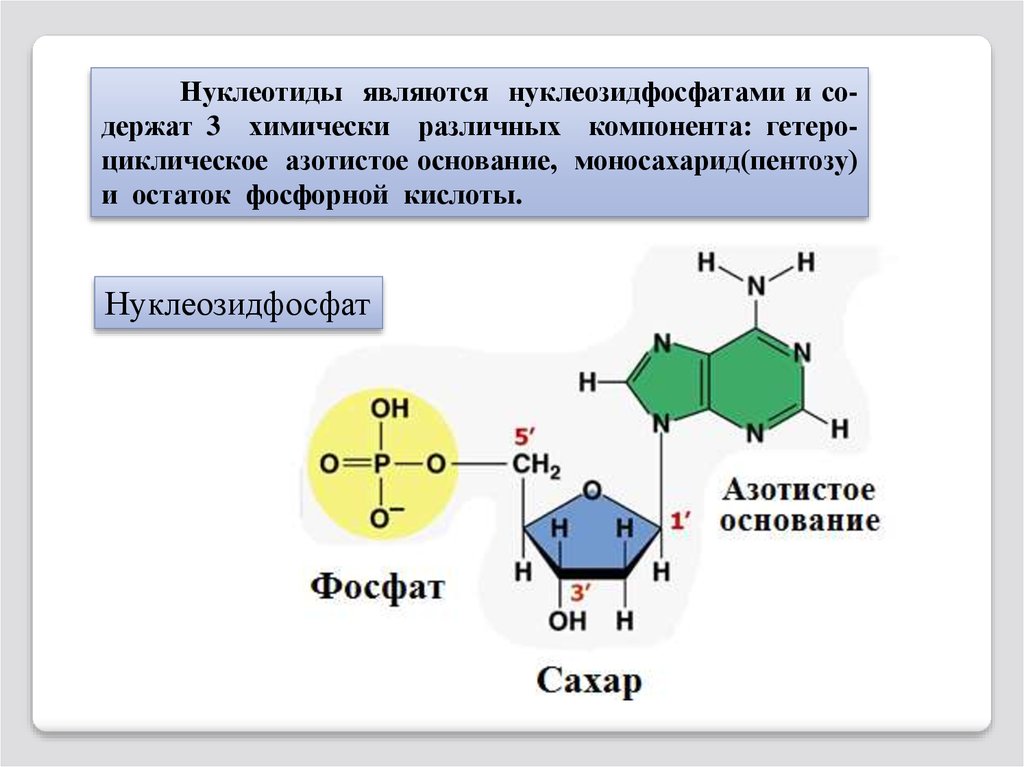
Нуклеотиды являются нуклеозидфосфатами и содержат 3 химически различных компонента: гетероциклическое азотистое основание, моносахарид(пентозу)и остаток фосфорной кислоты.
Нуклеозидфосфат
77.
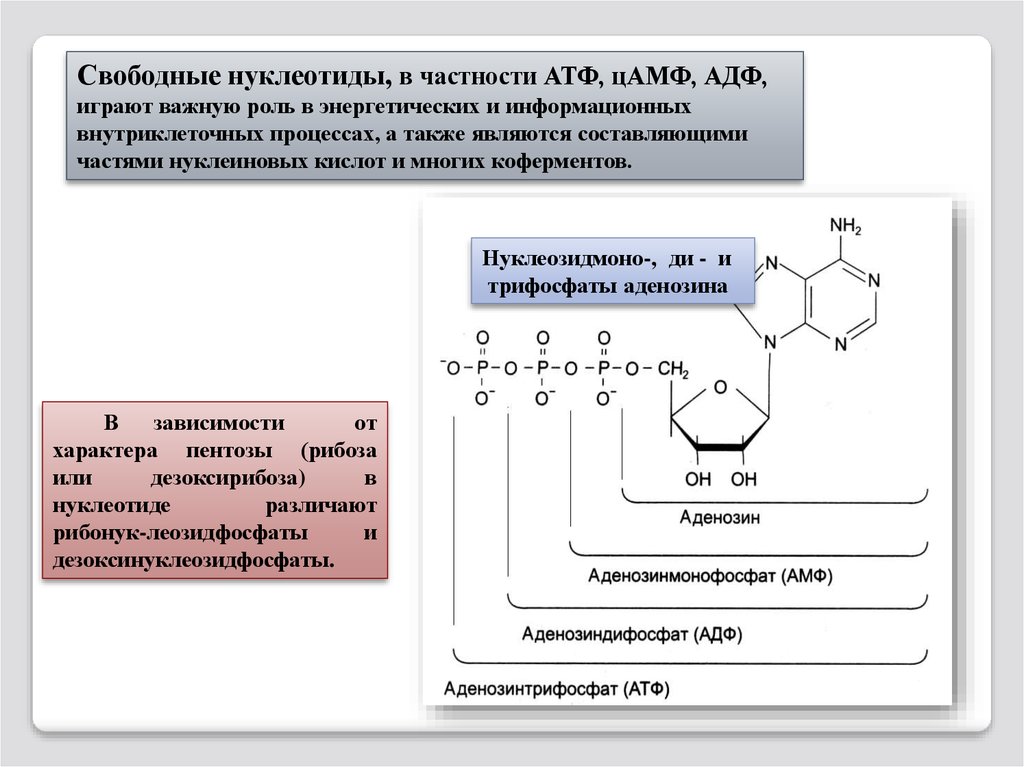
Свободные нуклеотиды, в частности АТФ, цАМФ, АДФ,играют важную роль в энергетических и информационных
внутриклеточных процессах, а также являются составляющими
частями нуклеиновых кислот и многих коферментов.
Нуклеозидмоно-, ди - и
трифосфаты аденозина
В
зависимости
от
характера пентозы (рибоза
или
дезоксирибоза)
в
нуклеотиде
различают
рибонук-леозидфосфаты
и
дезоксинуклеозидфосфаты.
78.
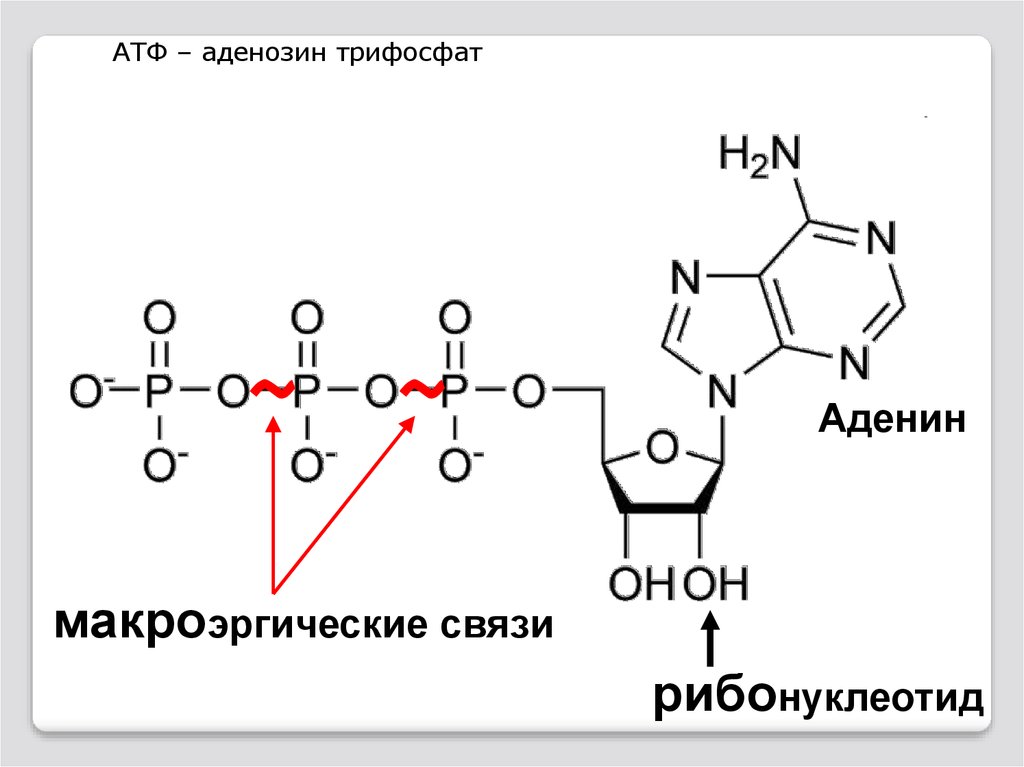
АТФ – аденозин трифосфатАденин
макроэргические связи
рибонуклеотид
79.
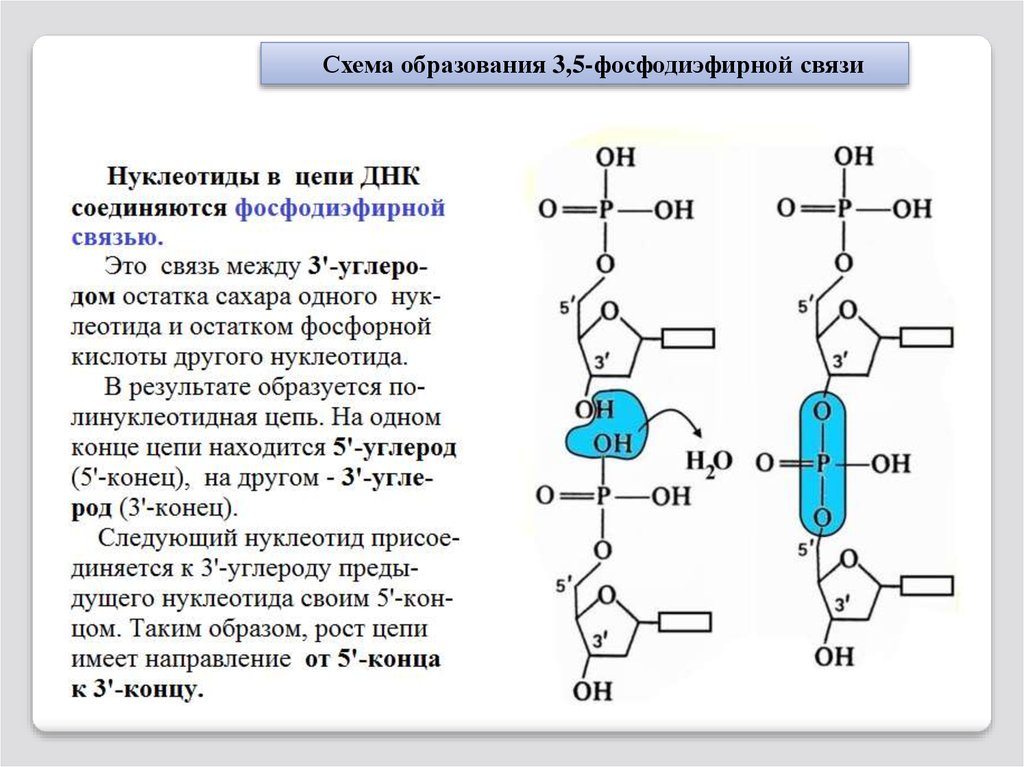
Схема образования 3,5-фосфодиэфирной связи80.
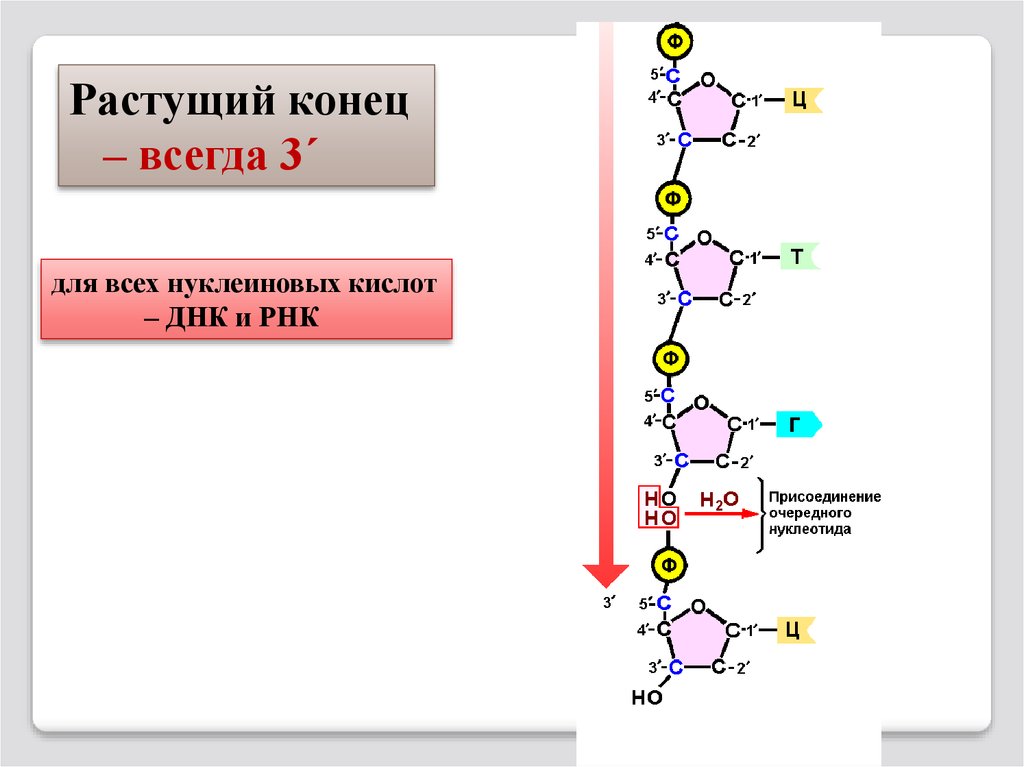
Растущий конец– всегда 3´
для всех нуклеиновых кислот
– ДНК и РНК
81.
82.
ДНК – это двуцепчечная молекула.2 цепи в ней соединяются друг с другом согласно принципу
комплементарности
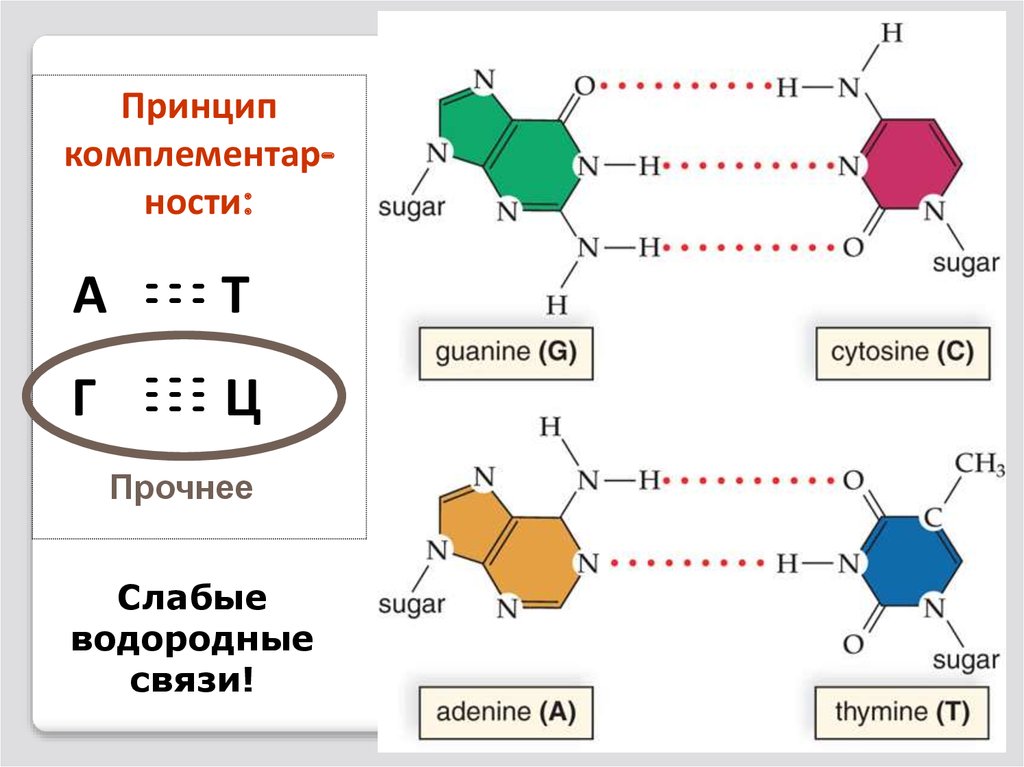
83.
Принципкомплементарности:
А
-- -- --
Т
Г
-- -- ----
Ц
Прочнее
Слабые
водородные
связи!
84. 1950 Правила Чаргаффа
Эрвин Чаргафф85.
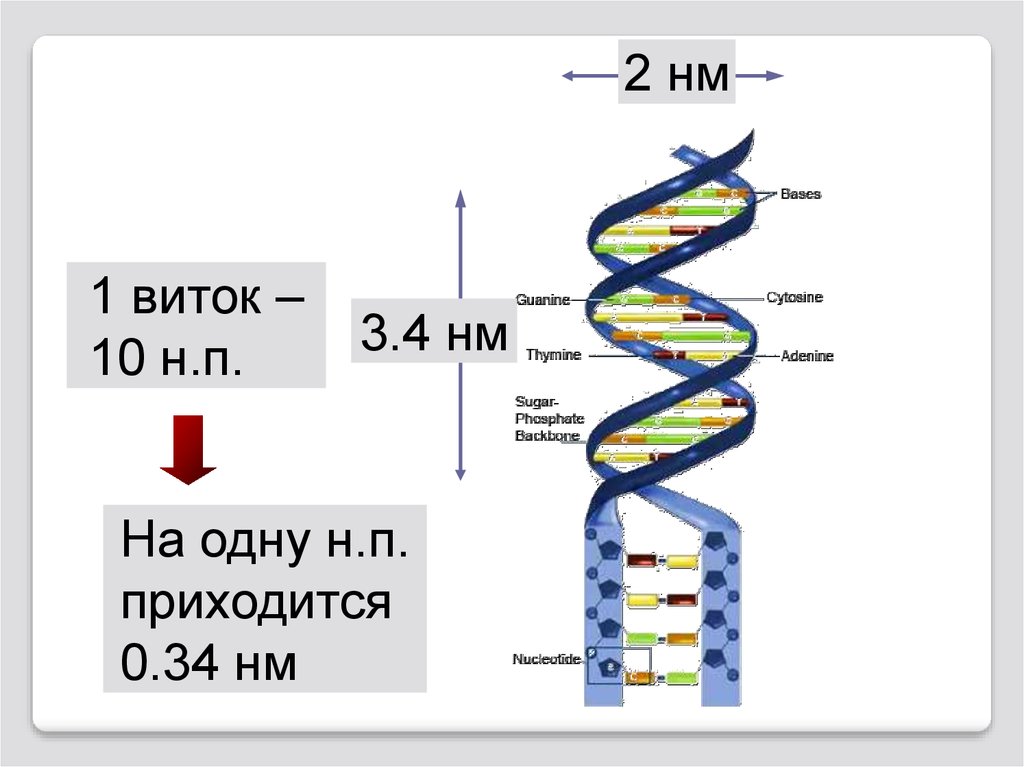
2 нм1 виток –
10 н.п.
3.4 нм
На одну н.п.
приходится
0.34 нм
86.
87.
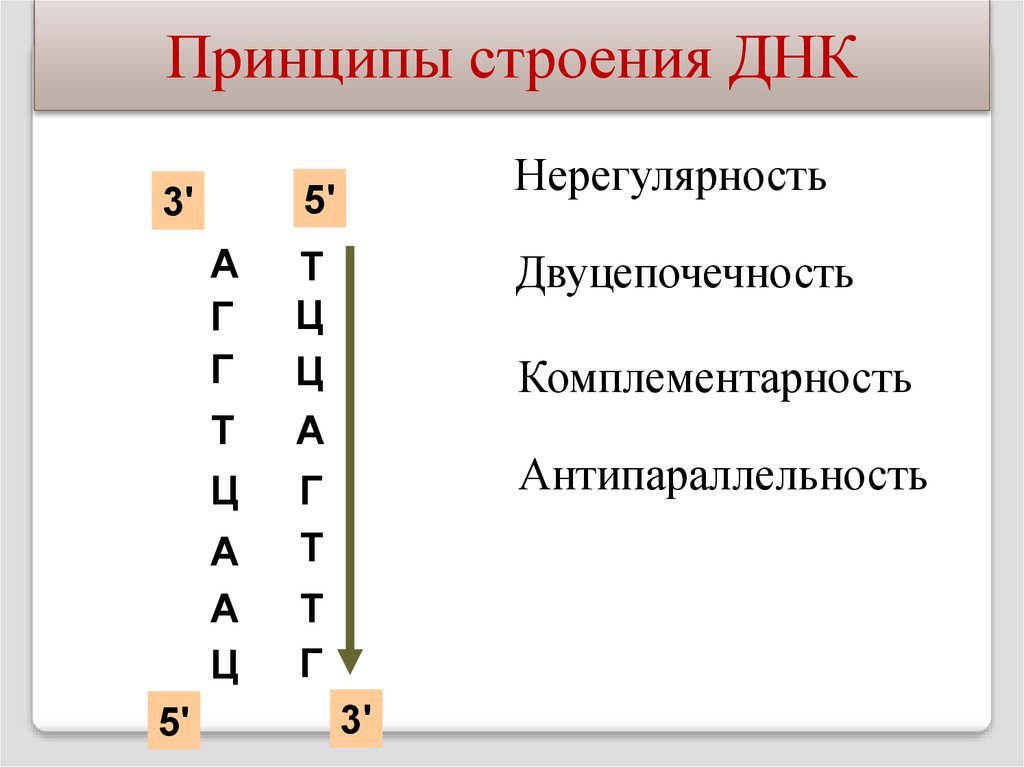
Принципы строения ДНК5'
3'
А
Г
Г
Т
Ц
А
А
Ц
5'
Нерегулярность
Т
Ц
Ц
А
Двуцепочечность
Комплементарность
Антипараллельность
Г
Т
Т
Г
3'
88.
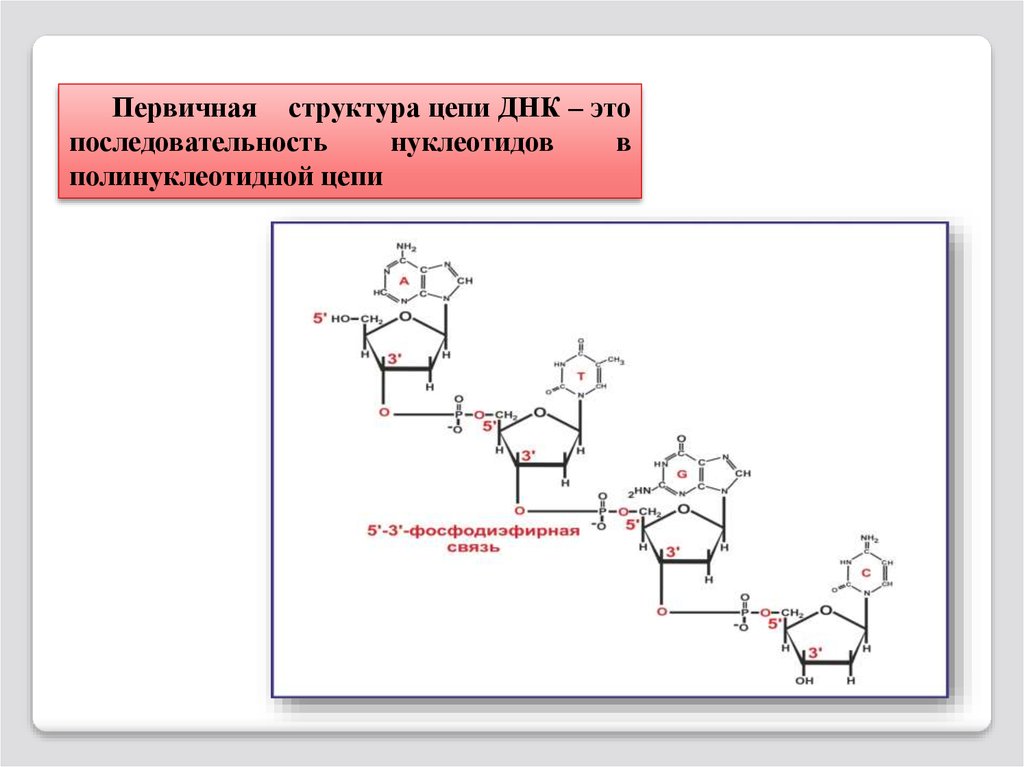
Первичная структура цепи ДНК – этопоследовательность
нуклеотидов
в
полинуклеотидной цепи
89.
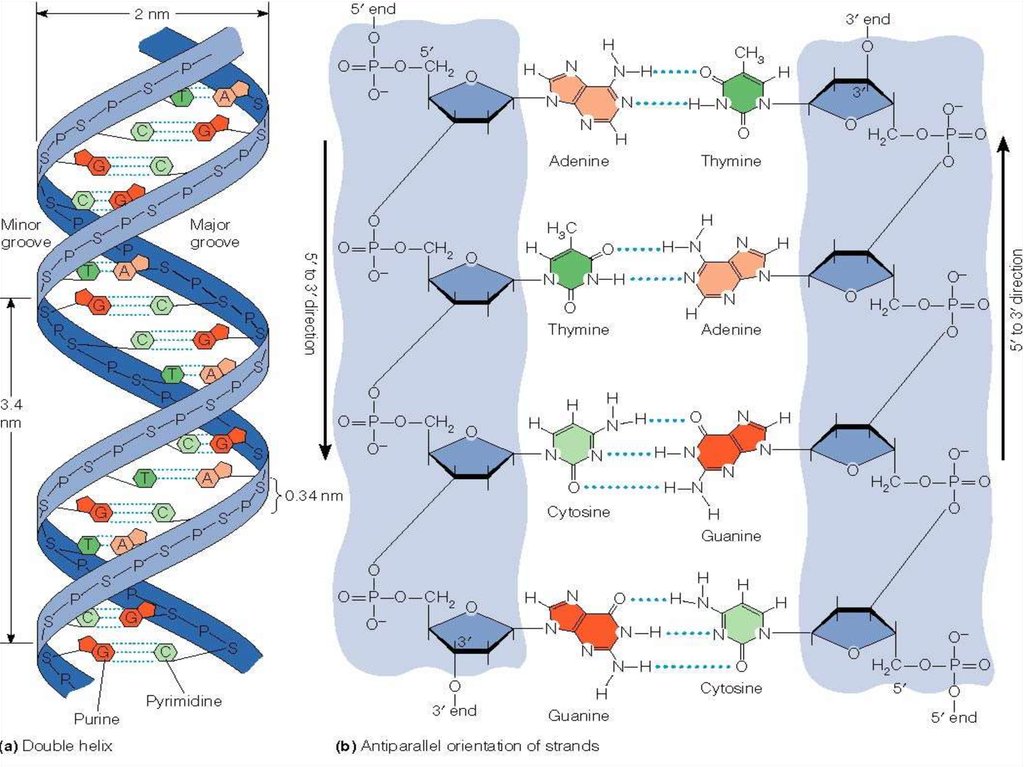
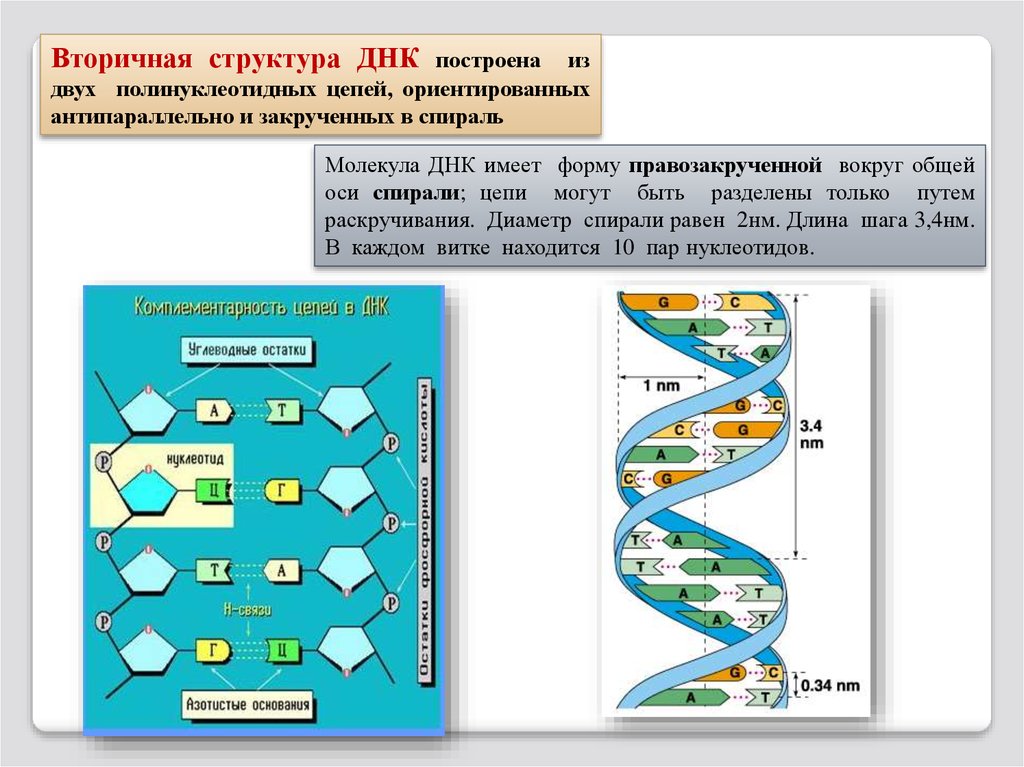
Вторичная структура ДНКпостроена из
двух
полинуклеотидных цепей, ориентированных
,
антипараллельно и закрученных в спираль
Молекула ДНК имеет форму правозакрученной вокруг общей
оси спирали; цепи могут быть разделены только путем
раскручивания. Диаметр спирали равен 2нм. Длина шага 3,4нм.
В каждом витке находится 10 пар нуклеотидов.
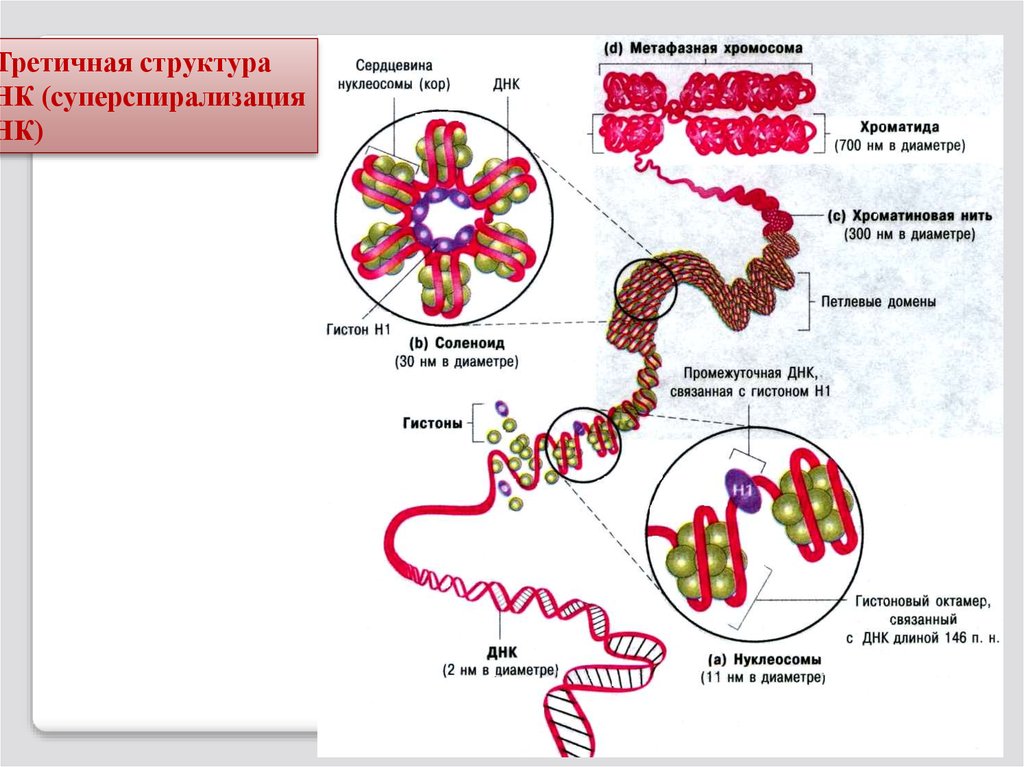
90.
Третичная структураНК (суперспирализация
НК)
91.
Форма молекул ДНК92.
A-ДНК —представляет собой правозакрученную двусхпиральную молекулу.Основания располагаются под углом 20
градусов; на виток приходится 11 пар.
Спираль расширяется, её диаметр равен 4
нм. Имеет более компактную форму.
Биологическая роль - А-форма ДНК
необходима в тех процессах, где образуются
ДНК-РНК комплексы, так как РНК может
принимать только А-форму спирали из-за
ОН-группы.
В-форма - типичная правозакрученная спираль УотсонаКрика с перпендикулярно расположенными основаниями и
диаметром 3,4 нм.
ДНК в клетке находится в
основном в В-форме, но отдельные её участки могут
находится в А- или Z-форме.
Z-форма - левозакрученная спираль с основаниями
расположенными под углом ~20º к оси спирали и 12
парами оснований в шаге. Линия, соединяющая фосфатные
группы, через каждые две пары нуклео- тидов имеет излом
и принимает зигзагообразный вид.
Z-форма играет роль в процессе рекомбинации и
регуляции действия генов, является временной структурой,
появляющейся в результате биологической активности и
быстро исчезающей.
93.
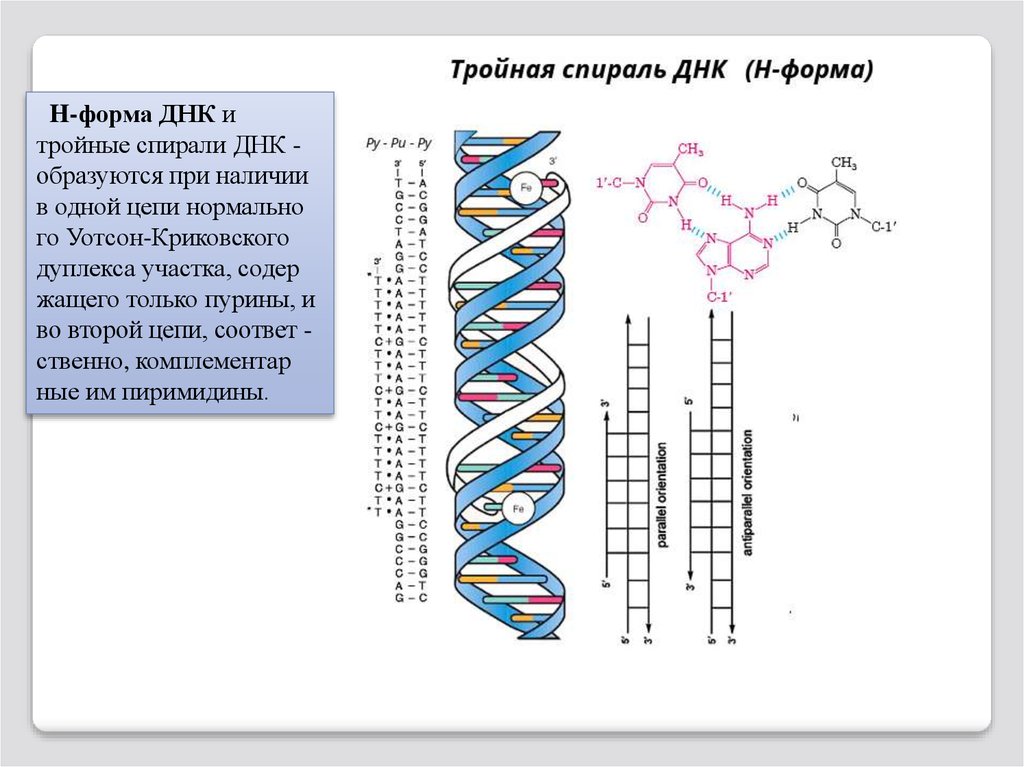
H-форма ДНК итройные спирали ДНК образуются при наличии
в одной цепи нормально
го Уотсон-Криковского
дуплекса участка, содер
жащего только пурины, и
во второй цепи, соответ ственно, комплементар
ные им пиримидины.
94.
95. Строение РНК
96.
Химическая структура РНКа) обе молекулы являются линейными полимерами;
б) мономеры –нуклеотиды являются фосфорилированнымиNгликозидами, которые соединяются
фосфодиэфирной связью;
в) в состав РНК входят также 4
нуклеотида: аденин (А),гуанин (Г),
цитозин (Ц) и урацил (У);
г) полинуклеотидная цепь РНК
полярна: имеет четко различимые
5ʹ-, и 3ʹ-концы (рис.102).
Отличия от ДНК
а) РНК – одноцепочный полимер;
б) сахарный остаток мономера рибоза, которая содержит
допо-л-нительную гидроксильную
группу;
в) среди главных (мажорных) азотистых оснований вместо тимина
содержится урацил, который отличается от тимина отсутствием
метильной группы в 5-ом положении;
г)в молекуле РНК высоко
содержание минорных оснований и
нуклеозидов, которые являются
модифицированными производными
как мажорных азотистых
основании, так и сахара.
97. Отличия РНК от ДНК
1.Одноцепочечные молекулы
2.
Сахар – рибоза вместо
дезоксирибозы
3.
У вместо Т
4.
Намного меньше – сравнимы
по размеру с белками.
98.
РНК – рибонуклеиновая кислота;по особенностям строения и функциям
делится на кодирующую белок и не кодирующую белок.
Кодирующая белок
Не кодирующая белок
иРНК (информационная)
или мРНК (матричная),
несет информацию о структуре белка
Не несет информацию о структуре белка и, следовательно, не
транслируются в белок.
99.
Не кодирующая белок РНКтранспортная РНК (тРНК)
Рибосомальная РНК (рРНК)
транспортно-матричная РНК (тмРНК),
микро РНК (миРНК),
малые ядерные РНК (мяРНК, snRNA),
малые ядрышковые РНК (мякРНК,
snoRNA),
антисмысловые РНК (aRNA),
микроРНК (miRNA),
piРНК (piwiRNA, piRNA),
длинные некодирующие РНК
малая интерферирующая РНК миРНК
(siRNA) и т. д.
100.
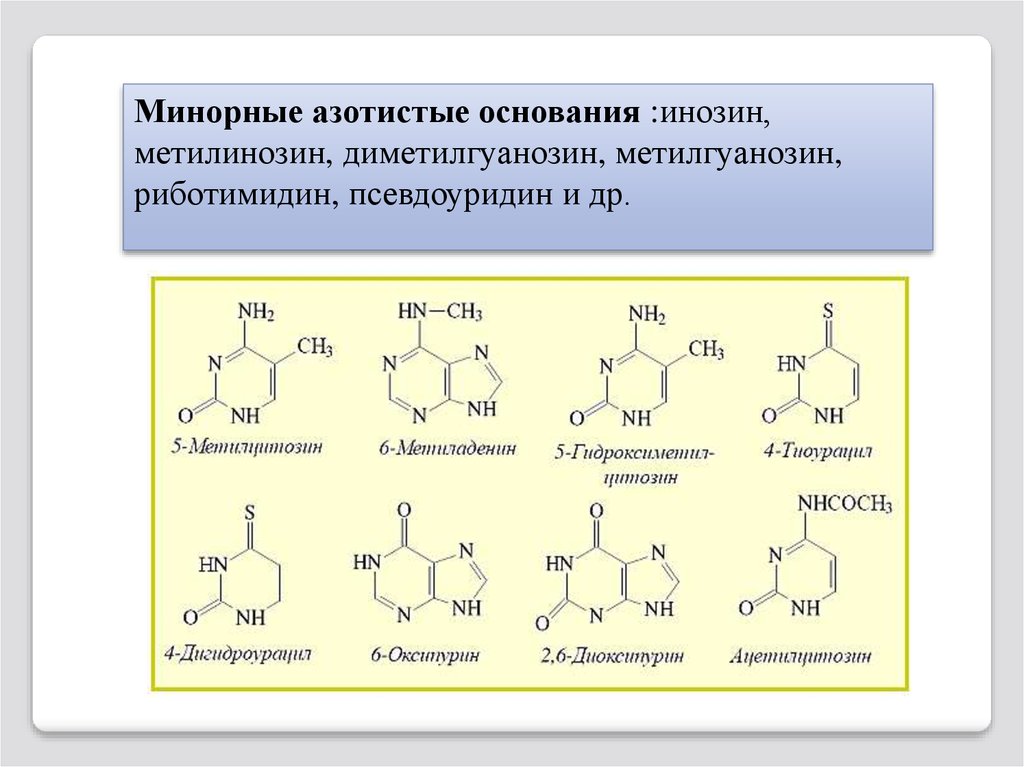
Минорные азотистые основания :инозин,метилинозин, диметилгуанозин, метилгуанозин,
риботимидин, псевдоуридин и др.
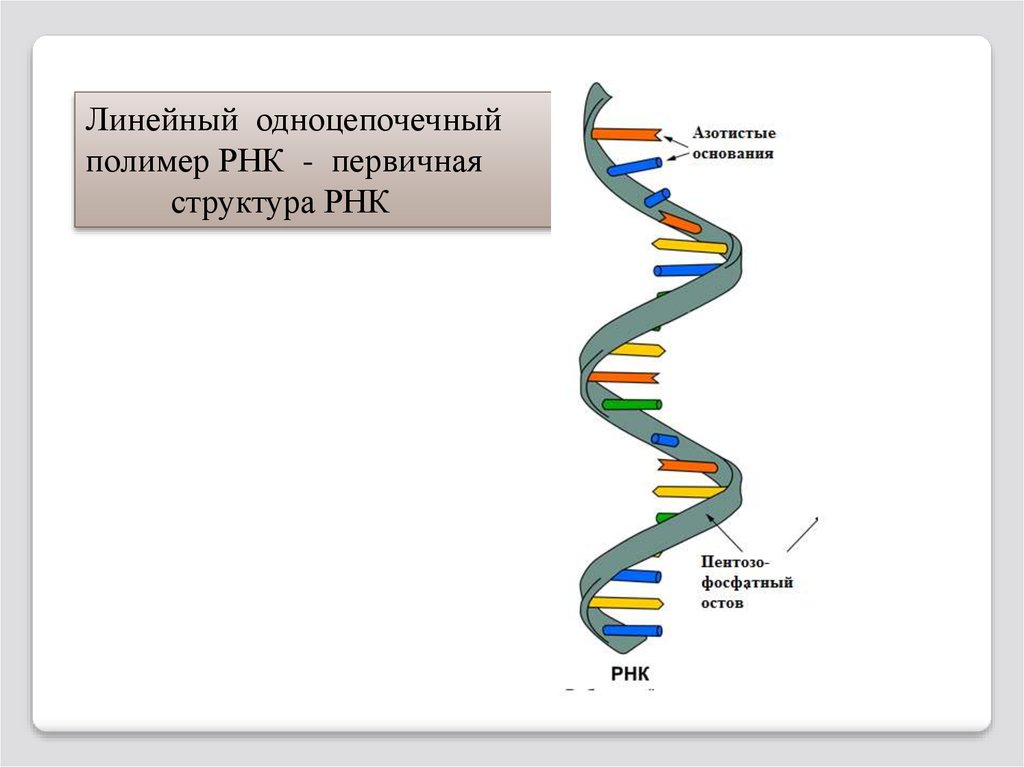
101.
Линейный одноцепочечныйполимер РНК - первичная
структура РНК
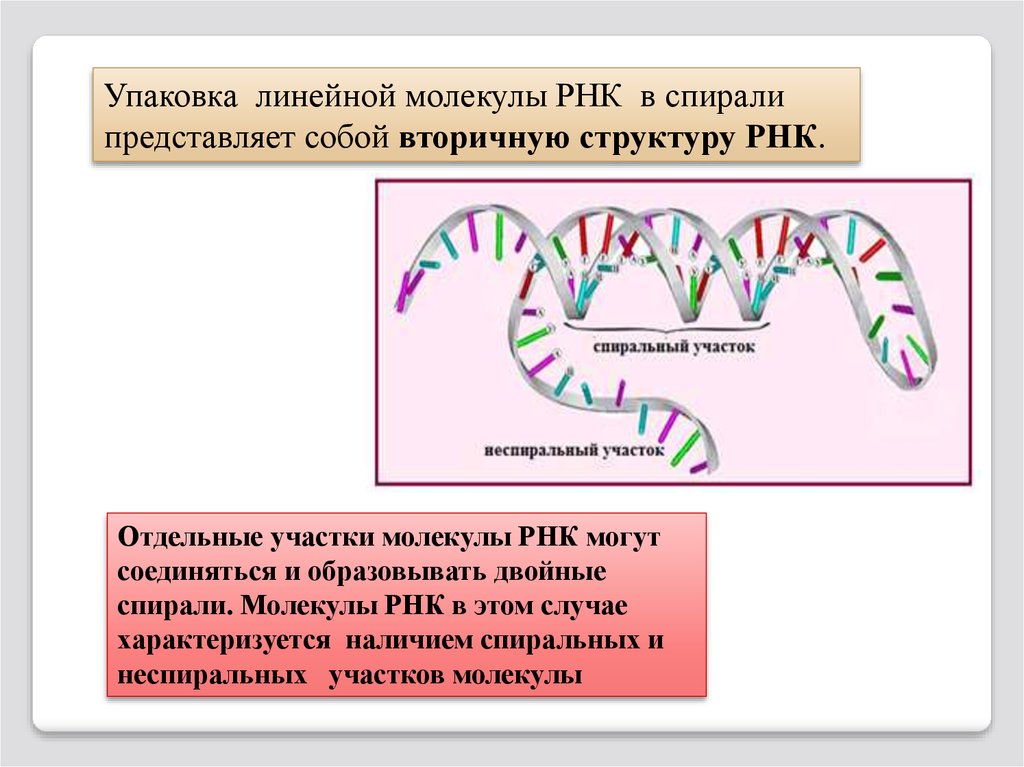
102.
Упаковка линейной молекулы РНК в спиралипредставляет собой вторичную структуру РНК.
Отдельные участки молекулы РНК могут
соединяться и образовывать двойные
спирали. Молекулы РНК в этом случае
характеризуется наличием спиральных и
неспиральных участков молекулы
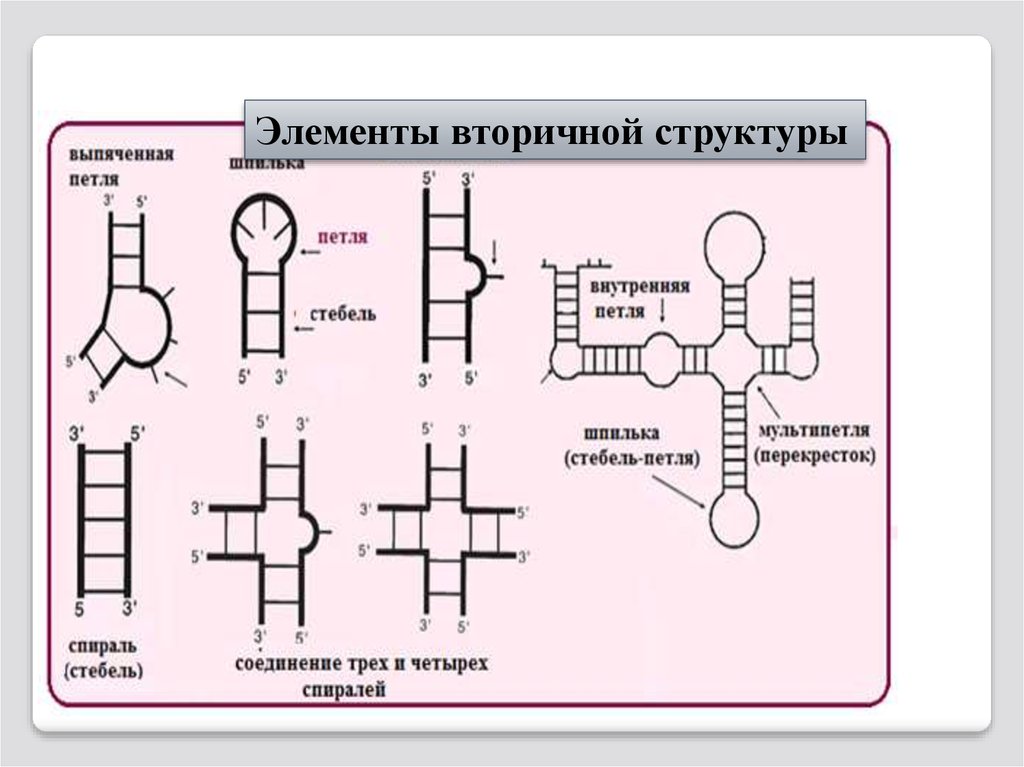
103.
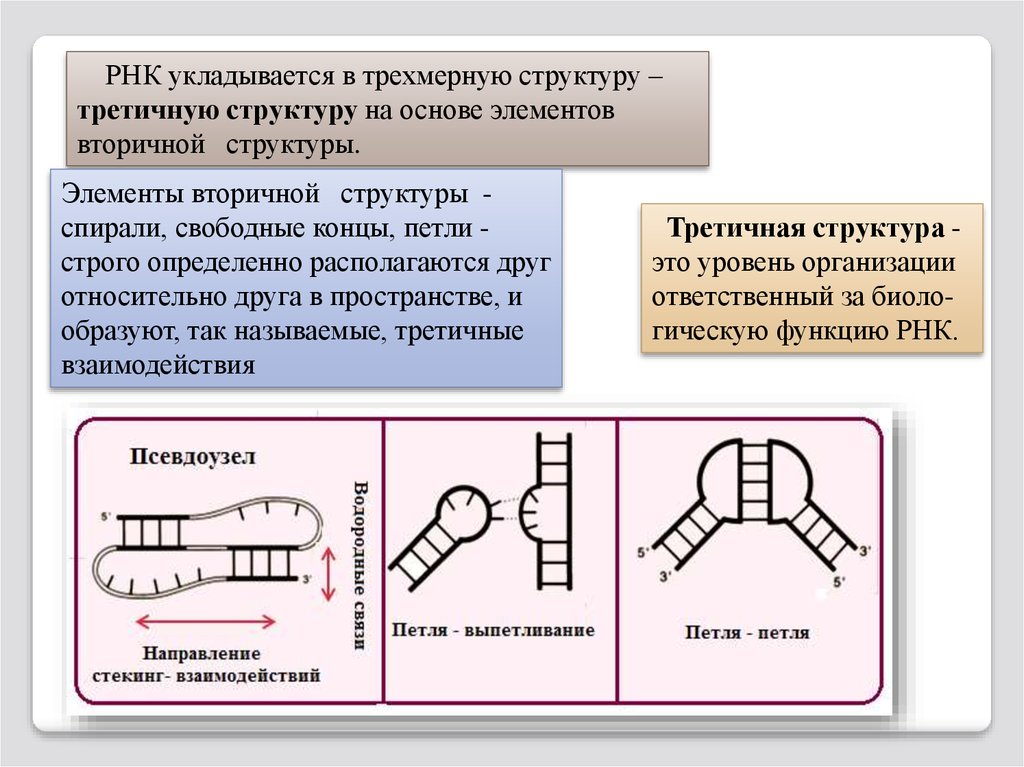
Элементы вторичной структуры104.
РНК укладывается в трехмерную структуру –третичную структуру на основе элементов
вторичной структуры.
Элементы вторичной структуры спирали, свободные концы, петли строго определенно располагаются друг
относительно друга в пространстве, и
образуют, так называемые, третичные
взаимодействия
Третичная структура это уровень организации
ответственный за биологическую функцию РНК.
105.
мРНК–матричная РНК составляет 3% от всей РНК клетки.Это короткоживущая молекула с молекулярной массой, колеблющейся в широких пределах и доходящей до 14*106кДа.
Функцией мРНК является перенос информации с молекулы ДНК на молекулу белка. То есть, мРНК является
матрицей для синтеза белка, посредником (messenger)
между ДНК и белком.
Первичная структура мРНК
106.
I. Колпачок (кэп) - участок из 1-4 модифицированных нуклеотидов,который находится на 5'-конце). Первым нуклеотидом всегда является
7-метилгуанилат.
II. 5'- и 3'-нетранслируемый участок (область) - последователь-ность
из нескольких десятков нуклеотидов. Участки мРНК, не не несущий
информации о структуре белка.
5'-нетранслируемый участок - это последовательностькомплиментарная
одному из отделов рРНК, входящему в малую субъединицу рибосомы,
поэтому она отвечает за первичное связывание мРНК с рибосомой.
3'- нетранслируемыйучасток-последовательность нуклеотидов,
превышающая по длине 5'-нетранслируемый участок. Является
субстратом для присоединения поли-(А)-«хвоста
III. Инициирующий кодон (AUG) –
IV. Кодирующая часть (транслируемая область)
V.Кодон терминации (стоп-кодон) - один из 3 бессмысленных кодонов:
УАА, УГА,УАГ.
VI.Поли-(А)-фрагмент - это последовательность из 150-200 адени- ловых
нуклеотидов (рис.). Облегчает выход мРНК из ядра и защищает её от
3'-экзонуклеаз в цитоплазме.
107.
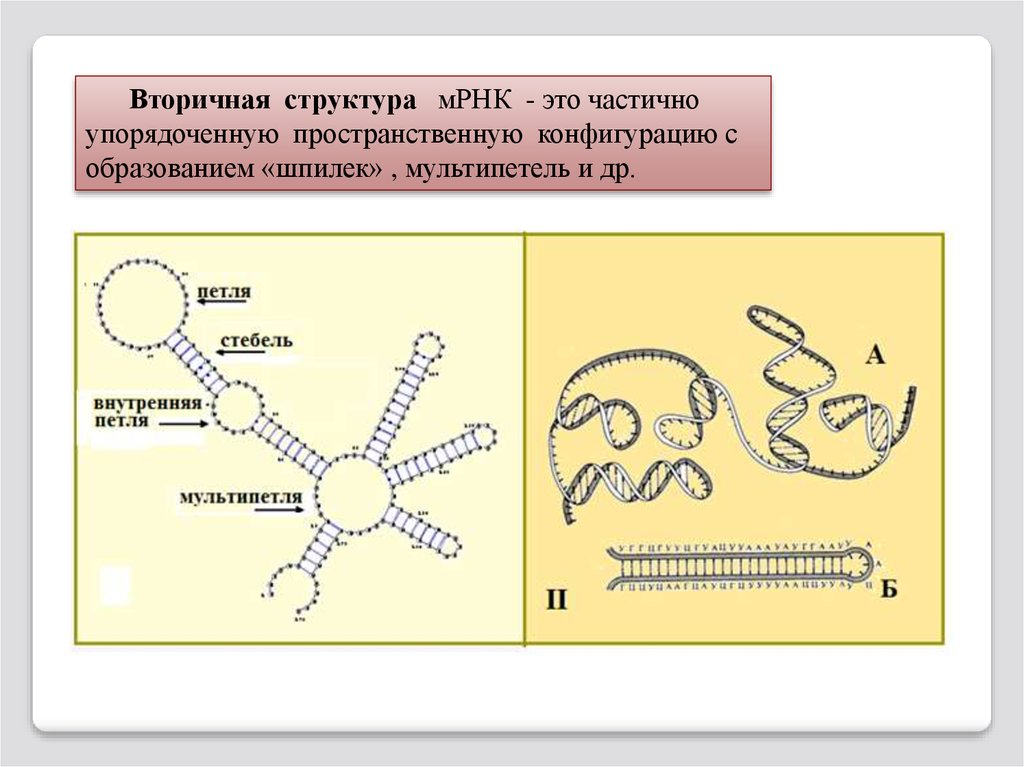
Вторичная структура мРНК - это частичноупорядоченную пространственную конфигурацию с
образованием «шпилек» , мультипетель и др.
108.
Третичная структура РНКформируется при определенных
значениях рh среды, ионной
силы и температура в структуре со множеством участков с
двойной спиралью (шпильки),
которые затем взаимодействуют
с образованием компактных ,
но бесформенных образований
а – компактная палочка,
б – компактный клубок,
в - развернутая цепь
109.
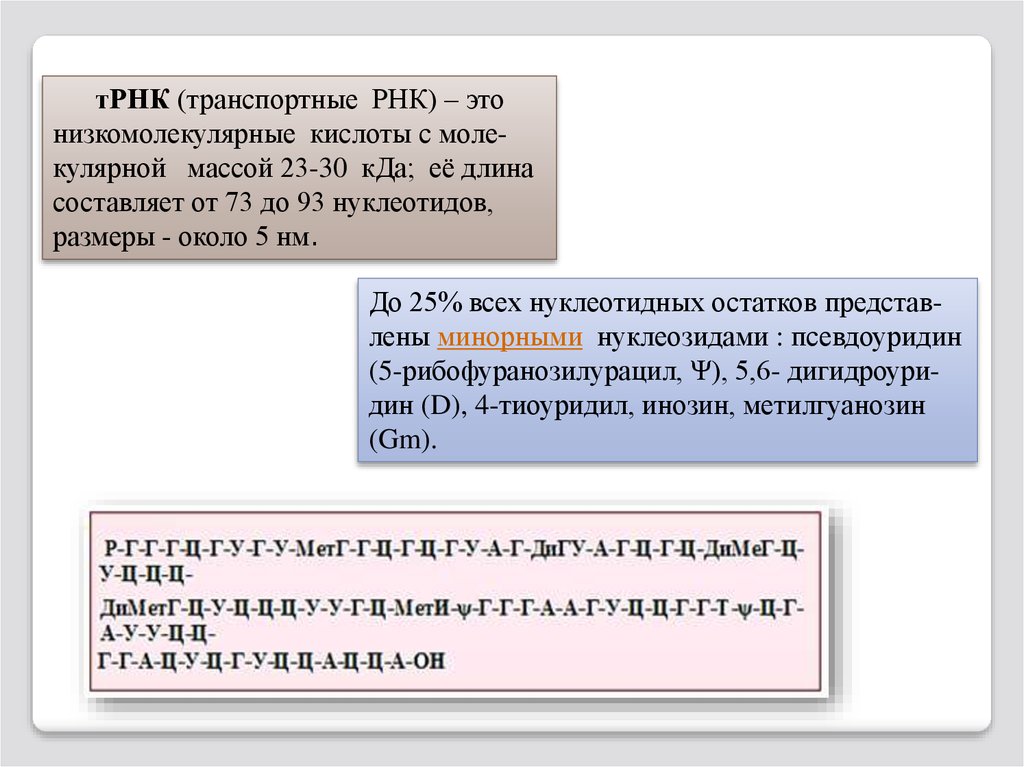
тРНК (транспортные РНК) – этонизкомолекулярные кислоты с молекулярной массой 23-30 кДа; её длина
составляет от 73 до 93 нуклеотидов,
размеры - около 5 нм.
До 25% всех нуклеотидных остатков представлены минорными нуклеозидами : псевдоуридин
(5-рибофуранозилурацил, Ψ), 5,6- дигидроуридин (D), 4-тиоуридил, инозин, метилгуанозин
(Gm).
110.
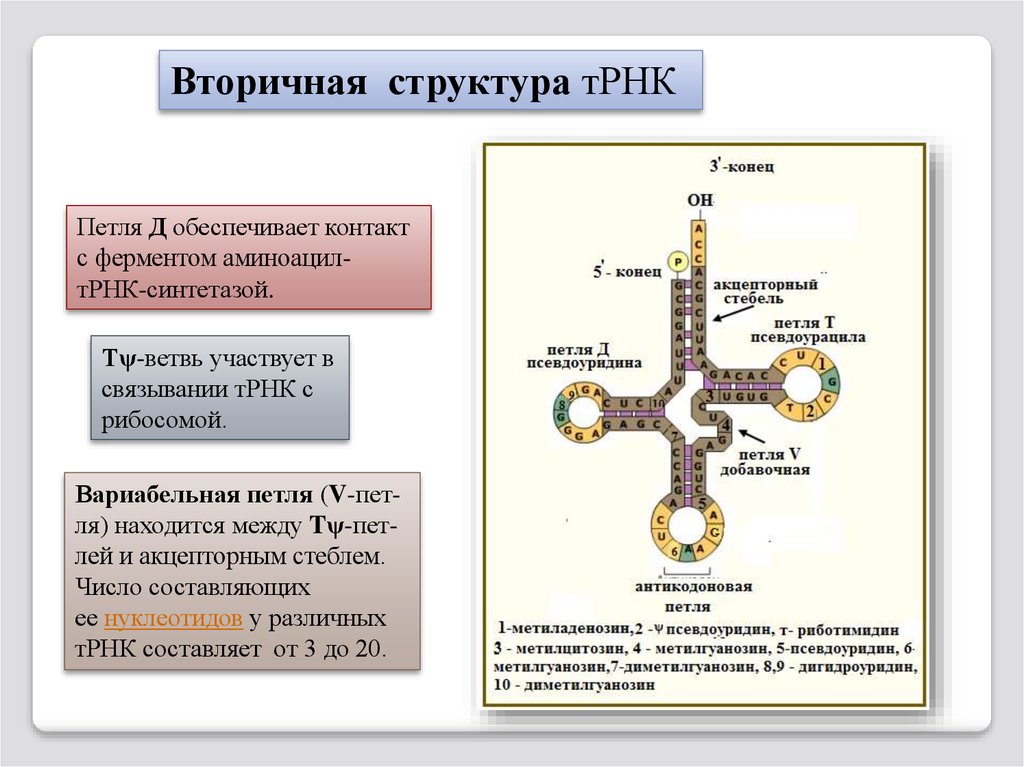
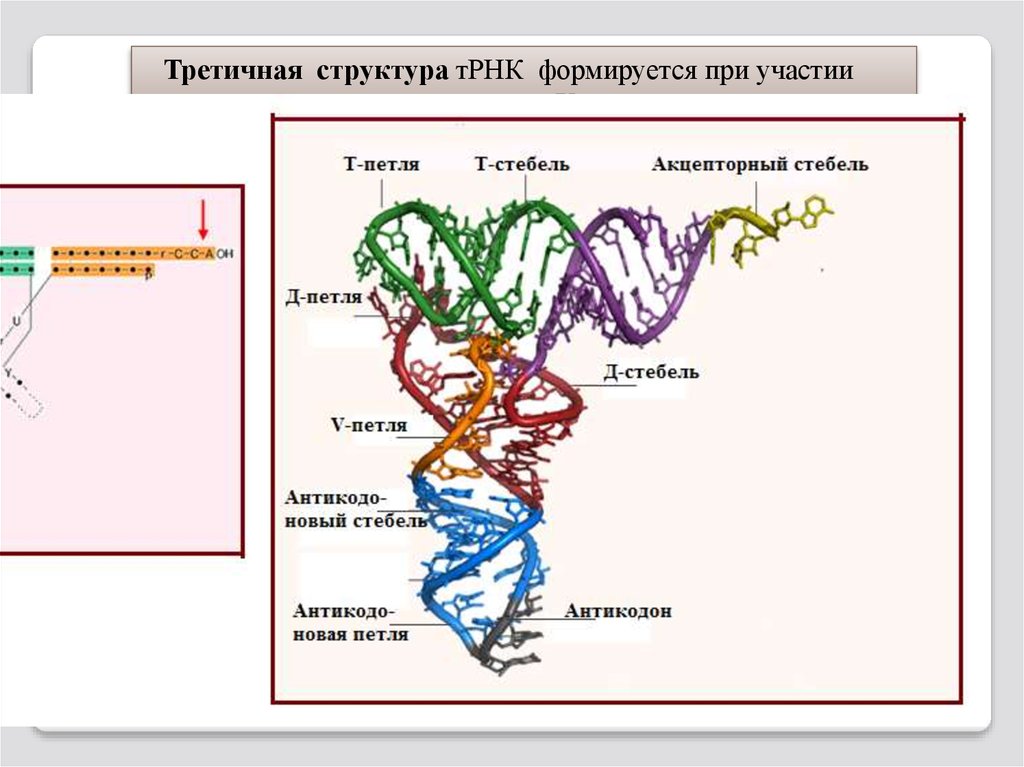
Вторичная структура тРНКПетля Д обеспечивает контакт
с ферментом аминоацилтРНК-синтетазой.
Tψ-ветвь участвует в
связывании тРНК с
рибосомой.
Вариабельная петля (V-петля) находится между Tψ-петлей и акцепторным стеблем.
Число составляющих
ее нуклеотидов у различных
тРНК составляет от 3 до 20.
111.
Третичная структура тРНК формируется при участииД- ветви , Tψ-ветви и V-петли
112.
Функции тРНК.Для синтеза белка они выполняют три функции:
- акцепторная - присоединяет к своему аминоацильному
остатку строго определённую аминокислоту ;
- транспортная - транспортирует аминокислоту к специфическому месту синтеза белка на рибосоме;
- адапторную - в комплексе с рибосомой способен специфически узнавать триплет генетического кода на матричной РНК,
после чего присоединённая к тРНК аминокислота включается в
растущую полипептидную цепь на рибосоме;
- затравки при обратной транскрипции (синтезе ДНК на РНКматрице);
- в переносеаминокислот через наружную мембрану клеток;
- в регуляции биосинтеза ряда аминокислот;
- в посттрансляционной модификации белков.
113.
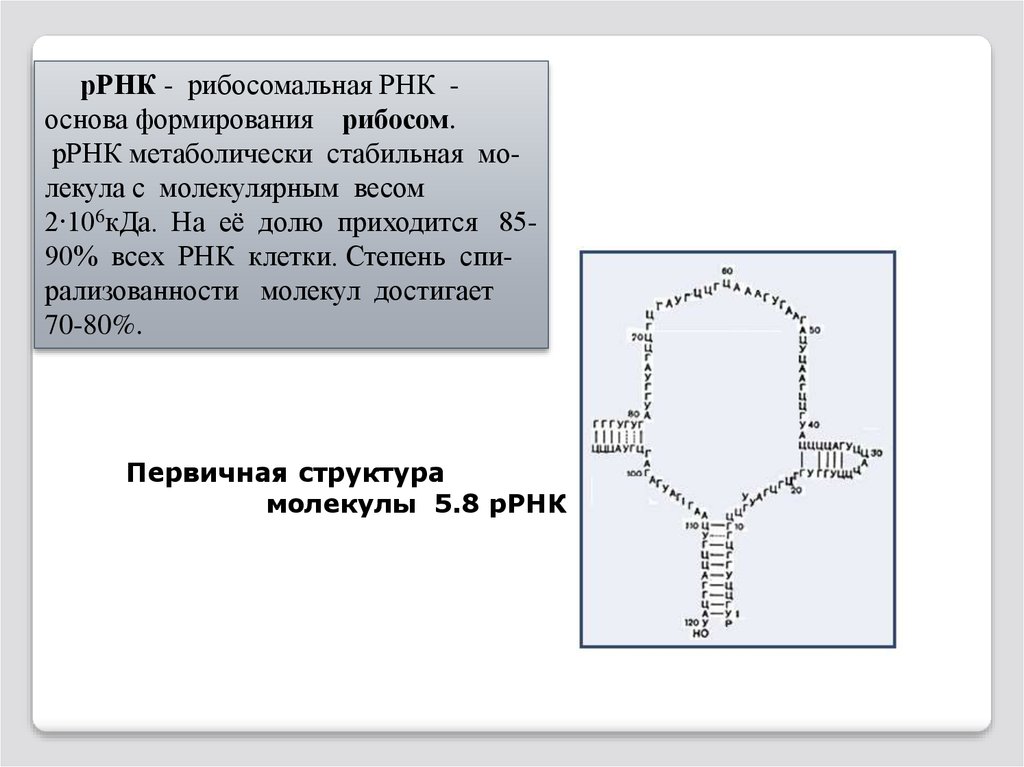
рРНК - рибосомальная РНК основа формирования рибосом.рРНК метаболически стабильная молекула с молекулярным весом
2∙106кДа. На её долю приходится 8590% всех РНК клетки. Степень спирализованности молекул достигает
70-80%.
Первичная структура
молекулы 5.8 рРНК
114.
115. Рибосомальная РНК
Самаябольшая из
всех видов
РНК –
2-3 тысячи
нуклеотидов
16 S рРНК
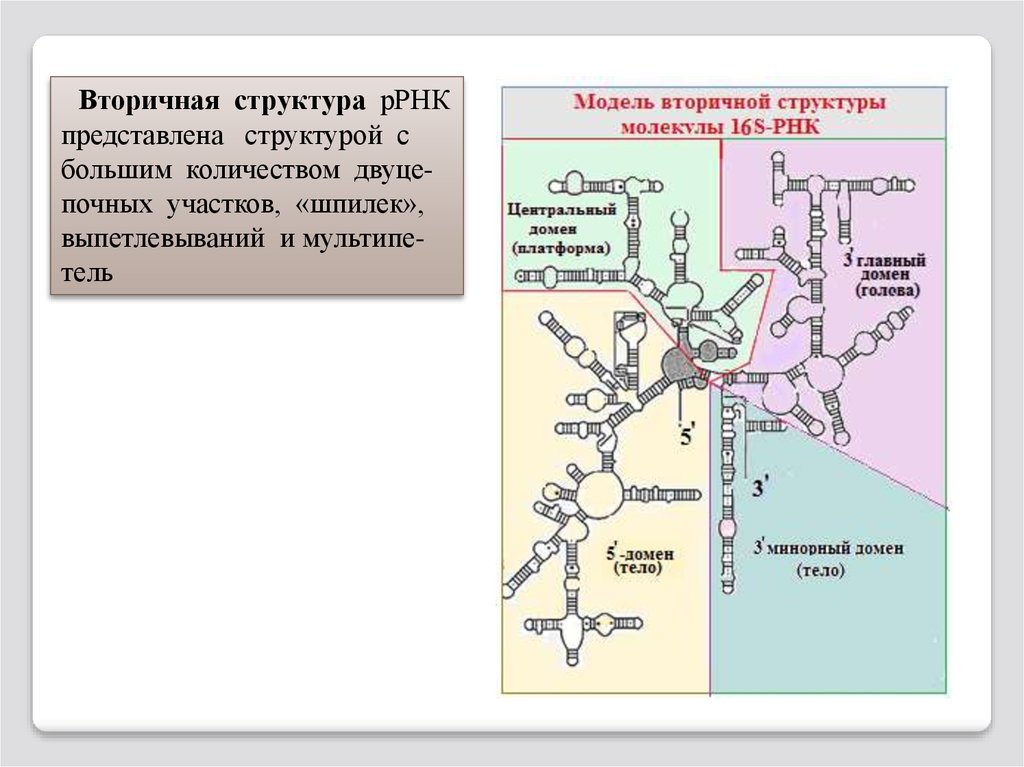
116.
Вторичная структура рРНКпредставлена структурой с
большим количеством двуцепочных участков, «шпилек»,
выпетлевываний и мультипетель
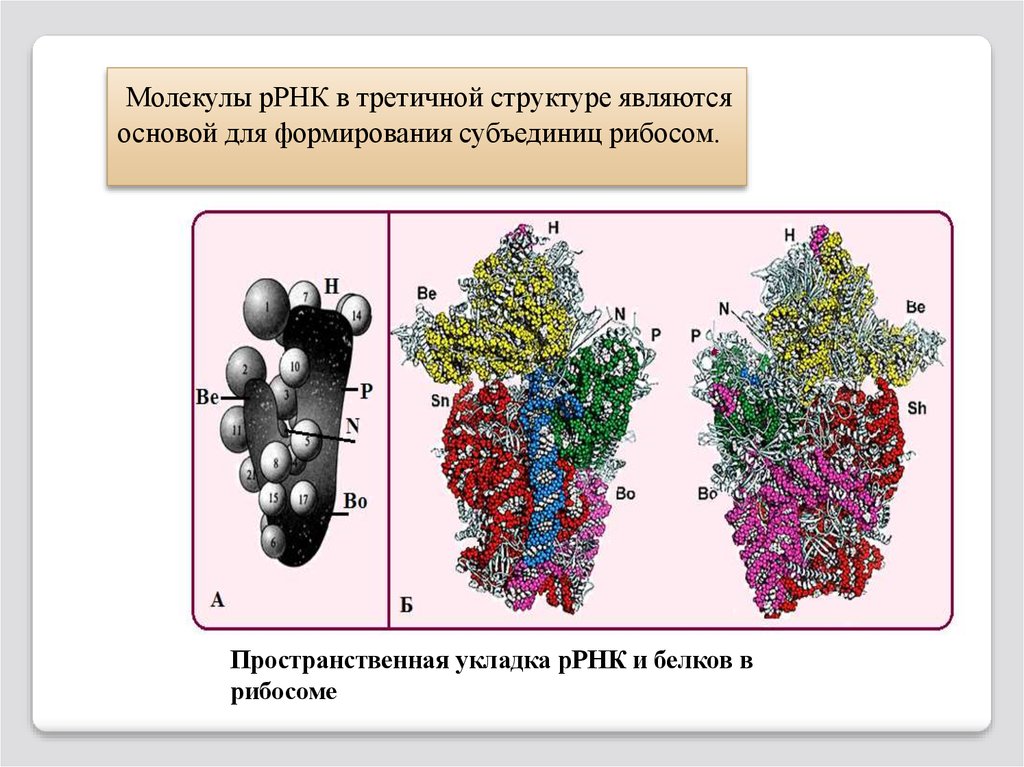
117.
Молекулы рРНК в третичной структуре являютсяосновой для формирования субъединиц рибосом.
Пространственная укладка рРНК и белков в
рибосоме
118.
Биологические функции молекулы РНК1 - генетическая репликативная функция - выполняется при вирусных
инфекциях: в клетке, зараженный вирусом, происходит репликация РНК
вируса с дальнейшей трансляцией белков вируса;
2 - кодирующая функция – программирование белкового синтеза
линейными последовательностями нуклеотидов РНК (РНК-матрица).
Триплеты нуклеотидов РНК являются программой для расстановки 20видов
аминокислот в полипептидной цепи белка;
3 - структурная функция – молекула РНК образует трехмерные
структуры - рибосомы;
4 - функция узнавания – способность узнавать и пространственно
взаимодей- ствовать с другими видами РНК ( мРНК и рРНК при трансляции)
и белками ( сплайсомы и информосомы );
5 - каталитическая функция - участие в специфическом катализе
химиической реакции рибозимами.






















































 biology
biology








