Similar presentations:
Тепловой эффект химических реакций
1. Тепловой эффект химических реакций
ТЕПЛОВОЙ ЭФФЕКТХИМИЧЕСКИХ
РЕАКЦИЙ
2. Химический эксперимент
ХИМИЧЕСКИЙ ЭКСПЕРИМЕНТОдним из признаков протекания химической
реакции является выделение тепла и света,
например, при горении - взаимодействии с
кислородом. Для начала горения требуется
предварительно нагревание, а затем реакция
протекает самопроизвольно и выделяется
большое количество теплоты.
3. Классификация химических реакций по тепловому эффекту
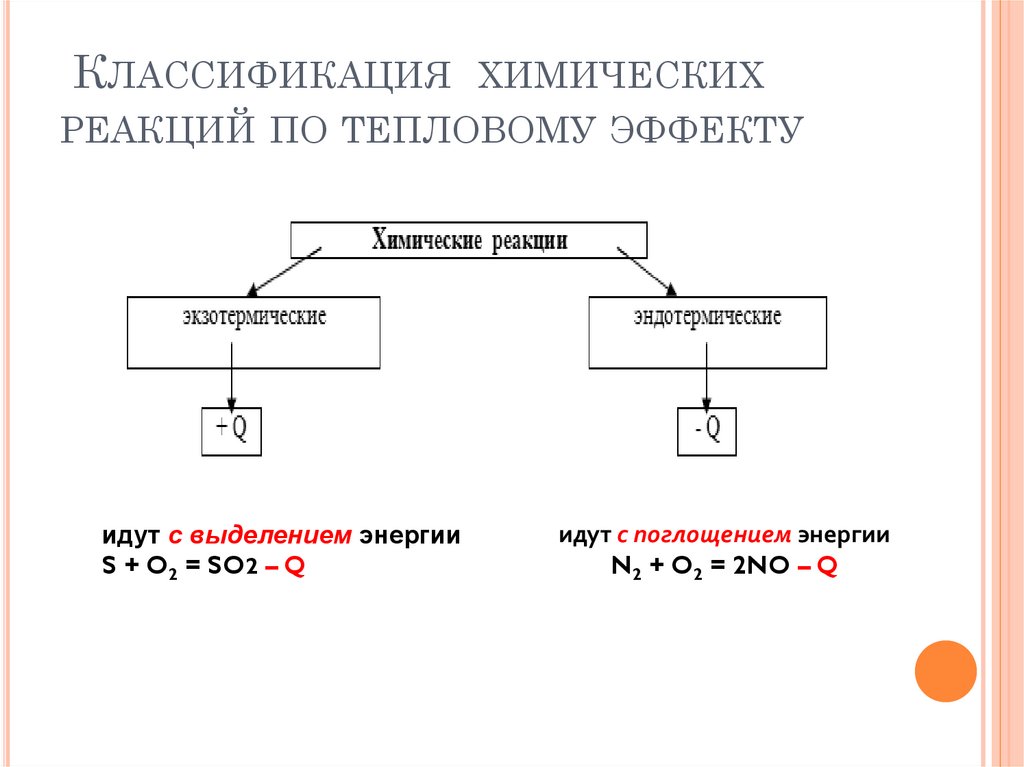
КЛАССИФИКАЦИЯХИМИЧЕСКИХ
РЕАКЦИЙ ПО ТЕПЛОВОМУ ЭФФЕКТУ
идут с выделением энергии
S + O2 = SO2 – Q
идут с поглощением энергии
N2 + O2 = 2NO – Q
4. от греческого «эндо-» «экзо-» внутрь наружу
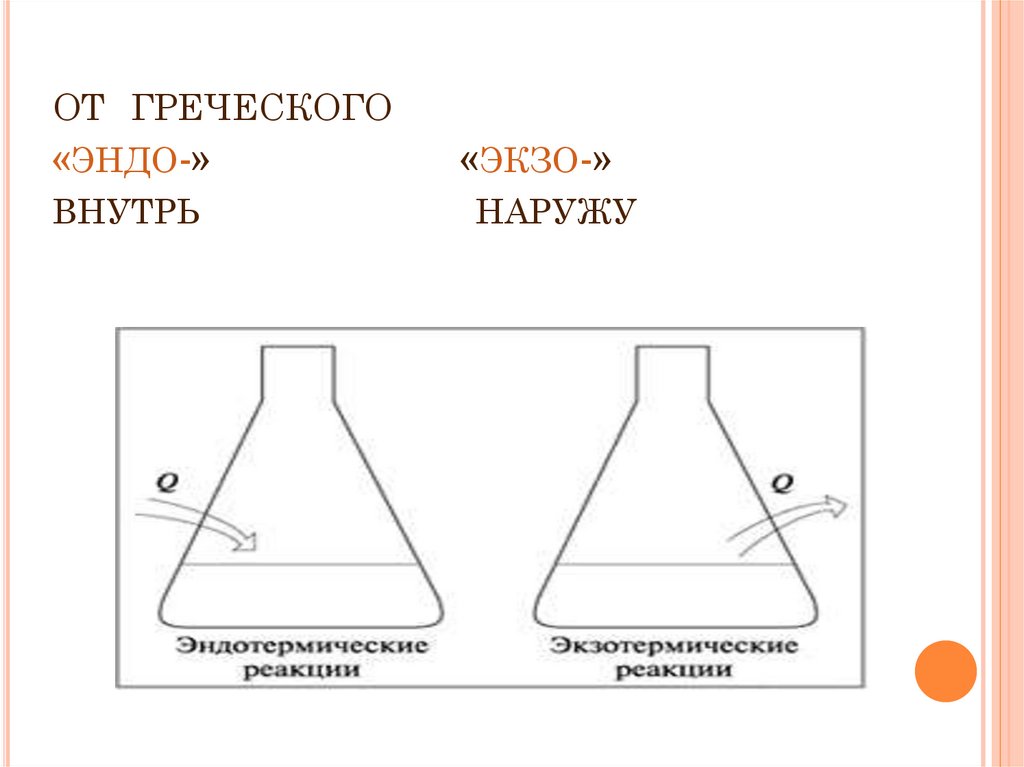
ОТ ГРЕЧЕСКОГО«ЭНДО-»
ВНУТРЬ
«ЭКЗО-»
НАРУЖУ
5.
Количество теплоты, которое выделяется илипоглощается при химической реакции,
называют тепловым эффектом реакции.
Тепловой эффект обозначается Q и измеряется
в Дж или кДж.
6.
Тепловой эффектреакции может
быть измерен с
помощью
калориметра.
Вместо Q в
уравнение
химической
реакции можно
подставить
численное
значение
теплового
эффекта.
7.
Химические уравнения, в которых указываетсятепловой эффект, называют
термохимическими.
Например:
2HgO —> 2Hg + O2 – 180 кДж,
С(тв) + O2(г) —> СO2(г) + 394 кДж
В термохимических уравнениях обязательно
указывают агрегатное состояние вещества.
8. Герман Иванович Гесс
ГЕРМАН ИВАНОВИЧ ГЕСС-Российский академик
-Основоположник термохимии
Термохимия
— раздел химии, в
задачу которого входит определение и
изучение тепловых эффектов реакции
9. Алгоритм решения задач по термохимическому уравнению
АЛГОРИТМ РЕШЕНИЯ ЗАДАЧ ПОТЕРМОХИМИЧЕСКОМУ УРАВНЕНИЮ
Кратко записать условия задачи (“дано”).
Записать термохимическое уравнение реакции
(ТХУ), одной чертой в уравнении реакции
подчеркнуть то, что известно и то, что необходимо
определить.
Провести вспомогательные вычисления. m=M*v
Составить пропорцию, используя вспомогательные
вычисления и условия задачи, и решить ее.
Записать ответ.
10. Задача
ЗАДАЧАПри взаимодействии 7 г железа с избытком серы
выделилось 12,15 кДж. На основании этих
данных составьте термохимическое уравнение.
11.
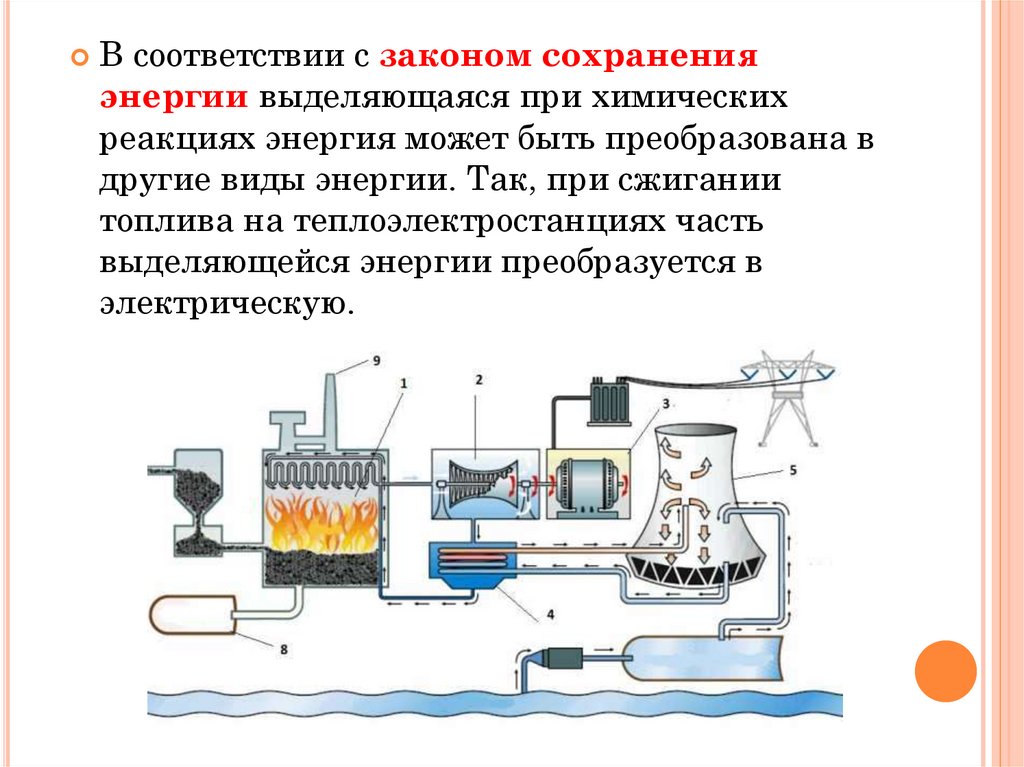
В соответствии с законом сохраненияэнергии выделяющаяся при химических
реакциях энергия может быть преобразована в
другие виды энергии. Так, при сжигании
топлива на теплоэлектростанциях часть
выделяющейся энергии преобразуется в
электрическую.
12. Домашнее задание
ДОМАШНЕЕ ЗАДАНИЕЗаписи в тетради.
Задача: Вычислите, сколько сгорело угля, если
при этом выделилось 33520 кДж теплоты.









 chemistry
chemistry








