Similar presentations:
Оксид серы
1.
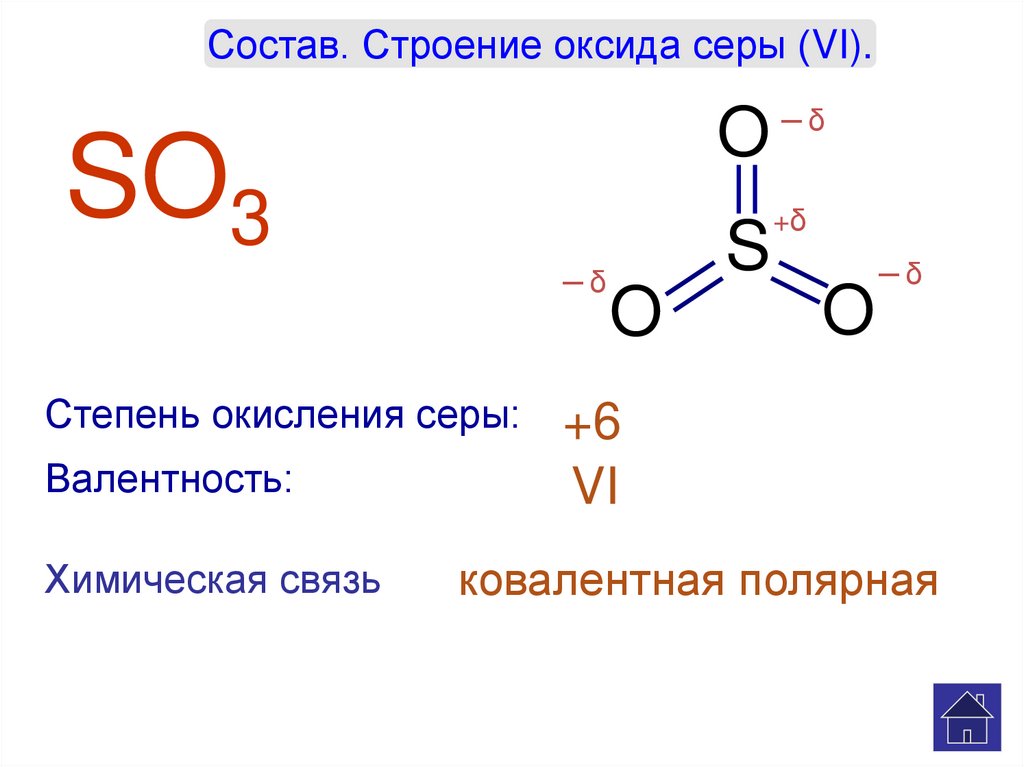
Состав. Строение оксида серы (VI).SO3
─δ
Степень окисления серы:
Валентность:
Химическая связь
O
O
─δ
S
+δ
O
─δ
+6
VI
ковалентная полярная
2. Физические свойства
В обычных условиях летучая бесцветнаяжидкость (tкип = 43°С) с удушливым запахом. При
температуре ниже 16,8°С застывает с
образованием смеси различных
кристаллических модификаций твердого SO3.
активно поглощается водой, также растворяется
в концентрированной серной кислоте с
образованием олеума.
3. Получение оксида серы (VI)
1.Окисление кислородом воздуха SO2 при нагревании
в присутствии катализатора
2SO2 + O2
2SO3
Охарактеризуйте данную реакцию по всем
возможным калассификациям.
Ответ:
2. Термическое разложение сульфатов:
2Fe2(SO4)3 = 2Fe2O3 + 6SO2 + 3O2
3. Взаимодействие SO2 озоном:
SO2 + O3 = SO3 + O2
4. Окисление SO2 оксидом азота (IV):
SO2 + NO2 = SO3 + NO
4. Характеристика реакции окисления оксида серы (IV)
1. Реакция окислительно-восстановительная.2. Реакция соединения, т.к. из двух соединений
образуется одно.
3. Обратимая реакция, т.к. протекает в двух
направлениях.
4. Реакция гомогенная, т.е. нет поверхности раздела
между реагирующими веществами, т.к. протекает
между газами.
5. Реакция каталитическая.
5. Химические свойства оксида серы (VI)
Опишите химические свойства оксида серы (VI) кактипичного кислотного оксида, приведя уравнения
реакций:
а) реакции с водой;
б) реакции с оксидом кальция;
в) реакции с гидроксидом натрия.
Рассмотрите данную реакцию с точки зрения ТЭД.
ответ
6. Химические свойства SO3
SO3 + H2O = H2SO4SO3 + CaO = CaSO4
SO3 + 2NaOH = Na2SO4 + H2O
SO3 + 2Na+ + 2OH― = 2Na+ + SO4 2– + H2O
SO3 + 2OH― = SO42– + H2O
SO3 + 2NaOH = NaHSO4 + H2O
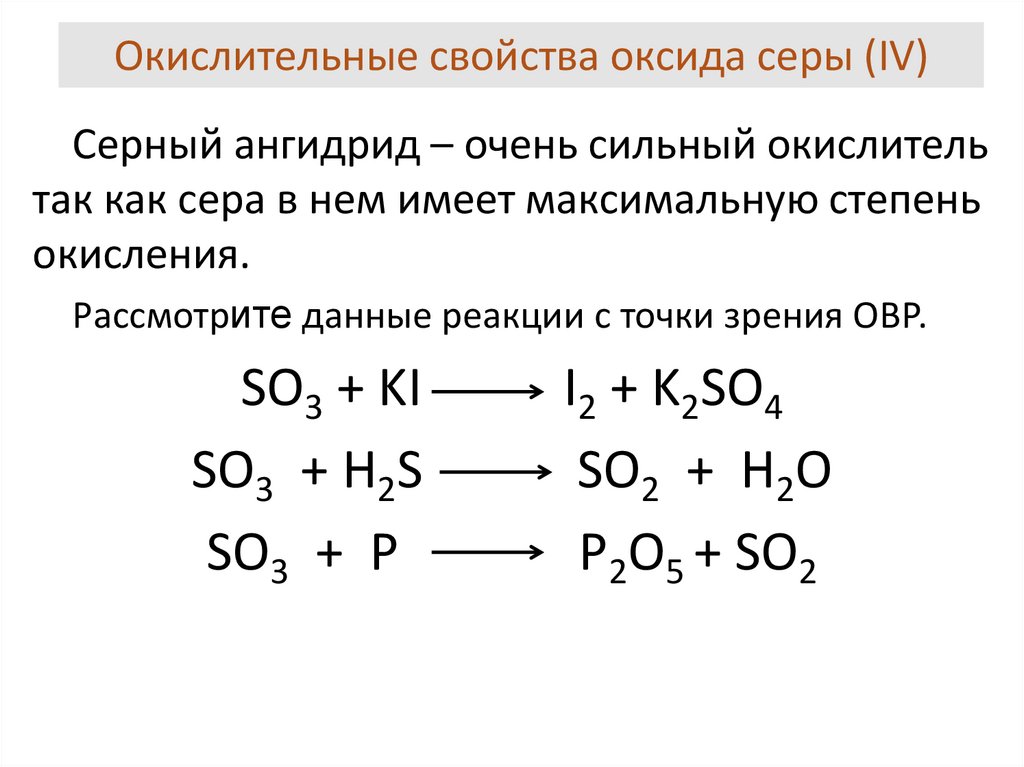
7. Окислительные свойства оксида серы (IV)
Серный ангидрид – очень сильный окислительтак как сера в нем имеет максимальную степень
окисления.
Рассмотрите данные реакции с точки зрения ОВР.
SO3 + KI
SO3 + H2S
SO3 + P
I2 + K2SO4
SO2 + H2O
P2O5 + SO2





 chemistry
chemistry








