Similar presentations:
Биологические мембраны, строение, функции. Транспорт веществ
1.
2. Немного истории кафедры нормальной физиологии Императорского университета г. Томск
3.
В 1888 году в Томске в составе Императорскогоуниверситета, произошло открытие медицинского
факультета!!!
Одной из первых кафедр, входивших
в состав факультета была кафедра
физиологии. Её основателем и первым
заведующим был Владимир
Николаевич Великий. В 1874 году он
окончил физико-математический факультет
(естественное отделение) Петербургского
Университета.
Великий заведовал кафедрой физиологии с
12 марта 1889 г. по 1903 год. С 5 января
1890 года по 12 января 1893 года исполнял
обязанности ректора Университета. Его
научные интересы были связаны с
проблемами иннервации лимфатических
сосудов, поджелудочной железы.
4.
С 1903г. по 1924г. кафедру возглавлял выдающийся отечественныйфизиолог, профессор Алексей Александрович Кулябко. В1888
году он окончил естественное отделение физико-математического
факультета Санкт-Петербургского университета. Будучи студентом
3 и 4 курса работал в физиологической лаборатории И.М. Сеченова
под руководством Н.Е. Введенского. В мае 1890 года был назначен
прозектором кафедры физиологии Томского Университета. Работая
прозектором, Алексей Александрович в
качестве вольного слушателя закончил медицинский факультет и
был удостоен в 1893 году звания лекаря с отличием.
В 1897 году в Военно-медицинской академии защитил докторскую
диссертацию: «К вопросу о желчных капиллярах». А.А. Кулябко
внес значительный вклад в развитие мировой науки. 3 августа 1902
г. он впервые в мире восстановил деятельность изолированного
сердца человека спустя 20 часов после смерти.
Эксперименты А.А. Кулябко по восстановлению функции сердца и головного
мозга, а так же целого организма стали, исходной методологической основой
для развития реаниматологии и трансплантологии сердца и других органов,
разработки и создания аппаратов вспомогательного и искусственного
кровообращения.
5.
Борис Иванович Баяндуров – ученик профессора Н.А.Попова. В 1930-1948 гг. он был первым заведующим
кафедрой нормальной физиологии Томского медицинского
института.
Изучал физиологию пищеварения, становление и развитие
функций головного мозга у птиц в филогенезе.
Итогом этой огромной работы явилась монография «ВНД у
птиц», которая была принята к печати специальным
разрешением Президиума АН СССР за подписью академика
Н.И.Вавилова. В 1946 году за монографию
«Трофическая функция головного мозга» он был удостоен
Сталинской (Государственной) премии второй степени. Под
руководством Б.И. Баяндурова были защищены 4
докторских и 13 кандидатских диссертаций. Перу проф.
Б.И. Баяндурова принадлежит более 160 научных статей,
опубликованных в отечественных и зарубежных журналах.
6.
В 1948-1975 гг. кафедрой заведовал профессор ЕвгенийФедорович Ларин.
В этот период на кафедре были развернуты широкие
исследования по физиологии органов пищеварения.
Основным направлением научных
исследований стало изучение функциональной
взаимосвязи печени с органами пищеварительного тракта
и другими системами организма, детально исследованы
механизмы рефлекторных реакций с рецепторов плевры и
мочевого пузыря. Была проведена большая работа по
изучению влияния минеральной воды курортов «Озеро
Карачи», «Озеро Шира» на секреторную и моторную
деятельность органов ЖКТ.
Заключительным этапом исследований Е.Ф. Ларина было
изучение роли двенадцати-перстной кишки и ее гормонов в
регуляции функций печени и гомеостаза.
7.
С 1975 года и по сей день кафедрой нормальной физиологииСибГМУ заведует Михаил Андреевич Медведев, профессор,
доктор медицинских наук, академик РАМН.
М.А. Медведев — продолжатель идей
основоположников сибирской научной
школы физиологов: профессора А.А.
Кулябко, лауреата Сталинской премии
профессора Б.И. Баяндурова, профессора
Е.Ф. Ларина. Михаил Андреевич получил
новые данные по механизмам эндокринной
регуляции моторной функции желудочнокишечного тракта, о месте гормонов
эндокринных желез в сложном механизме
нервных и гуморальных взаимоотношений,
их пролонгирующего воздействия.
М.А. Медведев — создатель томской научной школы физиологии и
биофизики гладких мышц желудочно-кишечного тракта.
8.
Биологические мембраны,строение, функции.
Транспорт веществ.
Севостьянова Наталия Владимировна
доктор медицинских наук,
профессор кафедры нормальной
физиологии
9. Биологическими мембранами (от лат. membrana – перепонка)
• Называют функциональные структуры клетки,ограничивающие цитоплазму и внутриклеточные
клеточные структуры.
10.
• Половинаобъема
клетки
занята
органеллами.
• Общая площадь поверхности мембран
внутриклеточных органелл в 10 раз!
превышает поверхность плазматической
мембраны.
11.
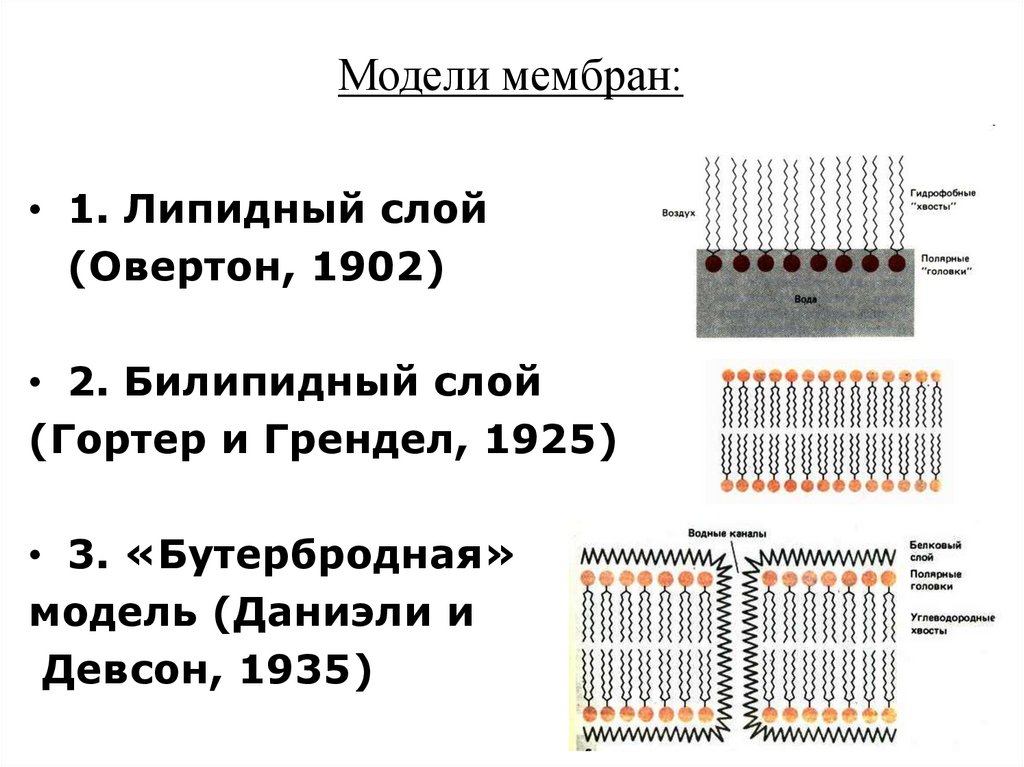
12. Модели мембран:
• 1. Липидный слой(Овертон, 1902)
• 2. Билипидный слой
(Гортер и Грендел, 1925)
• 3. «Бутербродная»
модель (Даниэли и
Девсон, 1935)
13. В 1925 г. Гортер и Грендель провели ацетоновую экстракцию теней эритроцитов (мембраны лопнувших в гипотоническом растворе
эритроцитов).После помещения на поверхность воды экстракт
образовал пленку, площадь которой оказалась в 2 раза
больше суммарной площади экстрагируемых мембран
эритроцитов. Из данного результата сделали вывод о
том, что мембрана образована двойным слоем липидов.
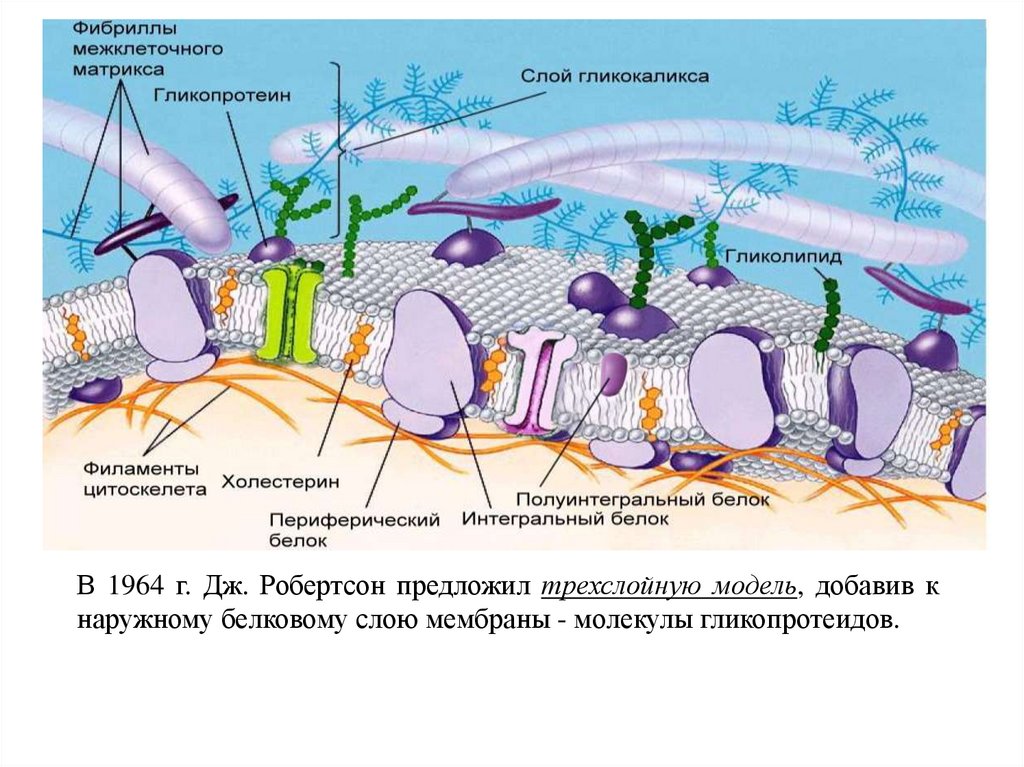
14.
В 1964 г. Дж. Робертсон предложил трехслойную модель, добавив кнаружному белковому слою мембраны - молекулы гликопротеидов.
15. 1966 г. Дж. Ленард и С. Сингер – предложили жидкомозаичную модель. Согласно этой модели белки «плавают» на поверхности
липидного слоя в виде отдельных глобулярных молекул иличастиц.
G. Vanderkooi, D. Green, 1970 г.
Белково-кристаллическая модель.
Отличается от жидкокристаллической лишь постулированием
существования в мембране жесткой белковой структуры,
возникающей в результате дальнодействующих белокбелковых связей.
16. Функции биологических мембран:
1. Барьерная функция - обусловливает создание концентрационныхградиентов, являющихся основой
механизма электрогенеза
(потенциал покоя, потенциал действия и др.).
2. Обеспечивают структурную организацию клеток и их компартментов
(отсеков).
3. Транспортные системы обеспечивают процессы метаболизма клеток
и поддержание внутриклеточного гомеостаза.
4. Регуляция внутриклеточных реакций и клеточного ответа.
6. Участие в реакциях превращения энергии.
7. Защитная функция.
8. Ферментативная.
9. Образование межклеточных контактов.
17. Структурные элементы биологической мембраны:
ЛипидыБелки
Углеводы
Вода
18. Химический состав
• Липидный бислой представленпреимущественно:
• фосфолипидами (глицерофосфатидами),
• сфингомиелинами
• стеролом— холестерином (холестеролом).
19. фосфолипиды
Липиды состоят изполярной (гидрофильной)
головки, шейки и
неполярных
(гидрофобных)
хвостов.
Головка образована:
остатком фосфорной
кислоты .
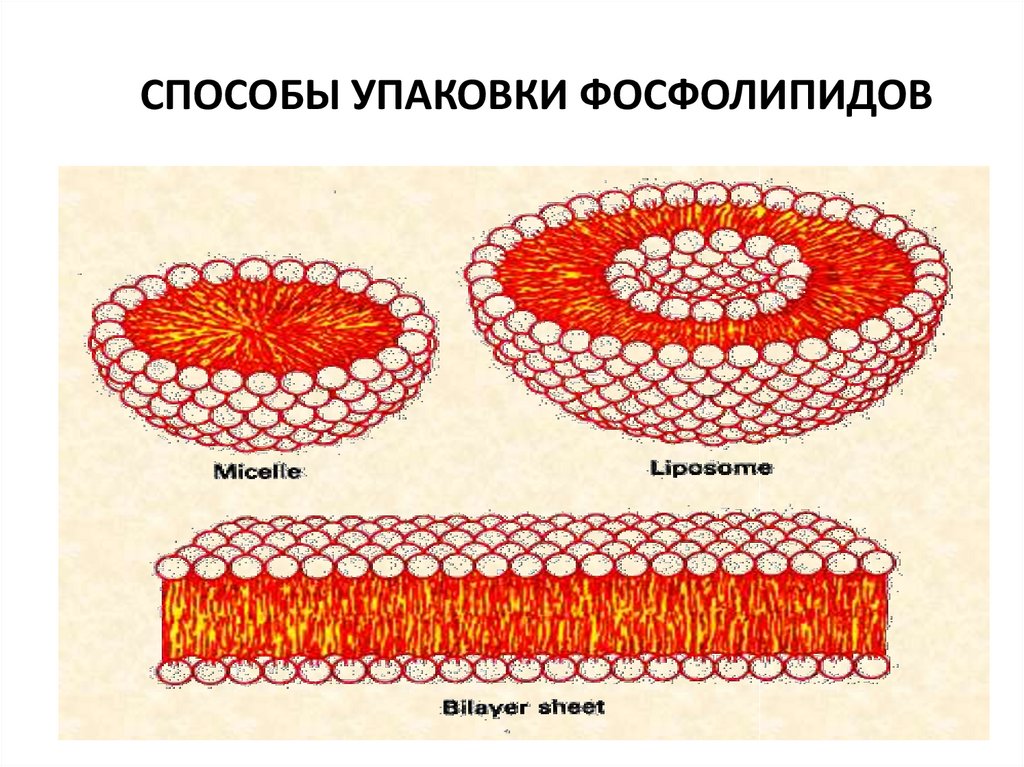
20. СПОСОБЫ УПАКОВКИ ФОСФОЛИПИДОВ
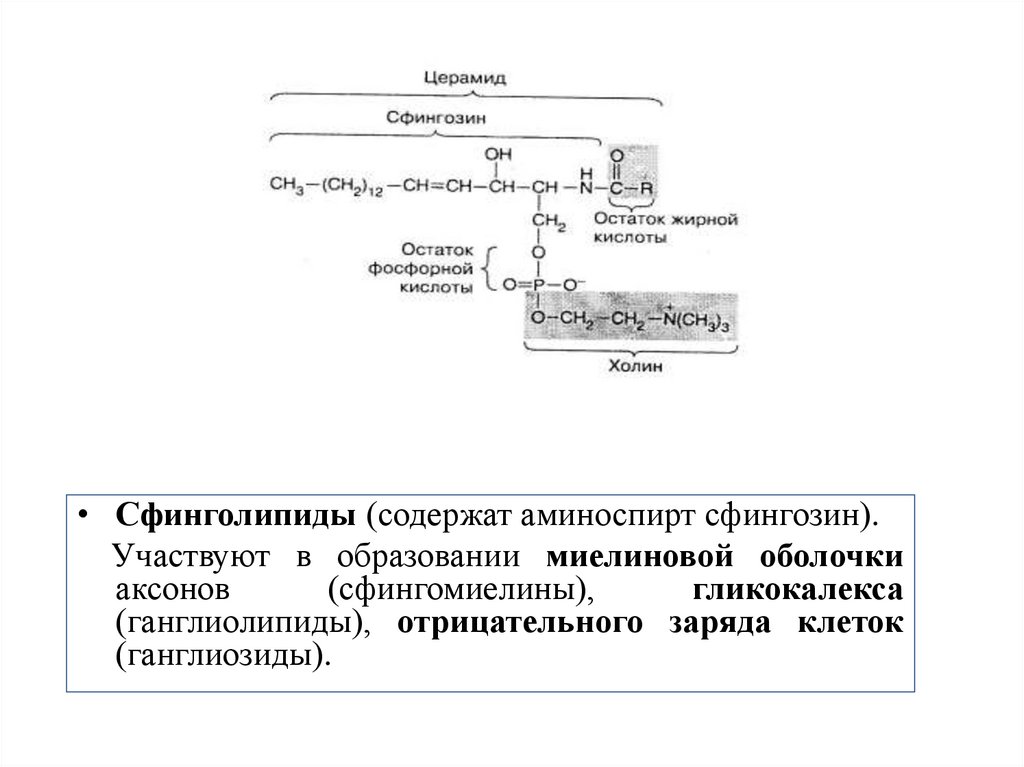
21.
• Сфинголипиды (содержат аминоспирт сфингозин).Участвуют в образовании миелиновой оболочки
аксонов
(сфингомиелины),
гликокалекса
(ганглиолипиды), отрицательного заряда клеток
(ганглиозиды).
22.
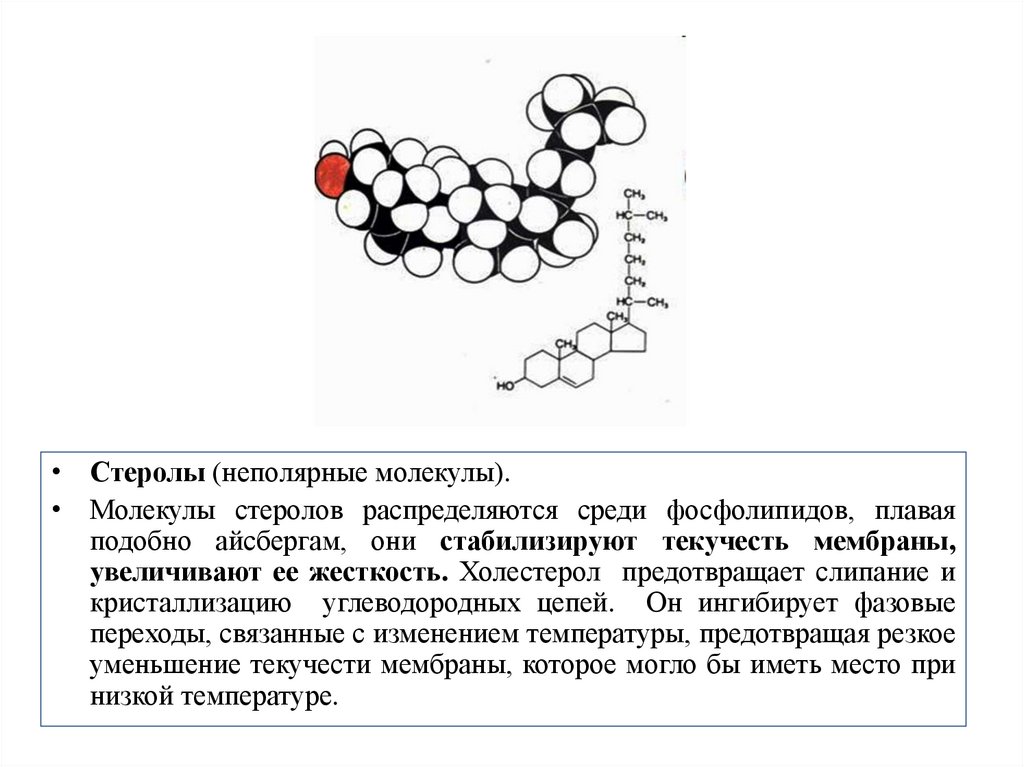
• Стеролы (неполярные молекулы).• Молекулы стеролов распределяются среди фосфолипидов, плавая
подобно айсбергам, они стабилизируют текучесть мембраны,
увеличивают ее жесткость. Холестерол предотвращает слипание и
кристаллизацию углеводородных цепей. Он ингибирует фазовые
переходы, связанные с изменением температуры, предотвращая резкое
уменьшение текучести мембраны, которое могло бы иметь место при
низкой температуре.
23. Функциональная классификация мембранных белков:
• 1. Белки – каналыОбеспечивают транспорт ионов.
• 2. Белки – транспортёры
Участвуют в транспорте веществ и ионов.
• 3. Белки – рецепторы
Осуществляют восприятие из внешней среды химических и физических
раздражителей.
• 4. Белки – ферменты
Участие в биохимических реакциях.
• 5. Структурные белки
Обеспечивают поддержание формы и структуры клеток, формируют
цитоскелет, участвуют в делении клеток и т.д.
24. Структурная классификация белков мембраны:
• Белки биологических мембран подразделяют на периферические иинтегральные (в том числе трансмембранные) .
Периферические мембранные белки находятся на одной из
поверхностей клеточной мембраны (наружной или внутренней) и легко
могут быть отделены от мембраны.
• Примеры периферических белков, связанных с наружной поверхностью
мембраны: белки адгезии, некоторые рецепторные белки (мембранные
рецепторы).
• Примеры периферических белков, связанных с внутренней
поверхностью мембраны: белки цитоскелета, ферменты, белки
системы вторичных посредников и др.
25. Функции углеводов
межклеточное узнавание,
межклеточные взаимодействия,
поддержание иммунного статуса клетки,
обеспечение стабильности белковых молекул в
мембране,
• взаимодействие с цитоскелетом.
26.
• Виды мембранного транспорта:• Прямой
Опосредованный
• Прямой (пассивный) транспорт:
1.
2.
3.
4.
простая диффузя;
фильтрация;
осмос;
электроосмос.
27.
• Диффузия – самопроизвольный процесс проникновениявещества из области большей концентрации в область
меньшей его концентрации, в результате теплового
хаотического движения молекул.
• Математически этот процесс описывается формулой Фика:
• dm/dt = -D·S·dс/dx
• dm/dt – скорость диффузии;
• D – коэффициент диффузии (Крога), зависит от природы и
молекулярной массы вещества и растворителя, от
температуры, свойств мембраны и ее функционального
состояния.
• S – площадь сечения через которую осуществляется диффузия.
• dс/dx – градиент концентрации, т.е. изменение концентрации
вещества с расстоянием.
28.
Опосредованный транспортАктивный транспорт
Без изменения структуры
Облегченная диффузия
(без затраты энергии)
С участием
каналов
АТФ-азы: 3Nа+ /2 К+; 2H +/Са2+
С участием переносчиков
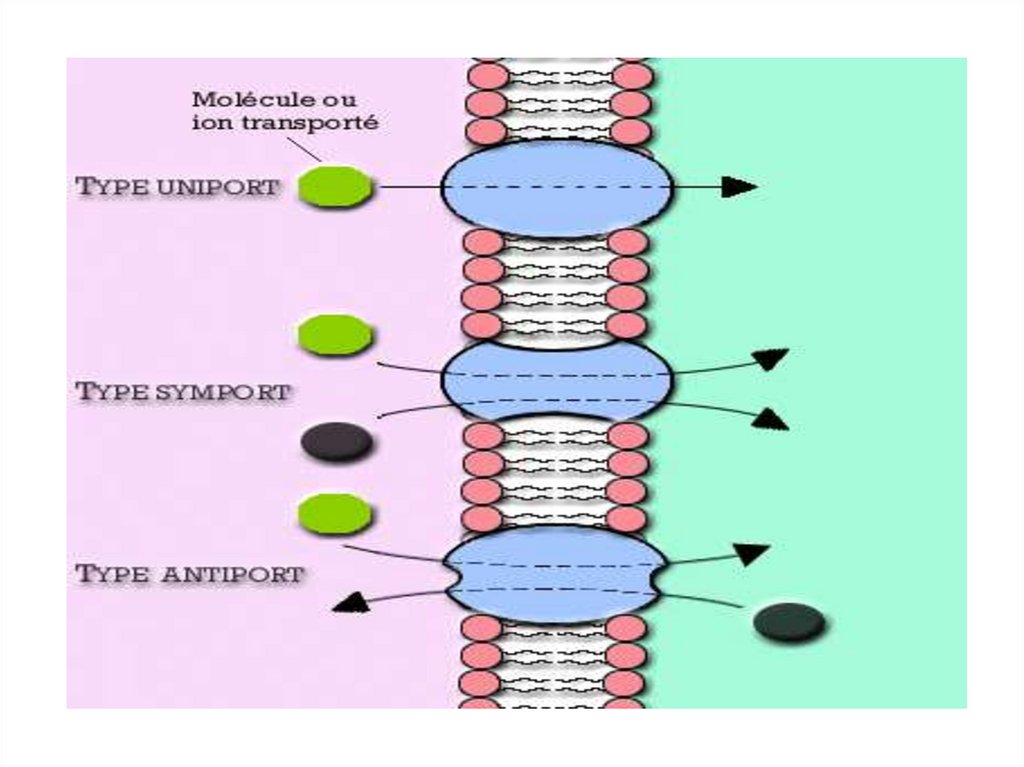
унипорт
Потен/чувств.
Хемо/чувств.
Мех/чувств.
котранспорт
антипорт
С изменением структуры
эндоцитоз
симпорт
экзоцитоз
29. Переносчики
• Переносчики (транспортёры) осуществляют транспортчерез биологические мембраны множества различных
ионов (Na+, Cl–, H+, HCO3– и др.) и органических веществ
(глюкоза, аминокислоты, креатин, норадреналин, лактат,
пируват и др.).
• Транспортёры
специфичны:
каждый
конкретный
переносчик переносит через липидный бислой,
определённое вещество, либо несколько молекул.
• Различают однонаправленный (унипорт), сочетанный
(симпорт) и разнонаправленный (антипорт) транспорт.
30.
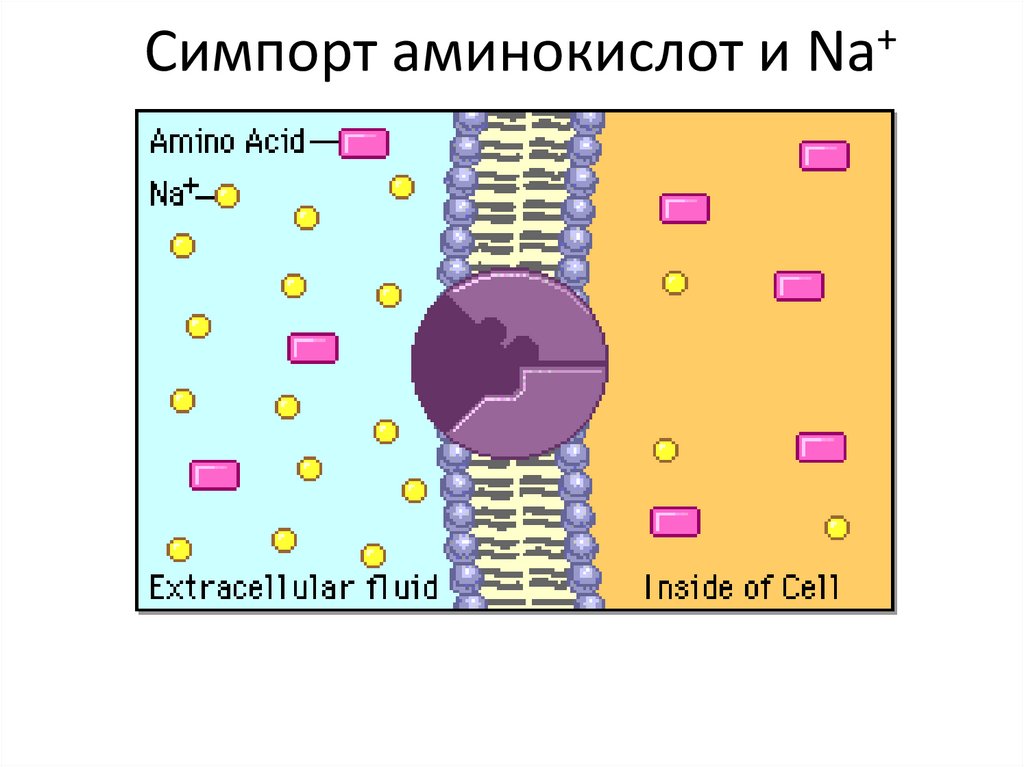
31. Симпорт аминокислот и Na+
32.
Антипорт:• Катионные обменники –
Nа+/Н+ – обмен, Nа+/Са+–обмен (2Nа/Са)
• Анионные обменники –
СL-/НСО3-
33. Простая диффузия Облегченная диффузия
обеспечивается работой
переносчиков, встроенных в
мембрану и отличается от
простой диффузии:
Высокой скоростью
переноса
Чувствительностью к
специфическим
ингибиторам
Насыщаемостью
34.
Ионные каналы – интегральные белки мембраны,выполняющие функции транспорта для соответствующих
ионов.
• Они различаются по избирательной пропускной способности
к соответствующим ионам (селективности) и типу активации
– электрическим, химическим или механическим стимулом,
соотвественно разделяясь на потенциало хемо и
механочувствительные.
• Селективность канала определяется специфическими
свойствами его устья – селективнстью фильтра и знаком
заряда, молекул формирующих устье, а также геометрией
канала.
• По селективности каналы делятся на:
• натриевые, калиевые, кальциевые и хлорные.
35.
• Потенциалозависимые ионные каналы управляютсямембранным потенциалом (МП).
Колебания
МП
приводят
к
конформационным
изменениям белковой структуры канала, что и
переводит канал в открытое либо закрытое состояние.
• В связи с этим модель канала предусматривает наличие
устройства, открывающего и закрывающего канал —
воротный механизм, или воротную частицу, положение
которой управляется сенсором, имеющим заряд и
реагирующим на изменение мембранного потенциала.
36. Строение потенциалозависимого ионного канала: 1 — липидный бислой, 2 — сенсор напряжения, 3— ворота, 4 — белковая
макромолекула, 5 — якорный белок, 6—углеводные цепи, 7 — селективный фильтр, 8 — водная
пора, Р — участок фосфорилирования канала, А — наружный
раствор, Б — цитоплазма.
37.
• Xемоуправляемые каналы ( лиганд–зависимыеионные каналы, рецептор–зависимые)
• Соединение лиганда с рецептором вызывает
конформационные изменения в канале, изменяющие
его функциональное состояние.
• Лиганд–зависимые каналы не столь избирательны,
как потенциало-зависимые и, будучи в открытом
состоянии, пропускают несколько разных, но
одинаково заряженных ионов.
38.
ионотропныеметаботропные
39. Активный транспорт
1. Осуществляется против электрохимическогоградиента;
2. Система в высшей степени специфична;
3. Необходимы источники энергии в виде АТФ ;
4. Энергия, высвобождается при гидролизе АТР
ферментами, встроенными в мембрану;
5. Насосы обменивают один вид ионов на другой;
6. Избирательно подавляются блокаторами.
40.
Первичный
активный
транспорт.
Движущая
сила
трансмембранного
переноса возникает при ферментативном
гидролизе макроэргических связей АТФ.
3Na+/2K+ или Ca2+-АТФазы (насосы).
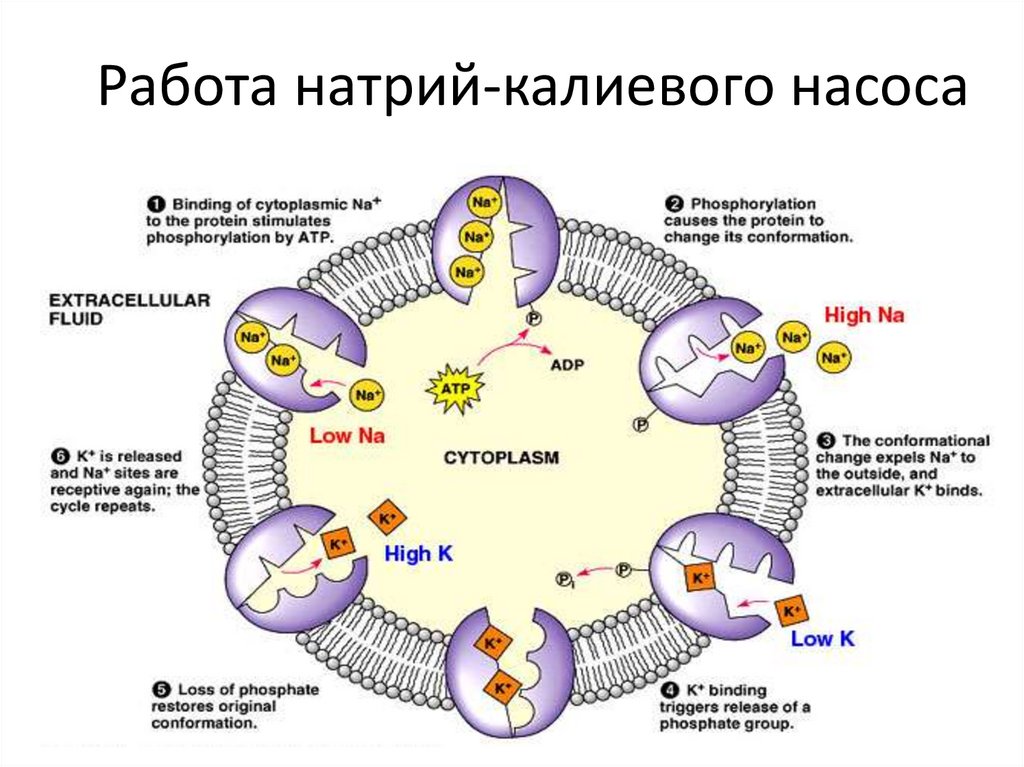
41. Первично-активный транспорт
Схема Na/K–АТФазы котораяза один цикл выносит из
клетки три иона Na+ против
градиентов
потенциала
и
концентрации и приносит в
клетку два иона К+. В ходе
этого процесса одна молекула
АТФ расщепляется на АДФ и
фосфат.
АТФаза существует как
тетрамер, образованный двумя
большими и двумя малыми
субъединицами
42. Работа натрий-калиевого насоса
43. Вторичный активный транспорт.
Движущая сила для трансмембранного переноса одноговещества (или ионов) против электрохимического градиента
возникает за счёт потенциальной энергии, запасённой за счёт
сочетанного переноса ионов (как правило, Na+) по
электрохимическому градиенту.
В большинстве случаев поступление Na+ в цитозоль из
межклеточного пространства и обеспечивает вторичный
активный транспорт разных ионов и веществ.
Известно 2 типа вторичного активного переноса:
симпорт и антипорт.
44. Вторичный активный транспорт
В качестве источника энергиииспользует
химический
или
электрохимический
градиент
какого-либо вещества
45. Эндоцитоз
1. Молекулы лиганда связываютсямолекулами рецептора,
расположенными в окаймленных
ямках (1);
2. Ямки образуются при связывании
молекул клатрина с
поверхностной мембраной.
3. Происходит инвагинация
окаймленной ямки (2)
4.
5.
6.
7.
Образуется окаймленная везикула (3),
Везикула сливается с вакуолью (4).
Вакуоль и ее содержимое претерпевают превращения (5),
Клатрин и молекулы рецептора возвращаются в
плазматическую мембрану до повторного использования (6)
46. Экзоцитоз
1. В ЭПРсинтезируется
предшественник секрета;
2. От ЭПР
везикула с
веществом
транспортируется к
аппарату
Гольджи;
3. В аппарате Гольджи из предшественника образуется конечный секрет;
4. Везикула с секретом доставляется к плазматической мембране;
5. Мембрана везикулы сливается с плазматической мембраной и вещество
высвобождается во внеклеточную среду
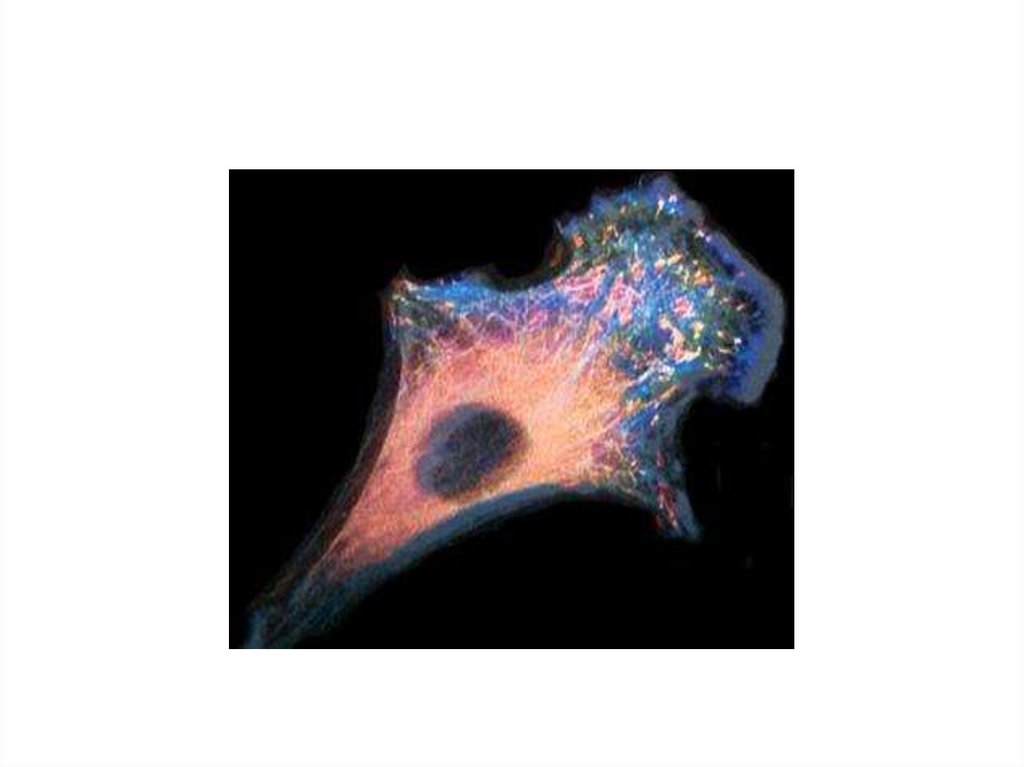
47. Цитоскелет клетки
48.
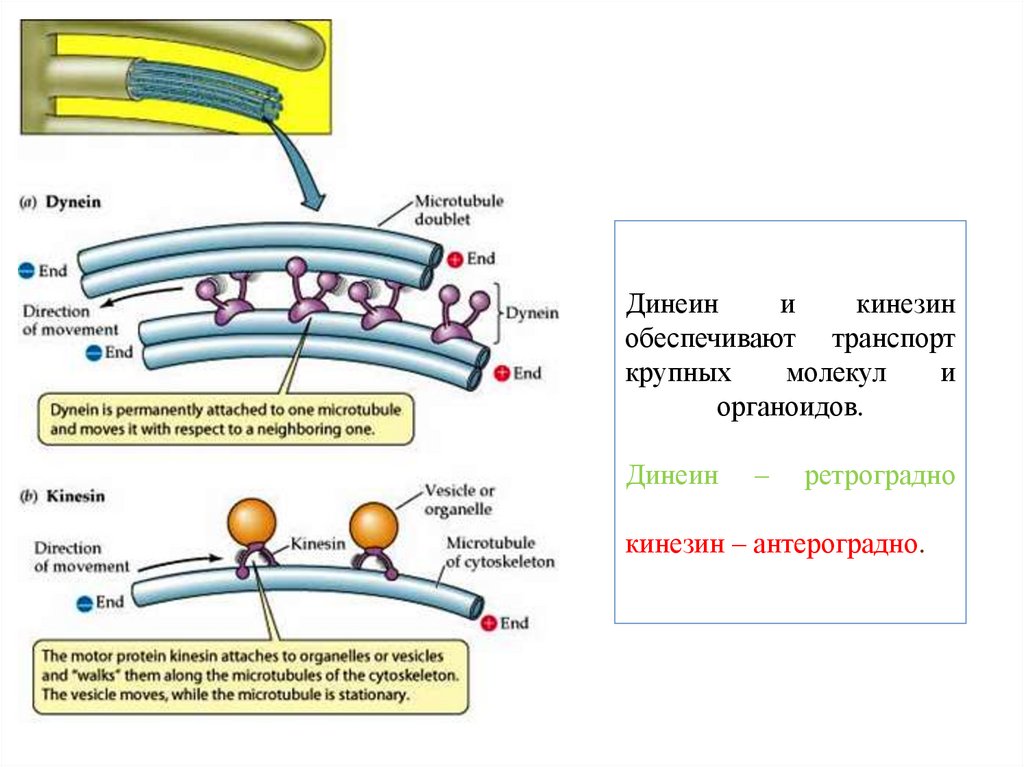
49. Динеин и кинезин обеспечивают транспорт крупных молекул и органоидов. Динеин – ретроградно кинезин – антероградно.
50.
51.
Основы электрофизиологииОбщая характеристика
возбудимых тканей.
Потенциал покоя.
Потенциал действия.
52.
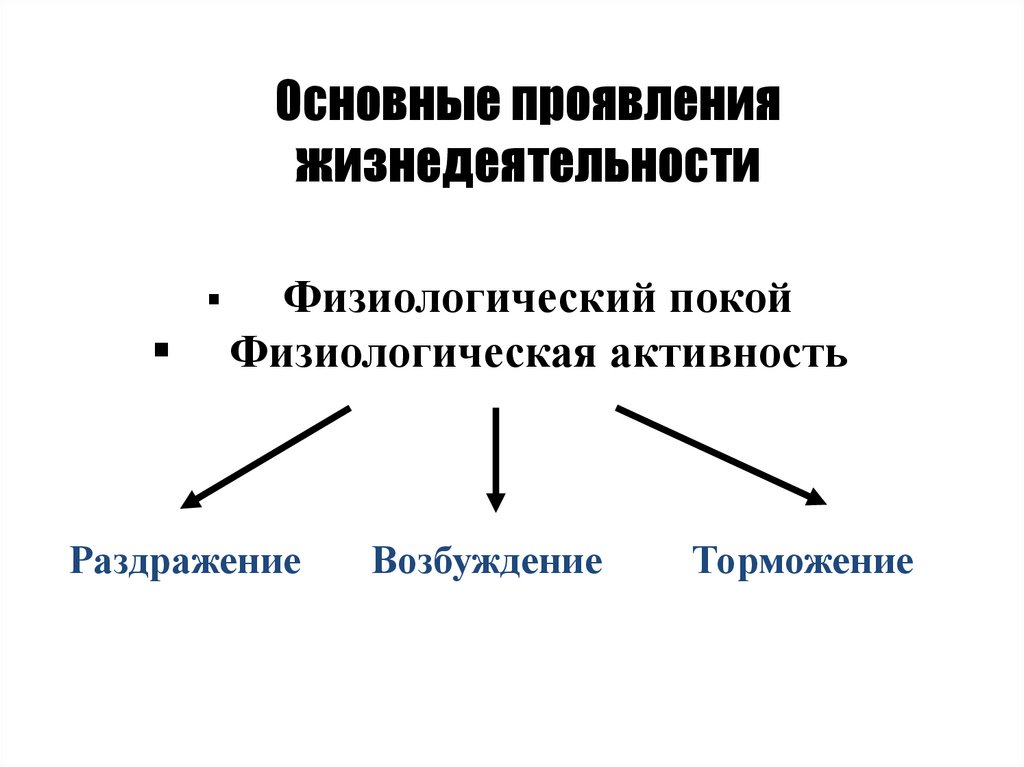
Основные проявленияжизнедеятельности
Физиологический покой
Физиологическая активность
Раздражение
Возбуждение
Торможение
53.
• Общая характеристика возбудимых тканей.• Все клетки нашего организма обладают свойством раздражимости.
• Раздражимость – это способность клеток переходить из состояния
физиологического покоя в состояние функциональной активности
при действии внешних или внутренних стимулов.
• Три вида тканей: нервная, мышечная и секреторная обладают
особой формой раздражимости – возбудимостью.
• Возбудимость – способность ткани реагировать возбуждением на
внешние стимулы.
• Возбуждение – реакция
мембранного потенциала.
на
раздражение
путем
изменения
54. Раздражение и виды раздражителей.
• Раздражение – это процесс воздействия на живойобъект внешних по отношению к нему факторов.
• Раздражители – факторы внешней среды, вызывающие
переход биосистемы в активное состояние.
Раздражители разделяют по следующим факторам:
природе раздражителей;
биологическому значению;
количественному признаку.
55. По природе раздражителя:
• 1. физические ( температура, звук, свет, электрическийток и т.д.).
• 2. химические (соли, кислоты, щелочи и т.д.).
• 3. физико-химические (изменение осмоса, парциального
давления газов, рН).
• 4. биологические (вирусы, бактерии, токсины антитела и
т.д.).
56.
• По биологическому значению:• 1. адекватные – раздражитель к которому в естественных
условиях
у
биосистем
есть
специализированные
воспринимающие структуры (рецепторы).
• Свет – для фоторецепторов;
• Упругие механические колебания среды – для рецепторов
слуха.
• 2. неадекватные – раздражители не являющиеся в
естественных условиях средством возбуждения для данных
биоструктур.
57.
• По количественному признаку или порогураздражения:
В зависимости от силы действия раздражители делятся на:
• 1. пороговые – минимальная сила раздражителя, способная
вызвать возбуждение.
подпороговые – сила раздражения ниже порога возбуждения.
• 2. максимальные – минимальная сила раздражителя,
вызывающая максимальный ответ ткани.
Раздражители, сила которых меньше или больше максимальной
называются, соответственно:
субмаксимальными и супермаксимальными.
58. Все возбудимые ткани обладают общими свойствами:
Возбудимостью
Проводимостью
Лабильностью
Аккомодацией
59.
•Возбудимостьколичественно
характеризуется
порогом
возбуждения,
который
определяется
минимальной
силой
раздражения, способной вызывать возбуждение.
•Проводимость – способность проводить возбуждение.
Оценивается по скорости распространения возбуждения (м/с).
•Лабильность – функциональная подвижность ткани.
Оценивается по максимальному числу импульсов, которое возбудимая
ткань способна воспроизвести в соответствии с частотой
раздражения.
Нерв – до 1000 П Д/с, мышца – 500 ПД/с, синапс – 50 ПД/с.
•Аккомодация – повышение порога возбуждения к медленно
нарастающему или постоянно действующему раздражителю.
60. Законы раздражения:
Закон силыЗакон времени
Закон крутизны
нарастания
раздражителя
61. Закон силы
Чем сильней раздражение, тем до определенногопредела сильнее ответная реакция биосистемы.
Закон
постулирован
для
целостного
биологического объекта.
Например, нервного ствола, состоящего из
отдельных аксонов; скелетной мышцы и т.д.
Связано это с тем, что каждое отдельное волокно
отвечает на раздражитель по типу «все или ничего», но
порог возбуждения у них отличается.
Поэтому суммарная активность объекта будет
находится в градуальной зависимости от силы
раздражителя.
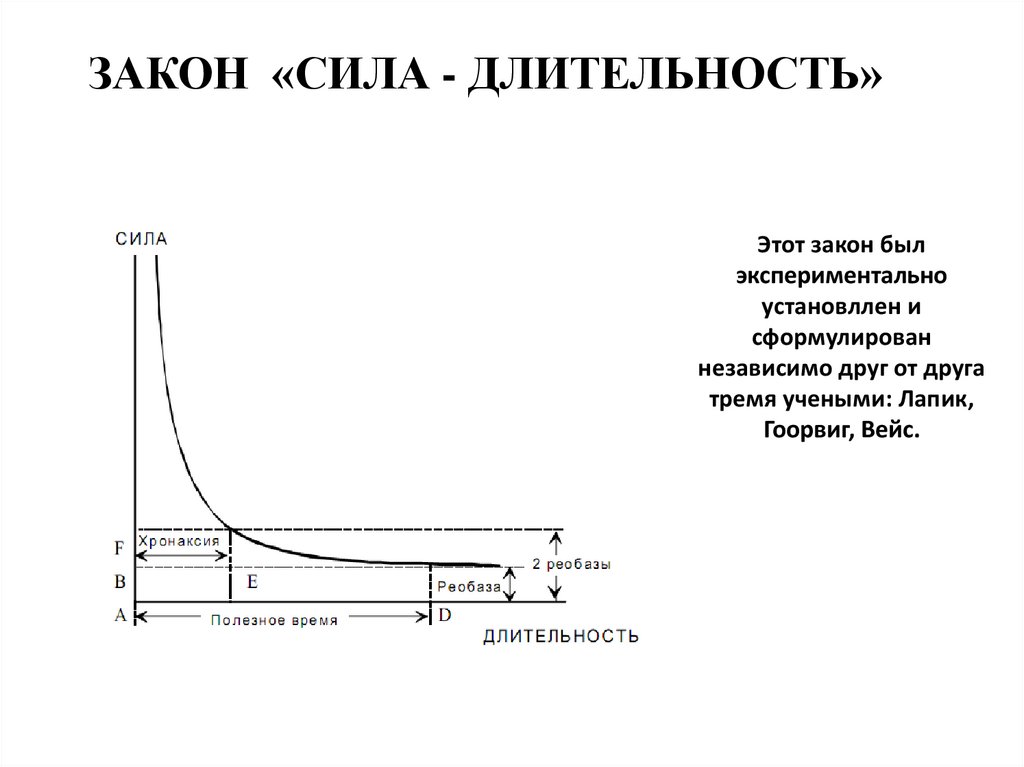
62. Закон времени
• Чем длительнее раздражение, тем сильней доопределенных пределов ответная реакция живой
ткани.
• В определенном диапозоне эта зависимость имеет
характер гиперболы. На ней выделяют реобазу, полезное
время и хроноксию.
• Реобаза - соответствует порогу возбуждения.
• Полезное время – минимальное время, в течение
которого раздражитель, равный одной реабазе, должен
действовать на ткань, чтобы вызвать возбуждение.
• Хроноксия – время, в течение которого должен
действовать раздражитель, равный двум реабазам,
чтобы вызвать возбуждение.
63. ЗАКОН «СИЛА - ДЛИТЕЛЬНОСТЬ»
Этот закон былэкспериментально
установллен и
сформулирован
независимо друг от друга
тремя учеными: Лапик,
Гоорвиг, Вейс.
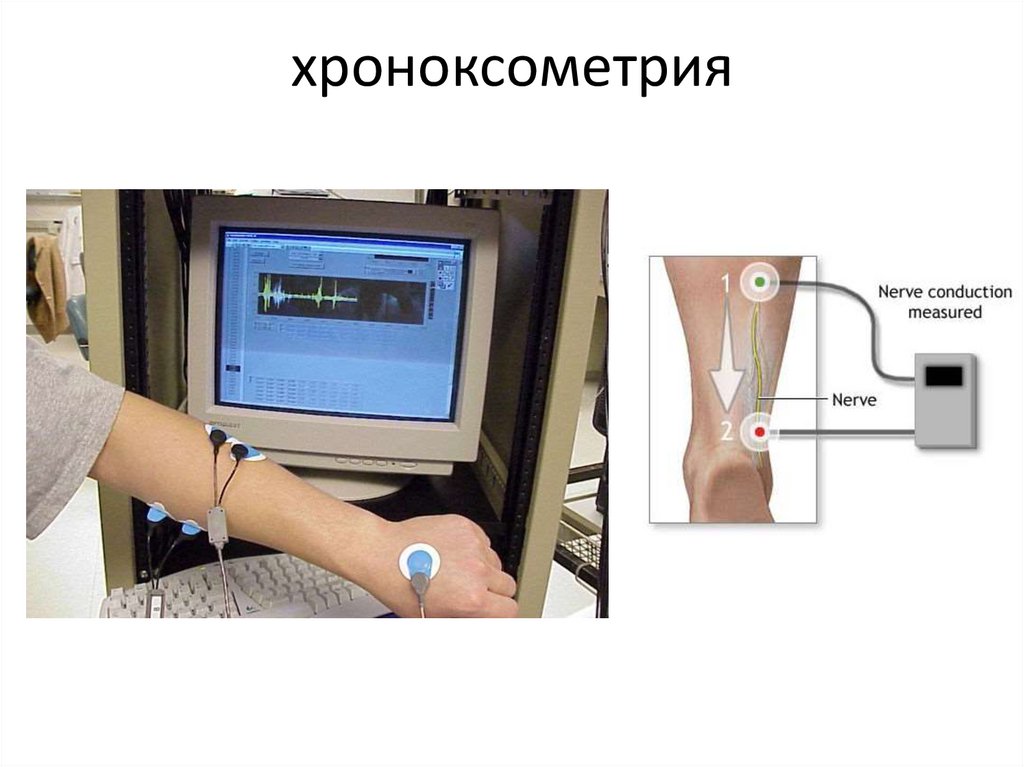
64. хроноксометрия
65. Закон крутизны нарастания раздражителя или градиента:
• Чем выше крутизна нарастания раздражителя вовремени, тем больше до известного предела величина
функционального ответа.
• В основе этого закона лежат физико-химические и
функциональные
изменения,
вызываемые
в
раздражаемом объекте.
• Возбуждение развивается в том случае, если
активационные
процессы
достигают
пороговой
критической величины раньше инактивационных.
66.
История открытиябиоэлектри чества.
67.
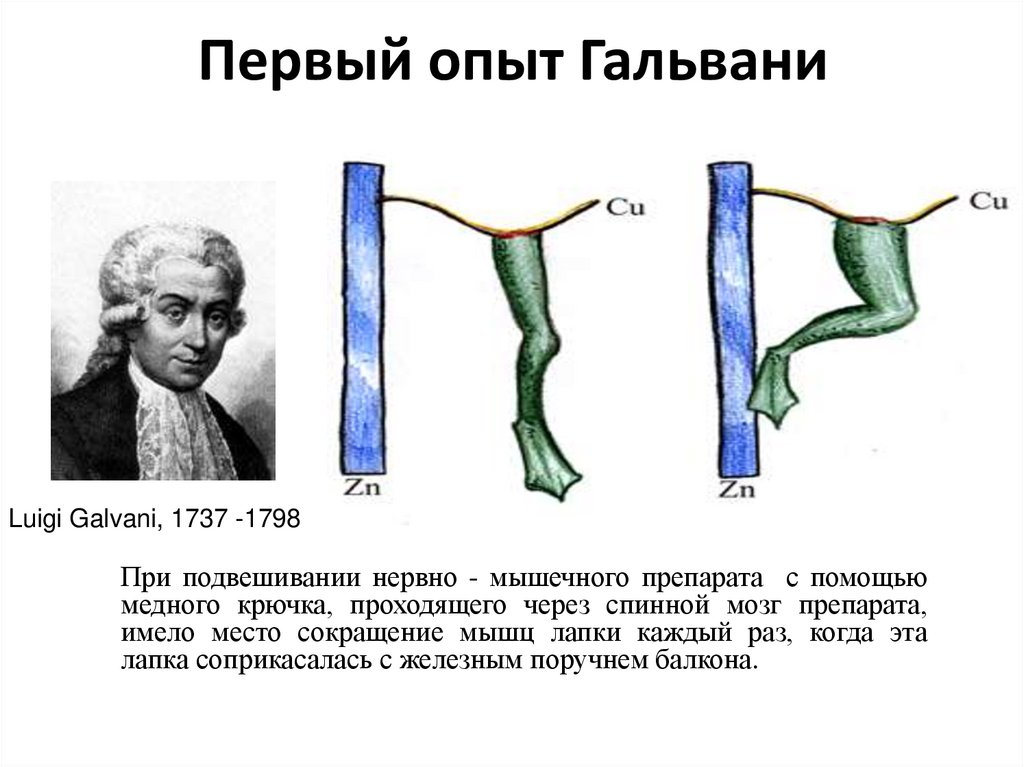
68. Первый опыт Гальвани
Luigi Galvani, 1737 -1798При подвешивании нервно - мышечного препарата с помощью
медного крючка, проходящего через спинной мозг препарата,
имело место сокращение мышц лапки каждый раз, когда эта
лапка соприкасалась с железным поручнем балкона.
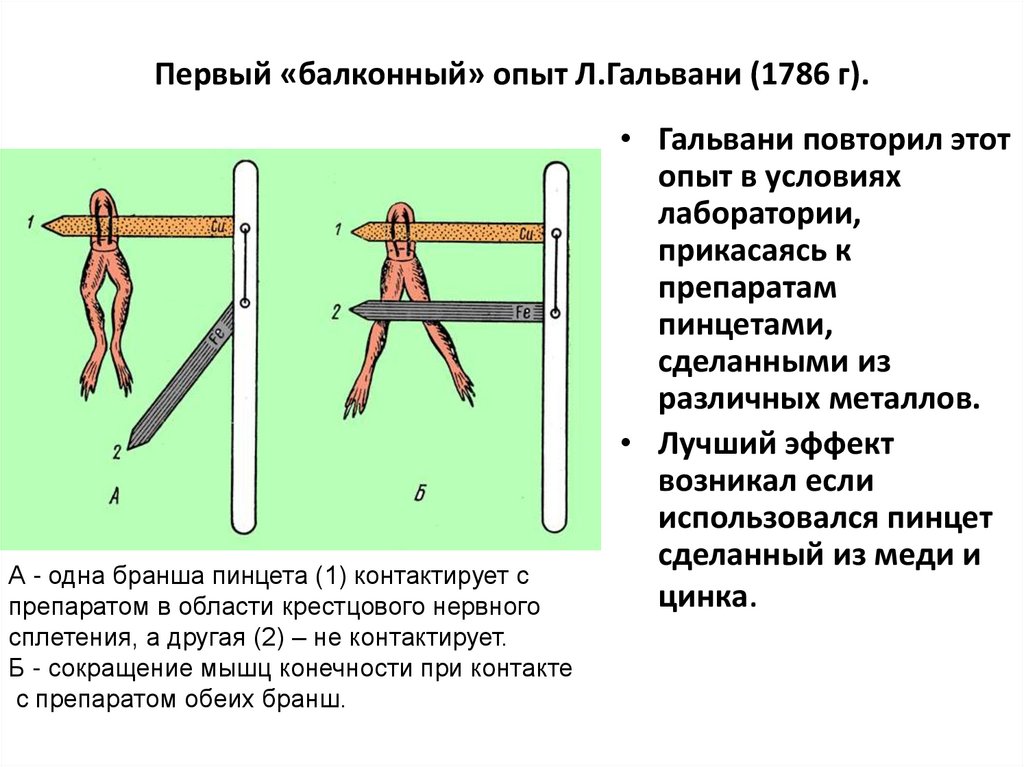
69. Первый «балконный» опыт Л.Гальвани (1786 г).
А - одна бранша пинцета (1) контактирует спрепаратом в области крестцового нервного
сплетения, а другая (2) – не контактирует.
Б - сокращение мышц конечности при контакте
с препаратом обеих бранш.
• Гальвани повторил этот
опыт в условиях
лаборатории,
прикасаясь к
препаратам
пинцетами,
сделанными из
различных металлов.
• Лучший эффект
возникал если
использовался пинцет
сделанный из меди и
цинка.
70.
ВОЛЬТОВ СТОЛБОднако ему возразил его
знаменитый соотечественник физик А. Вольта, который
считал, что в «балконном»
опыте мышца является лишь
чувствительным
«электрометром»
электричества, порождаемого
контактной
разностью
потенциалов разных металлов,
используемых
в
опытах
Гальвани.
Вольтов столб, состоящий из металлических дисков,
разделенных кружками мокрой ткани.
71. Алессандро Вольта
• Электрический ток возникает не в живыхклетках, а на границе контакта
разнородных металлов с электролитом.
• То есть источником тока является не
живая ткань («животное электричество»),
а металлы. Живая ткань является лишь
проводником электрического тока.
Alessandro Volta,
1745-1827
• А.Вольта создал генератор
электрического тока – гальванический
элемент (вольтов столб).
72. Гальванический элемент. Вольтов столб
• В 1800 году А.Вольта опустил в банку скислотой две пластинки — цинковую и
медную — и соединил их проволокой. После
этого цинковая пластина начала растворяться,
а на медной стали выделяться пузырьки газа.
• Вольта показал, что по проволоке протекает
электрический ток.
• Так был изобретён «элемент Вольта» —
первый гальванический элемент.
• Для удобства Вольта придал ему форму
вертикального цилиндра (столба), состоящего
из соединённых между собой колец цинка,
меди и сукна, пропитанных кислотой. Вольтов
столб высотою в полметра развивал
напряжение, чувствительное для человека
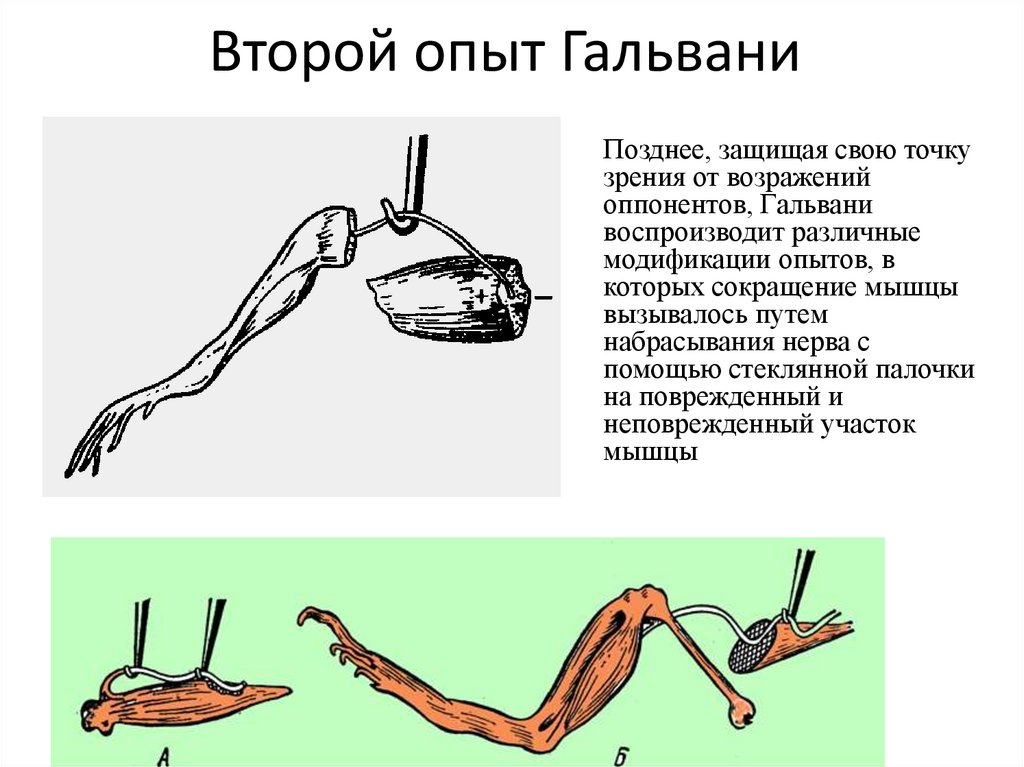
73. Второй опыт Гальвани
Позднее, защищая свою точкузрения от возражений
оппонентов, Гальвани
воспроизводит различные
модификации опытов, в
которых сокращение мышцы
вызывалось путем
набрасывания нерва с
помощью стеклянной палочки
на поврежденный и
неповрежденный участок
мышцы
74.
Открытия Гальвани были подтверждены в
работах Маттеучи (1837).
Маттеучи обнаружил явление вторичного или
индуцированного сокращения: при помещении
нерва одного нервно-мышечного препарата на
мышцу другого препарата и раздражителя нерва
этого препарата, Маттеучи наблюдал сокращение
мышцы обоих препаратов.
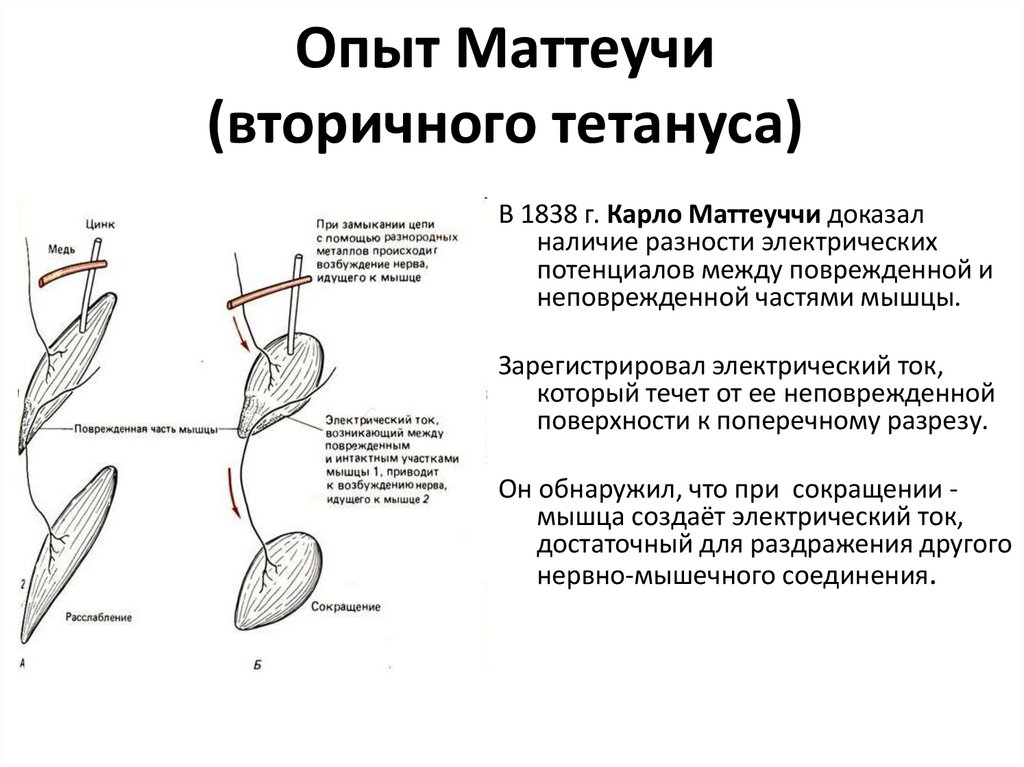
75. Опыт Маттеучи (вторичного тетануса)
В 1838 г. Карло Маттеуччи доказалналичие разности электрических
потенциалов между поврежденной и
неповрежденной частями мышцы.
Зарегистрировал электрический ток,
который течет от ее неповрежденной
поверхности к поперечному разрезу.
Он обнаружил, что при сокращении мышца создаёт электрический ток,
достаточный для раздражения другого
нервно-мышечного соединения.
76.
Работы Э.ДюбуаРеймона( выполненны в 1840-1860 гг. )
В этих работах благодаря высокочувствительному
гальванометру и ряду других технических новшеств
удалось впервые определить электрические процессы
в мышце, зарегистрировав потенциал наружной и
внутренней поверхности мембраны клеток.
Он впервые установил, что наружная мембрана
заряжена положительно по отношению к внутренней,
и эта разность потенциалов изменяется при
сокращении мышцы.
77.
Природа и происхождениепотенциал покоя (Ео)
мв
+30
0
-75
Ео
78.
ЮлиусБернштейн
В 1896 г. В.Ю. Чаговец впервые высказал гипотезу о ионном механизме
электрических потенциалов в живых клетках. Он сделал попытку применить
теорию электролитической диссоциации Аррениуса - для их объяснения.
В 1902 г. Бернштейном была развита мембранно-ионная теория, согласно
которой клеточная поверхность представляет собой полупроницаемую
мембрану, которая в состоянии физиологического покоя проницаема для
ионов калия и практически непроницаема для остальных вне - и
внутриклеточных ионов.
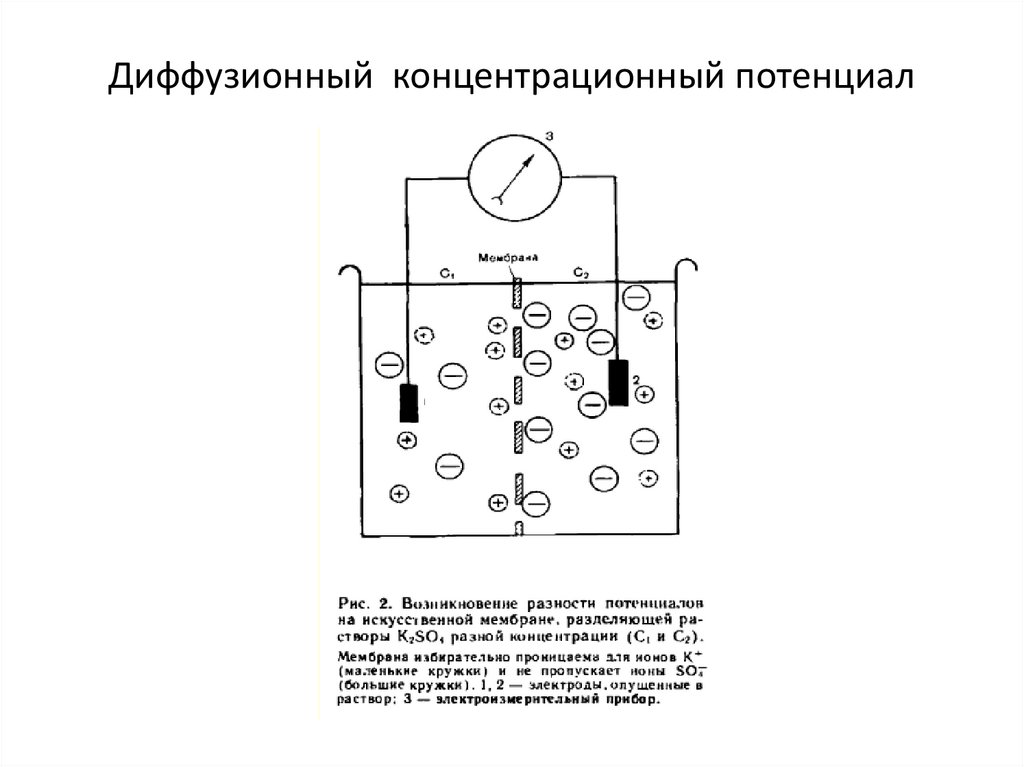
79. Диффузионный концентрационный потенциал
80. Уравнение НЕРНСТА
[ K +o]RT
Ек =
ℓn
nF
[ K +i]
Ек – равновесный калиевый потенциал;
R - универсальная газовая постоянная Больцмана;
T - температура среды;
n - валентность иона ( для К+ = 1);
F - число Фарадея;
К+ - концентрация калия с внешней (о) и внутренней
(i) стороны мембраны.
81.
В 1936 году английский зоолог Джон Юнг обнаружил укальмаров и каракатиц необычайно толстые аксоны,
которые впоследствии стали называть "гигантскими
аксонами". Их диаметр превышал 0,5 мм, что позволило
достаточно легко вводить в них микроэлектроды,
проводить химический анализ содержащейся в них
жидкости, вводить в них различные растворы и т.д.
«Гигантские аксоны» стали излюбленным объектом
для изучения биоэлектрических явлений в тканях, с их
помощью было получено много новых и интересных
данных.
82.
83.
84. Экспериментальная проверка гипотезы Бернштейна
• В 1962 г. Ходжкин с сотрудниками подтвердил гипотезуБернштейна:
• Из аксона кальмара выдавили аксоплазму и спавшуюся
оболочку заполнили искусственным солевым раствором.
Когда концентрация калия была близка к внутриклеточной, между внутренней и наружной мембраной установилась разность
потенциалов близкая к ПП (-50/-80 мВ), и волокно проводило
импульсы.
• При снижении концентрации
калия или увеличении –
мембранный потенциал менялся, или даже изменял свой знак
(потенциал становился положительным, если в наружном растворе
[ K +o] > [ K +i] ).
• Это доказывало, что концентрационный градиент калия
является основным фактором, определяющим величину ПП
нервного волокна.
85. Методы регистрации электрических потенциалов мембраны
86.
87. Проницаемость мембраны для ионов в покое
pK+ : pNa+ : pCl - = 1 : 0,04 : 0,4588. Уравнение ГОЛЬДМАНА
Pk [ Ko+] + PNa [ Nao+]+PCl [ Cli- ]RT
Ем
ℓn
=
nF
Pk[ Ki+]+ PNa [ Nai+] + PCl[ Clo–]
Ем – равновесный калиевый потенциал;
R - универсальная газовая постоянная;
T - температура среды;
n - валентность иона;
F - число Фарадея;
P – проницаемость иона для мембраны;
К+ - концентрация калия с внешней (о) и внутренней (i) стороны
мембраны.
Na+ - концентрация натрия с внешней (о) и внутренней (i) стороны
мембраны.
Cl- - концентрация хлора с внешней (о) и внутренней (i) стороны
мембраны.
89.
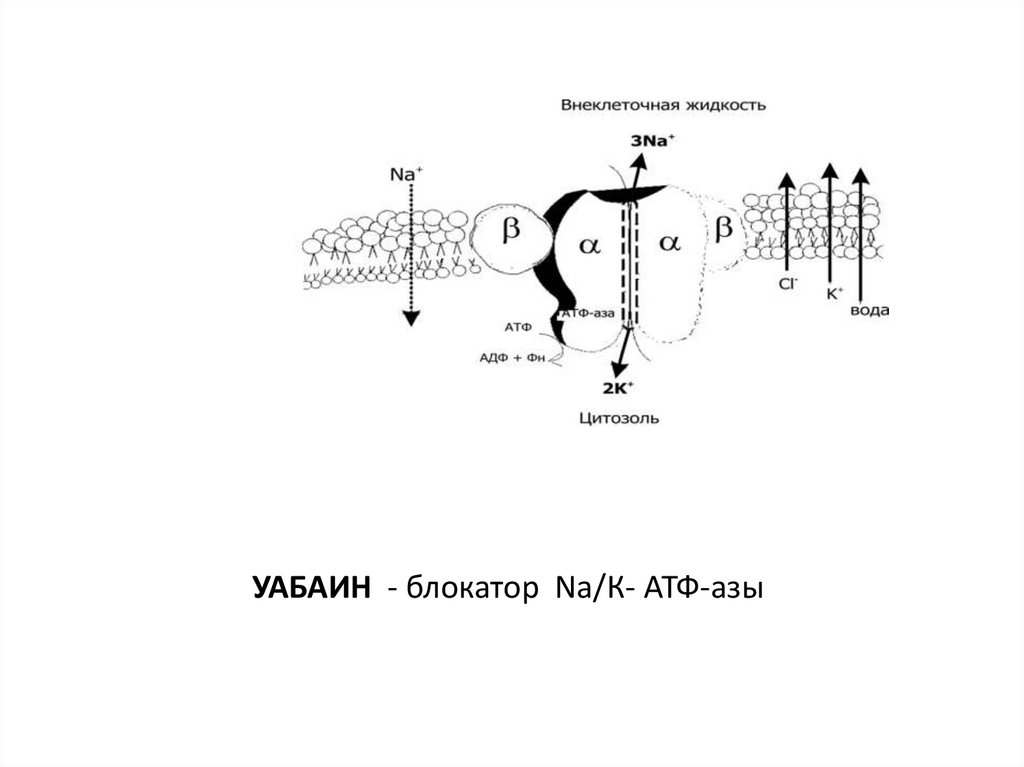
УАБАИН - блокатор Nа/К- АТФ-азы90.
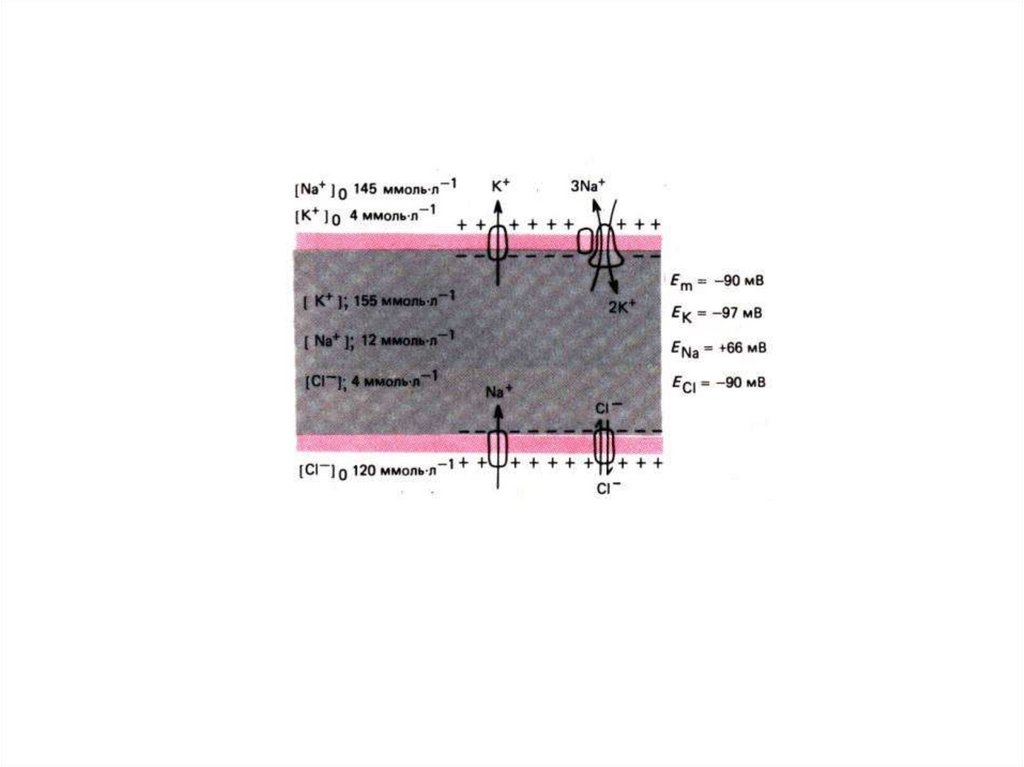
Потенциал покоя создается:1. Неравновесным распределением калия, натрия, хлора
внутри клетки по отношению к внешней среде.
2. Разной проницаемостью мембраны для этих ионов.
3. Основным потенциалобразующим ионом является
катион калия.
4. Постоянство потенциала покоя поддерживается работой
ионных насосов.
5. Электрогенность калий-натриевого насоса вносит
дополнительный вклад в создание мембранного
потенциала.
91.
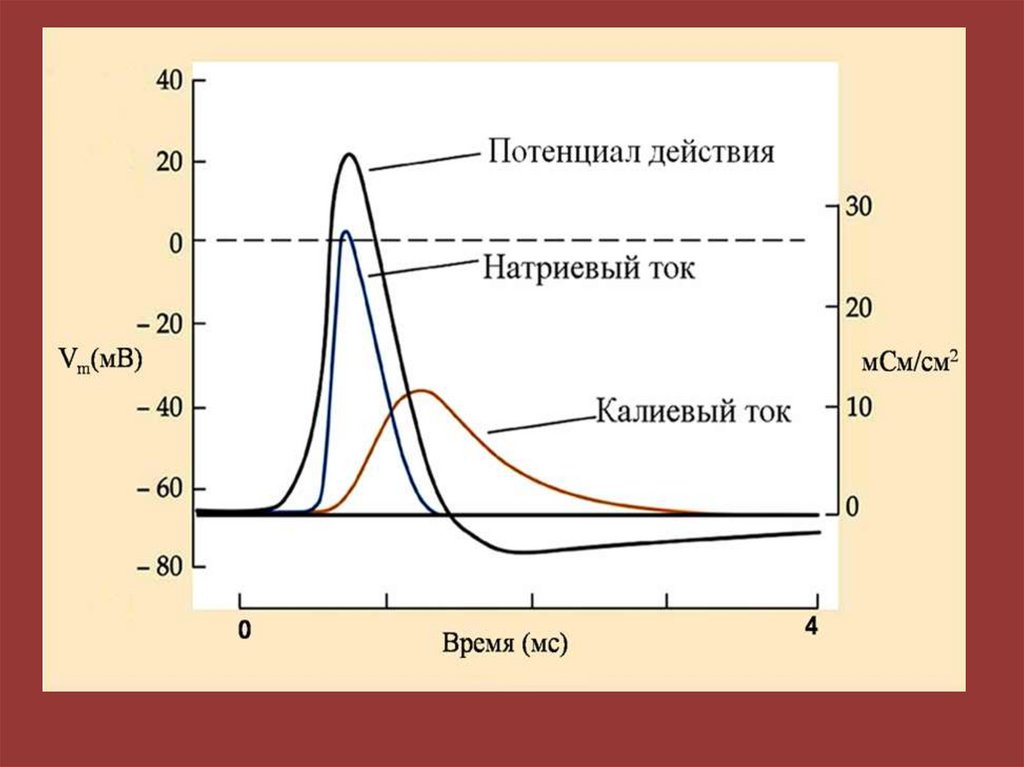
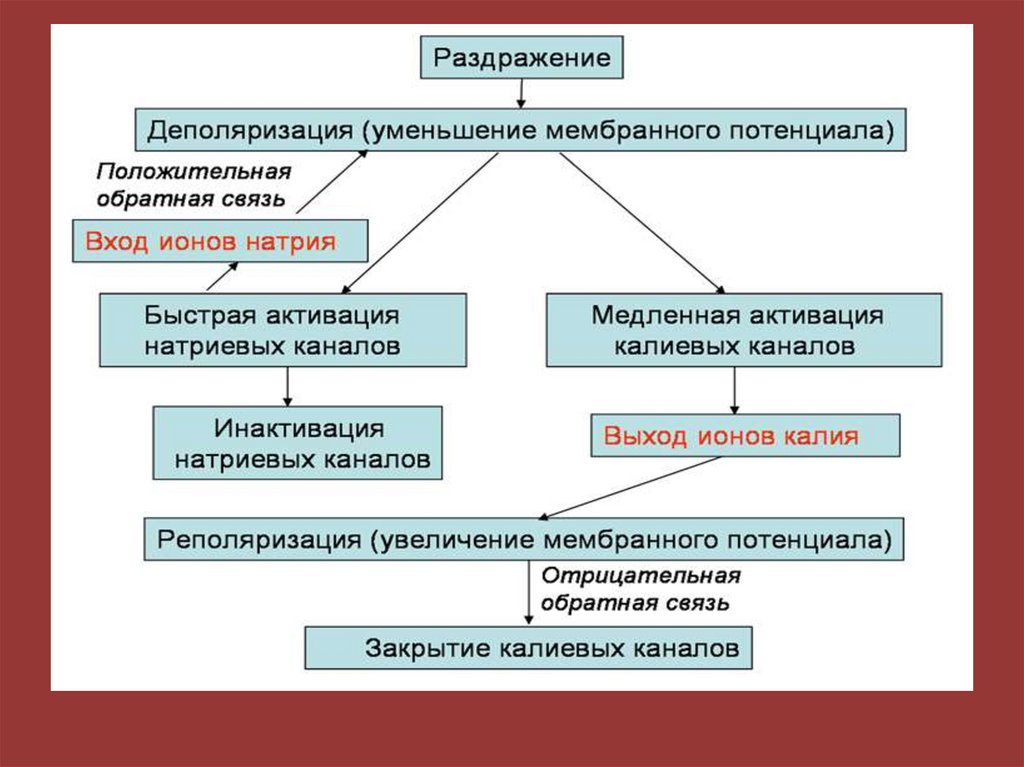
92. Потенциал действия
93.
Мембранно-ионная теория происхожденияпотенциала действия (ПД)
ПД – это быстрое изменение мембранного потенциала, которые
возникают в месте нанесения раздражения и распространяются
на всю мембрану клетки.
В основе возбуждения лежит изменение проницаемости
мембраны для натрия и калия, связанное с активацией
потенциалзависимых натриевых и калиевых каналов.
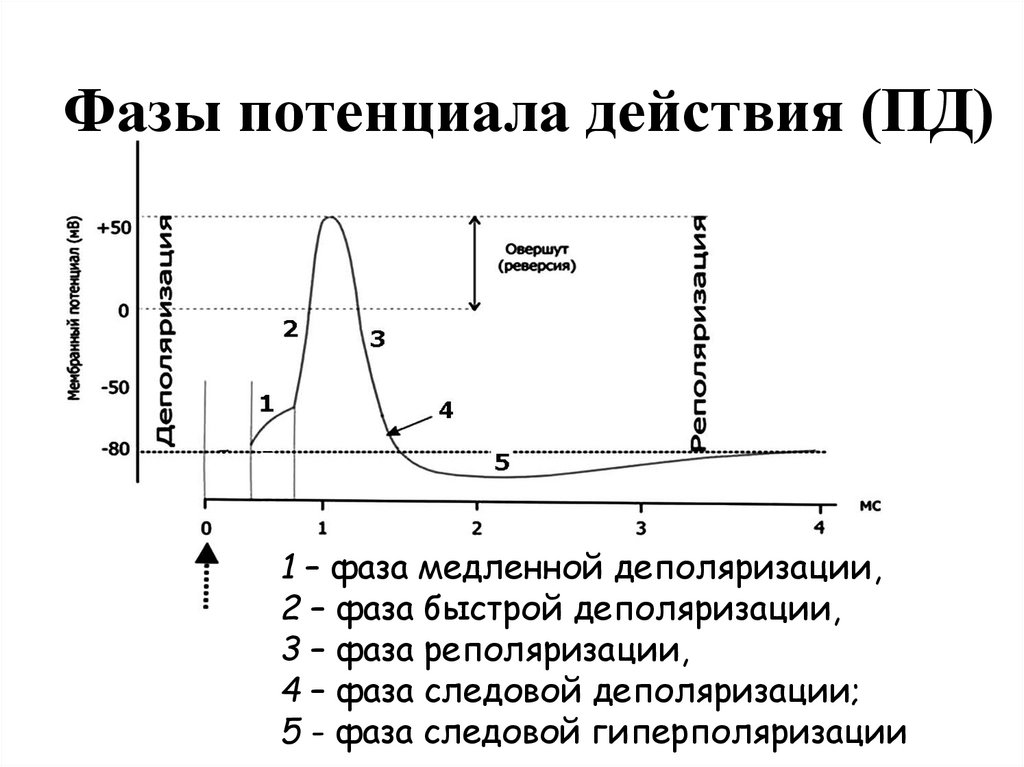
94. Фазы потенциала действия (ПД)
1 – фаза медленной деполяризации,2 – фаза быстрой деполяризации,
3 – фаза реполяризации,
4 – фаза следовой деполяризации;
5 - фаза следовой гиперполяризации
95.
При действии на клетку раздражителя проницаемостьмембраны для ионов Na+ резко повышается за счет активации
(открывания) натриевых каналов.
При этом ионы Na+ по концентрационному градиенту
интенсивно перемещаются из вне - во внутриклеточное
пространство. Вхождению ионов Na+ в клетку способствует и
электростатическое взаимодействие. В итоге проницаемость
мембраны для Na+ становится в 20 раз больше проницаемости для
ионов К+.
Поскольку поток Na+ в клетку начинает превышать калиевый ток
из клетки, то происходит постепенное снижение потенциала покоя,
приводящее к реверсии - изменению знака мембранного
потенциала. При этом внутренняя поверхность мембраны становится
положительной по отношению к ее внешней поверхности. Указанные
изменения мембранного потенциала соответствуют восходящей фазе
потенциала действия - фазе деполяризации.
96. Изменение проницаемости мембраны для ионов на пике ПД
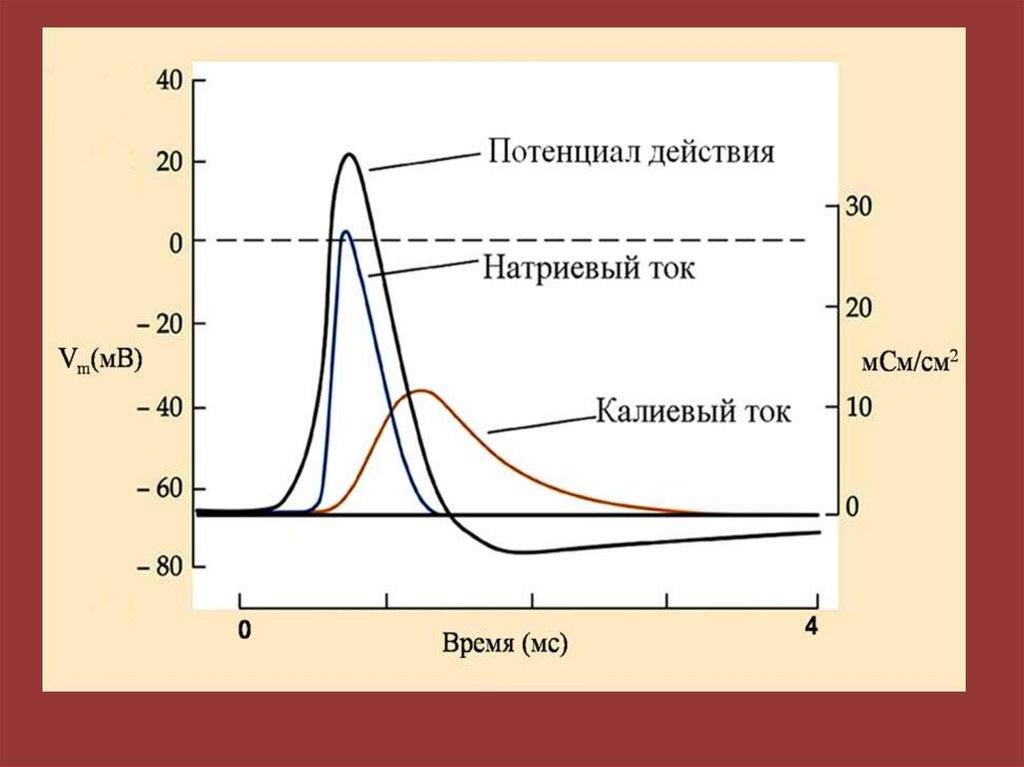
pK+ : pNa+ : pCl - = 1 : 20 : 0,4597.
В 1943 г. Ходжкин и Хаксли установили, чтомембранный потенциал во время развития ПД не
просто уменьшается до нуля, а меняет свой знак на
противоположный.
Эти данные противоречили гипотезе Бернштейна
о том, что во время ПД мембрана становиться
проницаемой для всех ионов.
98. Доказательства натриевой природы деполяризации :
Содержание Na+ во внеклеточной среде в 10 раз выше, т.е. входящий градиент.Ионы Na+ положительно заряжены, и их вход в клетку
должен привести к изменению потенциала на «+».
На высоте овершута ПД приближается к равновесному Na+ потенциалу.
Величина овершута зависит от содержания Na+ во
внеклеточной среде.
Если заменить Na+ во внеклеточной среде на холин хлорид,
то входящий ток ионов исчезает, а выходящий сохраняется
99.
Мембрана
характеризуется
повышенной
проницаемостью для ионов Na+ лишь очень короткое
время 0.2 - 0.5 мс.
• После этого проницаемость мембраны для ионов Na+
вновь понижается, а для К+ возрастает. В результате поток
Na+ внутрь клетки резко ослабляется, а ток К+ из клетки
усиливается.
В течение потенциала действия в клетку поступает
значительное количество Na+, а ионы К+ покидают клетку.
Восстановление
клеточного
ионного
баланса
осуществляется благодаря работе Na+/К+-АТФ-азы.
Итогом этих процессов и является реполяризация
мембраны: внутреннее содержимое клетки вновь
приобретает отрицательный заряд по отношению к
внешней поверхности мембраны.
100.
101.
102.
ИнактивацияNa+-канала
развивается
автоматически и степень ее зависит от
мембранного потенциала и времени.
Инактивацию можно подавить введя в
цитоплазму протеолитический фермент (проназу).
Это предполагает, что в инактивации участвует
белковая структура, расположенная у внутреннего
входа Na+-канала.
103.
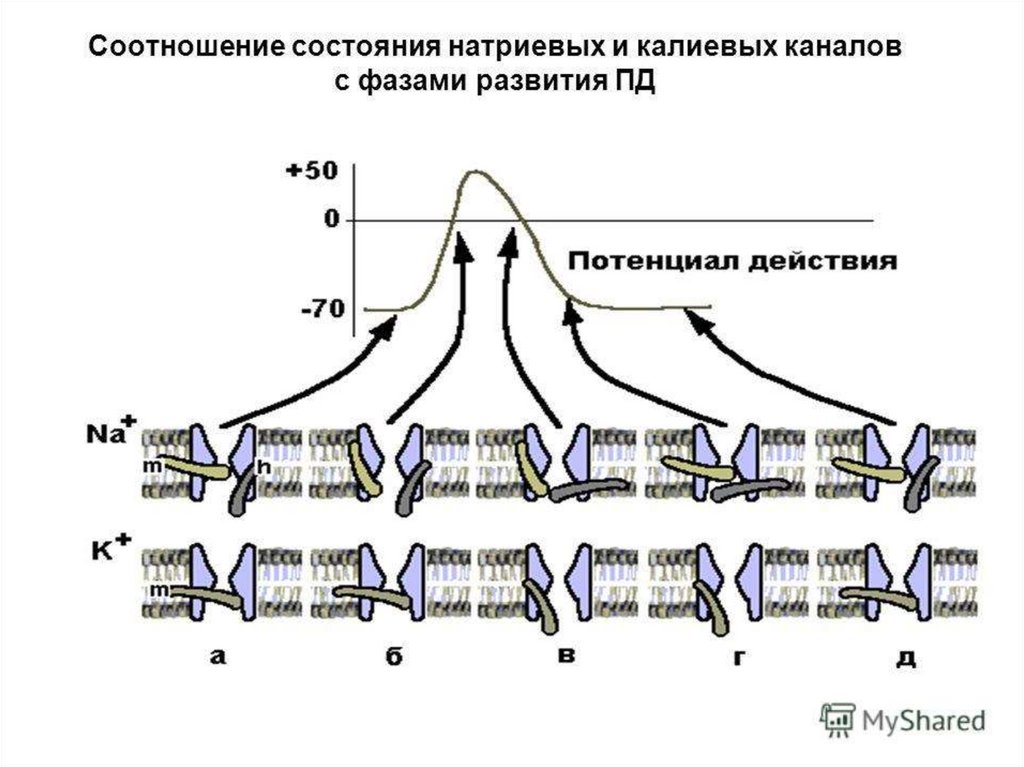
СОСТОЯНИЕ НАТРИЕВЫХ КАНАЛОВNa+
m
m
h
h
СОСТОЯНИЕ
ПОТЕНЦИАЛА
ПОКОЯ
СОСТОЯНИЕ
ДЕПОЛЯРИЗАЦИИ
МЕМБРАНЫ
Р Е А К Т И В А Ц И Я Na-канала
m
h
РЕПОЛЯРИЗАЦИЯ
МЕМБРАНЫ
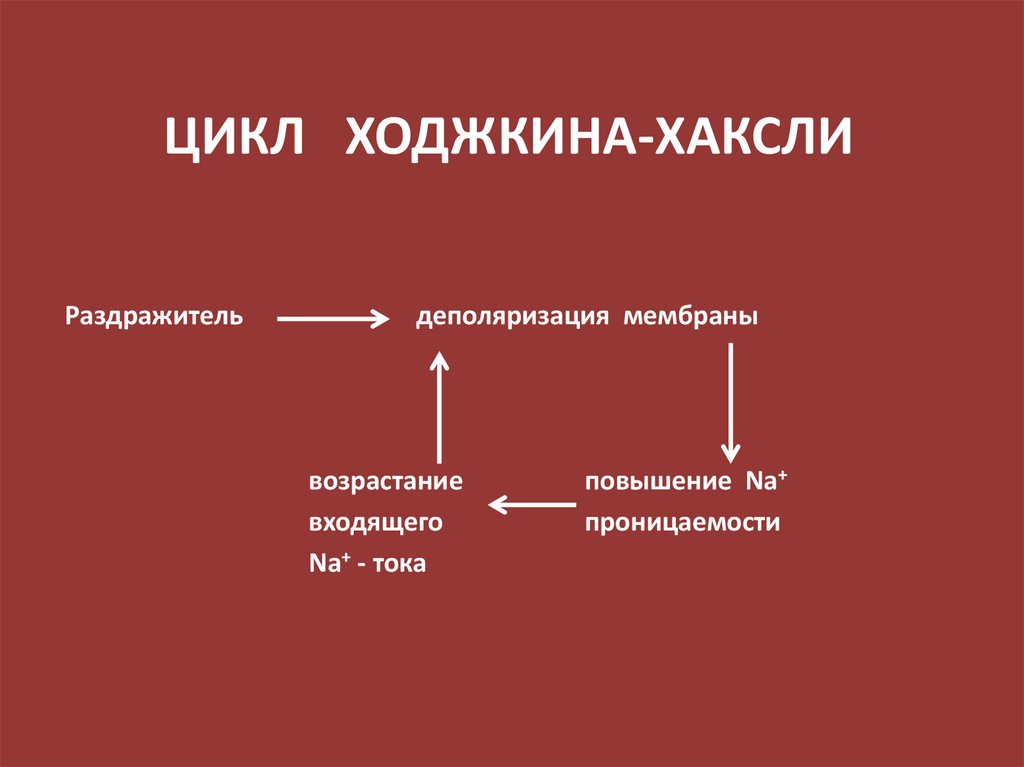
104. ЦИКЛ ХОДЖКИНА-ХАКСЛИ
Раздражительдеполяризация мембраны
возрастание
входящего
Na+ - тока
повышение Na+
проницаемости
105. Исследование строения Na+-канала
Узкая часть Na+-поры, служащая фильтром для ионов, несет одиночный отрицательный заряд (СООН -группа).Этот заряд притягивает катионы и отталкивает анионы.
Ион сопровождается молекулами воды, образующими
водородные связи с порой. В поре имеется достаточно места
для того, чтобы натрий мог войти в сопровождении 3-х
молекул воды и в тоже время образовать тесный контакт с 3-я
молекулами кислорода поры. В этом смысле Na+-канал
является «водной порой», хотя молекулы воды в ней не могут
также свободно двигаться, как в массе воды.
106.
Заряженные группировки белков Na+-каналареагируют
на
деполяризующее
действие
электрического
тока
конформационными
перестройками определенных участков белковой
молекулы.
Именно они и лежат в основе воротных
процессов, управляющих проводящим состоянием
канала.
107.
Кинетика блокирования ТТХ Na+-каналов показала, чтона участке мембраны площадью в 1 мкм2 располагается ~
100 Na+-каналов. Если считать, что d канала ~ 0,5 нм, общая площадь их сечения составляет менее 1/50 000 от
поверхности мембраны.
Активированный Na+-канал пропускает примерно 6000
ионов/мс. Время нахождения канала в открытом состоянии
– менее 1 мс и зависит от мембранного потенциала: при
смещении деполяризующего потенциала в положительную
сторону это время уменьшается.
108.
Nа+ - потенциалозависимые каналы, в мембраненервного
и
скелетного
мышечного
волокна,
характеризуются,
как
время
так
и
потенциалозависимостью.
Активируются на уровне ~ -60 мВ, полностью
инактивируются уже при деполяризации мембраны до
~ -40 мВ.
109.
110.
111.
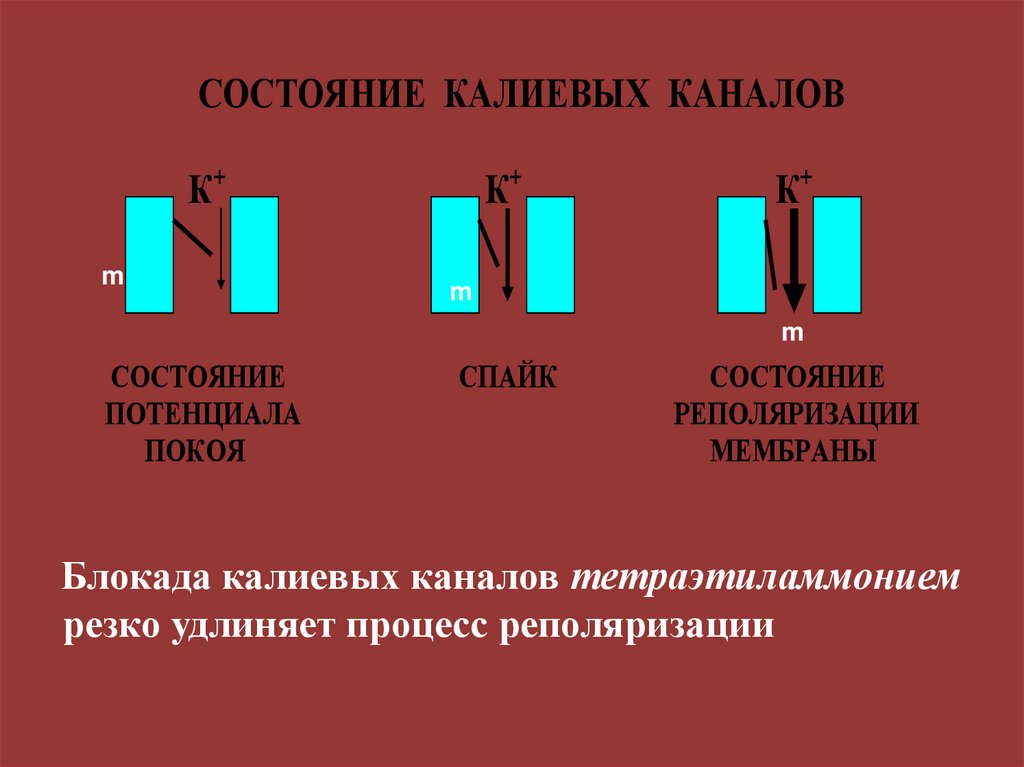
СОСТОЯНИЕ КАЛИЕВЫХ КАНАЛОВК+
m
К+
К+
m
m
СОСТОЯНИЕ
ПОТЕНЦИАЛА
ПОКОЯ
СПАЙК
СОСТОЯНИЕ
РЕПОЛЯРИЗАЦИИ
МЕМБРАНЫ
Блокада калиевых каналов тетраэтиламмонием
резко удлиняет процесс реполяризации
112.
113.
114.
115. Экспериментальные доказательство К+-природы реполяризации
Для проверки гипотезы о том, что выходящий ток по своей природеявляется калиевым, Ходжкин и Хаксли в 1953г., используя
радиоактивный калий, изучили перемещение К+ через мембрану под
действием постоянного тока.
Оказалось, что деполяризующий ток приводил к большому выходу
калия (К42).
Диаметр К+-канала меньше натриевого и составляет 0,3 нм. Ион
калия проходит через такой канал без гидратной оболочки, а ион Nа
пройти не может, хотя и меньше по диаметру, из-за стерического
несоответствия.
Установлено, что проводимость одиночного К+ -канала в 3 раза
выше, чем у натриевого. Однако, плотность калиевых каналов на
единицу площади мембраны в 5 раз меньше.
116. КАЛИЕВЫЙ КАНАЛ
Схема белка, образующего калиевый канал,погруженный в липидный бислой плазматической
мембраны.
Четыре
отрицательных
заряда
зафиксированы на «стенке» канала.
Б. Схематический энергетический профиль
канала, показанного на рис. А.
По
оси
ординат
отложены
величины
кинетической
энергии,
необходимые
для
прохождения канала; по оси абсцисс –расстояния
между внутренней и наружной поверхностями
мембраны.
Энергетические минимумы соответствуют местам
связывания положительно заряженных ионов с
фиксированными отрицательными зарядами в
стенке канала.
Энергетические
максимумы
соответствуют
препятствиям диффузии в канале.
Предполагается, что конформация канального
белка
спонтанно
осциллирует;
варианты
энергетических профилей изображены сплошными
и штриховыми линиями; эти осцилляции в
значительной степени облегчают связывание ионов
при преодолении энергетического барьера.
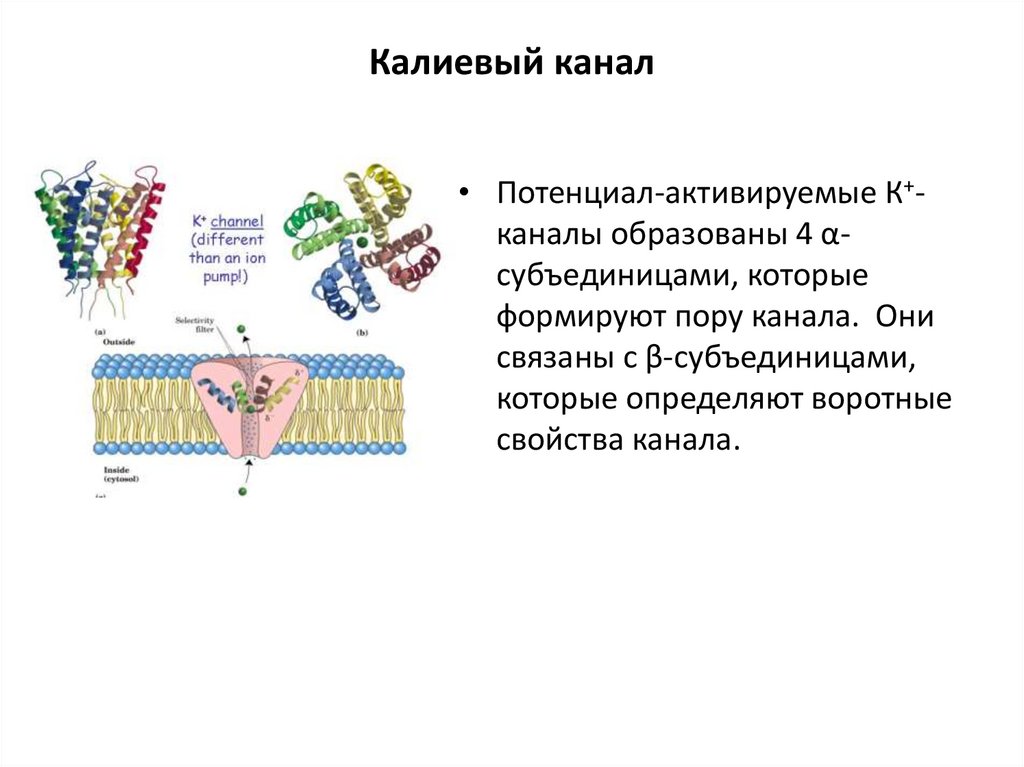
117. Калиевый канал
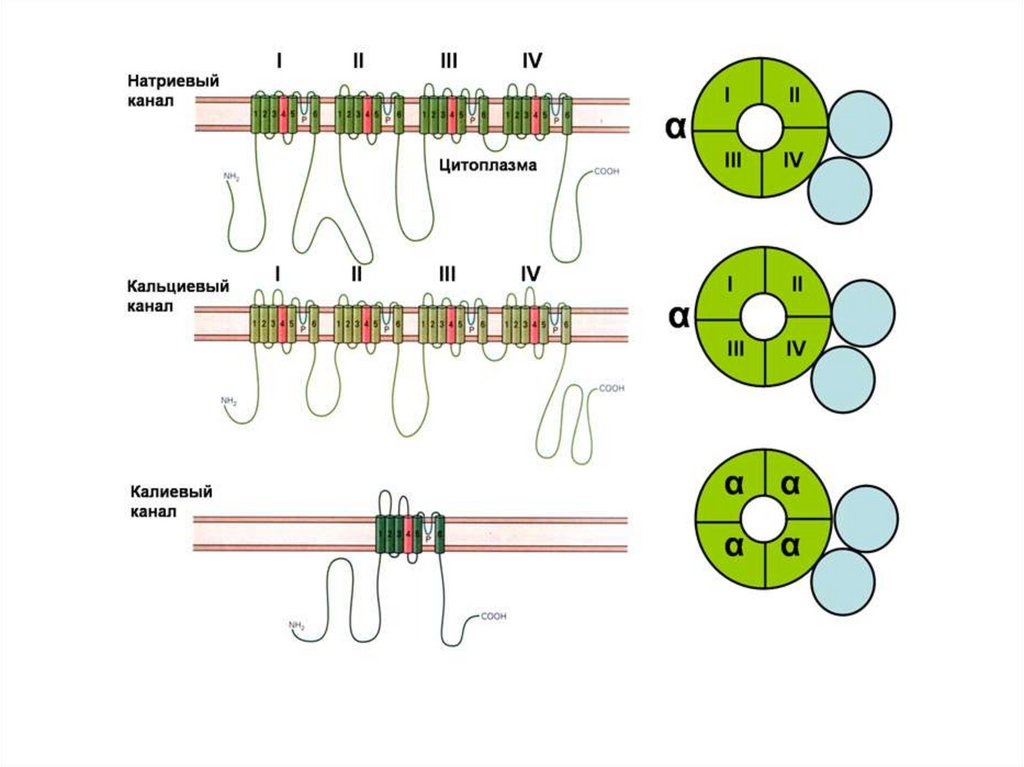
• Потенциал-активируемые К+каналы образованы 4 αсубъединицами, которыеформируют пору канала. Они
связаны с β-субъединицами,
которые определяют воротные
свойства канала.
118.
Потенциал действия:1. Возникает в ответ
раздражители.
на
пороговые
и
сверхпороговые
2. Обусловлен опережающим увеличением проницаемости
мембраны для натрия по сравнению с калиевой. При этом
деполяризация
определяется
натриевым
током,
реполяризация - калиевым.
3. Вслед за основными фазами потенциала действия
возникают
следовые
потенциалы.
Следовой
отрицательный связан с повышенной проводимостью
мембраны для натрия, положительный - для калия.
4. Потенциал действия распространяется
правилу “Все или ничего”.
и
подчиняется
5. При возбуждении активируется натрий-калиевый насос.
119.
120. ТРИ СОСТОЯНИЯ МЕМБРАНЫ
0Деполяризация
-90
-100
Поляризация
МПП или Е0
Гиперполяризация
121.
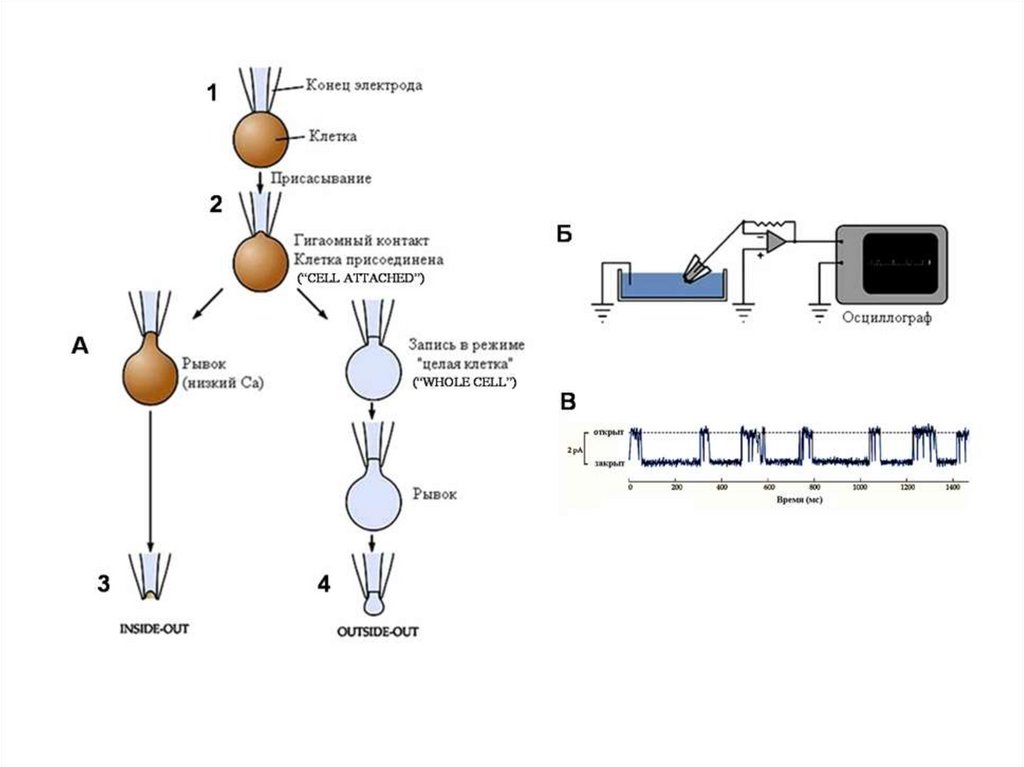
Схема локальной фиксации мембранного потенциала («пэтч–кламп»). Изображен продольный срезчерез регистрирующую микропипетку (обозначена черным цветом) с диаметром контактирующего с
мембраной кончика ≈1 мкм. Если кончик электрода абсолютно чист и поверхность клетки
освобождена от волокон соединительной ткани, то при подаче через пипетку отрицательного
давления образуется тесный контакт, который создает электрическую изоляцию каналов
находящегося в кончике пипетки микроучастка мембраны от остальной мембраны клетки (вставка).
Таким способом можно регистрировать токи каналов с помощью усилителя обратной связи,
соединенного с раствором электролита в пипетке.
122.
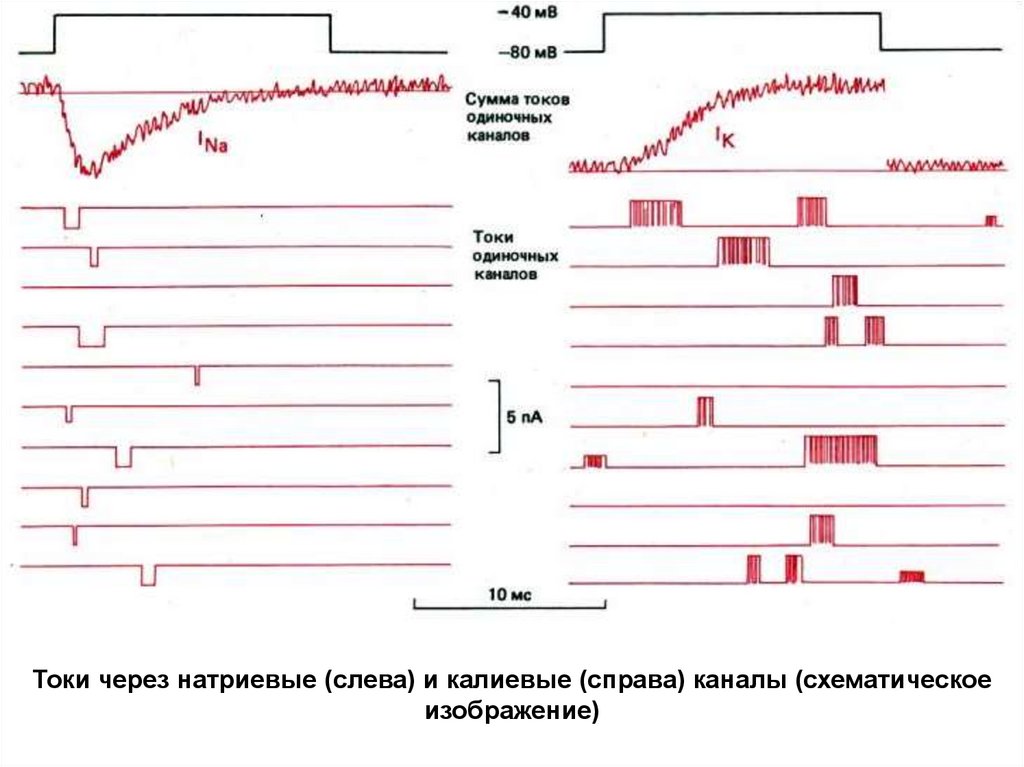
Токи через натриевые (слева) и калиевые (справа) каналы (схематическоеизображение)
123.
124.
125.
126.
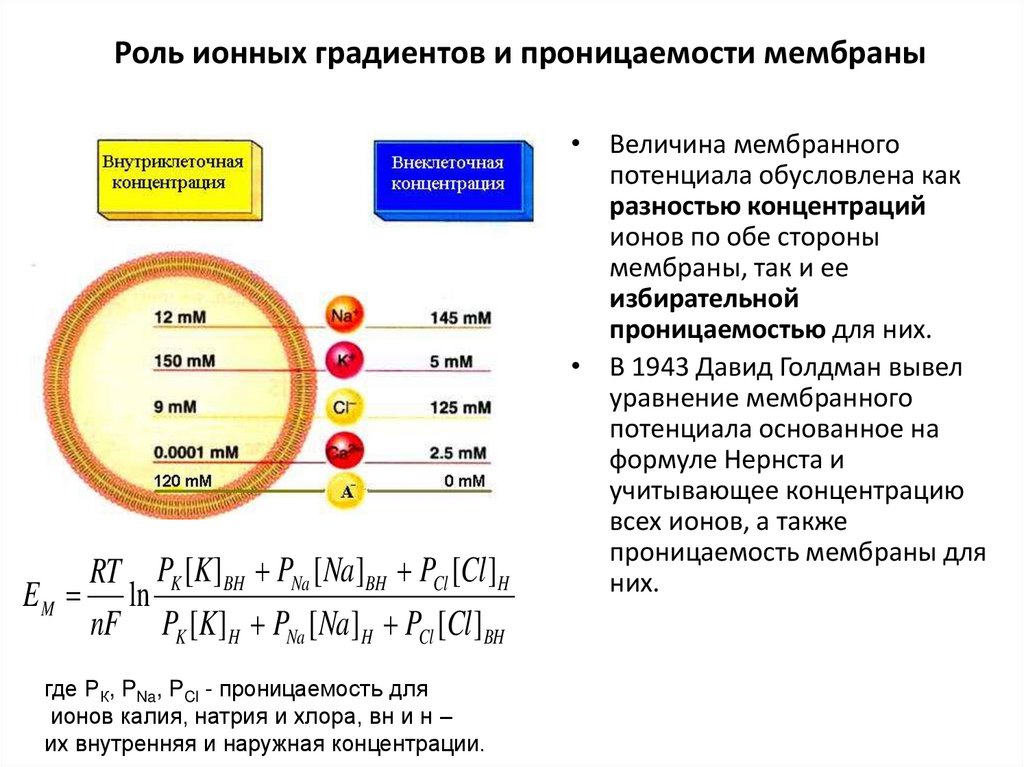
127. Роль ионных градиентов и проницаемости мембраны
RT PK [K ]BH PNa [ Na ]BH PCl [Cl ]HE M ln
nF PK [K ]H PNa [ Na ]H PCl [Cl ]BH
где РК, PNa, PCl - проницаемость для
ионов калия, натрия и хлора, вн и н –
их внутренняя и наружная концентрации.
• Величина мембранного
потенциала обусловлена как
разностью концентраций
ионов по обе стороны
мембраны, так и ее
избирательной
проницаемостью для них.
• В 1943 Давид Голдман вывел
уравнение мембранного
потенциала основанное на
формуле Нернста и
учитывающее концентрацию
всех ионов, а также
проницаемость мембраны для
них.
128.
129.
130.
131.
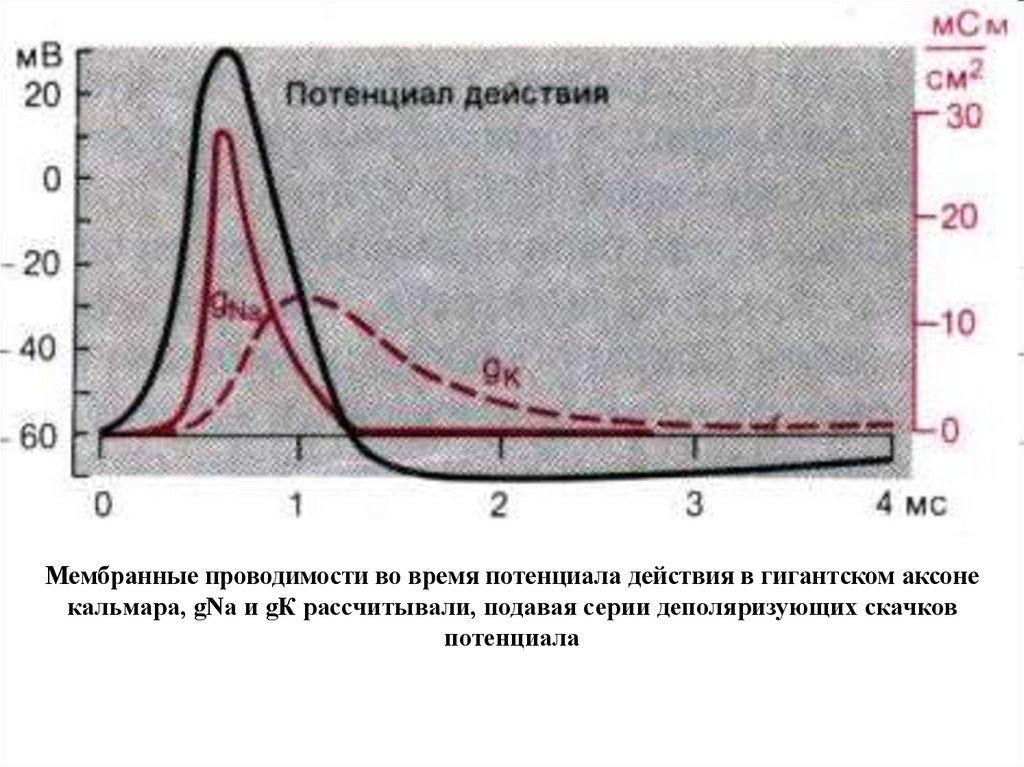
Мембранные проводимости во время потенциала действия в гигантском аксонекальмара, gNa и gК рассчитывали, подавая серии деполяризующих скачков
потенциала
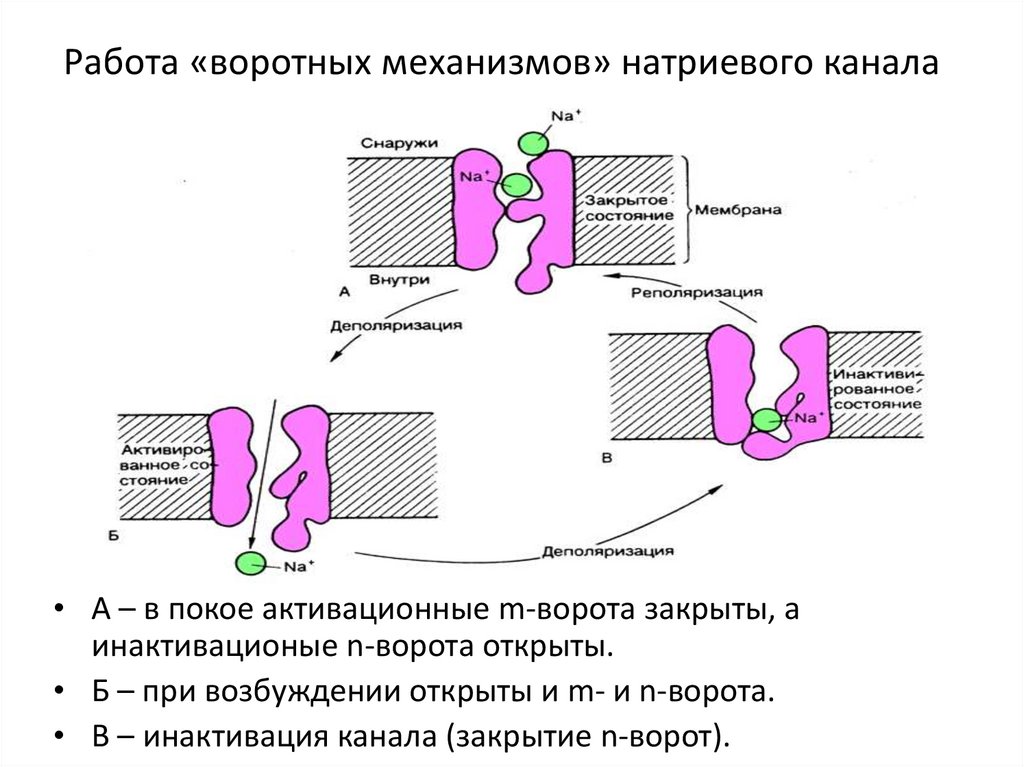
132. Работа «воротных механизмов» натриевого канала
• А – в покое активационные m-ворота закрыты, аинактивационые n-ворота открыты.
• Б – при возбуждении открыты и m- и n-ворота.
• В – инактивация канала (закрытие n-ворот).
133.
Современныепредставления
о
природе
биоэлектрических явлений в тканях базируются на
результатах работ Алана Ходжкина, Эндрью Хаксли,
Бернарда Катца.
Эти ученые в 40-50 годах нашего века
модифицировали и экспериментально обосновали
мембранно-ионную теорию Ю. Бернштейна.
В настоящее время их взгляды о природе
биоэлектрических явлений пользуются всеобщим
признанием.
Согласно
их
представлениям,
наличие
электрических потенциалов в живых клетках
обусловлено различной концентрацией ионов Na+,
K+, Ca2+ и Cl- внутри и вне клетки, а также различной
проницаемостью для них клеточной мембраны.
134.
Мембранно-ионная теория происхожденияпотенциала покоя (ПП)
Все клетки живого организма поляризованы. Между внутренней
средой клетки и внешней средой существует разность потенциалов мембранный потенциал (потенциал покоя).
Существование животного электричества открыл Гальвани в 1791 г.
Авторы современной теории: Ходжкин, Катц, Хаксли 1949-1952 гг.
Положения их теории:
Ионы вне и внутри клетки распределены неравномерно.
Катионов калия внутри клетки больше в 40-50 раз,
натрия меньше в 8-12 раз,
анионов хлора меньше в 30-40 раз.
Разность концентраций ионов создается работой ионных насосов
Проницаемость мембраны для разных ионов различна.
В состоянии покоя проницаемость для калия, натрия и хлора неодинаковы:
Р калия : Р натрия : Р хлора = 1 : 0,04 : 0, 45
135.
136.
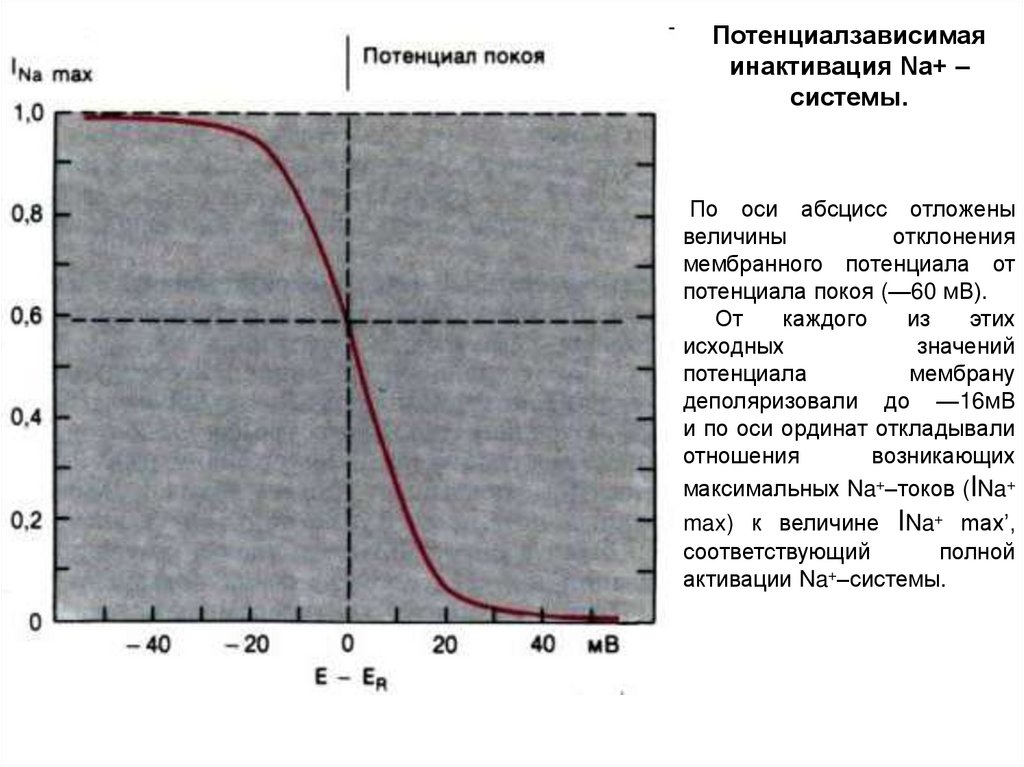
Потенциалзависимаяинактивация Na+ –
системы.
По оси абсцисс отложены
величины
отклонения
мембранного потенциала от
потенциала покоя (—60 мВ).
От
каждого
из
этих
исходных
значений
потенциала
мембрану
деполяризовали до —16мВ
и по оси ординат откладывали
отношения
возникающих
максимальных Na+–токов (INa+
max) к величине INa+ max’,
соответствующий
полной
+
активации Na –системы.






































































































 biology
biology








