Similar presentations:
Степень окисления. Бинарные соединения
1.
СТЕПЕНЬ ОКИСЛЕНИЯ.БИНАРНЫЕ СОЕДИНЕНИЯ
2.
Бинарные соединенияДвухэлементные
соединения
Сложные вещества, состоящие из двух
химических элементов
3.
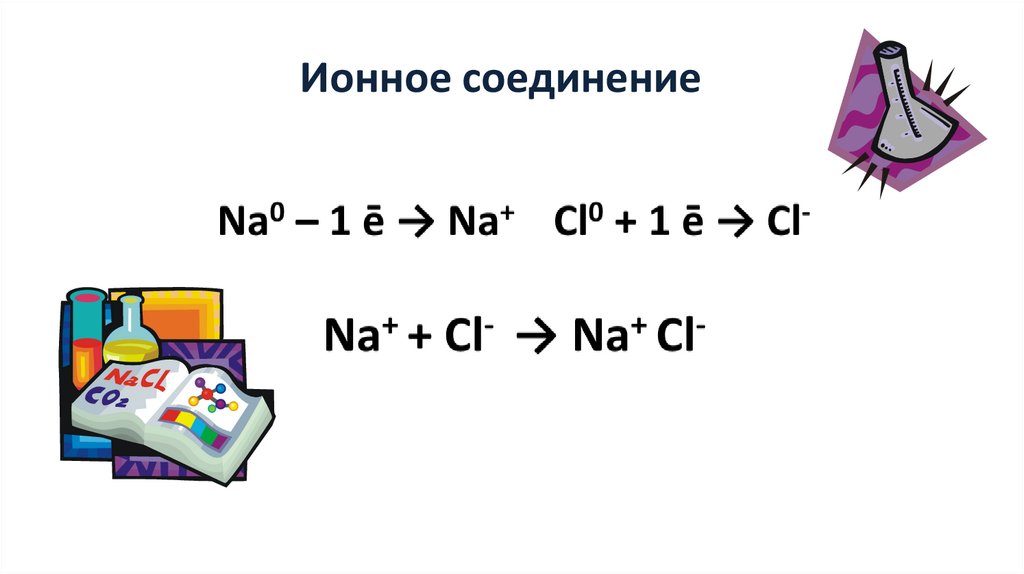
Ионное соединение4.
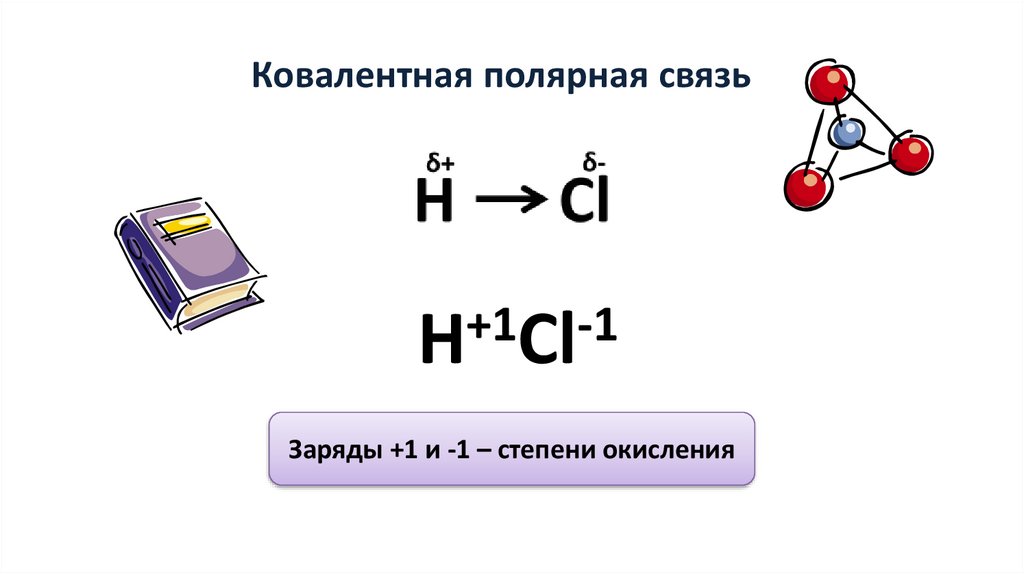
Ковалентная полярная связь+1
-1
Н Cl
Заряды +1 и -1 – степени окисления
5.
Степени окисления+2
-1
MgCl2
Степени
окисления
Заряды ионов
+1 -1
NaCl
Na+ Cl-
6.
Степень окисления – это условный заряд атомовхимического элемента в соединении, если
предположить, что оно состоит только из ионов.
Степень окисления может быть положительной, отрицательной,
нулевой
Положительную степень окисления имеют металлы и
неметаллы (кроме F, He, Ne)
Максимальная степень окисления равна номеру группы
(у N (+5))
Отрицательную степень окисления имеют только неметаллы
7.
Минимальная степень окисления = № группы – 8: у N (-3)Промежуточная степень окисления: у N (+3)
Степень окисления простых веществ равна 0: N2, H2, S8, Cu, O3 и др.
Степень окисления F (-1): NaF → F (-1)
Степень окисления кислорода (-2); СaO → (-2), OF2 → (+2)
У металлов степень окисления только положительная. У металлов А
групп она совпадает с валентностью
8.
В соединении Na2O, степень окисления Na (+1); в соединении BaS,степень окисления Ва (+2); в соединении Al2O3, степень окисления Al (+3)
Степень окисления Н всегда (+1), исключения – соединения с
металлами, где степень окисления Н (-1): CaH2, KH, LiH и др.
Степень окисления не всегда численно совпадает с валентностью
Валентность – это число связей, степень окисления – условный
заряд атомов
9.
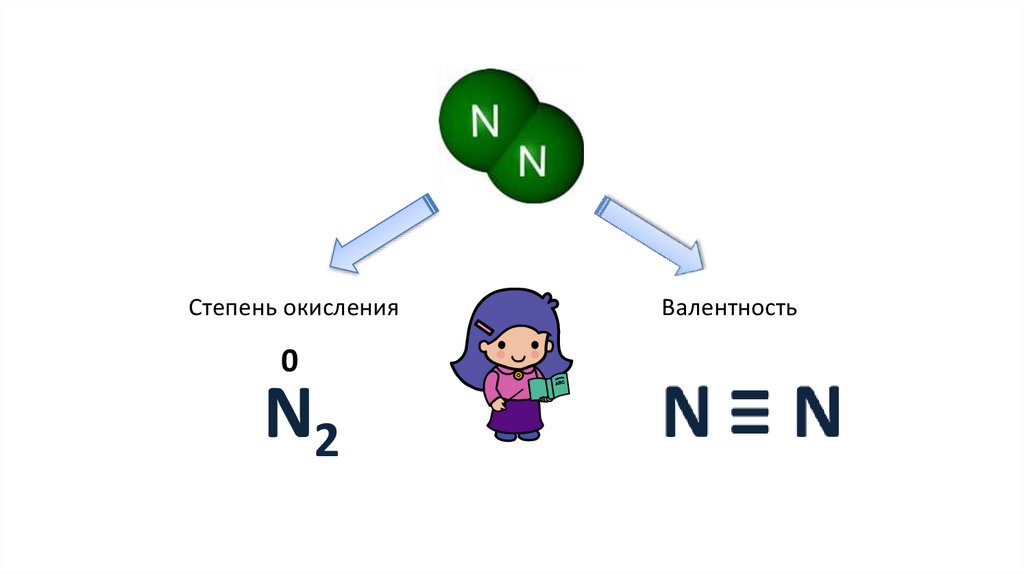
Степень окисления0
N2
Валентность
10.
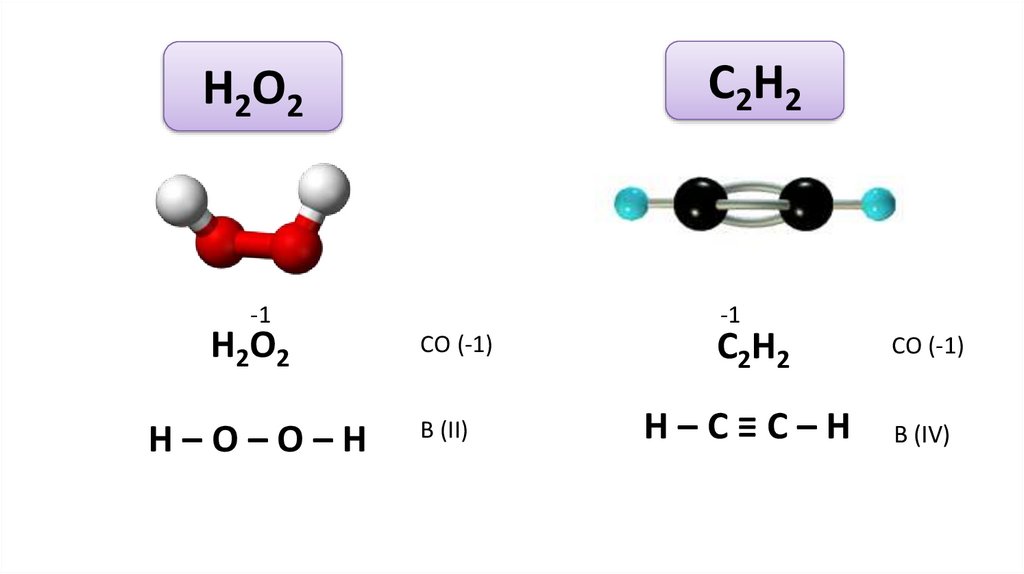
C2H2Н2О2
-1
Н2О2
Н–О–О–Н
-1
СО (-1)
В (II)
C2H2
СО (-1)
Н–С≡С–Н
В (IV)
11.
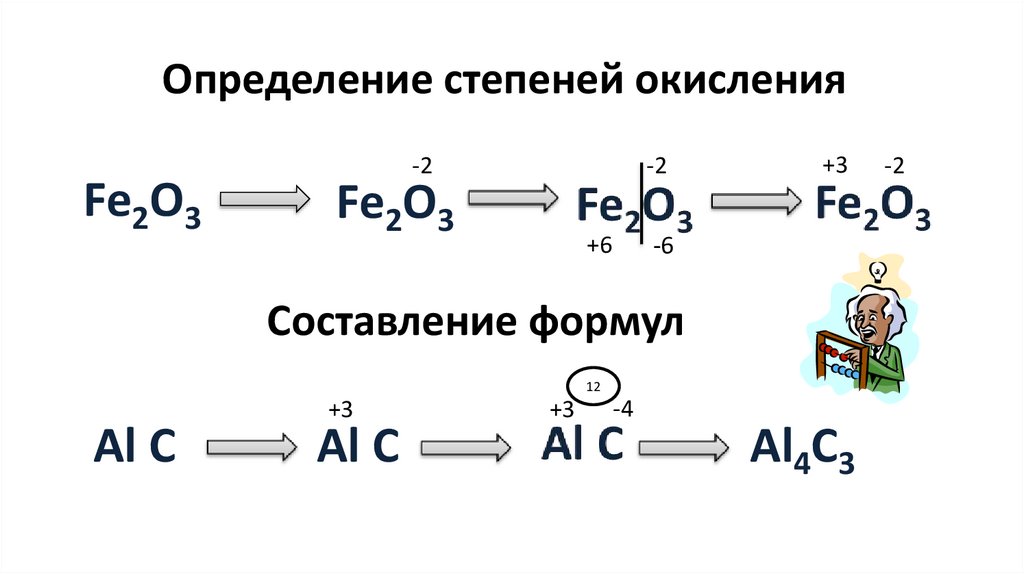
Определение степеней окисленияFe2O3
-2
-2
Fe2O3
+6
+3
-6
Составление формул
12
Al C
+3
Al C
+3
-4
Al4C3
-2
12.
Название бинарного соединения«ЭЛЕМЕНТ-ИД» + «ЭЛЕМЕНТА» (с. о., если переменная)
Оксид;
Хлорид;
Сульфид;
Нитрид
K2O
BaCl2
Na2S
Mg3N2
- оксид калия;
- хлорид бария;
- сульфид натрия;
- нитрид магния.
MnO2 - оксид марганца (IV);
CO2 - оксид углерода (IV);
P2O5 - оксид фосфора (V).
13.
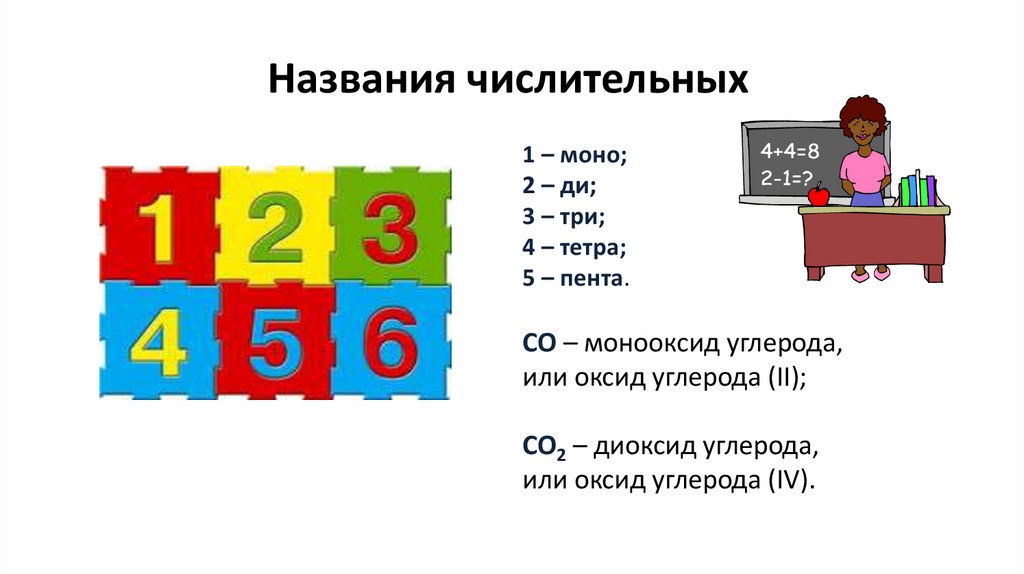
Названия числительных1 – моно;
2 – ди;
3 – три;
4 – тетра;
5 – пента.
СО – монооксид углерода,
или оксид углерода (II);
СО2 – диоксид углерода,
или оксид углерода (IV).
14.
В 1785 г. А. Лавуазье, А.Фуркруа, Л. Гитон де Мерво,
К. Бертолле разработали
принципы номенклатуры.
В настоящее время
принципы номенклатуры и
терминологии
разрабатывает ИЮПАК.








 chemistry
chemistry








