Similar presentations:
Азотная кислота
1.
АЗОТНАЯ КИСЛОТА2.
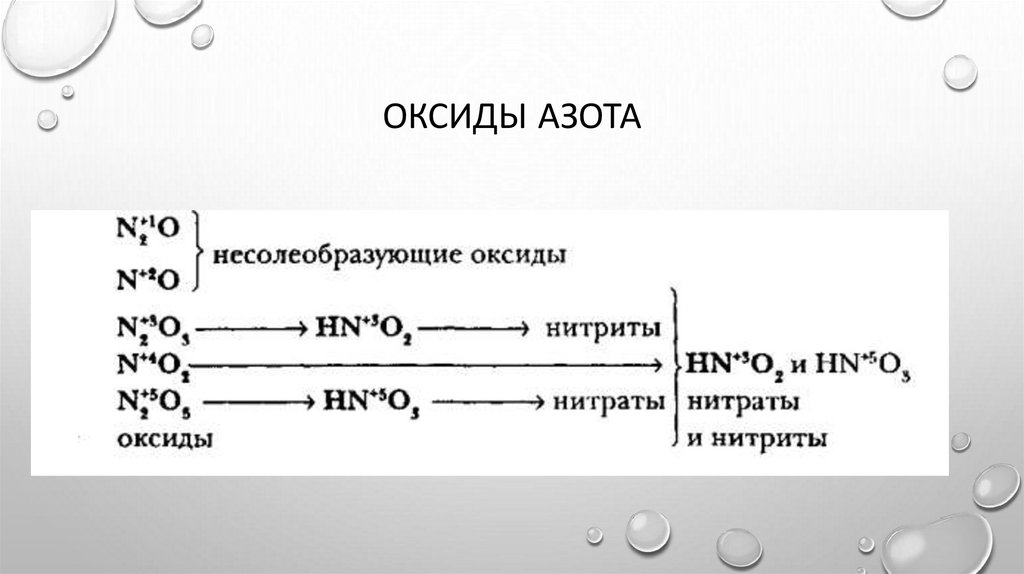
ОКСИДЫ АЗОТА3.
ОКСИД АЗОТА(IV)• ОКСИД АЗОТА (IV) ПРИ РАСТВОРЕНИИ В ВОДЕ ОДНОВРЕМЕННО ОБРАЗУЕТ ДВЕ КИСЛОТЫ — HNO2 И HNO3:
• 2NO2 + Н2O = HNO2 + HNO3
• ЕСЛИ ЕГО РАСТВОРИТЬ В ВОДЕ В ПРИСУТСТВИИ ИЗБЫТКА КИСЛОРОДА, ПОЛУЧАЕТСЯ ТОЛЬКО АЗОТНАЯ КИСЛОТА:
• 4NO2 + O2 + 2Н2О = 4HNO3
4.
АЗОТНАЯ КИСЛОТА• Азотная кислота HNO3. Это бесцветная жидкость, которая «дымится» на воздухе. При
хранении на свету концентрированная азотная кислота желтеет, так как частично
разлагается с образованием бурого газа NO2:
• 4HNO3 = 2Н2O + 4NO2↑ + O2↑.
• СВОЙСТВА:
• Одноосновная, летучая, кислородная, сильная, растворимая, непрочная.
5.
ХИМИЧЕСКИЕ СВОЙСТВА КИСЛОТ.• КИСЛОТА + ОСНОВАНИЕ ==>
СОЛЬ И ВОДА (РЕАКЦИЯ ОБМЕНА)
• КИСЛОТА + ОКСИД МЕТАЛЛА ==>
СОЛЬ И ВОДА (РЕАКЦИЯ ОБМЕНА)
• КИСЛОТА + СОЛЬ ==>
НОВАЯ КИСЛОТА + НОВАЯ СОЛЬ (РЕАКЦИЯ ЗАМЕЩЕНИЯ)
• КИСЛОТА И МЕТАЛЛ ==>
СОЛЬ + ВОДОРОД (РЕАКЦИЯ ОБМЕНА)
ПОСЛЕДНЕЕ ДЛЯ АЗОТНОЙ КИСЛОТЫ НЕ РАБОТАЕТ!
6.
ДОМАШНЕЕ ЗАДАНИЕНАПИСАТЬ ПРИМЕРЫ РЕАКЦИЙ, ПЕРЕЧИСЛЕННЫХ НА ПРЕДЫДУЩЕМ
СЛАЙДЕ
7.
ХИМИЧЕСКИЕ СВОЙСТВА• 1. РАЗЛОЖЕНИЕ
• 4HNO3 = O2+4NO2+2H2O.
• 2. ОВР
• В РЕАКЦИЯХ ОВР АЗОТНАЯ КИСЛОТА ЯВЛЯЕТСЯ ОКИСЛИТЕЛЕМ, Т.К. АЗОТ НАХОДИТСЯ В ВЫСШЕЙ
СТЕПЕНИ ОКИСЛЕНИЯ - +5. ВНЕ ЗАВИСИМОСТИ ОТ КОНЦЕНТРАЦИИ!
8.
9.
10.
11.
ВЗАИМОДЕЙСТВИЕ С МЕДЬЮКОНЦЕНТРИРОВАННАЯ
РАЗБАВЛЕННАЯ
• 4HNO3 + Cu = Cu(NO3)2 + 2NO2 + H2O
• 8HNO3 + 3Cu = 3Cu(NO3)2 + 2NO + 4H2O
• НАПИШИТЕ ЭЛЕКТРОННЫЙ БАЛАНС!
• N+5 + 3e = N+2
• Cu0 -2e = Cu+2
12.
ПОЛУЧЕНИЕ АЗОТНОЙ КИСЛОТЫ• Получают азотную кислоту 2 способами
1.
Электродуговым
2.
Аммиачным
Отличается только первая стадия
13.
ПРИМЕНЕНИЕ АЗОТНОЙ КИСЛОТЫ• Азотную кислоту применяют для производства:
1.
Удобрений
2.
Взрывчатых веществ
3.
Красителей
4.
Нитратов
5.
Пластмасс












 chemistry
chemistry








