Similar presentations:
Особенности метаболизма раковых клеток
1.
Особенности метаболизмараковых клеток
Выполнила: Никифорова В.
2.
What is cell metabolism?• Клеточный метаболизм описывает
внутриклеточные химические реакции,
превращающие питательные вещества и
эндогенные молекулы в энергию и вещества (белки,
нуклеиновые кислоты, липиды), поддерживающие
жизнь.
• АТФ – молекула, приводящая в действие все
клеточные процессы, образуется главным образом
двумя путями: гликолиз и окислительным
фосфорилированрием. (Если уровень кислорода
низкий, то включается анаэробный гликолиз)
3.
How is cancer-cell metabolismdifferent?
Раковые клетки расточительны. По сравнению с
нормальными клетками, они используют
непропорционально большую долю питательных
веществ из их окружения. Это связано в частности с тем,
что раковые клетки метаболизируют глюкозу в
анаэробном гликолизе. Более того, раковые клетки
неэффективно используют глютамин – одну из наиболее
распространенных аминокислот.
В нормальных клетках глютамин используется для того,
чтобы давать амино- и амидо- группы для синзета
аминокислот, и поставлять азот для образования
новых нуклеотидов. Раковые клетки, напротив,
выделяют в виде «отработки» много азота и углерода,
полученного из глютамина.
4.
Do any normal cells share theseproperties?
• Нормальные клетки могут осуществлять
анаэробный гликолиз и неэффективно использовать
глютамин тогда, когда они находятся вфазе
активного роста. Но если поставки
внутриклеточных питательных веществ истощаются,
клетка адаптируется путем реактивирования
окислительного фосфорилирования.
• Способность адаптироваться к нестабильному
потоку питательных веществ зависит от целостности
и количества супрессоров опухоли. Раковые клетки,
напротив, часто лишены этих белков, и проявляют
“зависимость” от потребления глюкозы и
глютамина.
5.
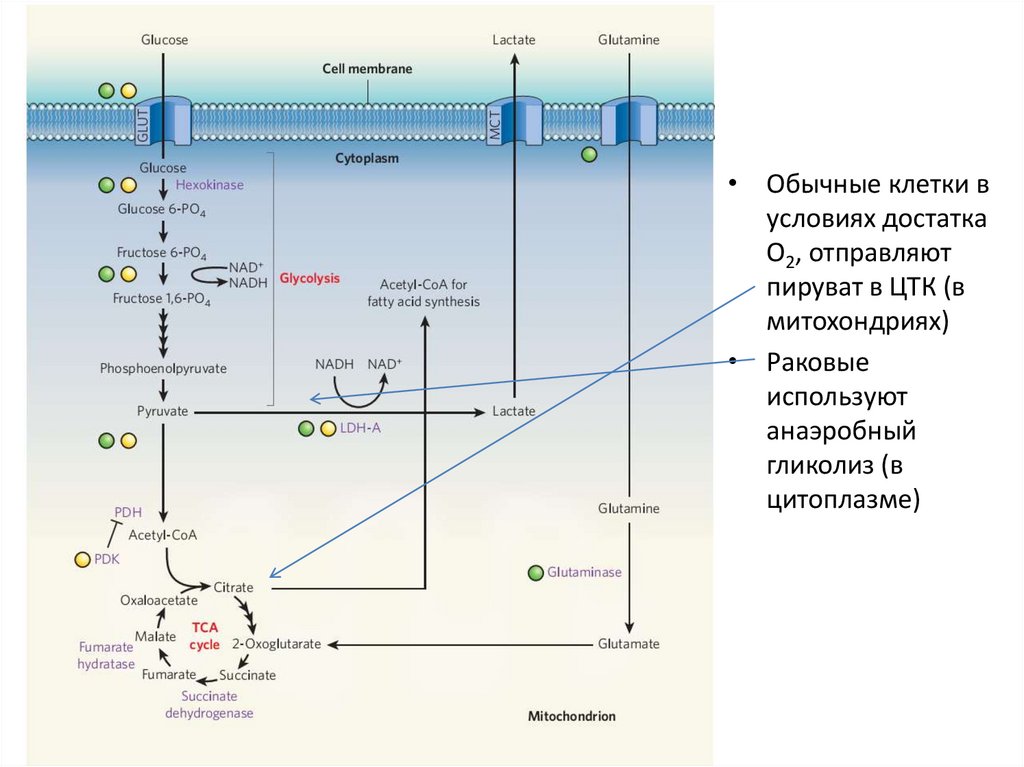
• Обычные клетки вусловиях достатка
О2, отправляют
пируват в ЦТК (в
митохондриях)
• Раковые
используют
анаэробный
гликолиз (в
цитоплазме)
6.
How do these abnormalities occur?• Повышенная активность PI3K-AKT сигнального пути
вызывает избыточное потребление питательных
веществ. AKT активирует факторы транскрипции HIF и
MYC, которые усиливают экспрессию транспортеров
глюкозы и гликолитических ферментов.
• Более того, HIF (Hypoxia-inducible factors )не дает
пирувату вступать в цикл трикарбоновых кислот.
Некоторые из этих действий могут быть специально
вызваны потерей p53. Онкогенный MYC может также
напрямую вызывать потребление глютамина в избытке
по сравнению с потребностями в азоте и углероде.
Клетки должны устранять продукты распада этого
метаболизма путем выделения избыточных углерода и
азота в виде лактата, аланина и аммиака.
7.
How do cancer cells benefit fromtheir abnormal metabolism?
• Несколькими путями. Во-первых, такой метаболизм
дает раковым клеткам постоянный приток строительных
блоков, необходимых для синтеза макромолекул, таких
как NADPH и ацетил-CoA, не говоря об ATP.
• Во-вторых, забирая больше положенных ресурсов,
раковые клетки “объедают” своих соседей и получают
пространство для роста.
• В-третьих, избыточное потребление питательных
веществ может увеличить выработку активных форм
кислорода, деактивирующих ингибирующие рост
ферменты фосфатазы, и увеличить частоту мутаций,
вызванных повреждением ДНК.
8.
As anaerobic glycolysis is inefficient, howdo cancer cells maintain ATP levels?
• Путем сжигания большего количества глюкозы.
• Высокие уровни ATP не благоприятны для раковой клетки.
• Рост клетки зависит от постоянных гликолитических и
митохондриальных потоков молекулярных прекурсов NADPH, ацетилCoA, рибозы и полученных из глюкозы аминокислот. Чтобы
поддерживать высокую скорость гликолиза необходимо постоянное
поступление акцептора фосфата – ADP. Если клеточный метаболизм
эффективен, всё ADP будет фосфорилировано в ATP, и дальнеший
метаболизм глюкозы будет ингибирован. Раковые клетки,
следовательно, не пускают полученный из глюкозы углерод в
аэробный гликолиз и отцепляют производство ATP от
митохондриального транспорта электронов.
• Это означает, что они потребляют метаболический кофактор NADH
без произвоства ATP, и способствуют использованию гликолитических
промежуточных веществ в не-ATP-генерирующих побочных путях.
9.
Can cancer cells use fat as a fuel?• Да, раковые клетки, однако, вносят
значительный вклад в синтез жиров. Их
особенностью являются создание
фосфолипидов для строительства мембран, а
также получения липид-производных
сигнальных интермедиатов, таких как
простагландины.
• Было бы неэффективно одновременно
разрушать свежесинтезированные жирные
кислоты для производства энергии.
10.
What is the effect of changingoxygen levels?
• Основной проблемой твердых опухолей является тот
факт, что часто они вырастают больших размеров, чем
позволяет кровоток, и клетки сталкиваются с гипоксией.
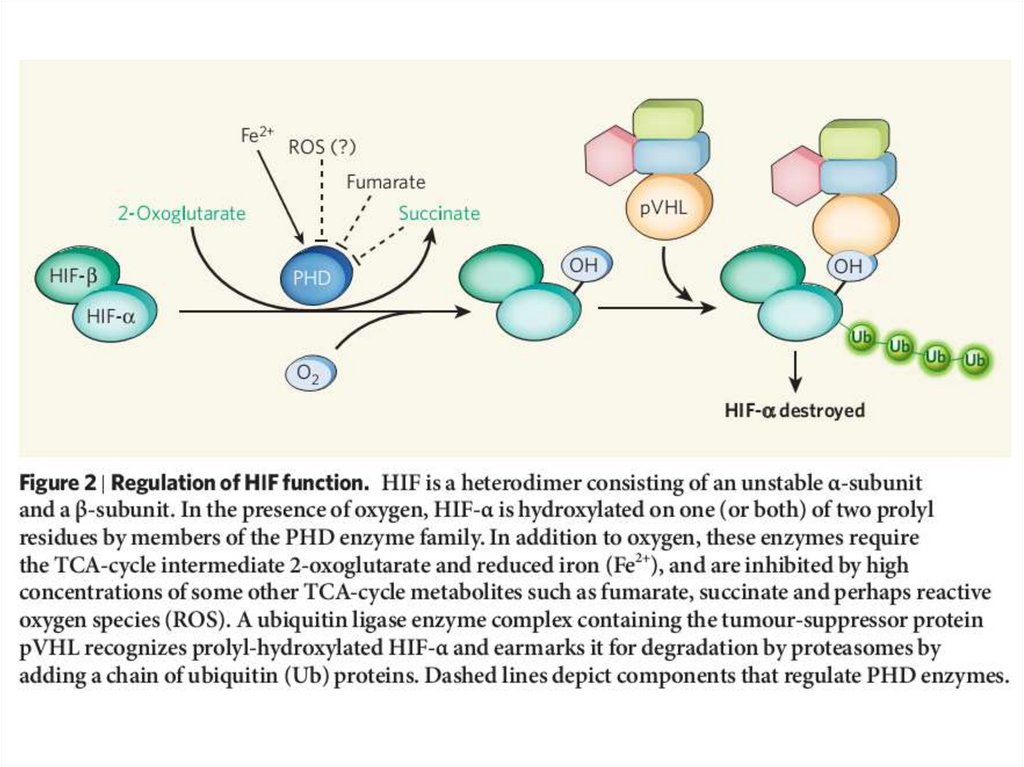
• В гипоксический условиях HIF накапливается и вызывает
транскрипцию примерно 200 генов, многие из которых
поддерживают выживание клетки. Они включают в себя
гены, которые способствуют гликолизу и подавляют
окислительное фосфорилирование. Наколпение HIF
подавляется активностью кислород-зависимых PHD
(пролил гидроксилазы домен) ферментов.
• Более того, изменения в уровнях активных форм
кислорода или метаболитов TCA-цикла, таких как
суккцинат и фумарат, могут способствовать накоплению
HIF.
11.
12.
How about changes in nutrientavailability?
• Клетки млекопитающих используют
внутриклеточные механизмы для контроля
потоков питательных веществ. Например,
они ощущают низкие уровни ATP через
повышение одного из продуктов его
гидролиза – AMP, который активирует
AMPK-киназу и LKB1 белок супрессор
опухоли.
13.
Why is glutamine crucial forcancer cells?
• Глютамин необходим для клеточного роста –
ненормальный рост биомассы является
отличительным признаком рака. Метаболиты
выступают промежуточными веществами в
транспорте восстановленного азота через кровоток.
Для производства нуклеотидов и «заменимых»
аминокислот, раковые клетки должны получать
достаточный поток восстановленного азота. Более
того, глютамин играет важную роль в усвоении
незаменимых аминокислот, а также может
поддерживать ЦТК в условиях малого количества
глюкозы, и может поддерживать производство
NADPH, который необходим для биосинтеза липидов
и нуклеотидов.
• Онкогенная активация MYC способствует
использованию глютамина, но ценой такой
активации является глютаминовая зависимость.
14.
How does the Warburg effect come in?Отто Варбург и коллеги были первыми,
кто сообщил о том, что раковые клетки
продолжают использовать
анаэробный гликолиз и продуцируют
лактат даже тогда, когда уровень
кислорода высоки. Этот факт известен
как эффект Варбурга. Несмотря на
масштабные усилия, Варбург не смог
найти мутации, которые останавливали
окислительный метаболизм в раковых
клетках. В последствии, многие биологи
поднимали вопрос о том, являются ли
наблюдения Варбурга реальным
отражением метаболизма раковых
клеток, или же это артефакт,
вызыванный гипоксией в его in vitro
экспериментах. Дальнейшие
исследования, однако, подтвердили
роль эффекта in vivo.
Отто Варбург (1883-1970)
15.
And how does it relate to thePasteur effect?
• Эффект Пастера описывает обратное соотношение
между анаэробным гликолизом и окислительным
фосфорилированием: когда кислород
присутствует, потребление глюкозы с
производством лактата подавляется в пользу
окислительного фосфорилирования.
• Эффект Варбурга является потерей эффекта Пастера.
Очевидно, что HIF является ключевым как для
одного, так и для другого эффекта. В нормальных
клетках, кислород подавляет активность HIF,
приводят к пониженному гликолизу и увеличенному
входу пирувата в ЦТК. В раковых клетках, кислород
не может более эффективно снижать активность HIF.
16.
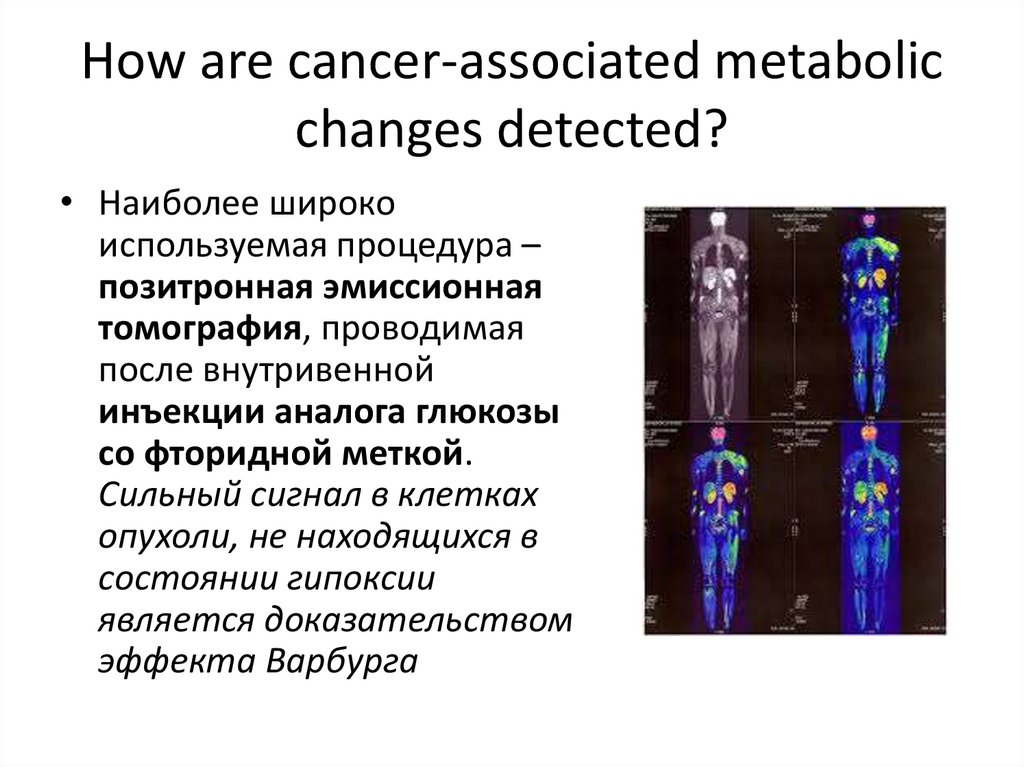
How are cancer-associated metabolicchanges detected?
• Наиболее широко
используемая процедура –
позитронная эмиссионная
томография, проводимая
после внутривенной
инъекции аналога глюкозы
со фторидной меткой.
Сильный сигнал в клетках
опухоли, не находящихся в
состоянии гипоксии
является доказательством
эффекта Варбурга
17.
Could targeting cancer-associatedglycolysis be used therapeutically?
• In vitro многие раковые клетки погибают при
ограничении глюкозы. Но блокирование гликолиза
не оказалось полезным в клинических условиях.
Например, фермент гексокиназа используется на
первой стадии гликолиза, но клинические
испытания с игнибиторами гексокиназы – 2деоксиглюкозой и лонидамином – были
прекращены, вероятно, из-за высокой токсичности
или неэффективности. Специфичность других
ингибиторов гексокиназы, таких как 3бромпируват, также сомнительна. Клиинчески
испытания TLN-232 – ингибитора гликолитического
фермента пируват-киназы, ещё продолжаются.
18.
Do any anticancer agents exploit themetabolic addictions of cancer cells?
• Да. Один из первых противораковых агентов – и первый внесший
ремиссию в лейкимию – был аминоптерин, который блокирует
активность фермента дигидрофолат редуктазы. Этот NADPHзависимый фермент играет центральную роль в синетзе нуклеиновых
кислот, и активируется путем высокого окислительновосстановительного состояния, вызванного аэробным гликолизом
и/или разложением глютамина.
• Метотрексат, похожее аминоптериновое соединение, остается
важным противораковым лекарством.
• Другие «антиметаболиты», мешающие биосинтезу нуклеотидов –
включая фторурацил, цитарабин, гемцитабин и тиогуанин – также
используются для лечения различных видов рака. Более того, Lаспарагин является незаменимой аминокислотой для клеток
лимфобластической лейкемии, и фермент L-аспарагиназа используют
для лечения этого рака. Она также функционирует и как глютаминаза,
превращая глютамин в глютамат.
19.
What about other potential therapies?Доклинические исследования указывают на несколько потенциально
успешных целей.
Ингибирование LDH-A фермента или монокарбоксилат-транспортеров
(MCTs), которые соответственно вызывают производство лактата и выделение
как части аэробного гликолиза, может иметь противоопухолевый эффект.
Фермент PDK, который частично вовлечен в направление пирувата на
производство лактата, является другим потенциальным противораковым
лекарством, которое в настоящее время тестируется.
Глютамин должен быть превращен в глютамат с помощью глютаминазы до
входа в ЦТК: раковые клетки, производящие MYC онкоген, перепроизводят
глютаминазу и погибают в результате нехватки глютамина. Хотя антагонисты
глютамина первого поколения, такие как 6-диазо-5-оксо-L-норлейцин и
ацивицин являются нейротоксичными, безопасные ингибиторы глютаминазы
активно разрабатываются.
Другой возможной целью является фермент-синтаза жирных кислот, которая
перепроизводится в многих видах раковых клеток. Более того,
ингибирование фермента моноацилглицерол-липазы, которая
перепроизводится в агрессивных видах рака, может замедлить рост опухоли.
20.
What are the latest advances?Интересное недавнее открытие заключается в том, что мутации гоноцитов,
которые влияют на ферменты цикла трикарбоновых кислот: фумарат
гидратазу и суккцинат дегидрогеназу, могут вызывать рак, вызывая
стабилизацию HIF и приводя к состоянию псевдо-гипоксии. Дефектная
суккцинат дигидрогеназа может также вызывать развитие опухолей нервного
гребня вне зависимости от HIF. Аналогично, мутации в изоцитрат
дегидрогеназе 1 и 2 были обнаружены в клетках рака мозга и лейкимии.
Вместо нормального продукта (интермедиата ЦТК 2-оксоглютарата) эти
мутировавшие ферменты производят 2-гидроксиглютарат, который может
влиять на активности 2-оксоглютарат-зависимых ферментов, к которым
относятся и регуляторы уровня HIF.
Некоторые гистон деметилазы также могут работать как 2-оксоглютаратзависмые диоксигеназы, повышая вероятность того, что кислород, активные
формы кислороды, и метаболиты вроде 2-оксоглютарата могут иметь прямое
влияние на ДНК-зависимые процессы, включая транскрипцию и клеточное
поведение.
Очевидно, что метаболические пути сильно взаимосвязаны с путями,
управляющими особенностями раковых клеток, таких как неограниченное
процветание и сопротивляемость к смерти. Многие метаболические
ферменты, интермедиаты и продукты, вовлеченные в процесс, могут стать
основой для плодтворного развития диагностики и терапии рака.
21.
Итог• Раковые клетки используют анаэробный путь
гликолиза, с образованием лактата.
• Зависимы от глютамина
• Высокий уровень АТФ не благоприятен, т.к.
избыток АМФ влечет увеличение количества
супрессоров опухоли. (Не образуют АТФ)
• Для лечения рака используются ингибиторы
метаболических ферметов (например,
гекоскиназы)
22.
Спасибо за внимание!• Jr W.K., Thompson C. Q&A: Cancer: clues
from cell metabolism // Nature. 2010. Vol.
465, № June. P. 3–5.
23.
• Грелин – циркулирущий гормон, вызывающий аппетит. Он происходитот прогормона путём посттрансляционной модификации (это
ковалентная химическая модификация белка после его синтеза на
рибосоме). На основе биоинформатических предсказаний, другой
пептид так же происходит из прогрелина. Исследователи изолировали
гормон из желудка крысы и назвали его обестатином – снижающим
ожирение («from the Latin‘‘obedere,’’ meaning to devour, and ‘‘statin,’’
denoting suppression»).
• Он противоположен по своему эффекту грелину – гормону
вызывающему аппетит. Поэтому исследователи провели эксперимент
давая крысам обестатин, что вызвало снижение потребления пищи,
ингибирование сжатия тонкого кишечника и снижение набора веса.
• Обестатин связан с orphan G protein–coupled receptor GPR39
• Эти два пептидных гормона с противоположным действием в
регулировании массы тела происходят из одного грелинового гена.
После пострансляционной модификации эти гормоны активируют уже
определенные рецепторы.




















 biology
biology