Similar presentations:
Аморфные и кристаллические вещества
1.
Урок по химиипо теме «Аморфные и
кристаллические
вещества»
2.
Девиз урока:«Чтобы переварить
знания,
нужно поглощать их с
аппетитом»
А. Франс
3.
Сложные веществаклассифицируют
по составу и свойствам
на…
4.
От чего зависятсвойства веществ?
От их строения.
5.
Эпиграф« Познать сущее нельзя извне,
можно только изнутри»
Н. Бердяев, философ.
6.
Проблема:Как строение веществ
влияет на их свойства?
7.
Тема урока:Аморфные и
кристаллические
вещества.
Кристаллические решётки.
8.
В каких агрегатных состоянияхмогут находится вещества?
жидкое
твёрдое
газ
9.
Особенности твёрдого состоянияперед жидким и газообразным.
Расстояние между частицами в твёрдых
веществах меньше, чем в газах.
Межатомные и межмолекулярные
взаимодействия в твёрдых веществах
гораздо сильнее.
Чёткое расположение частиц,
образующих вещество.
10.
Твёрдые вещества делят на:Аморфные –
Кристаллические-
не имеют чёткой
температуры
плавления, при
нагревании постепенно
размягчаются и
переходят в текучее
состояние.
имеют строго
определённую
температуру плавления,
характеризуются
правильным
расположением частиц
– в строго
определённых точках
пространства – узлах.
11.
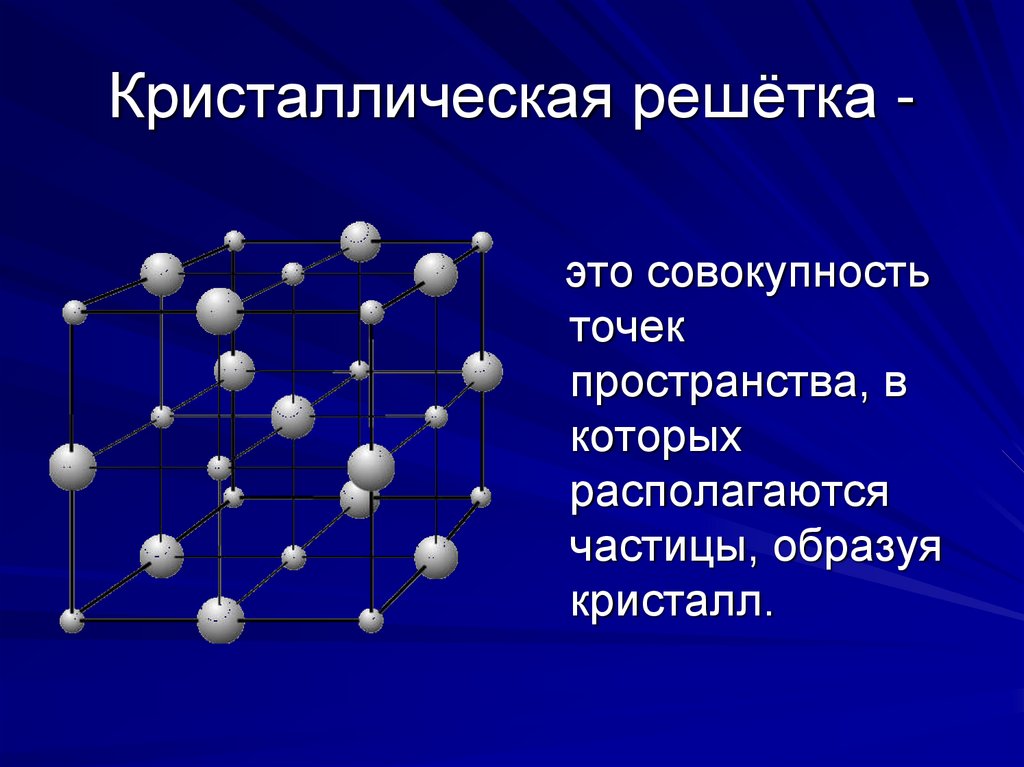
Кристаллическая решётка это совокупностьточек
пространства, в
которых
располагаются
частицы, образуя
кристалл.
12.
Типы кристаллических решёток:Атомные
Ионные
Молекулярные
Металлические
13.
Зависимость свойств веществ от их строения.Тип решётки
Молекулярная
Ионная
Атомная
Металлическая
Вид связи между
Виды
частиц частицами
в узлах
Примеры
веществ
Физические
свойства
веществ
14.
Зависимость свойств веществ от их строения.Тип решётки
Вид связи между
Виды
частиц частицами
в узлах
Молекулярная
Молеку
лы
Ионная
Атомная
Металлическая
Внутри молекулковалентная, между
молекулами – слабые
силы притяжения
Примеры
веществ
Физические
свойства
веществ
H2O, HCl, H2S,
H2,Cl2,O2,O3,P4,
S8 и др.
Непрочные,
летучие,
легкоплавкие,
способные к
возгонке
15.
Зависимость свойств веществ от их строения.Тип решётки
Вид связи между
Виды
частиц частицами
в узлах
Молекулярная
Молеку
лы
Ионная
Ионы
Атомная
Металлическая
Примеры
веществ
Физические
свойства
веществ
Внутри молекулковалентная, между
молекулами – слабые
силы притяжения
H2O, HCl, H2S,
H2,Cl2,O2,O3,P4,
S8 и др.
Непрочные,
летучие,
легкоплавкие,
способные к
возгонке
Ионная
Все соли,
оксиды и
гидроксиды
металлов.
Твёрдые,
прочные,
нелетучие,
тугоплавкие
16.
Зависимость свойств веществ от их строения.Тип решётки
Вид связи между
Виды
частиц частицами
в узлах
Молекулярная
Молеку
лы
Ионная
Атомная
Металлическая
Примеры
веществ
Физические
свойства
веществ
Внутри молекулковалентная, между
молекулами – слабые
силы притяжения
H2O, HCl, H2S,
H2,Cl2,O2,O3,P4,
S8 и др.
Непрочные,
летучие,
легкоплавкие,
способные к
возгонке
Ионы
Ионная
Все соли,
оксиды и
гидроксиды
металлов.
Твёрдые,
прочные,
нелетучие,
тугоплавкие
Атомы
Ковалентная
C,Si,Ge,
Очень твёрдые,
очень прочные,
очень
тугоплавкие.
17.
Зависимость свойств веществ от их строения.Тип решётки
Вид связи между
Виды
частиц частицами
в узлах
Примеры
веществ
Физические
свойства
веществ
Молекулярная
Молеку
лы
Внутри молекулковалентная, между
молекулами – слабые
силы притяжения
H2O, HCl, H2S,
H2,Cl2,O2,O3,P4,
S8 и др.
Непрочные,
летучие,
легкоплавкие,
способные к
возгонке
Ионная
Ионы
Ионная
Все соли,
оксиды и
гидроксиды
металлов.
Твёрдые,
прочные,
нелетучие,
тугоплавкие
Атомная
Атомы
Ковалентная
C,Si,Ge,
Очень твёрдые,
очень прочные,
очень
тугоплавкие.
Металлическая
Атомионы
Металлическая
Все металлы
Ковкие,
пластичные,
тягучие, электрои
теплопроводные
18.
Вывод:свойства веществ зависят от строения
их кристаллической решётки.
Если известно строение вещества,
можно предположить их свойства, и
наоборот, если известны свойства, то
можно определить их строение.
19.
Домашнее заданиеЗаполнить таблицу.
2. По желанию творческое
задание: смоделировать
кристаллическую решетку
любого вещества и дать ей
полную характеристику
1.

















 chemistry
chemistry








