Similar presentations:
Уравнение состояния идеального газа
1.
Уравнение состоянияидеального газа
Дата:
2.
Три пути ведут к знанию:Путь размышления – это путь
самый благородный,
Путь подражания – это путь
самый легкий,
И путь опыта – это путь самый
горький.
Конфуций
древний мыслитель и философ Китая
3.
Путь размышления – это путь самыйблагородный
Какие способы измерения или вычисления
атмосферного давления, например, в нашем
кабинете вы можете предложить?
4.
Путь размышления – это путь самыйблагородный
Предложите способ определения
атмосферного давления в нашем кабинете с
помощью линейки и термометра
5.
Для вычисления атмосферногодавления в нашем кабинете мы пришли
к необходимости установить
зависимость между давлением, объемом
и температурой
Вывести физический закон,
устанавливающий зависимость между
тремя макроскопическими параметрами
— p, V, T.
6.
Для чего нужно уравнениесостояния?
1)Уравнение состояния позволяет определить
одну величин, характеризующих состояние,
например, температуру, если известны две
другие величины.
2) Зная уравнение состояния можно сказать, как
протекают процессы при определенных
внешних условиях: например, как будет
меняться давление газа, если увеличить его
объем при неизменной температуре.
3) Зная уравнение состояние, можно
определить, как меняется состояние системы,
если она совершает работу, или получает
теплоту от окружающих тел.
7.
Бенуа Поль Эмиль Клапейрон(1799 - 1864)
Родился в 1799, в
Париже — французский
физик и инженер.
Воспитывался в
парижской
политехнической школе
(1816—1818).
Установил уравнения
состояния для идеального
газа постоянной массы
В 1820 отправился со
своим товарищем Ламе в
Россию, где был
профессором в институте
путей сообщения.
8.
Дмитрий Иванович Менделеев1837-1907
Родился (8 февраля)
1834, Тобольск —
русский учёныйэнциклопедист,
общественный
деятель.
Обобщил уравнение
Клапейрона для
произвольной массы
газа
9.
1. От чего зависит давление газа?2. Сформулируйте зависимость давления
идеального газа от концентрации и
температуры?
3. Что называется концентрацией?
5. Выразите число молекул N через
микропараметры
6. Какую физическую величину называют
постоянной Авогадро?
7.Каков физический смысл постоянной
Больцмана? Чему она равна?
10.
Подумайте, какимобразом можно связать
три последних
выражения, которые
содержат интересующие
нас макропараметры р,
V, T?
11.
План работы1.Вывести уравнение состояния
идеального газа МенделееваКлапейрона
2.Ввести универсальную газовую
постоянную R. Выяснить физический
смысл универсальной газовой
постоянной R.
3. Вывести связь между давлением,
объемом и температурой идеального
газа в двух любых состояниях –
уравнение Клапейрона.
12.
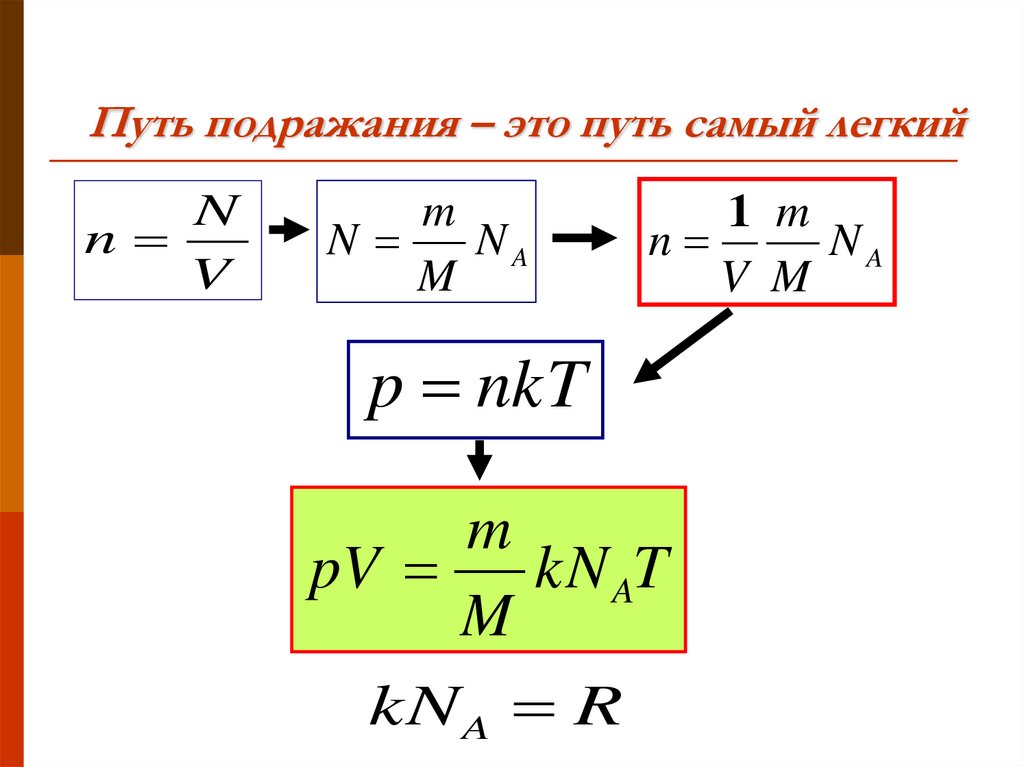
Путь подражания – это путь самый легкийN
n
V
m
N
NA
M
1 m
n
NA
V M
p nkT
m
pV
kN AT
M
kN A R
13.
Уравнение состояния идеального газа –уравнение Клапейрона - Менделеева
m
pV
RT
M
R 8,31 Дж /( моль К )
универсальная
газовая
постоянная
R=8,31 Дж/(моль·К) – универсальная газовая
постоянная – объем одного моля любого газа при
нормальных условиях. В этом состоит физический
смысл универсальной газовой постоянной
14.
И путь опыта –это путь самый горький.
1.
2.
3.
4.
5.
В баллоне вместимостью 30л находится водород под
давлением 5МПа при температуре 270С. Определите его
массу, считая водород идеальным газом.
Каково давление сжатого воздуха, находящегося в
баллоне вместимостью 20л при температуре 120С, если
масса этого воздуха 2 кг? Молярная масса воздуха равна
29 г\моль.
Какой объем занимает 2 моль идеального газа при
условиях, соответствующих условиям в фотосфере
Солнца? (температура 6000К, давление 125 Па)
Плотность некоторого газообразного вещества 2,5 кг\м3
при температуре 100 С и нормальном атмосферном
давлении (р = 105 Па). Найти молярную массу этого
вещества.
Газ при давлении 0,2 МПа и температуре150С имеет
объем 5 л. Чему будет равен объем этой массы газа при
нормальных условиях?














 chemistry
chemistry








