Similar presentations:
Азотистые основания. Нуклеозиды. Нуклеотиды. Нуклеиновые кислоты. Лекция 7
1. Лекция 7.
Азотистые основания.Нуклеозиды. Нуклеотиды.
Нуклеиновые кислоты.
2.
• Нуклеиновыекислоты
(НК)
–
природные
биополимеры
нуклеотидов,
построенные
из
нуклеотидов,
связанных
3',5'-фосфодиэфирными
связями.
Вещества
наследственности.
Высокомолекулярные (мол. масса от 5 тыс. до 10
млн.) твердые вещества кислотной природы,
умеренно и плохо растворимые в воде, растворимы в
щелочах,
нерастворимы
в
органических
растворителях.
• По составу, строению и функциям НК делятся на 2
класса:
• ДНК – дезоксирибонуклеиновые кислоты, построены
из
дезоксирибонуклеотидов
–
сохраняют
наследственную (генетическую) информацию.
• РНК - рибонуклеиновые кислоты, построены из
рибонуклеотидов – участвуют в сохранении и
использовании генетической информации.
3.
• Все НК in vivo связаны с белками:• ДНК кодируют и сохраняют генетическую
информацию в клеточных ядрах (ядерная
ДНК)
и
в
матриксе
митохондрий
(митохондриальная
ДНК),
образуют
нуклеопротеидные комплексы.
• РНК содержатся в ядрах и митохондриях,
рибосомах и цитозоле, делятся на:
• Информационные (матричные) РНК –
кратковременно
сохраняют
генетическую
информацию
• Транспортные РНК – транспортируют
аминокислоты к рибосомам
• Рибосомальные РНК – входят в состав
рибосом
4. Гидролиз нуклеопротеинов.
• Протекает ступенчато: нуклеопротеины вкислой (или нейтральной in vivo) до НК, НК в
щелочной среде до нуклеотидов, а затем до
нуклеозидов, а нуклеозиды – в кислой
среде до азотистых оснований и пентоз ((2дезокси)-D-рибозы)):
• Нуклеопротеин + Н2О/Н+ → НК + белок
• НК + Н2О/OH- → нуклеотиды → нуклеозиды
+ фосфаты
• Нуклеозиды + Н2О/H+ → азотистые
основания + пентоза
5. Азотистые основания нуклеиновых кислот.
• Азотистыеоснования
–
гетероциклические
ароматические
соединения
–
бесцветные
кристаллические
высокоплавкие
вещества,
термически и термодинамически устойчивые, плохо
растворимые в воде (лучше – в горячей) и
органических растворителях, слабые основания.
• Классифицируются на: пиримидиновые (тимин (Т),
цитозин (Ц), урацил (У)) и пуриновые (аденин (А),
гуанин (Г)). Т содержится только в ДНК, а У – только в
РНК.
• В составе НК также имеются модифицированные
азотистые основания.
• Азотистые основания метаболизируют окислением
с образованием производных – гипоксантина,
ксантина и мочевой кислоты. Мочевая кислота
(2,6,8-триоксопурин) – конечный продукт метаболизма
пуриновых азотистых оснований.
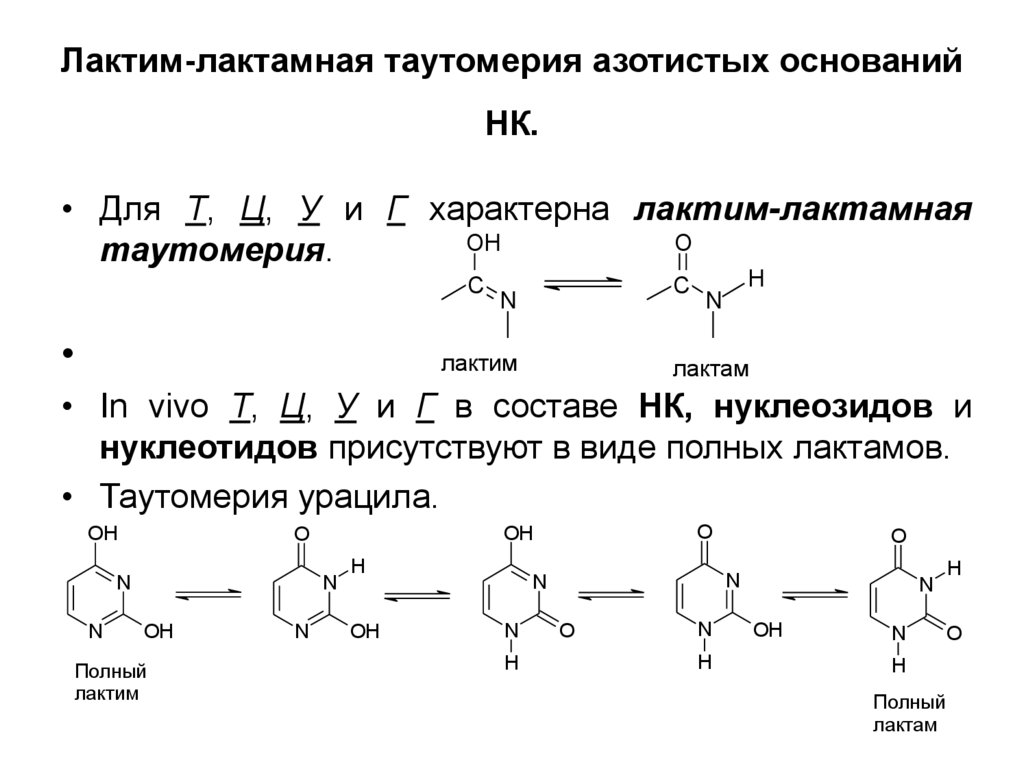
6. Лактим-лактамная таутомерия азотистых оснований НК.
• Для Т, Ц, У и Г характерна лактим-лактамнаяOH
O
таутомерия.
C
C
N
лактим
H
N
лактам
• In vivo Т, Ц, У и Г в составе НК, нуклеозидов и
нуклеотидов присутствуют в виде полных лактамов.
• Таутомерия урацила.
OH
N
N
N
OH
Полный
лактим
N
O
OH
O
H
OH
N
N
N
H
O
O
N
H
N
OH
N
H
Полный
лактам
H
O
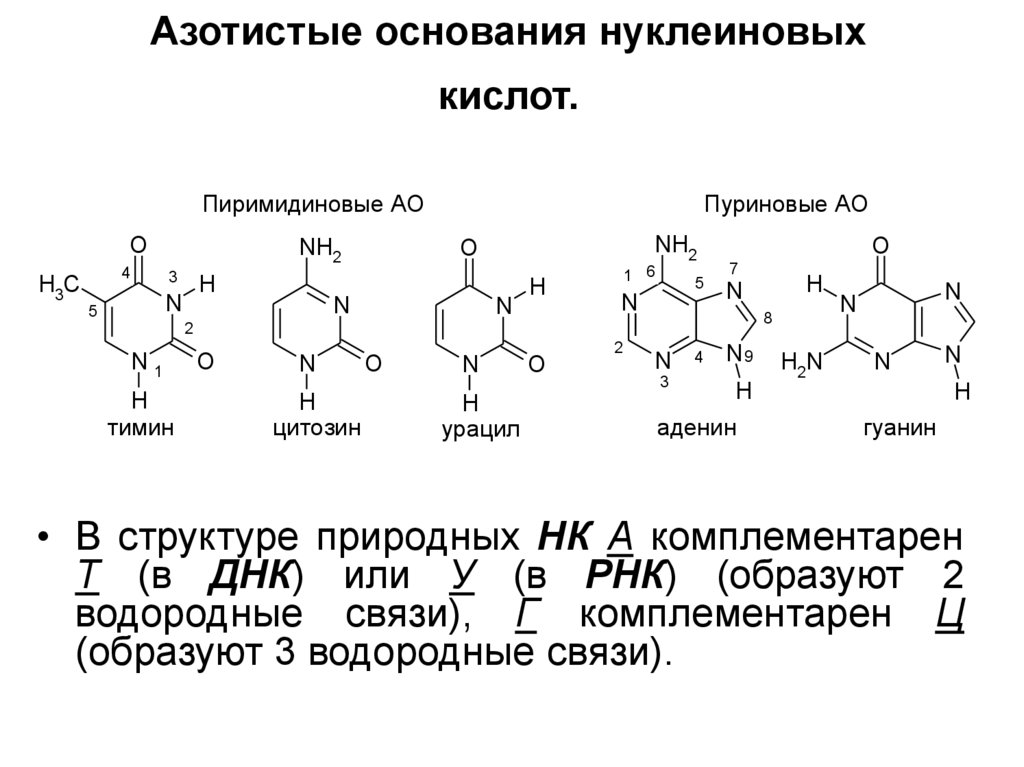
7. Азотистые основания нуклеиновых кислот.
Пиримидиновые АОO
4
H3C
NH2
3
H
N
5
Пуриновые АО
NH2
O
N
N
H
1 6
5
N
O
7
8
2
N1
H
тимин
O
N
H
цитозин
O
N
H
урацил
O
2
H
N
N
3
4
N9
H2N
N
N
N
H
аденин
N
H
гуанин
• В структуре природных НК А комплементарен
Т (в ДНК) или У (в РНК) (образуют 2
водородные связи), Г комплементарен Ц
(образуют 3 водородные связи).
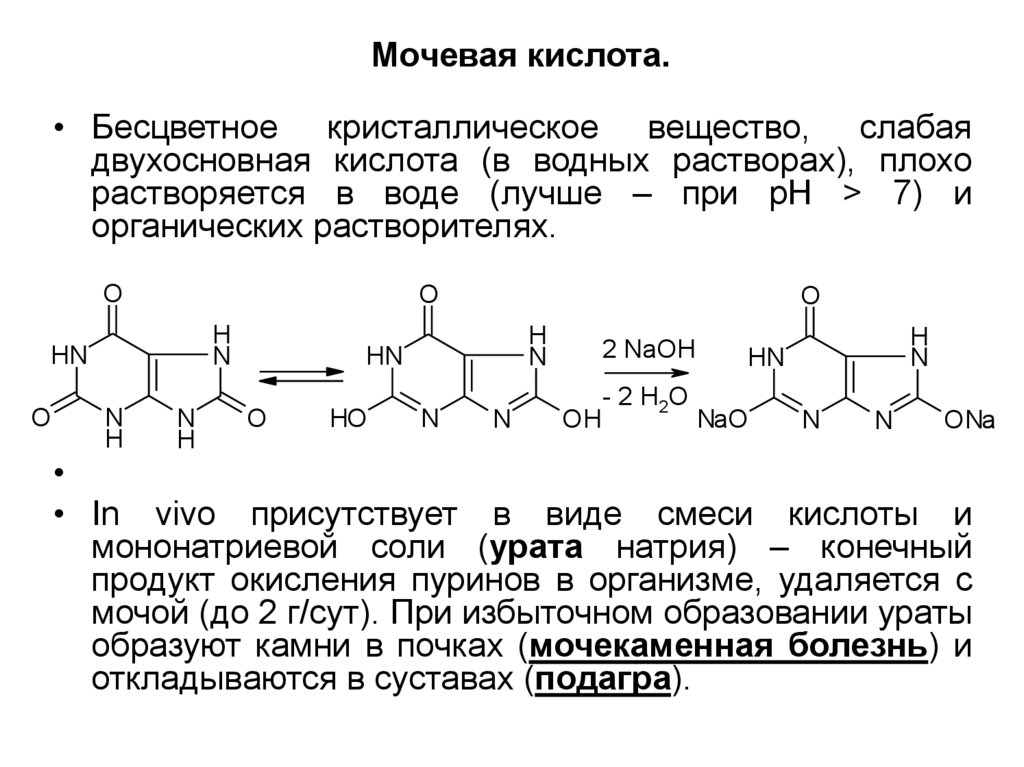
8. Мочевая кислота.
• Бесцветное кристаллическое вещество, слабаядвухосновная кислота (в водных растворах), плохо
растворяется в воде (лучше – при рН > 7) и
органических растворителях.
O
O
H
N
HN
O
N
H
N
H
O
H
N
HN
O
HO
N
N
2 NaOH
OH
- 2 H2O
H
N
HN
NaO
N
N
ONa
• In vivo присутствует в виде смеси кислоты и
мононатриевой соли (урата натрия) – конечный
продукт окисления пуринов в организме, удаляется с
мочой (до 2 г/сут). При избыточном образовании ураты
образуют камни в почках (мочекаменная болезнь) и
откладываются в суставах (подагра).
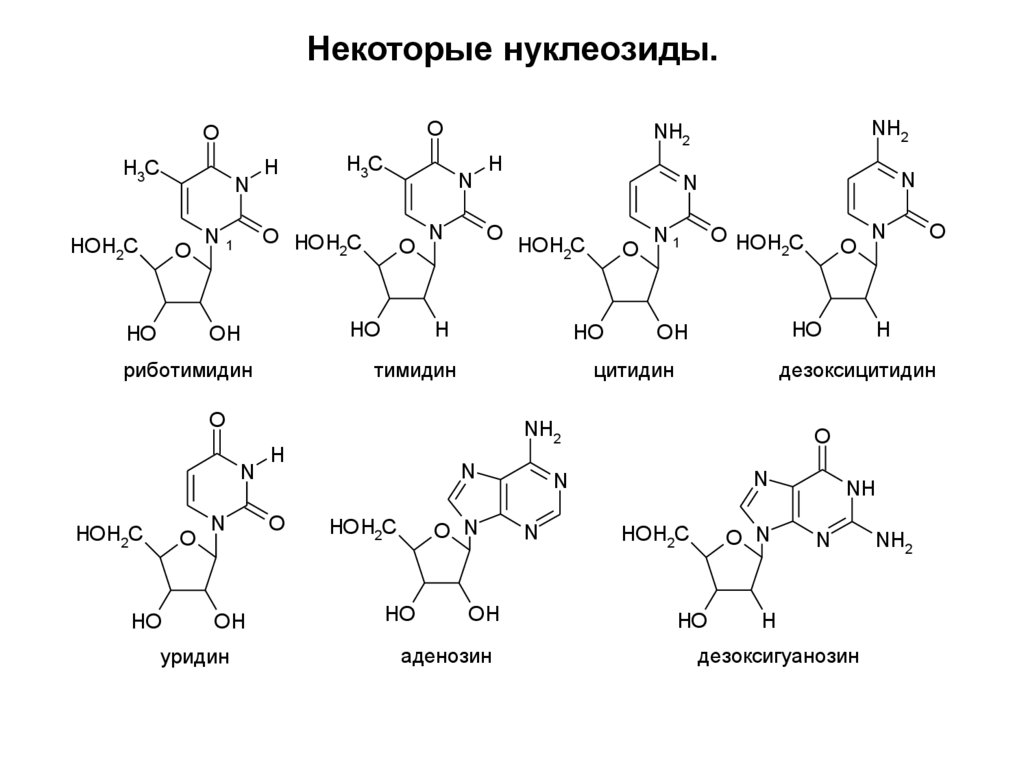
9. Нуклеозиды.
• Нуклеозиды – природные β-N-гликозиды D-рибозы(рибонуклеозиды)
или
2-дезокси-D-рибозы
(дезоксирибонуклеозиды)
с
азотистыми
основаниями НК – твердые вещества, умеренно
растворимые
в
воде
и
нерастворимые
в
органических
растворителях
–
компоненты
нуклеотидов и НК.
• По природе углевода делятся на рибонуклеозиды и
дезоксирибонуклеозиды.
• По природе азотистого основания делятся на
пиримидиновые и пуриновые.
• Альдопентоза связана с азотистым основанием β-Nгликозидной связью, устойчивой в щелочной и
нейтральной средах; в кислой среде in vitro
нуклеозиды
распадаются
на
компоненты
(пуриновые легче, чем пиримидиновые). Пурины
прикреплены
к
альдопентозе
атомом
N-9,
пиримидины – атомом N-1.
10. Некоторые нуклеозиды.
OO
H3C
N
HOH2C
O
HO
N1
H
H3C
N
O HOH C
2
O
HO
OH
риботимидин
N
H
O
HO
N
OH
уридин
HOH2C
H
O
HO
тимидин
N1
O HOH C
2
H
O
HOH2C
O N
HO
OH
аденозин
O
H
O
N
N
N
N
дезоксицитидин
цитидин
N
O
HO
OH
NH2
N
O
N
N
O
HOH2C
NH2
NH2
HOH2C
O N
HO
NH
N
H
дезоксигуанозин
NH2
11. Биороль нуклеозидов и азотистых оснований НК.
• Составляющие компоненты нуклеотидов иНК.
• Модифицированные
синтетические
и
полусинтетические азотистые основания
(5-фторурацил, 6-меркаптопурин и др.) и
нуклеозиды (фторафур, 3'-азидотимидин,
рибавирин и др.) – большая группа
лекарственных
препаратов
(противоопухолевые,
противовирусные,
противогрибковые
и
антибактериальные
средства).
12. Нуклеотиды.
• Нуклеотиды – большая группа фосфорныхэфиров нуклеозидов, очень разнообразных по
составу, строению, свойствам, биологической роли,
применению. Включают 3 основных компонента:
азотистое основание, альдопентозы D-рибозу или
2-дезокси-D-рибозу, 1-3 остатка фосфорной кислоты
в положениях 3' или 5' (обычно) остатка
альдопентозы.
• Нуклеотиды – это твердые вещества кислотной
природы, хорошо растворимые в воде и основаниях,
практически
нерастворимые
в
органических
растворителях. Умеренно устойчивы только в
нейтральной среде, в кислой среде легко теряют
азотистые основания, а в щелочной – фосфаты
(гидролизуются).
• Существуют и разрабатываются лекарственные
препараты олигонуклеотидной природы.
13.
• Нуклеотиды можно классифицировать:• По количеству нуклеотидных звеньев:
• Мононуклеотиды – состоят из 1 азотистого
основания, 1 углевода и остатков фосфорной кислоты
(АМФ, ЦДФ, АТФ, ц-АМФ, ФМН и др.).
• Динуклеотиды – состоят из двух мононуклеотидных
остатков,
связанных
макроэргической
фосфоангидридной связью – 2 азотистых оснований, 2
углеводов и 2 остатков фосфорной кислоты. (НАД+,
НАДН, НАДФН, ФАД и др.).
• Специальные нуклеотиды – состоят из 1
азотистого основания, 1 остатка D-рибозы, 2 остатков
фосфорной кислоты и дополнительной группы –
сульфата (ФАФС) или углевода (УДФ-глюкоза, УДФглюкуроновая кислота и др.).
14.
Мононуклеотиды классифицируют:
По природе азотистого основания:
Пуриновые – содержат А, Г
Пиримидиновые – содержат Т, Ц, У
Флавиновые (ФМН) – содержат изоаллоксазин
По природе альдопентозы:
Рибонуклеотиды – содержат β-D-рибофуранозу
Дезоксирибонуклеотиды – содержат 2-дезокси-β-Dрибофуранозу
• ФМН содержит пятиатомный спирт рибитол
• По количеству остатков фосфорной кислоты:
• Нуклеозидмонофосфаты (1 остаток)
выделяют циклические нуклеотиды (ц-АМФ, ц-ГМФ)
• Нуклеозиддифосфаты (2 остатка)
• Нуклеозидтрифосфаты (3 остатка)
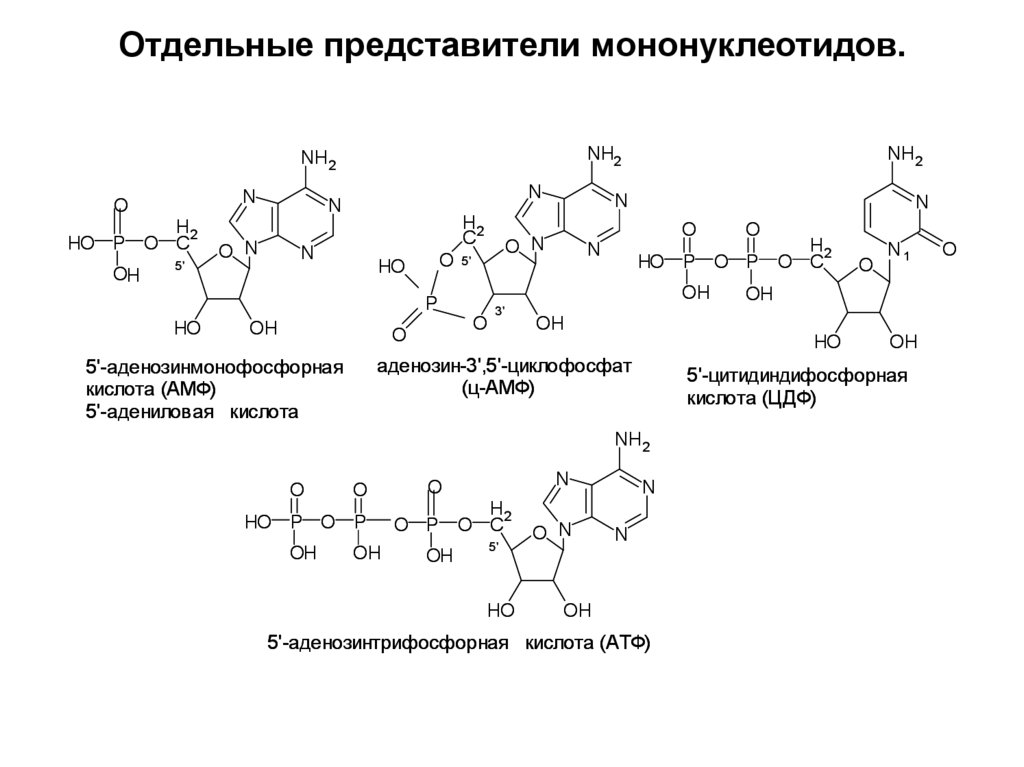
15. Отдельные представители мононуклеотидов.
NH2NH2
N
O
HO P
OH
H2
O C
5'
N
N
O N
H2
C
N
O
HO
OH
O
O
N
N
HO
3'
O
O
O
P O
P
O P
OH
OH
P
O P
H2
O C
OH
N
H2
O C
5'
HO
O
N1
OH
HO
O N
OH
5'-цитидиндифосфорная
кислота (ЦДФ)
NH2
HO
O
OH
аденозин-3',5'-циклофосфат
(ц-АМФ)
5'-аденозинмонофосфорная
кислота (АМФ)
5'-адениловая кислота
O
OH
P
HO
N
O N
5'
NH2
N
N
OH
5'-аденозинтрифосфорная кислота (АТФ)
O
16. Биороль мононуклеотидов.
• Нуклеозидтрифосфаты (АТФ, ГТФ, ЦТФ и др.)используются в биосинтезе НК и специальных
нуклеотидов (УДФ-глюкоза, ФАФС).
• Используются для регуляции метаболических
процессов, АМФ и АДФ стимулируют
выработку энергии в клетках, ц-АМФ и ц-ГМФ
передают гормональный сигнал в клетку.
• УДФ-глюкоза используется для синтеза
гликогена, УДФ-глюкуроновой кислоты.
• УДФ-глюкуроновая
кислота
и
ФАФС
используются
для
детоксикации
ксенобиотиков и в биосинтезе полисахаридов
- ГАГ соединительной ткани.
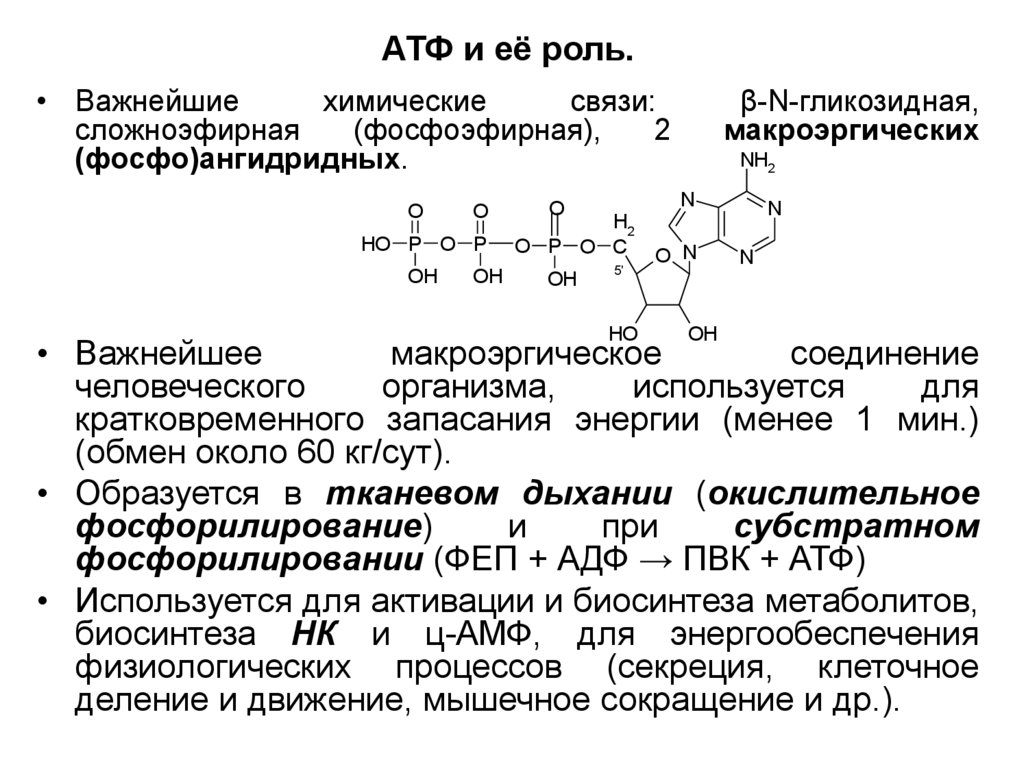
17. АТФ и её роль.
• Важнейшиехимические
связи:
сложноэфирная
(фосфоэфирная),
2
(фосфо)ангидридных.
O
O
HO P O P
OH
OH
NH2
N
O
H2
O P O C
OH
β-N-гликозидная,
макроэргических
5'
HO
O N
OH
N
N
• Важнейшее
макроэргическое
соединение
человеческого
организма,
используется
для
кратковременного запасания энергии (менее 1 мин.)
(обмен около 60 кг/сут).
• Образуется в тканевом дыхании (окислительное
фосфорилирование)
и
при
субстратном
фосфорилировании (ФЕП + АДФ → ПВК + АТФ)
• Используется для активации и биосинтеза метаболитов,
биосинтеза НК и ц-АМФ, для энергообеспечения
физиологических процессов (секреция, клеточное
деление и движение, мышечное сокращение и др.).
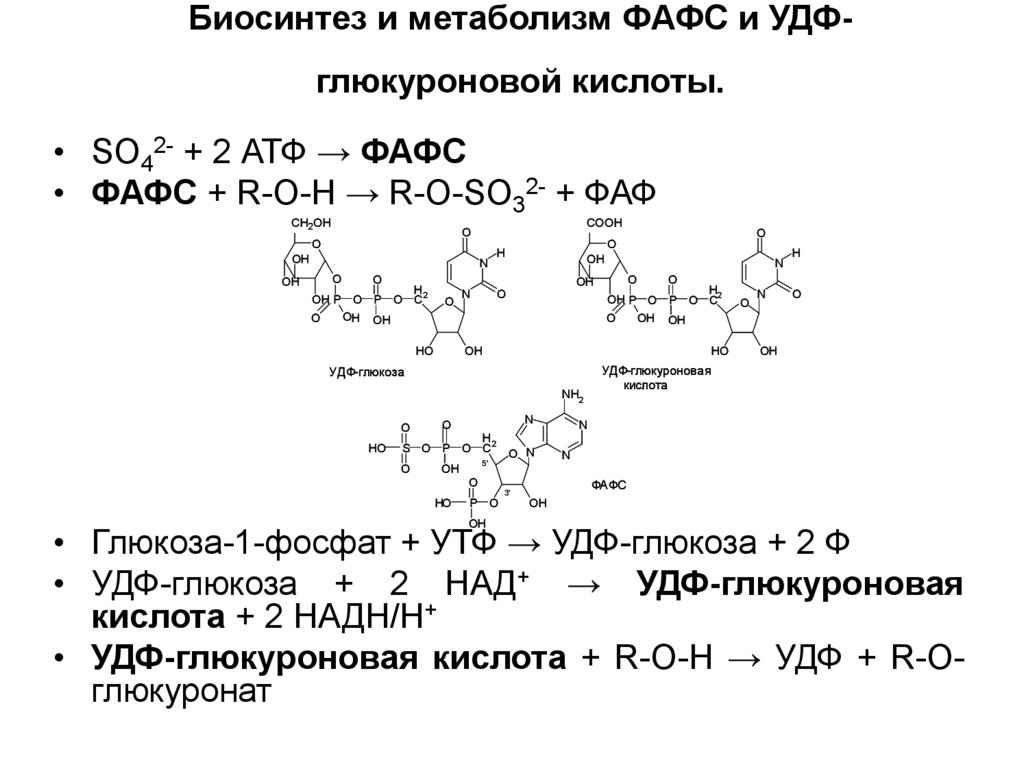
18. Биосинтез и метаболизм ФАФС и УДФ-глюкуроновой кислоты.
Биосинтез и метаболизм ФАФС и УДФглюкуроновой кислоты.• SO42- + 2 АТФ → ФАФС
• ФАФС + R-O-H → R-O-SO32- + ФАФ
CH2OH
COOH
O
O
OH
OH
N
H
OH
O
O
H
OH P O P O C2
OH OH
O
OH
O
HO
N
O
O
O
H
OH P O P O C2
O
OH OH
HO
УДФ-глюкоза
NH2
HO
N
OH
O
O
O
OH
N
H
S O P O C2
5'
O N
3'
P O
OH
O
N
H
O
OH
УДФ-глюкуроновая
кислота
N
N
ФАФС
O
HO
O
O
OH
• Глюкоза-1-фосфат + УТФ → УДФ-глюкоза + 2 Ф
• УДФ-глюкоза + 2 НАД+ → УДФ-глюкуроновая
кислота + 2 НАДН/H+
• УДФ-глюкуроновая кислота + R-O-H → УДФ + R-Oглюкуронат
19. Динуклеотиды.
• Классифицируются на:• Пиридинсодержащие (НАД+ ↔ НАДН, НАДФ+ ↔
НАДФН) – содержат никотинамидный нуклеотид,
азотистые основания А и никотинамид, для
биосинтеза необходим никотинамид (витамин РР)
• Флавинсодержащие (ФАД ↔ ФАДН2) – содержит
флавиновый мононуклеотид (ФМН), азотистые
основания А и изоаллоксазин, для биосинтеза
необходим рибофлавин (витамин В2)
• Это важнейшие коферменты в ОВР in vivo; НАД+,
НАДФ+, ФАД – окислители; НАДН, НАДФН, ФАДН2 –
восстановители.
• НАДН, ФАДН2 – субстраты тканевого дыхания,
энергия их окисления кислородом запасается в
форме АТФ (окислительное фосфорилирование).
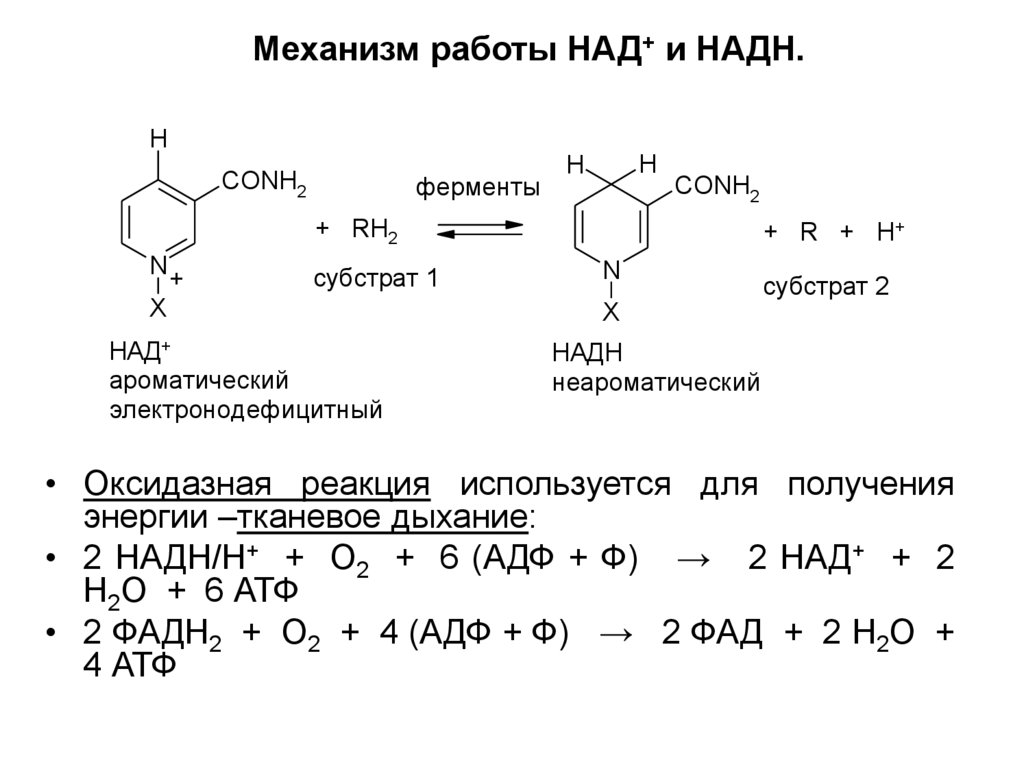
20. Механизм работы НАД+ и НАДН.
HCONH2
ферменты
H
H
CONH2
+ RH2
N
+
субстрат 1
X
НАД+
ароматический
электронодефицитный
+ R + H+
N
субстрат 2
X
НАДН
неароматический
• Оксидазная реакция используется для получения
энергии –тканевое дыхание:
• 2 НАДН/Н+ + О2 + 6 (АДФ + Ф) → 2 НАД+ + 2
Н2О + 6 АТФ
• 2 ФАДН2 + О2 + 4 (АДФ + Ф) → 2 ФАД + 2 Н2О +
4 АТФ
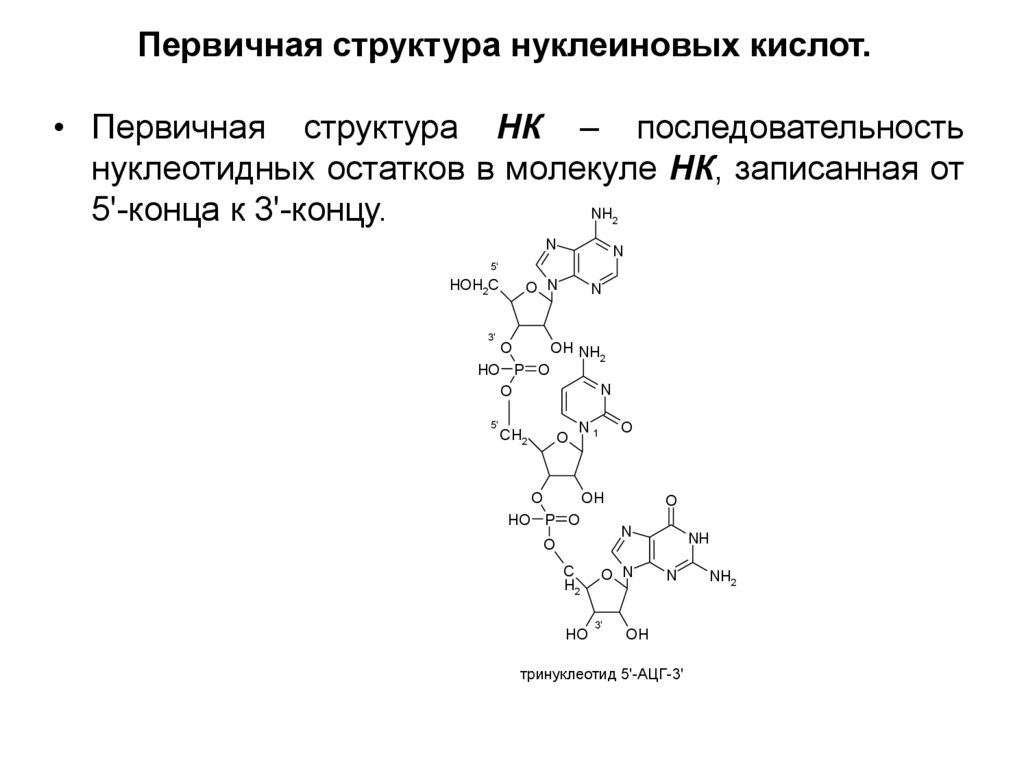
21. Первичная структура нуклеиновых кислот.
• Первичная структура НК – последовательностьнуклеотидных остатков в молекуле НК, записанная от
NH
5'-конца к 3'-концу.
2
N
N
5'
HOH2C
O N
N
3'
O
OH NH
2
HO P O
N
O
5'
CH2
O
N1
O
O
OH
HO P O
N
O
C
H2
HO
O
O N
3'
NH
N
OH
тринуклеотид 5'-АЦГ-3'
NH2
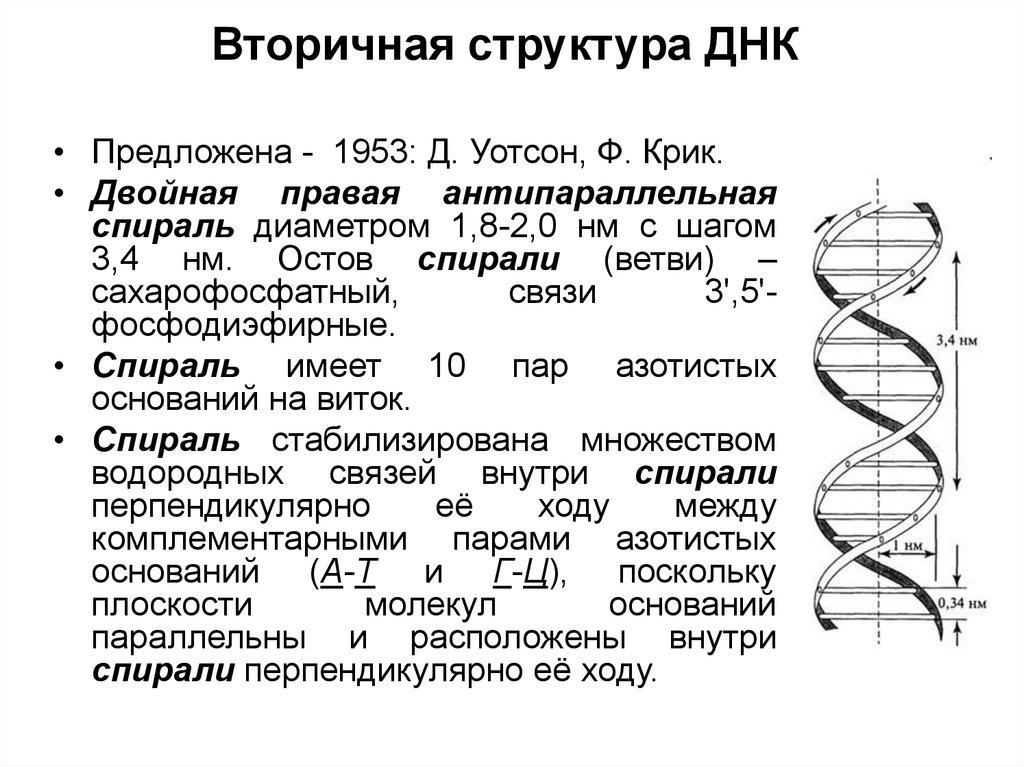
22. Вторичная структура ДНК
• Предложена - 1953: Д. Уотсон, Ф. Крик.• Двойная правая антипараллельная
спираль диаметром 1,8-2,0 нм с шагом
3,4 нм. Остов спирали (ветви) –
сахарофосфатный,
связи
3',5'фосфодиэфирные.
• Спираль имеет 10 пар азотистых
оснований на виток.
• Спираль стабилизирована множеством
водородных связей внутри спирали
перпендикулярно
её
ходу
между
комплементарными парами азотистых
оснований (А-Т и Г-Ц), поскольку
плоскости
молекул
оснований
параллельны и расположены внутри
спирали перпендикулярно её ходу.
23.
• Ядерная ДНК по составу подчиняетсяправилам Чаргаффа:
• Количество А равно количеству Т, а
количество Г – количеству Ц (А = Т, Г =
Ц).
• Количество пуриновых азотистых
оснований
равно
количеству
пиримидиновых (А + Г = Т + Ц).
• Транспортные и рибосомальные РНК не
подчиняются правилам Чаргаффа.
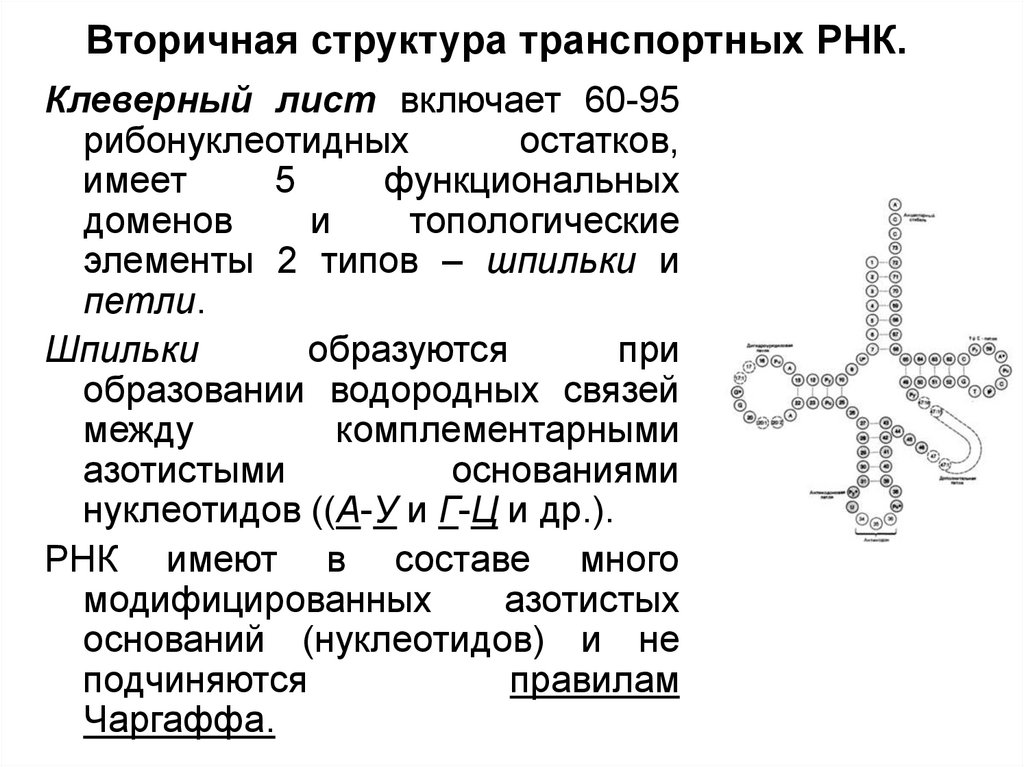
24. Вторичная структура транспортных РНК.
Клеверный лист включает 60-95рибонуклеотидных
остатков,
имеет
5
функциональных
доменов
и
топологические
элементы 2 типов – шпильки и
петли.
Шпильки
образуются
при
образовании водородных связей
между
комплементарными
азотистыми
основаниями
нуклеотидов ((А-У и Г-Ц и др.).
РНК имеют в составе много
модифицированных
азотистых
оснований (нуклеотидов) и не
подчиняются
правилам
Чаргаффа.













 chemistry
chemistry








