Similar presentations:
Антибактериальные химиотерапевтические средства. Введение
1.
Антибактериальныехимиотерапевтические средства
Введение
T 0C
41
40
39
?
38
37
дни
36
1
2. Актуальность
Проблемыинфекционной
патологии
неизменно
сохраняют актуальность для
современной
медицины
и
носят
междисциплинарный
характер.
2
3. Химиотерапеветические средства
ДефиницияХимиотерапеветические
средства
–
вещества,
обладающие
избирательной
токсичностью в отношении определенных
возбудителей инфекционных и паразитарных
заболеваний.
3
4. Химиотерапевтические средства представлены следующими группами:
1)2)
3)
4)
5)
антибактериальные препараты,
противовирусные,
противогрибковые,
противопротозойные,
противоглистные средства.
4
5.
Антибактериальные химиотерапевтическиесредства –
группа
лекарственных
средств,
характеризующаяся
избирательностью
действия в отношении определенных видов
возбудителей
(спектр
антимикробного
действия), низкой токсичностью для человека.
Антибактериальные
препараты
избирательность действия
низкая токсичность для человека
5
6. Антибактериальные химиотерапевтические средства
Антибиотики;Сульфаниламиды;
Производные хинолона;
Синтетические антибактериальные средства
разного химического строения (производные 8оксихинолина, производные нитрофурана,
производные хиноксалина, оксазолидиноны);
5) Противосифилитические;
6) Противотуберкулезные средства.
1)
2)
3)
4)
6
7.
78.
Особенности антибиотиков1. Мишень-рецептор находится не в тканях
человека, а в клетке микроорганизма.
2. Активность антибиотиков не является
постоянной, а снижается со временем, что
обусловлено
формированием
лекарственной
устойчивости (резистентности).
8
9.
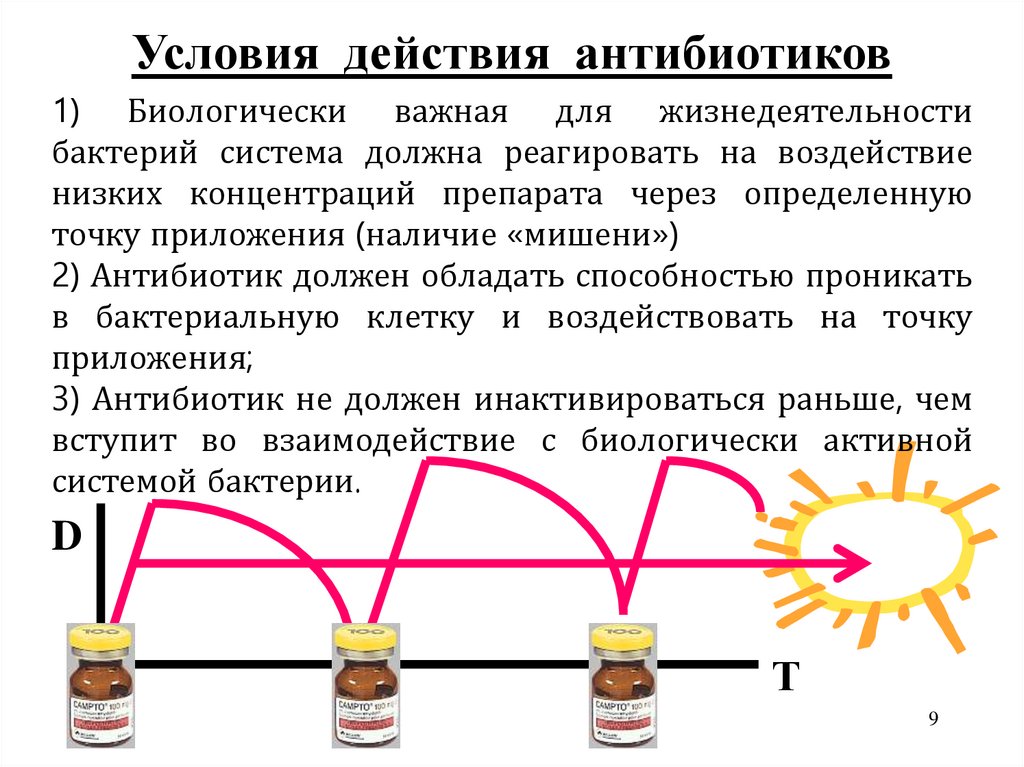
Условия действия антибиотиков1) Биологически важная для жизнедеятельности
бактерий система должна реагировать на воздействие
низких концентраций препарата через определенную
точку приложения (наличие «мишени»)
2) Антибиотик должен обладать способностью проникать
в бактериальную клетку и воздействовать на точку
приложения;
3) Антибиотик не должен инактивироваться раньше, чем
вступит во взаимодействие с биологически активной
системой бактерии.
D
Т
9
10.
Принципырациональной
антибактериальной
терапии
10
11. Основные принципы рациональной антибактериальной терапии
Для профилактики актуальной проблемысовременной
антибактериальной
фармакотерапии
–
антибиотикорезистентности –
приоритетное значение имеет разумное и
рациональное
использование
антибактериальных химиотерапевтических
средств.
11
12.
Обоснованныепоказания
для
назначения
антибактериального средства.
Этиологическая верификация инфекции - определение типа
микроорганизма бактериологическим методом.
Определение чувствительности выделенного возбудителя к
антимикробным препаратам (методами диффузии в агар с
помощью дисков /диско-диффузионный метод/ и Е-тестов,
методом разведения в жидкой или плотной питательной
среде),
определение
категории
чувствительности
(чувствительные, резистентные, умеренно-резистентные) и
назначение препарата сообразно полученным данным.
При неизвестном возбудителе, в экстренных случаях, когда
по медицинским показаниям нет возможности дожидаться
результатов бактериологического метода, инициально
назначаются антибиотики широкого спектра действия с
учетом предсказуемых уровней резистентности в пределах
данного географического региона. Впоследствии терапия
корректируется
в
соответствии
с
результатами
бактериологического метода.
12
13.
Testingthe
susceptibility
of
Staphylococcus aureus
to antibiotics by the
Kirby-Bauer
disk
diffusion
method.
Antibiotics diffuse out
from
antibioticcontaining disks and
inhibit growth of S.
aureus resulting in a
zone of inhibition.
13
14.
Какможно
раннее
начало
проведения
антибактериальной терапии, т.к. в начале
заболевания количество микробных тел невелико и
они находятся в состоянии энергичного роста и
размножения. В этой стадии микроорганизмы
наиболее чувствительны к антибактериальным
препаратам. Время начала антибактериальной
терапии
в
большинстве
случаев
имеет
определяющее прогностическое значение.
Стратификация пациента. Выбор приемлемого
антибиотика должен предполагать учет известных
факторов риска неблагоприятного исхода и оценку
степени тяжести заболевания. По возможности
назначается наиболее активный и наименее
токсичный препарат.
14
15.
Выбор оптимального пути введения препарата.Зависит
от
локализации
инфекционновоспалительного
процесса.
Так,
при
инфекционном
поражении
кишечника,
целесообразно назначение плохо всасывающихся
средств, реализация действия которых будет в
просвете кишечника.
Учет
фармакокинетических
характеристик
препарата также определяется локализацией
инфекционного процесса. Например, выбор
цефалоспоринов
при
перитоните
(хорошо
проникают
через
серозные
оболочки),
бензилпенициллина при менингите (проникает
через ГЭБ).
15
16.
Адекватный режим дозирования. Дозы антибиотиковдолжны
быть
достаточными
для
проявления
антибактериального
(бактерицидного
или
бактериостатического) эффекта. С этой целью иногда
терапию начинают введением ударных доз для
максимально быстрого достижения в плазме крови
терапевтических концентраций лекарства.
Адекватная
длительность
лечения,
строго
соответствующая необходимому курсу антибактериальной
терапии (как правило, 7-10 дней). Клиническое улучшение
(общее облегчение состояния пациента, снижение
температуры тела) не является основанием для
прекращения
приема
препарата.
При
наличии
клинического улучшения возможен перевод пациента с
парентерального
применения
антибиотика
на
пероральный путь.
Например, при пневмонии такого рода критериями служат (Ramirez
J.A., 1995): а) уменьшение кашля, объема экспекторируемой мокроты,
одышки; б) нормальная температура тела при двух ее измерениях с 8часовым интервалом; в) нормальное количество лейкоцитов в
периферической
крови;
г)
отсутствие
нарушений
гастроинтестинальной абсорбции.
16
17.
При отсутствии клинического улучшенияв течение 2-3 дней – необходима смена
препарата. Объективными клиническими
критериями,
отражающими
положительную динамику являются:
снижение
температуры
тела,
нормализация острофазовых показателей
(количество лейкоцитов, характеристика
лейкоцитарной формулы, СОЭ, СРБ и
др.),
субъективными
–
общее
самочувствие, нормализация аппетита.
17
18.
Комбинированнаяантибактериальная
терапия для предупреждения развития
устойчивости микроорганизмов. Показана
при тяжелых инфекциях, хроническом
течении
заболевания
(например,
туберкулезе), а также при микст-инфекциях
с
выделением
различных
по
чувствительности
к
антибиотикам
микробных ассоциаций.
Перманентный
мониторинг
побочных
эффектов и осложнений.
18
19.
Комплайнс (приверженность пациента к лечебнымрекомендациям).
Серьезными
препятствиями
выполнению больным врачебных предписаний
являются
множественность
лекарственных
назначений, развитие нежелательных реакций,
необходимость приема препарата чаще 2 раз в
сутки,
влияние
проводимого
лечения
на
сложившийся жизненный стереотип, минимальные
последствия
(в
представлении
больного)
невыполнения врачебных рекомендаций.
Соотношение цена/эффективность. Идеальный
антибиотик – это не самый дешевый препарат.
Оценивая прямые затраты на лечение (г.о. в
амбулаторных
условиях),
необходимо
со
стоимостью лекарственного средства соотносить
длительность временной утраты трудоспособности,
частоту терапевтических неудач, в том числе и
повлекших за собой госпитализацию.
19
20.
Основыхимиотерапевтической
микробиологии
20
21.
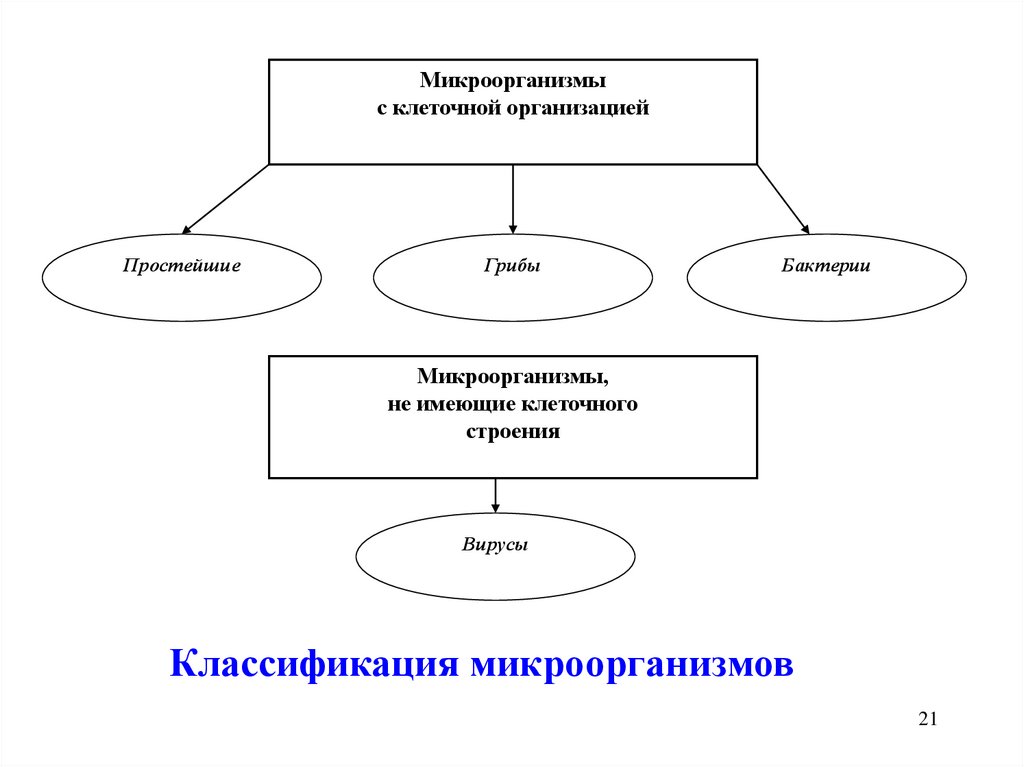
Микроорганизмыс клеточной организацией
Простейшие
Грибы
Бактерии
Микроорганизмы,
не имеющие клеточного
строения
Вирусы
Классификация микроорганизмов
21
22.
По строению микроорганизмы делятсяна:
Прокариоты
Эукариоты
22
23.
Дифференцирующиепризнаки
Эукариоты
Прокариоты
Представители
Водоросли, грибы, простейшие,
растения, животные
Размеры клеток, мкм
>5
<5
Структура ядра
Окружено ядерной
мембраной
Мембрана отсутствует
Структура хромосомы
Более одной нити ДНК
Одна замкнутая нить ДНК
Строение цитоплазматической
мембраны
В состав входят стеролы
Стеролы отсутствуют
Строение клеточной стенки
Нет или на основе хитина или
целлюлозы
Комплекс пептидогликана или
псевдопептидогликана
Способ размножения
Половое или бесполое
Бинарное деление
Bacteria (Eubacteria
бактерии),
(Archaeabacteria
архебактерии)
-
истинные
Archaea
-
Цитоплазматические структуры
Митохондрии
+
-
Аппарат Гольджи
+
-
Эндоплазматический
ретикулум
+
-
Рибосомы
80S
70S
23
24.
Трехмерная модель эукариотической клетки24
25.
В 1884 году датский врач-бактериолог ХансКристиан Иоахим Грам (Gram, Hans
Christian Joachim, 1853-1938) обнаружил, что
если бактерии обработать сначала красителем
кристаллическим
фиолетовым
(генцианвиолетом), а затем йодом, то
бесцветные в обычных условиях клетки
окрашиваются.
Техника дифференцирования бактерий по
морфологическим признакам –
метод окраски бактерий по Граму.
25
26.
Gram, HansChristian Joachim,
1853-1938
26
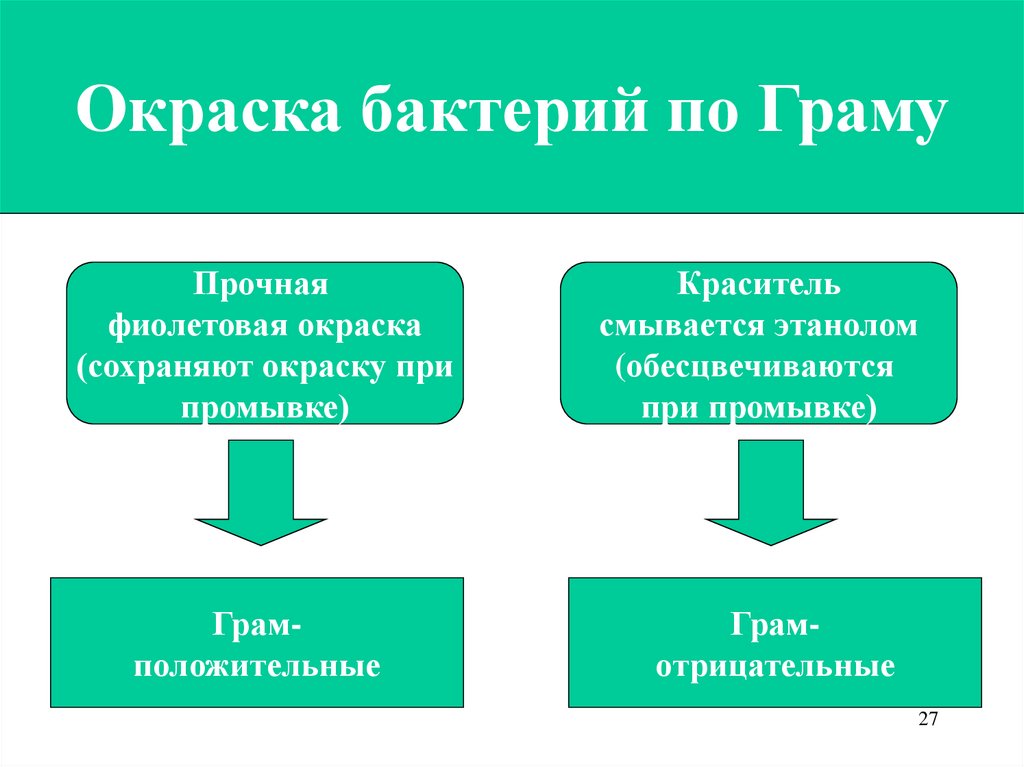
27.
Окраска бактерий по ГрамуПрочная
фиолетовая окраска
(сохраняют окраску при
промывке)
Грамположительные
Краситель
смывается этанолом
(обесцвечиваются
при промывке)
Грамотрицательные
27
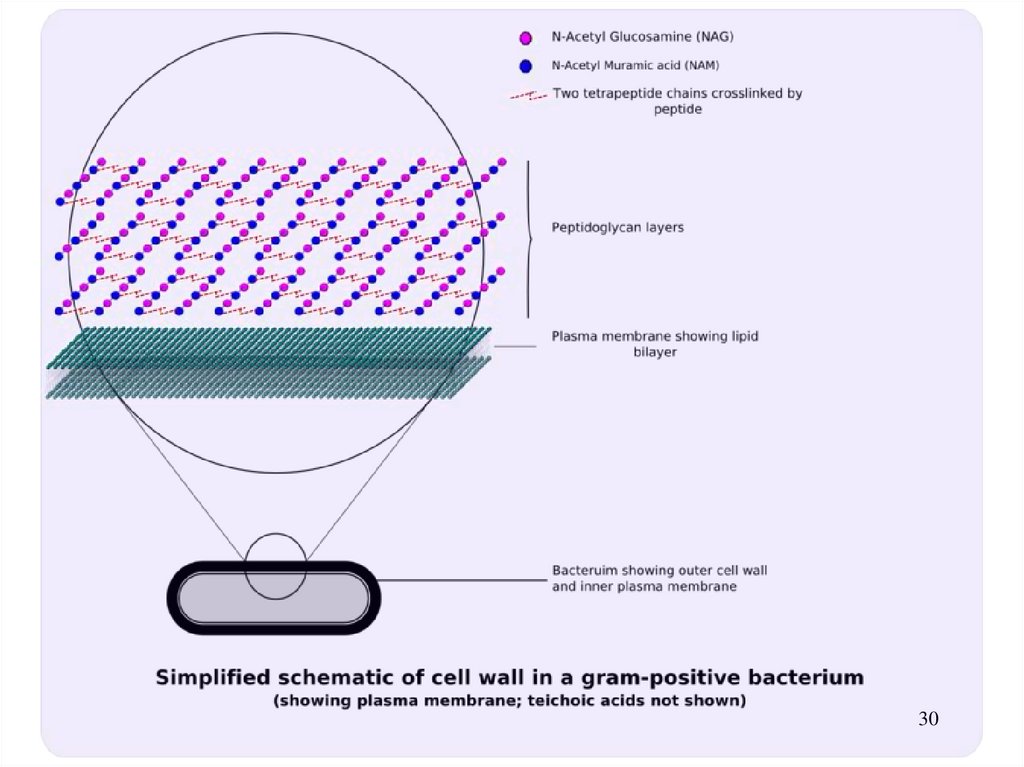
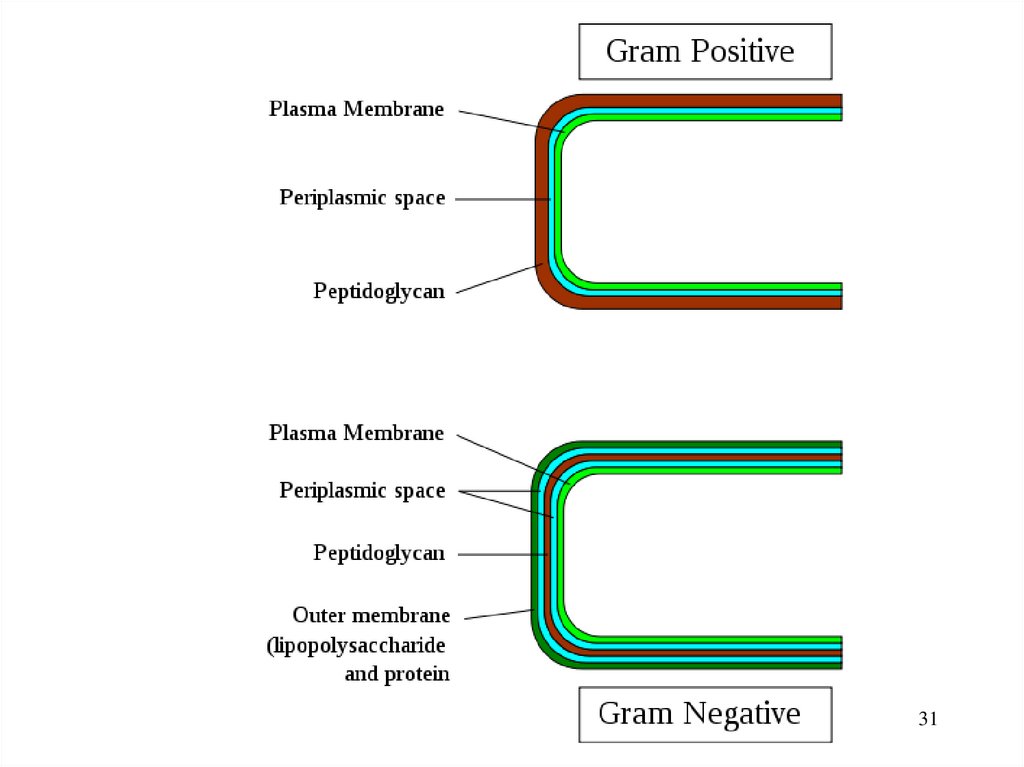
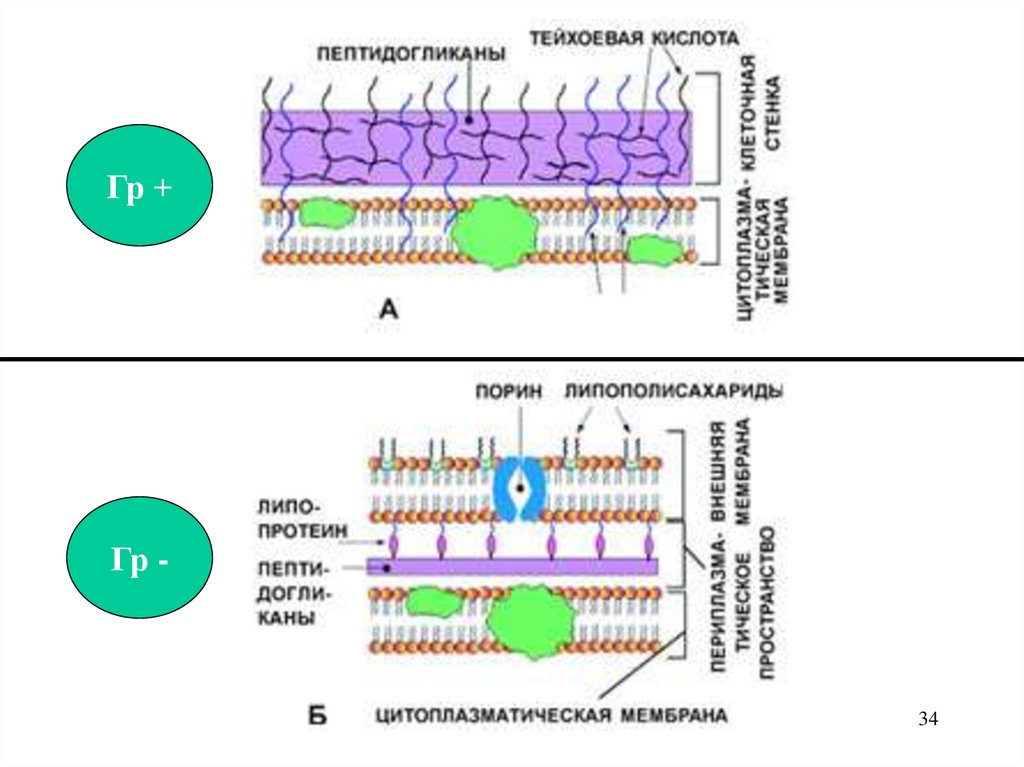
28.
Грамположительные бактерииЦитоплазматическая мембрана снаружи окружена
толстым слоем особых молекул – пептидогликанов ригидный слой (мукопептидный). Этот слой, пронизан
сетью полимерных молекул тейхоевой кислоты.
Низкомолекулярный
комплекс
кристаллического
фиолетового
с
йодом
удерживается
в
пептидогликановом слое, обеспечивая прочную
окраску.
Между
пептидогликаном
и
наружной
ЦПМ
располагаются периплазматические пространства.
В строении клеточной стенки, в отличие от
грамотрицательных бактерий, наружная мембрана
28
отсутствует.
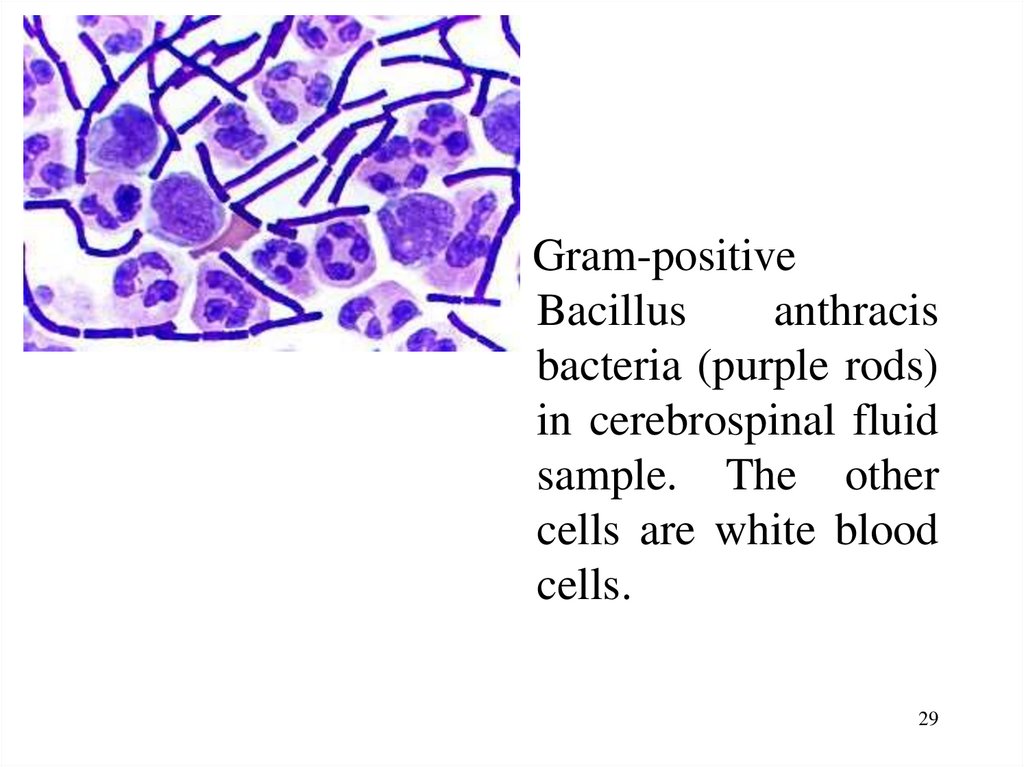
29.
Gram-positiveBacillus
anthracis
bacteria (purple rods)
in cerebrospinal fluid
sample. The other
cells are white blood
cells.
29
30.
3031.
3132.
Gram-negative Pseudomonas aeruginosabacteria
32
33.
Грамотрицательные бактерииПептидогликановый слой гораздо тоньше, зато
у них есть дополнительная внешняя мембрана,
которая содержит заряженные молекулы
липополисахаридов (липидный бислой) и
белки-порины, образующие поры.
Молекулы красителя легко проникают через эти
поры, но не задерживаются и с такой же
легкостью выходят при промывке - метод
дифференциальной
окраски
(систематики)
бактерий.
33
34.
Гр +Гр -
34
35.
3536.
Антибиотики (от греч. аnti – против, bias –жизнь) - это химические соединения
биологического происхождения, оказывающие
избирательное повреждающие или губительное
действие на микроорганизмы.
Под избирательным действием понимают
активность
только
в
отношении
микроорганизмов
при
сохранении
жизнеспособности клеток макроорганизма и
действие не на все, а на определенные роды и
виды микроорганизмов.
36
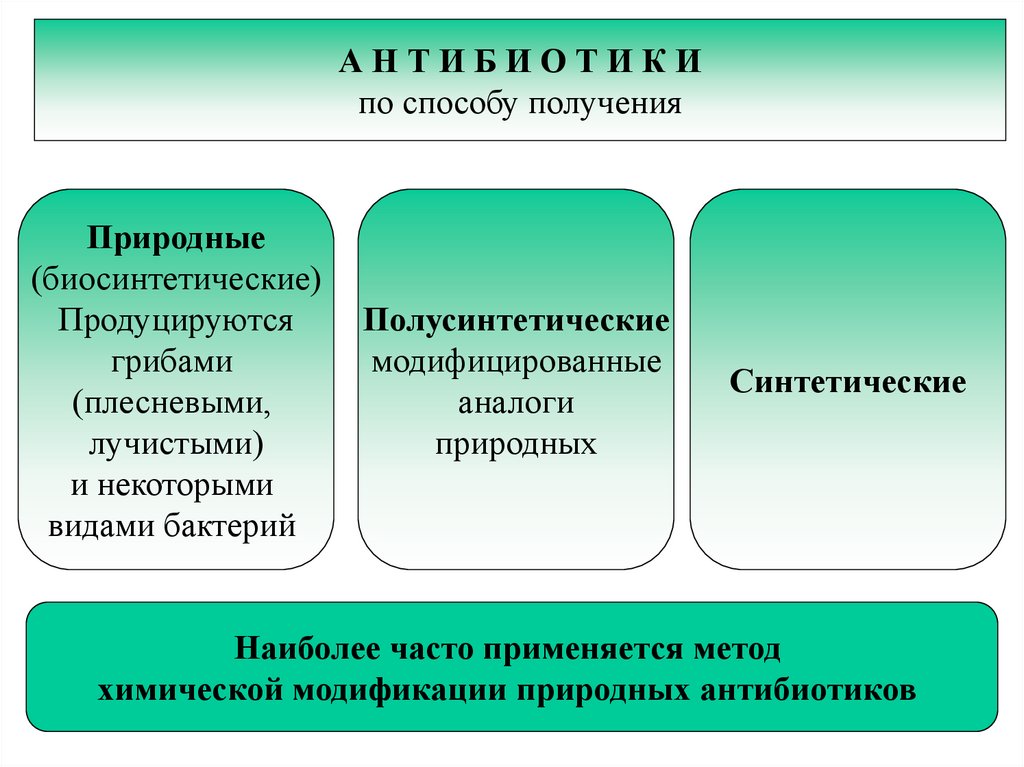
37.
АНТИБИОТИКИпо способу получения
Природные
(биосинтетические)
Продуцируются
грибами
(плесневыми,
лучистыми)
и некоторыми
видами бактерий
Полусинтетические
модифицированные
аналоги
природных
Синтетические
Наиболее часто применяется метод
химической модификации природных антибиотиков
37
38.
АНТИБИОТИКИпо характеру действия
Бактерицидные
Бактериостатические
38
39.
АНТИБИОТИКИпо характеру действия
1. Антибиотики с бактерицидным действием
(влияющие на клеточную стенку и
цитоплазматическую мембрану).
2.
Антибиотики
с
бактериостатичесским
действием
(влияющие на синтез макромолекул).
39
40.
АНТИБИОТИКИпо характеру действия
Выделение
бактерицидных
и
бактериостатических
антибиотиков
имеет основное практическое значение
при
лечении
тяжелых
инфекций,
особенно у пациентов с нарушениями
иммунитета, когда обязательно следует
назначать бактерицидные препараты.
40
41.
АНТИБИОТИКИпо виду действия
Антибактериальные
Противоопухолевые
Противогрибковые
41
42.
АНТИБИОТИКИпо широте спектра антибактериальной активности
«Широкого»
спектра
«Узкого»
спектра
Четкие критерии такого деления
на сегодняшний день отсутствуют
42
43.
Широта спектра действияОшибочным является представление о том, что
препараты широкого спектра активности более
«сильны», а применение антибиотиков с узким
спектром в меньшей степени способствует развитию
резистентности и т.д. При этом не учитывается
приобретенная резистентность, вследствие чего, к
примеру, тетрациклины, которые в первые годы
применения были активны в отношении большинства
клинически значимых микроорганизмов, в настоящее
время потеряли значительную часть своего спектра
активности именно из-за развития приобретенной
резистентности у пневмококков, стафилококков,
гонококков, энтеробактерий.
43
44.
Широта спектра действияЦефалоспорины III генерации обычно
рассматривают как препараты с широким
спектром активности, однако они не действуют
на MRSA, многие анаэробы, энтерококки,
листерии, атипичные возбудители и др.
В этой связи наиболее целесообразно
рассматривать антибиотики с точки зрения
клинической эффективности при инфекции
определенной локализации, т.к. клинические
доказательства эффективности, полученные в
клинических испытаниях имеют несомненно
более важное значение.
44
45.
Антибиотики / АнтисептикиАнтибиотики
кардинальным
образом
отличаются от антисептиков.
Последние действуют на микроорганизмы не
избирательно
и
применяются
для
их
уничтожения в живых тканях. Дезинфектанты
также предназначены для неизбирательного
уничтожения микроорганизмов вне живого
организма (предметы ухода, поверхности и
т.д.).
45
46.
Основные механизмы действияряда антибиотиков
Механизм
Примеры
Нарушение синтеза
клеточной стенки
Пенициллины
Цефалоспорины
Карбапенемы
Монобактамы
Гликопептиды
Циклосерин
Нарушение синтеза белка
на уровне рибосом
Тетрациклины
Левомицетин
Макролиды
Азалиды
Аминогликозиды
Линкозамиды
Нарушение синтеза РНК
Нарушение
проницаемости ЦПМ
Рифампицин
Полимиксины
Нистатин
Амфотерицин В
46
47. Требования, предъявляемые к антибактериальным препаратам
Разработка и создание новых антибиотиков направлены
на получение «идеального» препарата, сочетающего в
себе следующие свойства:
расширенный спектр антибактериальной активности, что
позволит применять препарат при широком круге
инфекционных заболеваний;
воздействие препарата на микрофлору, резистентную к уже
имеющимся антибиотикам;
возможность как парентерального, так и перорального
применения;
благоприятный
профиль
безопасности
(хорошая
переносимость, минимальный риск развития побочных
эффектов);
удовлетворительная
экономическая
составляющая
(стоимость производства препарата).
47
48.
4849.
Для антибиотиков характерна высокаяизбирательность действия в отношении
микроорганизмов и сравнительно низкая
токсичность в отношении макроорганизма,
что
объясняется
следующими
особенностями организации бактерий.
49
50.
Отличительнаяособенность
строения
бактериальных
клеток
от
клеток
млекопитающих – их цитоплазматическая
мембрана окружена снаружи внешней
жесткой оболочкой – клеточной стенкой.
Клеточная
оболочка
служит
каркасом
бактериальной
клетки
и
обеспечивает
постоянство ее «внешнего вида» - формы (Str,
Е.coli).
St.aureus
E.coli
50
51.
Клеточная стенка бактерий по химическому составукардинально отличается от мембран клеток
макроорганизма. В состав бактериальной клеточной
стенки входит мукопептид муреин, содержащий Nацетил-глюкозамин, N-ацетилмурамовую кислоту, а
также пептидные цепочки, включающие некоторые Lи D-аминокислоты.
Нарушение синтеза бактериальными клетками
пептидогликана, например, группой бета-лактамных
антибиотиков,
сопровождается
бактерицидным
эффектом без токсического воздействия на клетки
человека
(у
млекопитающих
отсутствует
пептидогликан и пенициллинсвязывающие белки).
51
52.
У клеток млекопитающих, в отличие отбактериальных клеток, помимо общей
плазматической
мембраны,
все
интрацеллюлярные
органеллы
имеют
собственные, зачастую двойные мембраны.
Различия в темпах роста и размножения.
52
53.
5354.
г.–
Александр
Флеминг,
английский биолог обнаружил антибиоз
между плесневым грибом рода Penicillium и
бактериальными
культурами
стафилококков,
что
сопровождалось
лизисом бактерий.
Действующее начало А.Флеминг назвал
пенициллином (открытие пенициллина).
Однако его попытки получить чистое
бактерицидное вещество не привели к
успеху.
1929
54
55.
В 1935 г. Э. Чейн (Эрнест Каин) приглашенпрофессором патологии Г. Флори в Оксфорд, чтобы
развернуть работу по лизоциму - антибактериальному
ферменту.
Э. Чейн предлагает Г. Флори сконцентрироваться на
более обещающем пенициллине, открытом тем же А.
Флемингом семью годами позже.
Сам А. Флеминг был скептически настроен к своему
детищу, заявив, что «…этим не стоит заниматься». Не
только ему, но и более известному биохимику Дж.
Рейстрику не удалось выделить достаточно
стабильный «экстракт».
55
56.
25 мая 1940 г. под грохот бомб, падающих на улицы Лондона,был завершен первый тест антибактериальной «протекции»
пенициллина на мышах.
Затем наступил биохимический триумф Э. Чейна, показавшего,
что пенициллин имеет структуру бета-лактама. Оставалось
только наладить производство нового чудо-лекарства. Его
чудодейственные свойства были доказаны в том же Оксфорде, в
одну из клиник которого 15 октября того же года поступил
местный полицейский, жаловавшийся на непроходящую
«заеду» в углу рта (ранка была инфицирована золотистым
стафилококком и нагноилась). К середине января инфекция
захватила лицо мужчины, шею и перекинулась на руку и легкое.
И тогда врачи отважились ввести больному неслыханный до
сего момента пенициллин. В течение месяца пациент
чувствовал себя неплохо: но драгоценные кристаллы,
полученные из Оксфорда, кончились, и 15 марта 1941 г.
бывший полицейский скончался.
56
57.
1940 г. – Е. Чейн с сотрудниками (Флори) выделиличистую культуру первого пенициллина (получен в
очищенном виде), что знаменовало начало эры
антибактериальной терапии.
1942
г.
–
в
России
получены
первые
высокопродуктивные штаммы пенициллина З.В.
Ермольевой (из гриба Penicillium crustosum).
1949 г. – Кроуфт с помощью кристаллографических
исследований доказал, что типичной структурной
частью молекулы пенициллина является беталактамное кольцо.
1957 г. – Е. Чейн получил первый полусинтетический
пенициллин.
57
58.
Sir Ernst Boris Chain(19 June 1906 – 12 August 1979)
was a German-born
British biochemist, and a 1945 corecipient of the
Nobel Prize for Physiology or Medicine
for his work on penicillin.
58
59.
Howard Walter Florey,Baron Florey
(24 September 1898 – 21
February 1968) was an
Australian pharmacologist
who shared the Nobel Prize
in Physiology or Medicine in
1945 with Ernst Boris Chain
and Sir Alexander Fleming
for his role in the extraction
of penicillin.
59
60.
З.В. Ермольева60
61.
6162.
При использовании антибактериальныхпрепаратов к ним может развиваться
резистентность
(устойчивость)
микроорганизмов, являющаяся чертой их
биологической
эволюционной
приспособляемости.
62
63.
Природная (истинная) резистентностьимеет первичный характер;
характеризуется отсутствием у микроорганизмов
мишени действия антибиотика или недоступности
мишени вследствие первично низкой проницаемости
или ферментативной инактивации;
при наличии у бактерий природной устойчивости
антибиотики клинически неэффективны.
Природная резистентность является постоянным
видовым признаком микроорганизмов и легко
прогнозируется.
Например,
микобактерии
туберкулеза обладают природной устойчивостью к
пенициллинам.
63
64.
Приобретенная резистентностьсвойство отдельных штаммов бактерий сохранять
жизнеспособность
при
тех
концентрациях
антибиотиков, которые подавляют основную часть
микробной популяции,
носит вторичный характер.
Возможны ситуации, когда большая часть
микробной популяции проявляет приобретенную
устойчивость. Появление у бактерий приобретенной
резистентности не обязательно сопровождается
снижением
клинической
эффективности
антибиотика.
64
65.
Формирование резистентности во всех случаяхобусловлено генетически: приобретением новой
генетической информации или изменением уровня
экспрессии собственных генов.
Например,
стрептококки и возбудители сифилиса – спирохеты
не
обладают
природной
резистентостью
к
пенициллинам.
Резистентность
может
быть
следствием размножения устойчивых штаммов в
ходе естественного отбора после уничтожения
чувствительных
штаммов
лекарственными
веществами. Т.о., резистентность развивается при
отборе естественных мутантов. Обычно штаммы,
обладающие врожденной устойчивостью, составляют
ничтожную часть исходной культуры.
65
66.
Ассоциированная резистентностьУстойчивость микроорганизмов к антибиотикам
более чем одного химического класса
одновременно (например, к бета-лактамам,
аминогликозидам
и
фторхинолонам
одновременно).
66
67.
Перекрестная резистентностьУстойчивость
микроорганизмов
к
антибиотикам одного химического класса
(например, к нескольким представителям
аминогликозидов,
нескольким
фторхинолонам).
67
68.
Если к антибиотику возникла устойчивость,его необходимо заменить препаратом резерва.
Резервные антибиотики по одному или по
ряду
свойств
уступают
основным
антибиотикам (меньшая активность, низкий
профиль безопасности, быстрое развитие
резистентности). В этой связи антибиотики
резерва назначаются при устойчивости
возбудителя к основным антибиотикам или
при их непереносимости.
68
69. Биохимические механизмы устойчивости бактерий к антибиотикам
1) Модификация мишени действия.2) Инактивация антибиотика.
3) Активное выведение антибиотика из
микробной клетки (эффлюкс).
4) Нарушение проницаемости внешних
структур микробной клетки.
5) Формирование метаболического "шунта".
69
70. Направления развития устойчивости к бета-лактамным антибиотикам
1) Синтез бета-лактамаз (индукция хромосомальныхбета-лактамаз и их гиперпродукция; синтез
плазмидных бета-лактамаз широкого спектра
действия, инактивирующих антибиотик на пути к
внутренней мембране – месту локализации ПСБ);
2) Активное выведение (транспорт) антибиотика из
клетки – эффлюкс;
3) Изменение структуры пенициллинсвязывающего
белка;
4) Снижение проницаемости внешней мембраны
(потеря поринов).
70
71.
Т.о.,антибиотикорезистентность,
как
биологический феномен определяет как
тактику фармакотерапии, так и направления
фармакологии
по
поиску
новых
антибиотиков,
фармацевтической
промышленности,
вынужденной
производить все новые антибактериальные
препараты.
71
72. Общие специфические свойства антибиотиков
1) Мишень действия находится не в тканяхчеловека, а в клетке микроорганизма.
2) Активность
антибиотиков
не
является
постоянной, а снижается со временем, что
обусловлено формированием лекарственной
устойчивости (резистентности).
3) Антибиотикорезистентность
является
неизбежным биологическим явлением, и
предотвратить ее практически невозможно.
72




























































 medicine
medicine








