Similar presentations:
Валентные состояния атома серы
1.
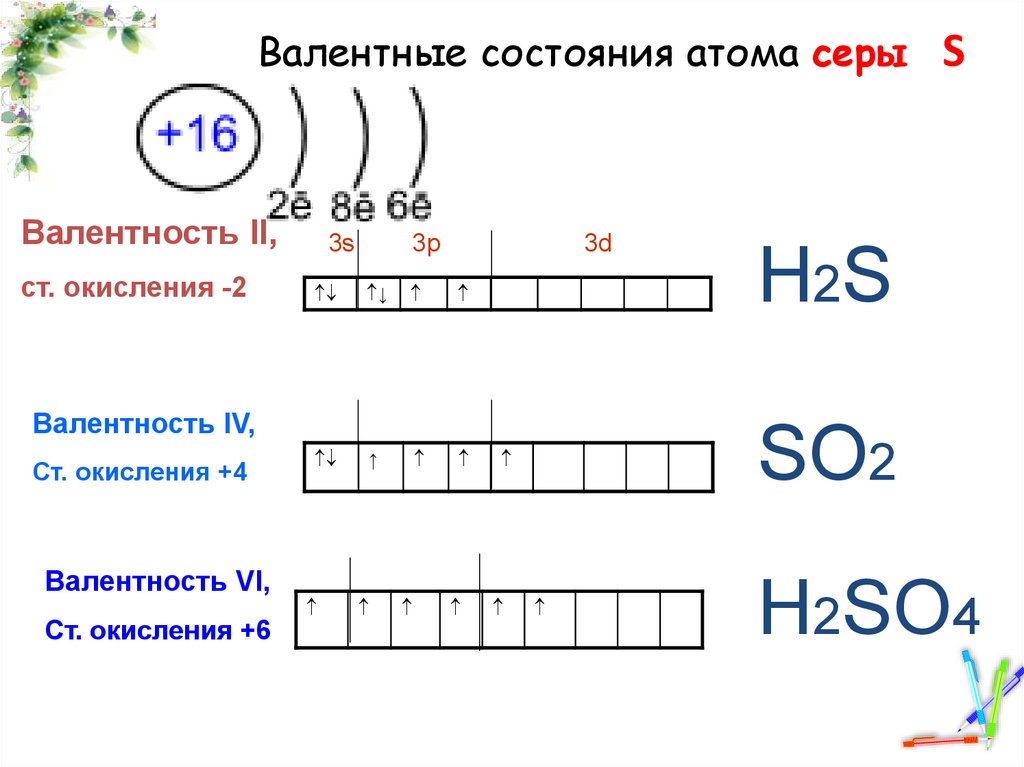
Валентные состояния атома серыВалентность II,
ст. окисления -2
3s
3p
3d
↓
↑
Валентность IV,
Ст. окисления +4
Валентность VI,
Ст. окисления +6
Н2S
SО2
S
Н2SО4
2.
Физические свойства серы• Твёрдое
кристаллическое
вещество желтого
цвета, без запаха
• Плохо проводит теплоту и
не проводит
электрический ток
• Сера в воде практически
не растворяется
• Температура плавления
1200С
3.
Нахождение серы в природеСера является на
16-м месте по
распространённост
и в земной коре..
4.
Добыча самородной серы5.
Сера также встречается в видесульфатов - солей серной кислоты мирабилит
6.
Пирит – «огненный камень»(соединение серы в природе)
7.
Сера вприроде
Сера входит в
состав белков.
Особенно
много серы в
белках волос,
рогов, шерсти.
Кроме этого
сера является
составной
частью
биологически
активных
веществ:
витаминов и
гормонов.
8.
Аллотропныемодификации
серы
Ромбическая
Моноклинная
Пластическая
9.
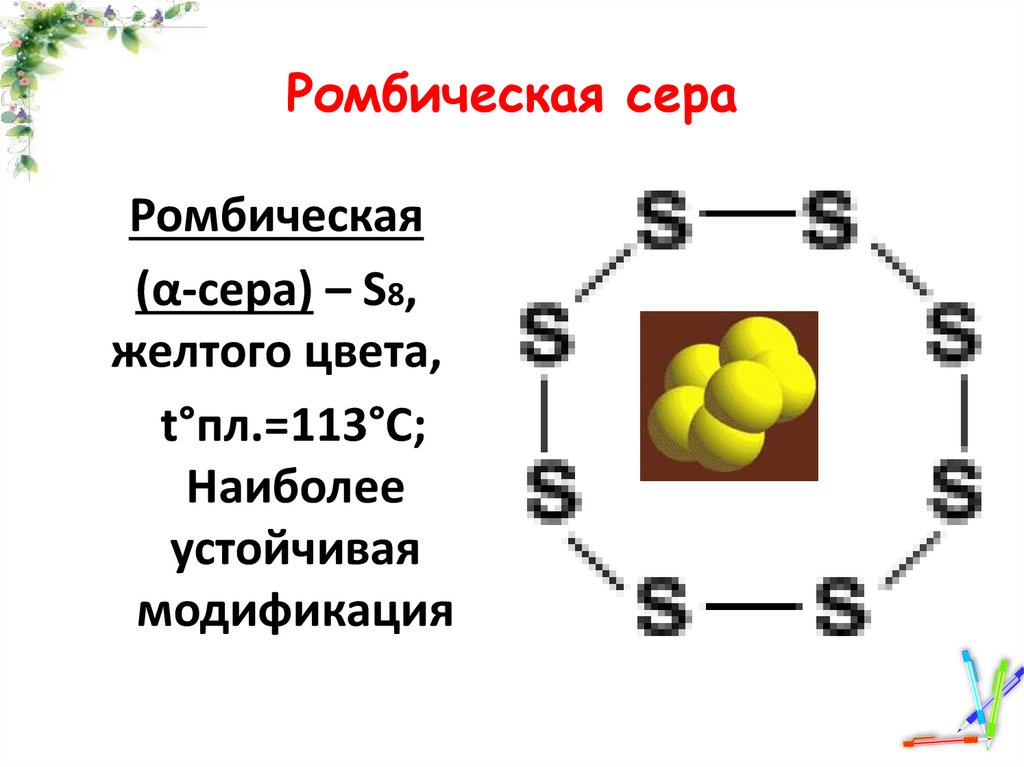
Ромбическая сераРомбическая
(α-сера) – S8,
желтого цвета,
t°пл.=113°C;
Наиболее
устойчивая
модификация
10.
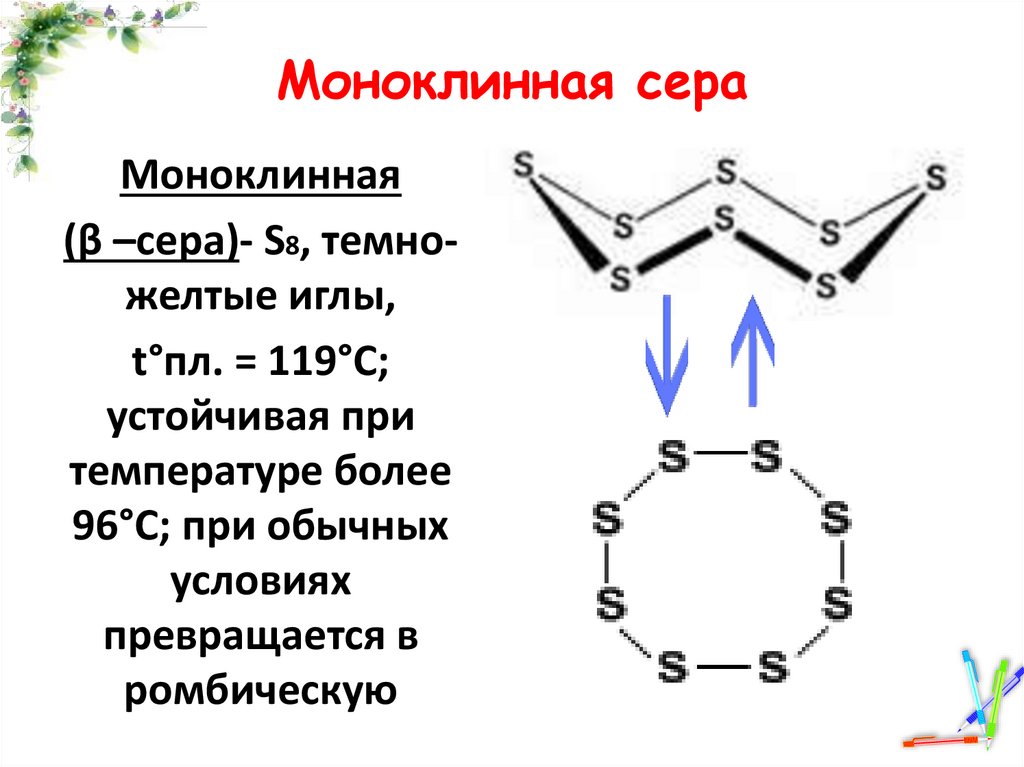
Моноклинная сераМоноклинная
(β –сера)- S8, темножелтые иглы,
t°пл. = 119°C;
устойчивая при
температуре более
96°С; при обычных
условиях
превращается в
ромбическую
11.
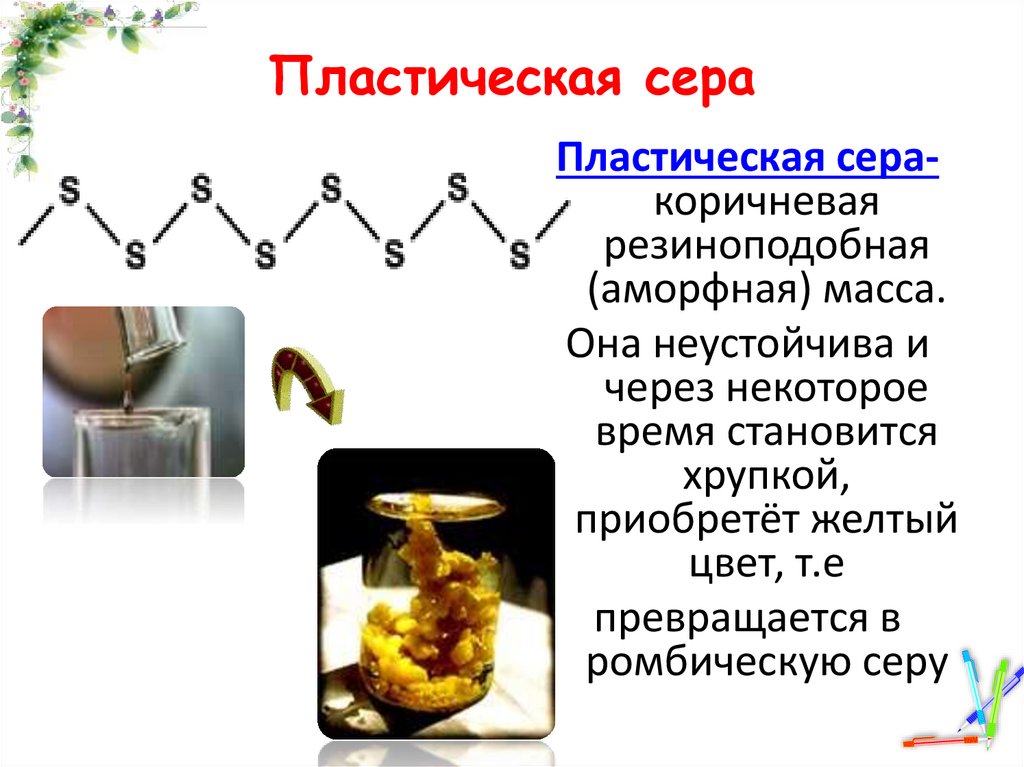
Пластическая сераПластическая серакоричневая
резиноподобная
(аморфная) масса.
Она неустойчива и
через некоторое
время становится
хрупкой,
приобретёт желтый
цвет, т.е
превращается в
ромбическую серу
12.
Серой богаты бобовые растения(горох, чечевица), овсяные хлопья, яйца
13.
Химические свойства серы(восстановительные)
Сера проявляет в реакциях с
сильными окислителями:
S - 2ē
+4
S - 4ē S ;
+6
S - 6ē S
+2
S ;
14.
Химические свойства серы(окислительные)
0
S
+ 2ē
-2
S
15.
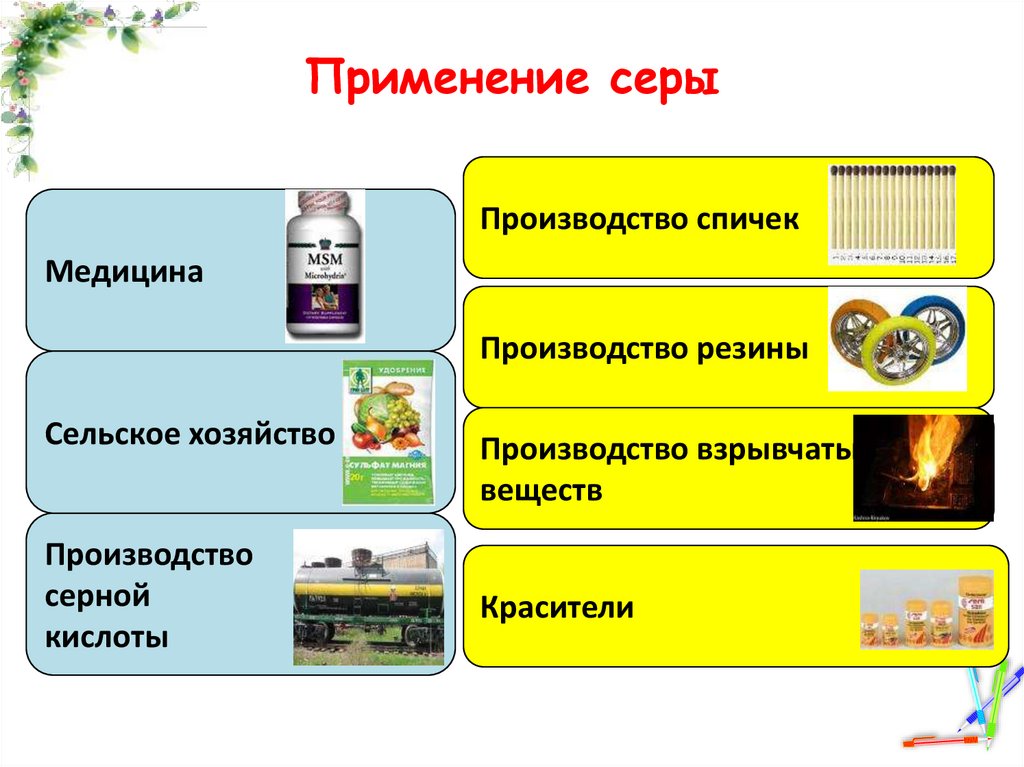
Применение серыПроизводство спичек
Медицина
Производство резины
Сельское хозяйство
Производство
серной
кислоты
Производство взрывчатых
веществ
Красители









 chemistry
chemistry








