Similar presentations:
Электролиз. Электролиз хлорида натрия
1.
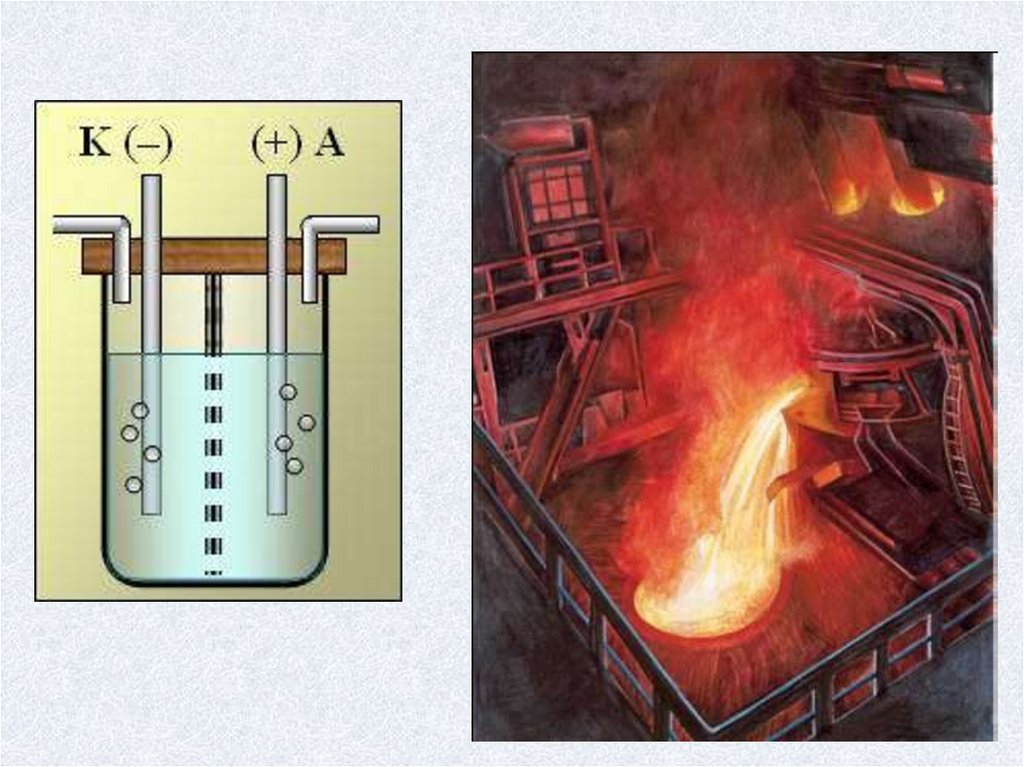
Электролиз.2.
3.
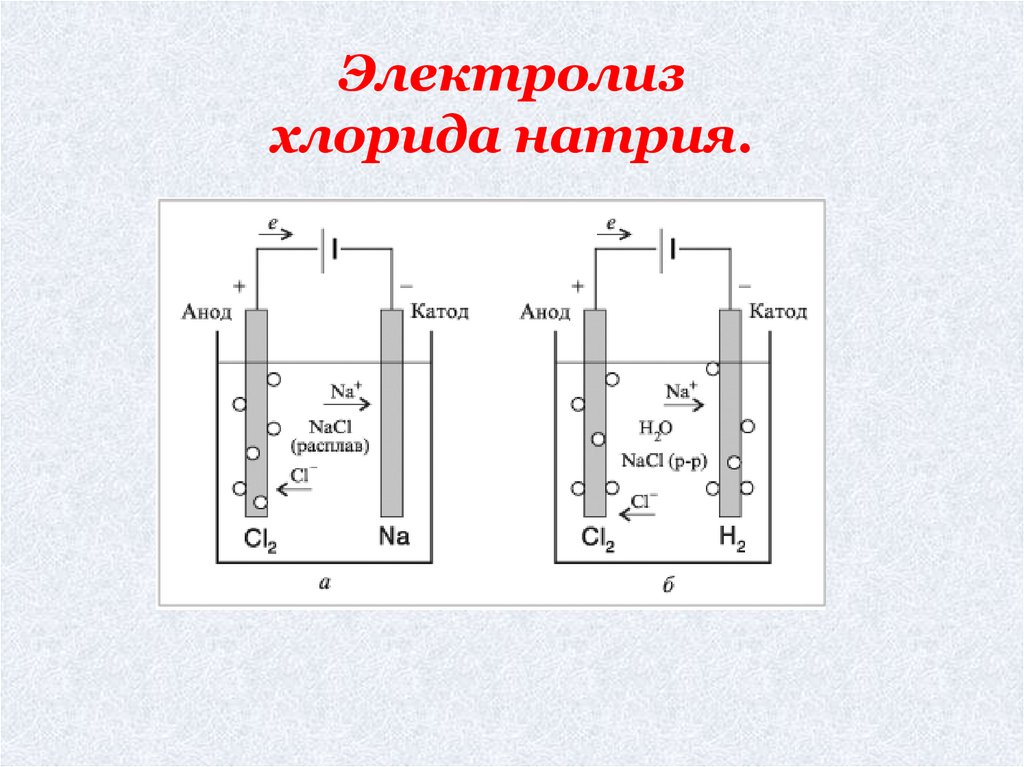
Электролизхлорида натрия.
4.
Электролиз расплавов.5.
Электролиз растворов.6.
Электролиз растворов.7.
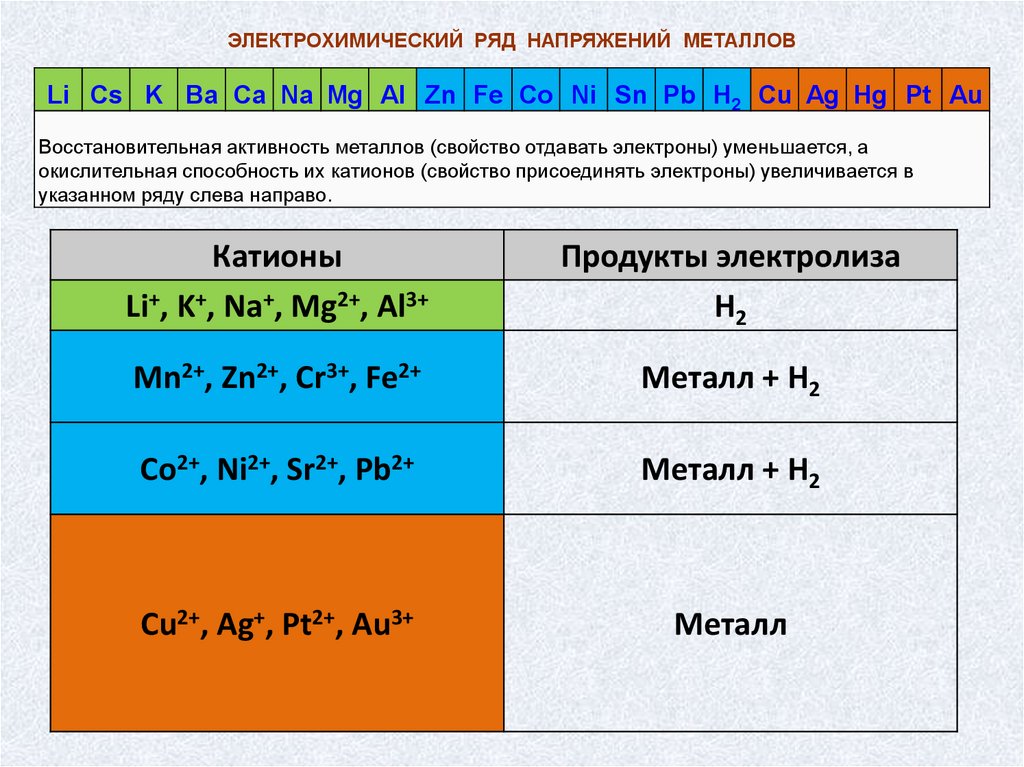
ЭЛЕКТРОХИМИЧЕСКИЙ РЯД НАПРЯЖЕНИЙ МЕТАЛЛОВLi Cs K Ba Ca Na Mg Al Zn Fe Co Ni Sn Pb H2 Cu Ag Hg Pt Au
Восстановительная активность металлов (свойство отдавать электроны) уменьшается, а
окислительная способность их катионов (свойство присоединять электроны) увеличивается в
указанном ряду слева направо.
Катионы
Li+, K+, Na+, Mg2+, Al3+
Продукты электролиза
H2
Mn2+, Zn2+, Cr3+, Fe2+
Mеталл + H2
Co2+, Ni2+, Sr2+, Pb2+
Металл + H2
Cu2+, Ag+, Pt2+, Au3+
Металл
8.
АнионыПродукты электролиза
PO43−, CO32−, SO42−, NO3−,
NO2−, ClO4−
О2
Cl−, Br−, I−, S2−
Cl2, Br2, I2, S
OH–
4OH– – 4ē = O2 +2H2O
Вода
2H2O – 4ē = O2+ 4H+
9.
Мнемоническое правилоУ анода анионы окисляются.
На катоде катионы восстанавливаются.
В первой строке все слова начинаются с
гласной буквы, во второй — с согласной.
Или проще:
КАТод — КАТионы (ионы у катода)
АНод — АНионы (ионы у анода)






 chemistry
chemistry








