Similar presentations:
Первый закон термодинамики. Необратимость тепловых процессов в природе
1.
Вот такая история…2.
Повторим:1. Что такое внутренняя энергия?
2. От чего зависит внутренняя энергия идеального газа?
3. Как вычислить внутреннюю энергию идеального газа?
4. Какими способами можно изменить
внутреннюю энергию?
5. Как вычислить количество теплоты,
сообщаемое телу?
6. Как вычислить работу, совершаемую
внешними силами над газом?
7. А работу, совершаемую газом?
Вспомним:
Как формулируется закон сохранения энергии?
3.
Можно ли применить закон сохраненияэнергии к тепловым процессам?
Может ли внутренняя энергия одновременно
изменяться за счет совершения работы и за
счет передачи теплоты?
На эти вопросы отвечает…
первый закон термодинамики
4.
Тема урока:Первый закон термодинамики.
Необратимость тепловых процессов в
природе
5.
Цели урока:- Выяснить, в чем заключается 1 закон термодинамики,
каков его смысл;
- Выяснить, в чем состоит особенность тепловых
процессов в природе;
- Научиться использовать приобретенные знания и
умения в практических жизненных ситуациях.
6.
Ерюткин Евгений СергеевичОтветьте на вопросы:
1.
2.
3.
4.
5.
Какими способами можно изменить внутреннюю энергию?
В чем заключается смысл 1 закона термодинамики?
Сформулируйте 1 закон термодинамики:
Как формулируется 1 закон термодинамики для тепловых процессов?
Что можно сказать о механической энергии термодинамической
системы?
6. Что такое вечный двигатель?
7. Почему нельзя создать вечный двигатель?
8. В чем состоит необратимость тепловых процессов?
9. В чем заключается 2 закон термодинамики?
10. Каков смысл 2 закона термодинамики?
7.
Итак, самое главное…8.
Отвечаем на вопросы:1.Какими способами одновременно можно изменить внутреннюю энергию?
2.В чем заключается смысл 1 закона термодинамики?
3.Запишите формулу 1 закона термодинамики:
4.Как формулируется 1 закон термодинамики для тепловых процессов?
5.Что можно сказать о механической энергии термодинамической системы?
9.
6.Что такое вечный двигатель?7.Почему нельзя создать вечный двигатель?
8.В чем состоит необратимость тепловых процессов?
9.В чем заключается 2 закон термодинамики?
10.Каков смысл 2 закона термодинамики?
10.
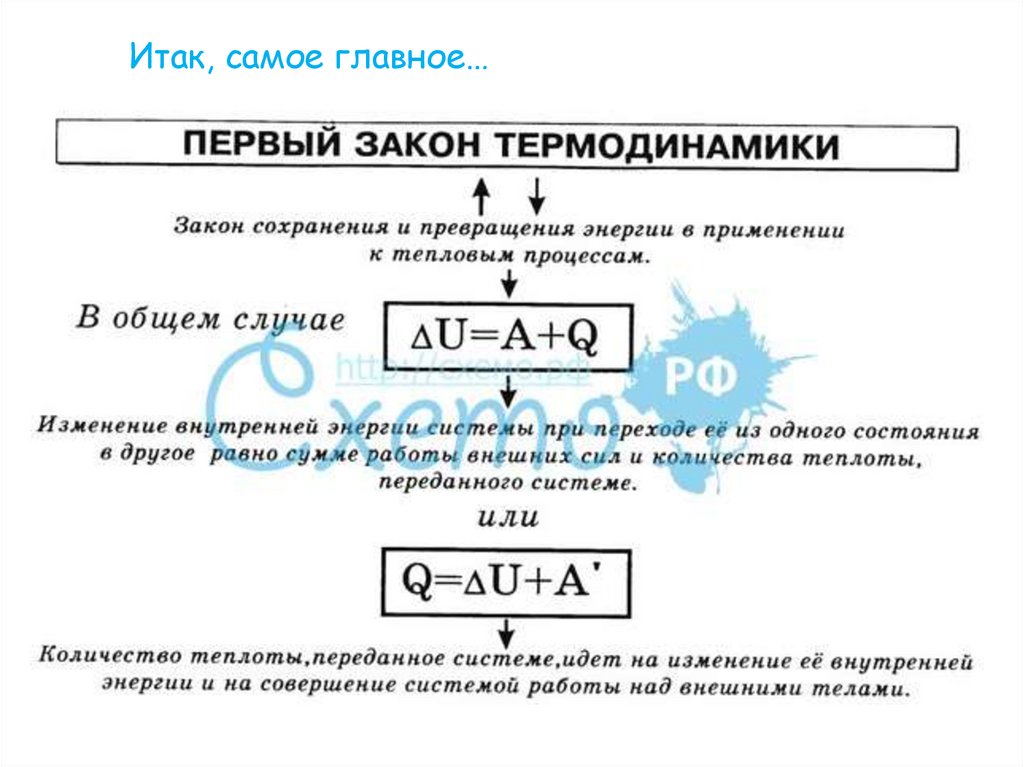
Тренировочные задания1.Примените первый закон термодинамики для
данного процесса:
A
ΔU=?
Q
11.
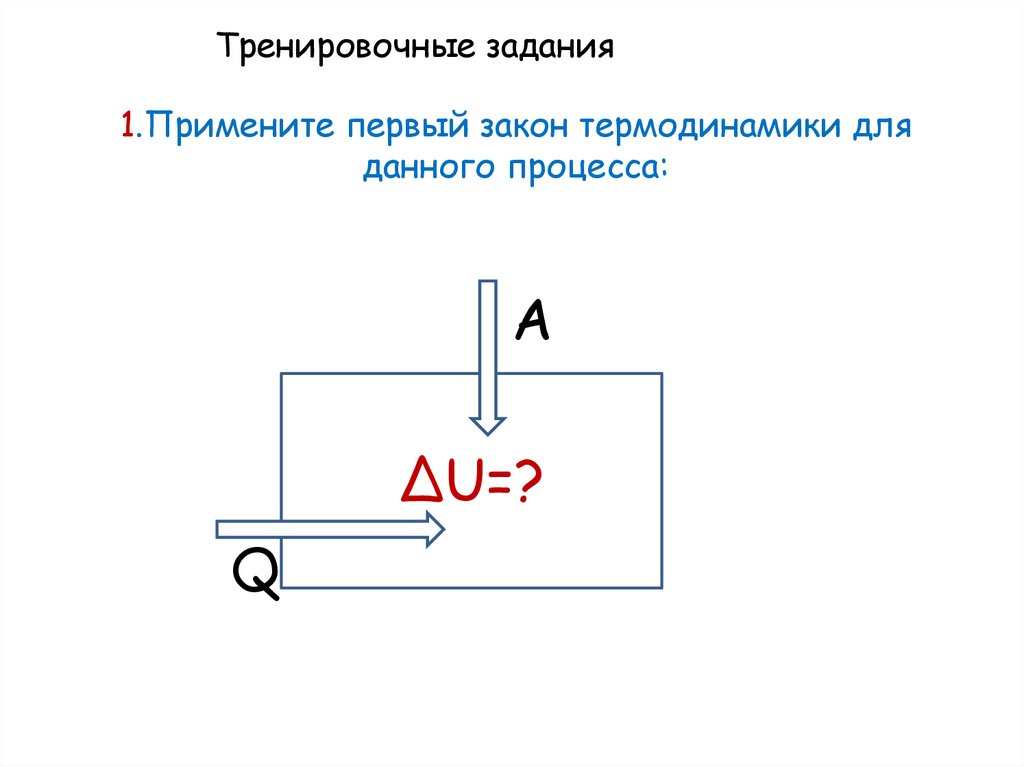
Тренировочные задания2.Примените первый закон термодинамики для
данного процесса:
A’
ΔU=?
Q
12.
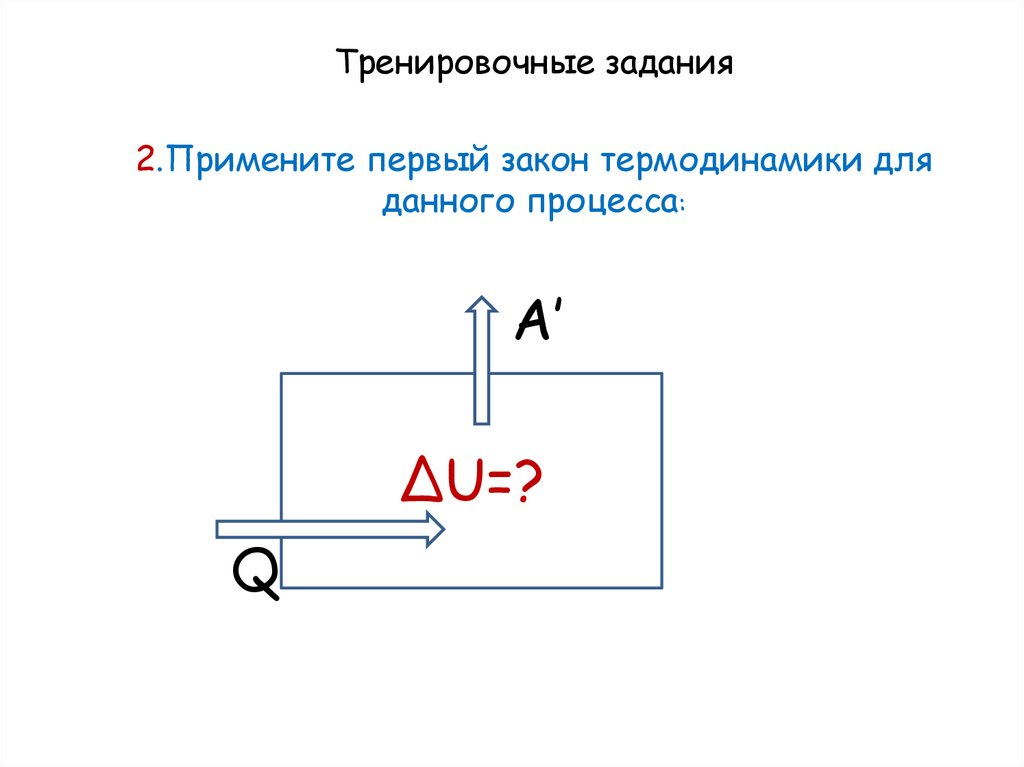
Тренировочные задания3.Примените первый закон термодинамики для
данного процесса:
ΔU=?
Q
13.
Тренировочные задания4.Подумайте:
При передаче газу количества теплоты 17
кДж он совершает работу, равную 50 кДж.
Чему равно изменение внутренней энергии
газа?
Охладился газ или нагрелся?
14.
Тренировочные задания5.Подумайте:
Можно ли применить первый закон
термодинамики для системы «человек»?
Как?
15. 6.Логические цепочки. Возможно ли течение процесса в обратную сторону?
Тренировочные задания6.Логические цепочки.
Возможно ли течение процесса в обратную
сторону?
• Младенец- дошкольник -школьникюноша -взрослый человек – старик?
• Яйцо- цыпленок-курица?
Как можно назвать эти процессы?
16. Домашнее задание
§ 78, 80, 81, вопросы, упр.15 (2)Дополнительно:
§ 79
По желанию: подготовить сообщение:
«История открытия 1 закона термодинамики»
17.
Тест1. Идеальный газ получил количество теплоты,
равное 300 Дж, и совершил работу, равную 100 Дж.
Как изменилась внутренняя энергия газа?
А. увеличилась на 400 Дж
Б. увеличилась на 200 Дж
В. уменьшилась на 400 Дж
Г. уменьшилась на 200 Дж
2. Идеальный газ совершил работу, равную 100 Дж, и
отдал количество теплоты, равное 300 Дж. Как при
этом изменилась внутренняя энергия?
А. увеличилась на 400 Дж
Б. увеличилась на 200 Дж
В. уменьшилась на 400 Дж
Г. уменьшилась на 200 Дж
18.
3. Идеальный газ совершил работу, равную 300 Дж.При этом внутренняя энергия уменьшилась на 300
Дж. Каково значение количества теплоты в этом
процессе?
А. отдал 600 Дж
Б. отдал 300 Дж
В. получил 300 Дж
Г. не отдавал и не получал теплоты.
4. Идеальный газ совершил работу, равную 300 Дж.
При этом его внутренняя энергия увеличилась на 300
Дж. В этом процессе газ
А. отдал 600 Дж
Б. отдал 300 Дж
В. получил 600 Дж
Г. получил 300 Дж
19.
Проверь себяОтветы
и
комментарии к ним
1. Б
ΔU =Q - A΄ = 300Дж – 100Дж = 200Дж
2. В
ΔU = -Q - A΄= – 100Дж - 300Дж = - 400Дж
3. Г
ΔU = A΄= 300 Дж; Q = 0
4. В
Q = Δ U + A‘= 300Дж + 300Дж = 600Дж
Критерии оценивания:
4 задачи –“5”
3 задачи –“4”
2 задачи –“3”
20.
Итоги урока- Выяснили, в чем заключается 1 закон термодинамики,
каков его смысл (это закон сохранения энергии для
тепловых процессов)
- Выяснили, в чем состоит особенность тепловых
процессов в природе (тепло самопроизвольно может
передаваться только от горячих тел к холодным)
- Учились использовать приобретенные знания и
умения в практических жизненных ситуациях.
21.
Вспомним начало урока…Закон сохранения энергии универсален,
т.е. этот закон распространяется не только
на механические, тепловые и другие
физические процессы.
Он справедлив и для химических явлений
и процессов, биологических и даже для
общественных.
«Из ничего не творится ничего»
Лукреций Кар, «О природе вещей»

















 physics
physics








