Similar presentations:
Энергия ионов в мембране и водных растворах
1.
Энергия ионов в мембране и водных растворахЭлектрохимический потенциал – показатель энергии иона
0 RT ln c zF
μ0 – взаимодействия иона с р-рителем.
Отсутствие связей – высокая энергия
масло
ε =2
I – в грубом масштабе (вода−неполярный р-ритель)
II – краевые эффекты (взаимодействия)
III – понижение барьера из-за малой толщины h
IV – связывание ионов с фикс. зарядами
1
2.
Энергия иона в мембране и водных растворахНизкая проницаемость БЛМ для ионов обусловлена высоким энергетическим барьером
μ0 – отражает взаимодействия иона со средой.
Недостаток эл-стат связей повышает энергию
Единицы
измерения
Ф/м ∙ В2/м2 ∙м3 = Ф∙В2 = Кл∙В = Дж
Проверка ф-лы максвеллова напряжения в случае плоского конденсатора:
E dV E V
2
2
В случае одного иона
в непрерывной среде
S
2
W
h
E
0 2 S
2h
C 2
2
F
ze
e 4 0 R 2
2
3.
Элемент объема - тонкий слой толщиной dR на поверхности сферы радиусом RdV 4 R 2 dR
Интегрируем от
Подставляем E2 и dV в исходную ф-лу
R r
до
R
П
.о
Ур-ие Борна
r – радиус иона, εo =
8.85∙10–12 Ф/м
z 2 e2 1 1
W
8 0 r 2 1
Упражнение: Рассчитать высоту энергетич. барьера для переноса одновалентного иона
радиусом 0.1 нм из воды (ε = 80) в неполярную фазу с ε = 3. Выразить энергию в
расчете на 1 моль ионов.
3
4.
Физические механизмы действия ионофоров: переносчикиВысота энерг. барьера (на один ион)
ΔW ≡ E* =
Переносчики: валиномицин – нейтр. переносчик К+, депсипептид (валин и орг к-ты)
Заряд комплекса – такой же как у K+, но размер больше.
Na+ обладает меньшим размером, меньше связей, выше E*
(малое число связей – меньше эфф. значение εc).
В системе СГС (отличие в ф-лах на 4πε0):
b
εk-ε комплексона
εk
εm
Здесь учтено, что ион находится в среде
(комплексоне) радиусом b, а весь комплекс
радиусом b находится в сплошной среде
(мембране) с диэл постоянной εm.
4
5.
Подвижные переносчики: валиномицин, динотрофенолХарактерное время диффузии
(случай одномерной диффузии)
K +V
K+
K+
2
x 2 Dt
V
Скорость транспорта
лимитируется диффузией
Упражнение: Рассчитать количество ионов, переносимых переносчиком через липидный
бислой толщиной h = 4 нм в предположении, что коэф. диффузии ионофора в мембране
составляет D = 10−8 см2/с
Др. переносчики: нигерицин (Н+/K+), моненсин (Na+/H+), А23187 (Са2+/2H+).
Индуцируют электронейтр. обмен, но есть минорные заряженные комплексы.
Липофильные слабые к-ты (2,4-динитрофенол, FCCP) – перенос H+ в незаряженной форме
AH
Н+
H+
A−
5
6.
Физические механизмы действия ионофоров: каналыz 2 e2 1 1
E*
8 0 r m w
Грамицидин А: пептид из 15 аминок-т
Канал обеспечивает замену
низкой εm на высокую εp (ε поры)
В канале ион взаимодействует с
полярными группами (энергия ↓)
3.2 нм
Длина димера ~ длины гидрофобной зоны
У ковалентно связанных димеров – время открытого
состояния составляет ~10 c (в норме 0.2 с)
Токи одиночных каналов грамицидина А.
При конц-иях ~ 10-12 M ( ср. микропипетки)
Разные типы димеров
(одно и двухтяжевые)
Фотоинактивация ГрА каналов
6
7.
Ионные равновесия. Электрохим равновесие между водными р-рами.Равновесный потенциал, ур-ие Нернста
0 RT ln c zF
μo – одинаковы в обоих растворах (вода)
in out o
Для K+
Для Na+
RT co
RT co
ln 2.3
lg
zF ci
zF ci
cout/сin = 1/100
cout/сin = 10/1
φK ≈ -120 мВ
φNa ≈ +60 мВ
1 2
Ур-ие Нернста
φK и φNa ограничивают
диапазон изменений φm при
условии незначительной
роли электрогенного насоса.
потенциал
φNa
После преобразования:
zF
ci c0 exp(
)
RT
0
φK
время
Ур-ие Больцмана
7
8.
Ионные равновесия. Электрохим равновесие между водными р-рами.Равновесный потенциал, ур-ие Нернста
0 RT ln c zF
μo – одинаковы в обоих растворах (вода)
in out o
Для K+
Для Na+
RT co
RT co
ln 2.3
lg
zF ci
zF ci
cout/сin = 1/100
cout/сin = 10/1
φK ≈ -120 мВ
φNa ≈ +60 мВ
1 2
Ур-ие Нернста
φK и φNa ограничивают
диапазон изменений φm при
условии незначительной
роли электрогенного насоса.
потенциал
φNa
После преобразования:
zF
ci c0 exp(
)
RT
0
φK
время
Ур-ие Больцмана
8
9.
Доннановское равновесие- Непроникающие ионы (катионы с суммарным зарядом Q)
-Свободно проникающие катионы
-Свободно проникающие анионы
Q
В объеме чистого р-ра конц-ии с+
и с−
одинаковы: с+ = с− = с.
В доннановской фазе число анионов превышает число свободных катионов.
Из записи ур-ия Нернста для малых катионов и анионов, приравняв φ,
получаем с+·с−
= с 2.
Условие электронейтральности для доннановской фазы:
c+ + Q = c−. Отсюда получаем с+ ·(с+ + Q) = c2
Q
Q2
2
c c
2
4
Частные случаи: Q<<c+ и Q>>c+
См. учебник Биофизика т. 2. (но есть
типографские ошибки в отдельных ф-лах).
Конц-ия в доннановской фазе
9
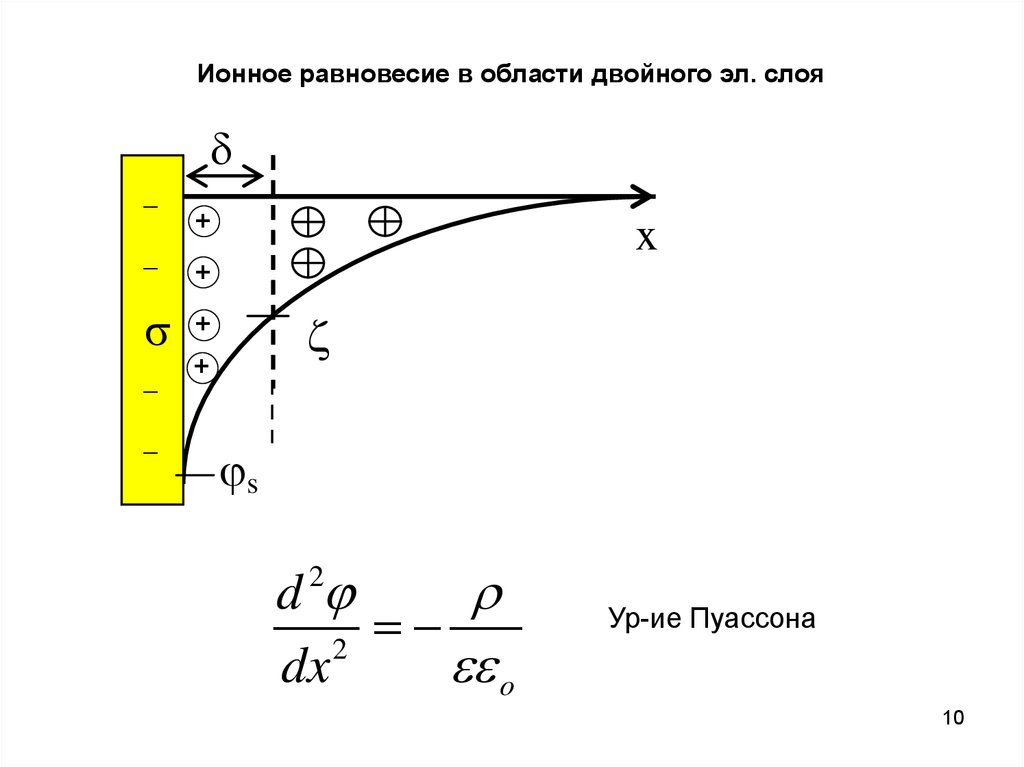
10.
Ионное равновесие в области двойного эл. слоя+
+
+
+
x
s
v
d
2
dx
o
E
2
Ур-ие Пуассона
10
11.
Поверхностный потенциалd 2
2
dx
o
ρ = zF (c+ – c–)
Ур-ие Пуассона [В/м2] – распределение φ
плотность зарядов [Кл/м3] на расстоянии х;
z – абс значение z: 1, 2
zF
cx c0 exp(
)
RT
Распределение
Больцмана
d 2
zF
zF
zF
) co exp(
)
co exp(
2
dx
o
RT
RT
Ур-ие Пуассона −Больцмана
11
12.
При малых х:e x 1 x;
e x 1 x
Ур-ие Пуассона-Больмана упрощается до ур-ия Дебая
d 2z F c0
2
dx
RT 0
2
2
Решение:
2
d 2
2
2
dx
φ = φo exp(–x/λ),
1
RT o
2 z 2 F 2co
Длина экранирования,
дебаевская длина
Упражнение: Рассчитать толщину дебаевского слоя возле мембраны
в 0.1 М растворе KCl и в дистиллированной воде
12
13.
φРазность поверхностных потенциалов создает эл поле в мембране:
как её обнаружить?
Решение ур-ия Дебая говорит о том, как меняется
потенциал с расстоянием, позволяет рассчитать λ,
но не говорит о величине φs.
Потенциодинамические кривые тока:
х
Профиль эл потенциала
при разных конц-иях с в
растворах с двух сторон
В отсутствии внутримембранного поля
минимум тока при φ=0 (нет электрострикции)
При наличии внутримембранного поля
минимум тока сдвинут по отношению к φ=0
(минимум тока при компенсации внешнего и
внутреннего эл поля).
ток
ток
φ
φ
Время
13












 chemistry
chemistry








