Similar presentations:
Молекулярный уровень организации жизни
1. Молекулярный уровень организации жизни
МОУ Лицей № 1302005г
Молекулярный уровень
организации жизни
2. Основные органические вещества в клетке
• Белки (состоят из аминокислот)• Полисахариды (состоят из
моносахаридов)
• Липиды (состоят из глицерина и жирных
кислот)
• Нуклеиновые кислоты (состоят из
нуклеотидов)
• АТФ
• Витамины
3. Понятие биополимера
Биополимер – молекула органическоговещества, имеющая вид цепочки,
состоящей из много численных звеньев
Мономер – звено биополимера
Регулярный полимер
Нерегулярный полимер
4. Белки – полимеры, состоящие из аминокислот
В состав белков входит 20 аминокислот.Среди них 9 незаменимых и 11 заменимых.
РАДИКАЛ
АМИНОГРУППА
R
I
NH2 - CH – C = O
I
OH
КАРБОКСИЛЬНАЯ
ГРУППА
5. Аминокислоты отличаются строением радикалов
Структурные формулы некоторыхаминокислот
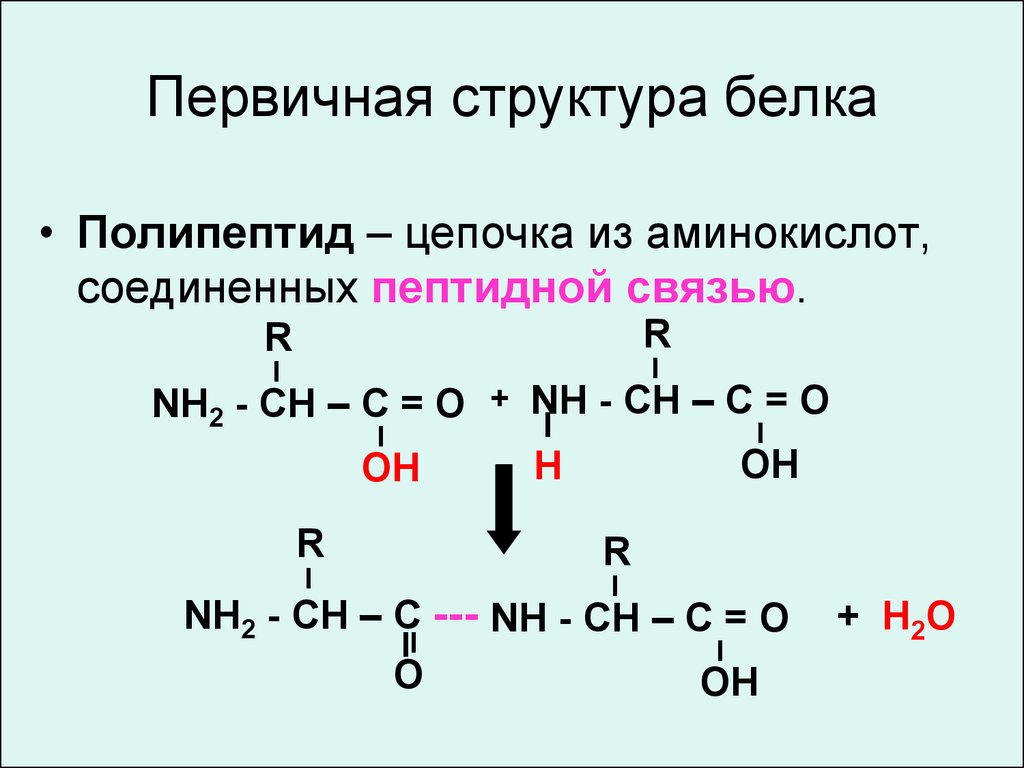
6. Первичная структура белка
• Полипептид – цепочка из аминокислот,соединенных пептидной связью.
R
R
I
I
NH2 - CH – C = O + NH - CH – C = O
I
OH
R
I
I
I
OH
H
R
I
NH2 - CH – C --- NH - CH – C = O
II
I
O
OH
+ H2O
7. Полипептид
Полипептид имеет С-конец и N-конецДлина среднего полипептида – 500 а.к.
ПЕПТИДНАЯ СВЯЗЬ
С-конец
АМИНОКИСЛОТЫ
N-конец
8. Вторичная структура белка
Полипептид закручивается вспираль.
Структура образуется за
счет водородных связей
между С=О группами и NH
группами разных
аминокислот
ВОДОРОДНЫЕ
СВЯЗИ
9. Третичная структура белка
Спираль закручивается вглобулу.
Структура образуется за счет
взаимодействия радикалов
разных аминокислот.
При этом гидрофобные
радикалы оказываются
внутри, а гидрофильные –
снаружи.
10. Четвертичная структура белка
Несколько третичных структуробъединяются за счет взаимодействия
гидрофильных радикалов.
Четвертичная структура характерна не для всех
белков
Гемоглобин – белок,
имеющий IV структуру
(сложный). Его белковая
часть ГЛОБИН состоит из
четырех глобул
11. Свойства белков
1. Денатурация2. Ренатурация
3. При to 90-100oC
происходит
необратимая
денатурация.
12. Функции белков
Функция белковСтруктурная
Каталитическая
Транспортная
Регуляторная
Сократительная
Запасающая
Защитная
Энергетическая
Пример белка
Кератин
Каталаза, Амилаза
Гемоглобин
Инсулин
Актин, Миозин
Альбумин, Ферритин
Антитела, Фибриноген
1г любого белка =17,6 кДж
13. Углеводы (сахара)
Основные углеводыв клетке
Простые
Сложные
(моносахариды)
(состоят из простых)
Пентозы
•Рибоза
•Дезоксирибоза
Гексозы
Дисахариды
•Глюкоза
•Фруктоза
•Галактоза
•Сахароза
•Лактоза
•Мальтоза
Полисахариды
•Крахмал
•Гликоген
•Целлюлоза
•Хитин
14. Свойства углеводов
1.2.
3.
Чем короче углевод,
тем он лучше
растворим в воде и
тем слаще его вкус.
При охлаждении
полисахариды
расщепляются до
моносахаридов.
При взаимодействии
крахмала с йодом
возникает синий цвет
Крахмал –
безвкусный,
нерастворим
Глюкоза –
сладкая,
растворима
Гликоген– безвкусный, нерастворим
15. Функции углеводов
1. Структурнаяцеллюлоза, хитин, рибоза, дезоксирибоза
2. Запасающая
крахмал, гликоген
3. Энергетическая 1г углеводов=17,6КДж
Глюкоза, сахароза=глюкоза+глюкоза,
лактоза=молочный сахар, мальтоза
4. Защитная
16. Липиды – органические вещества, нерастворимые в воде
Структура жира
Полярные
головки
Неполярные
хвосты
Жиры
Масла
Воски
Фосфолипиды
Стероиды
(холестерин,
тестостерон,эстраген,
витамины А,Д,Е,К)
В воде фосфолипиды
образуют бислой
17.
Свойства липидовФункции липидов
В водной среде
фосфолипиды образуют
бислой
Структурная
Фосфолипиды обр.
клеточные мембраны
Водоотталкивающая
Жиры обр.
водоотталкивающий слой
на коже и перьях
Теплоизоляционная
Защитная
Нерастворимы в воде
Низкая теплопроводность
Высокая энегоемкость
Энергетическая
1г жира=38,9КДж
Регуляторная
Витамины, гормоны
Запасающая
18. Нуклеиновые кислоты – полимеры, состоящие из нуклеотидов
Строение нуклеотидаОН
ФОСФАТ
I
О=Р-ОН
I
О
ПЕНТОЗА
РИБОЗА ИЛИ
ДЕЗОКСИРИБОЗА
АЗОТИСТОЕ ОСНОВАНИЕ
АДЕНИН
ГУАНИН
ТИМИН
ЦИТОЗИН
УРАЦИЛ
19. Нуклеотиды соединяются фосфодиэфирными мостиками
ОНI
О=Р-ОН
I
О
О
I
О=Р-ОН
I
О
Структуру ДНК
открыли Уотсон и Крик
в 1953г
20. Строение нуклеиновых кислот
Строение ДНКСтроение РНК
Пентоза=дезоксирибоза
Пентоза=рибоза
Азотистые основания –
Азотистые основания –
А,Т,Г,Ц
А,У,Г,Ц
Фосфат и пентоза чередуются регулярно
Азотистые основания чередуются нерегулярно
Двунитчатая структуру
Однонитчатая структура
Комплементарность
_
А=Т, Г=Ц
Молекула закручивается
в двойную спираль
21. Строение ДНК
22.
Свойства ДНКФункции ДНК
Стабильность
Хранение
наследственной
информации
Способность к
самоудвоению
Передача
наследственной
информации из
поколения в поколение
Свойства РНК
Функции РНК
Лабильность
Непособность к
самоудвоению
иРНК
Участвуют в
синтезе белков
тРНК
рРНК – образует
структуру рибосом
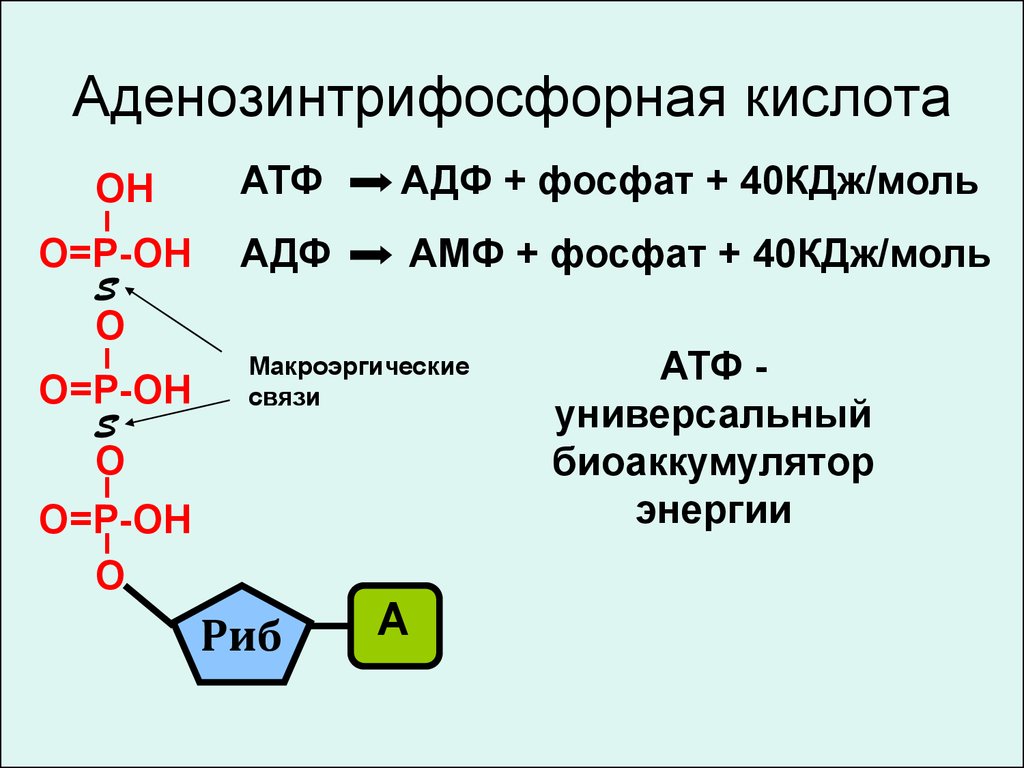
23. Аденозинтрифосфорная кислота
ОHI
О=Р-ОН
S
АТФ
АДФ + фосфат + 40КДж/моль
АДФ
АМФ + фосфат + 40КДж/моль
О
I
О=Р-ОН
S
Макроэргические
связи
О
I
О=Р-ОН
I
О
Риб
А
АТФ универсальный
биоаккумулятор
энергии
24. Ферменты – ускорители биологических реакций
Фермент – белок третичной или четвертичной структурыСубстрат
Активный центр
фермента
Продукт
Кофермент – вещество,
необходимое для работы
фермента
25. Витамины –неполимерные вещества, необходимые для жизни клетки в микроколичествах
ВодорастворимыеЖирорастворимые
В1-12, С, РР
А, Д, Е, К
Свойства: Разрушаются при температуре и на свету
Функции: Являются коферментами
























 biology
biology








