Similar presentations:
Азотсодержащие гетероциклические соединения. 10 класс
1.
Азотсодержащиегетероциклические
соединения
10 класс
профильный уровень
2.
224.04.2024
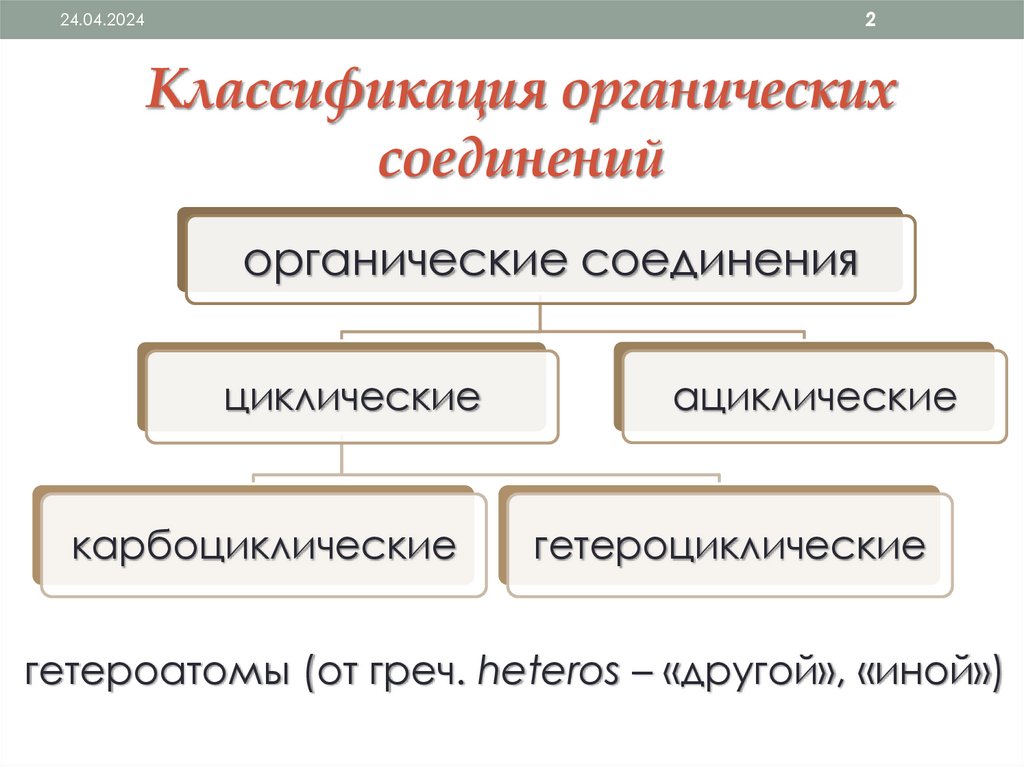
Классификация органических
соединений
органические соединения
циклические
карбоциклические
ациклические
гетероциклические
гетероатомы (от греч. heteros – «другой», «иной»)
3.
324.04.2024
Биологическое значение
гетероциклы играют важную роль в
биологических процессах, входят в состав
многих природных веществ:
1. нуклеиновых кислот;
2. хлорофилла;
3. витаминов;
4. гема крови
их используют для производства лекарств и
красителей
4.
424.04.2024
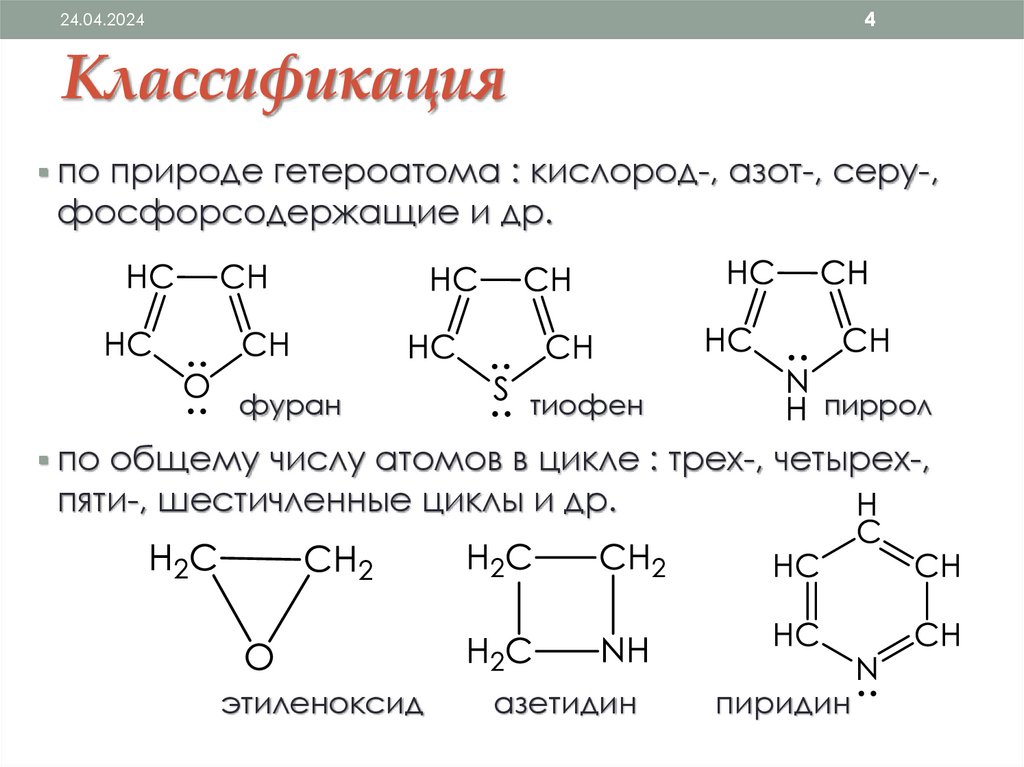
Классификация
по природе гетероатома : кислород-, азот-, серу-,
фосфорсодержащие и др.
фуран
тиофен
пиррол
по общему числу атомов в цикле : трех-, четырех-,
пяти-, шестичленные циклы и др.
этиленоксид
азетидин
пиридин
5.
524.04.2024
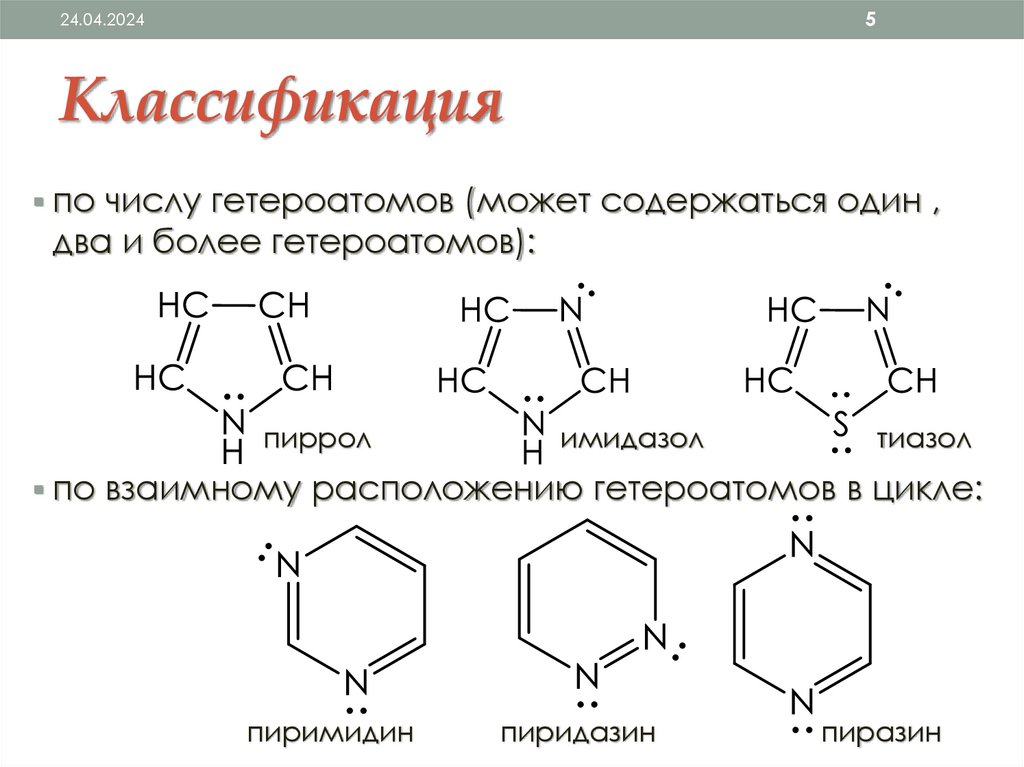
Классификация
по числу гетероатомов (может содержаться один ,
два и более гетероатомов):
пиррол
имидазол
тиазол
по взаимному расположению гетероатомов в цикле:
пиримидин
пиридазин
пиразин
6.
624.04.2024
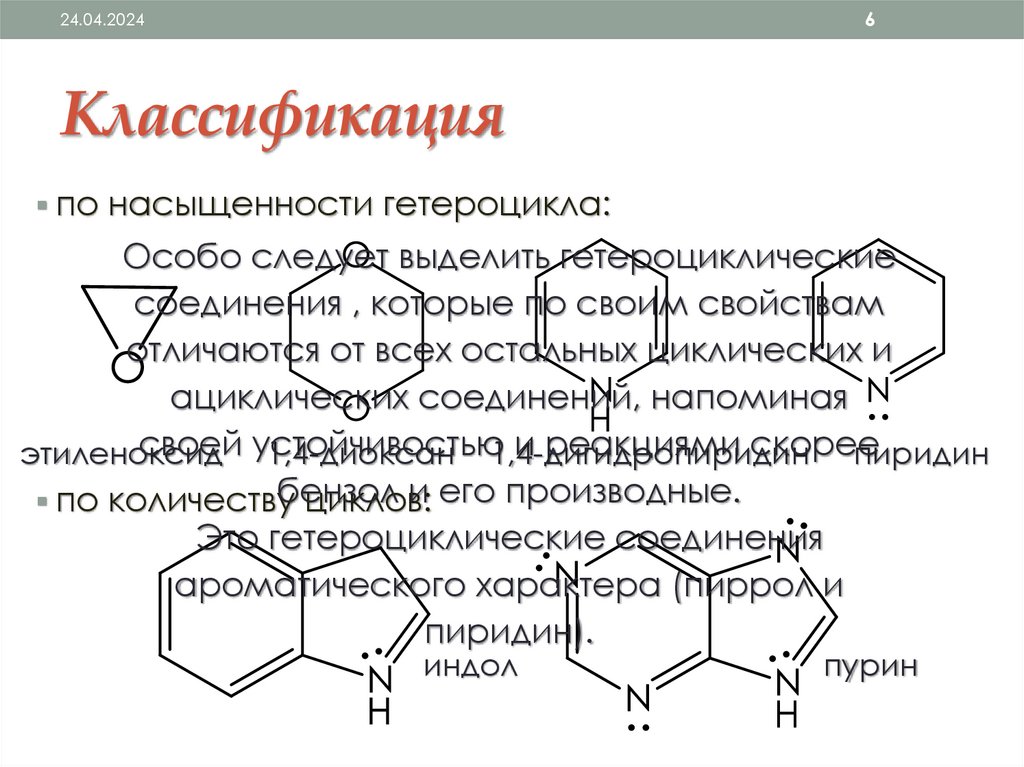
Классификация
по насыщенности гетероцикла:
Особо следует выделить гетероциклические
соединения , которые по своим свойствам
отличаются от всех остальных циклических и
ациклических соединений, напоминая
своей устойчивостью
и реакциями скорее
этиленоксид
1,4-диоксан 1,4-дигидропиридин
пиридин
бензол
и его производные.
по количеству
циклов:
Это гетероциклические соединения
ароматического характера (пиррол и
пиридин).
индол
пурин
7.
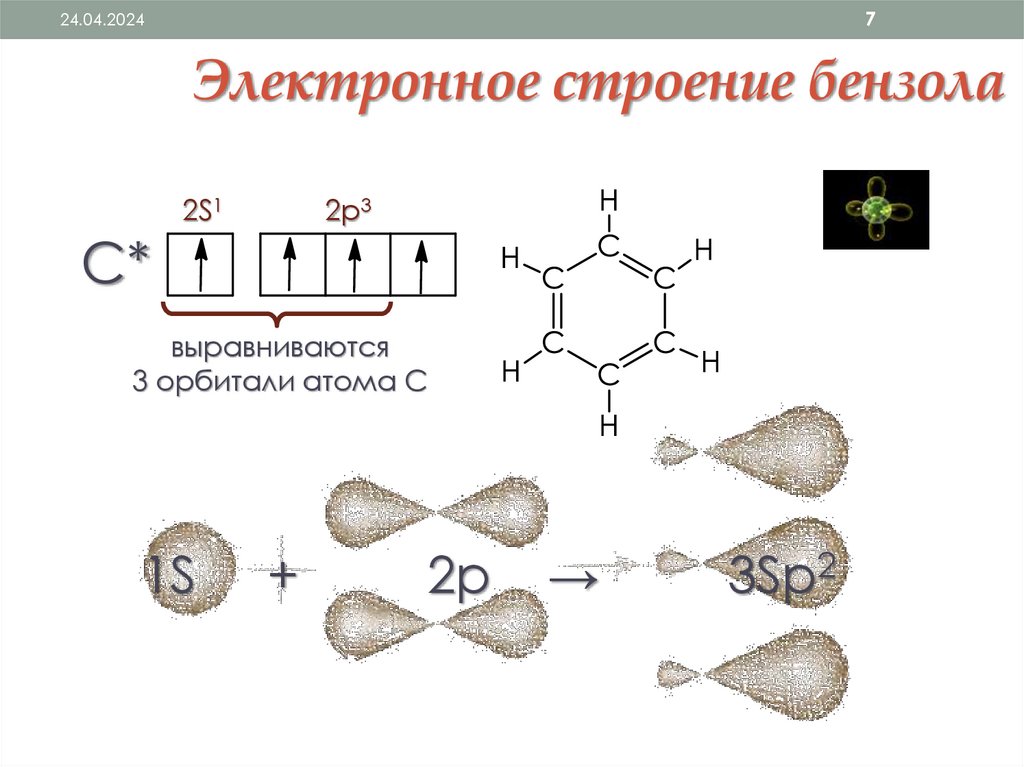
724.04.2024
Электронное строение бензола
С*
2S1
2p3
выравниваются
3 орбитали атома С
1S
+
2p
→
3Sp2
8.
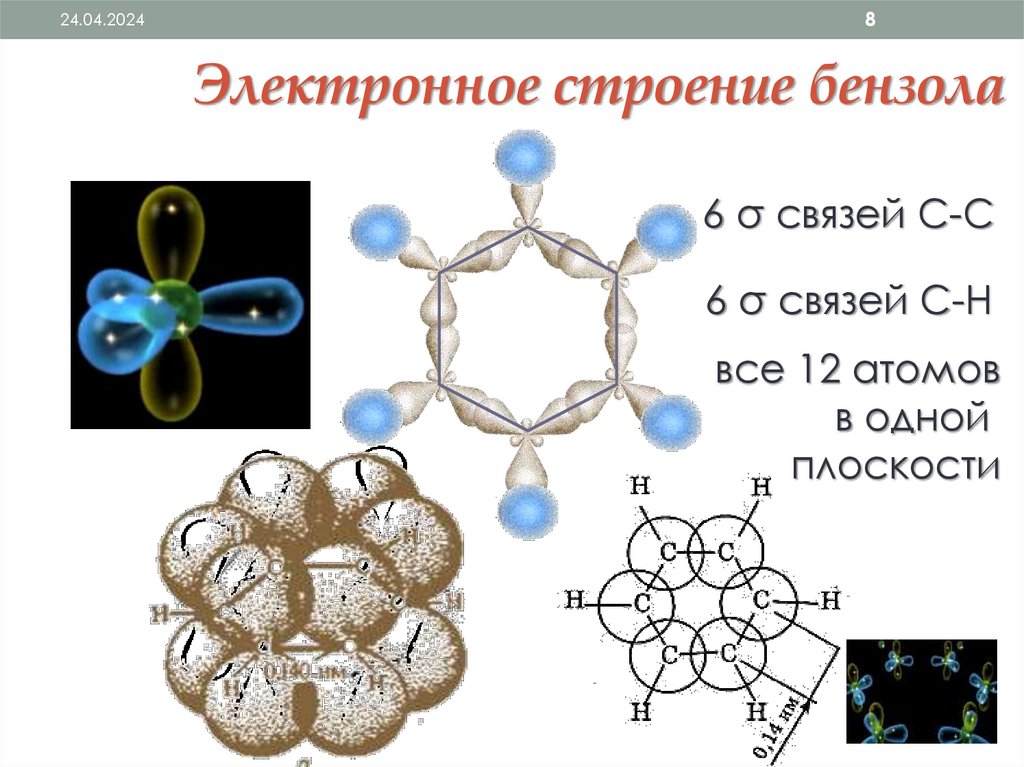
24.04.20248
Электронное строение бензола
6 σ связей С-С
6 σ связей С-Н
все 12 атомов
в одной
плоскости
9.
924.04.2024
Сравнительная характеристика
I. нахождение в природе
II. получение
III. состав и строение
IV. свойства
V. применение
10.
1024.04.2024
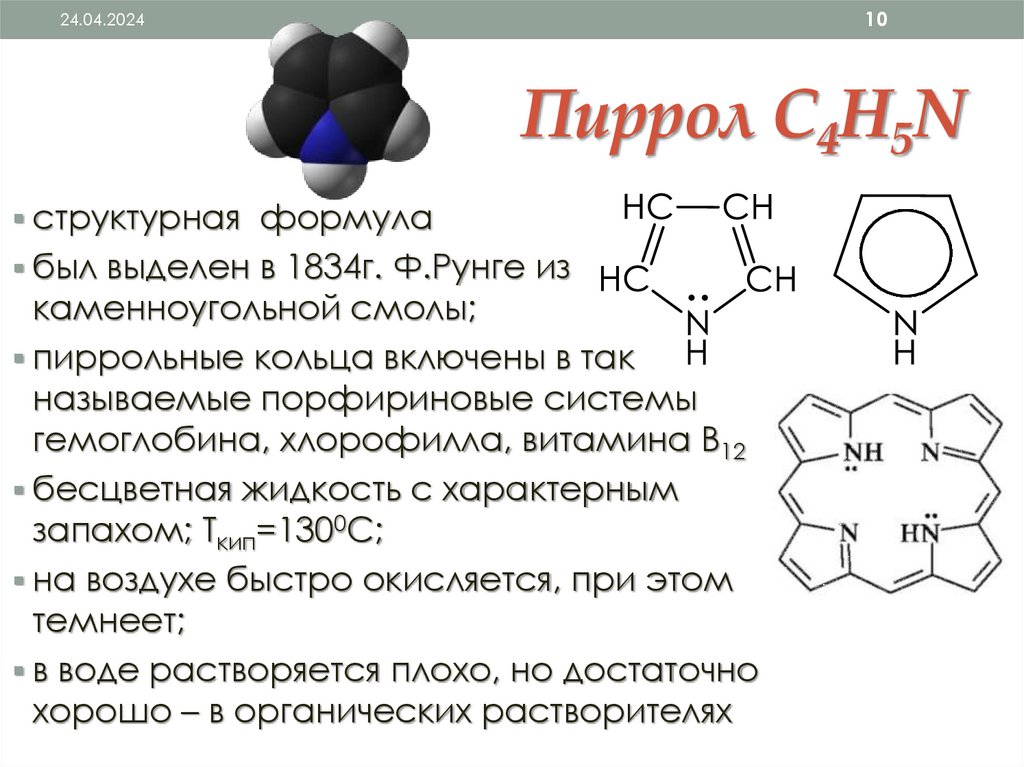
Пиррол С4Н5N
структурная формула
был выделен в 1834г. Ф.Рунге из
каменноугольной смолы;
пиррольные кольца включены в так
называемые порфириновые системы
гемоглобина, хлорофилла, витамина В12
бесцветная жидкость с характерным
запахом; Ткип=1300С;
на воздухе быстро окисляется, при этом
темнеет;
в воде растворяется плохо, но достаточно
хорошо – в органических растворителях
11.
1124.04.2024
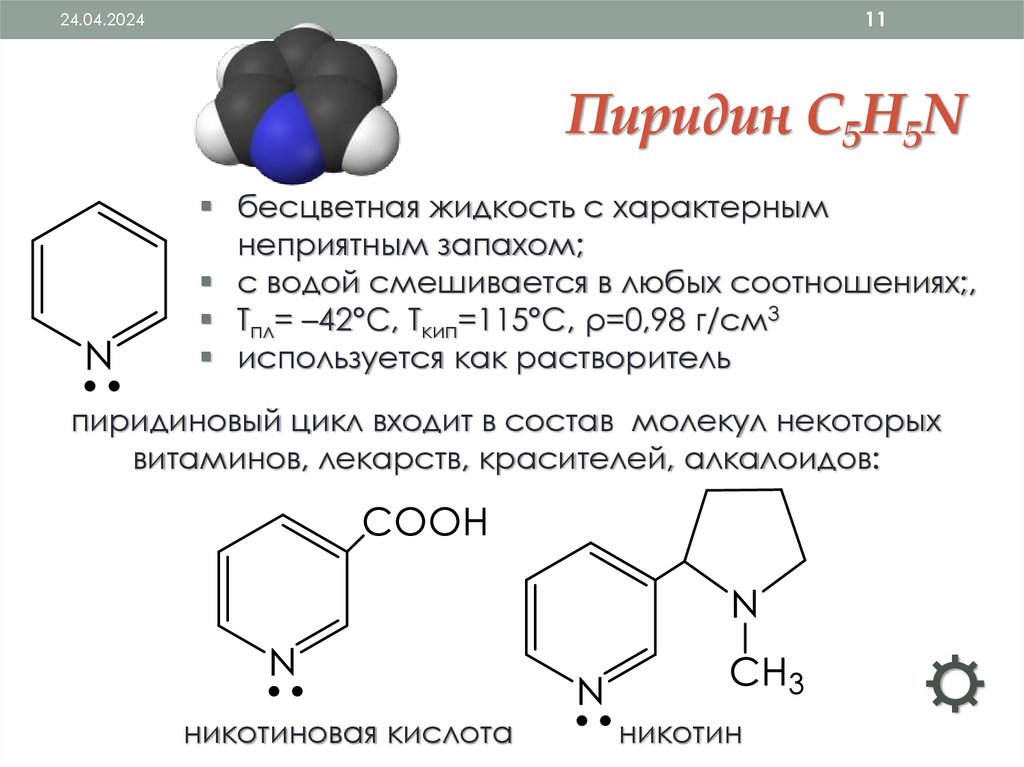
Пиридин С5Н5N
бесцветная жидкость с характерным
неприятным запахом;
с водой смешивается в любых соотношениях;,
Tпл= –42°C, Ткип=115°С, ρ=0,98 г/см3
используется как растворитель
пиридиновый цикл входит в состав молекул некоторых
витаминов, лекарств, красителей, алкалоидов:
никотиновая кислота
никотин
☼
12.
1224.04.2024
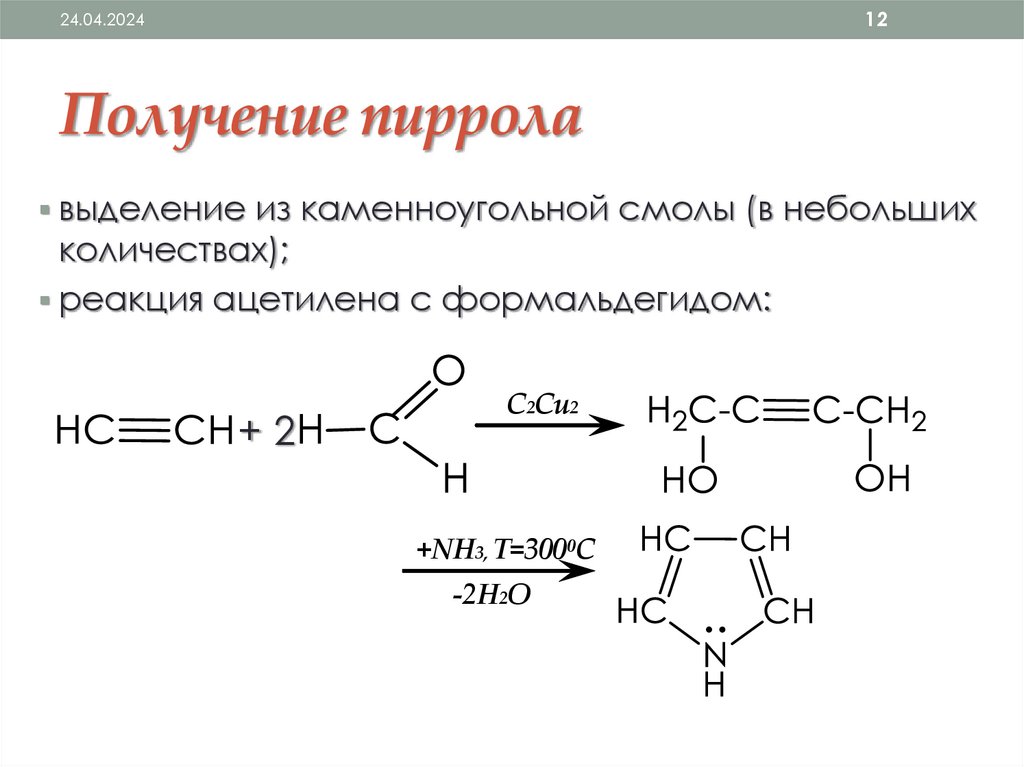
Получение пиррола
выделение из каменноугольной смолы (в небольших
количествах);
реакция ацетилена с формальдегидом:
+2
C2Cu2
+NH3, Т=3000С
-2H2O
13.
1324.04.2024
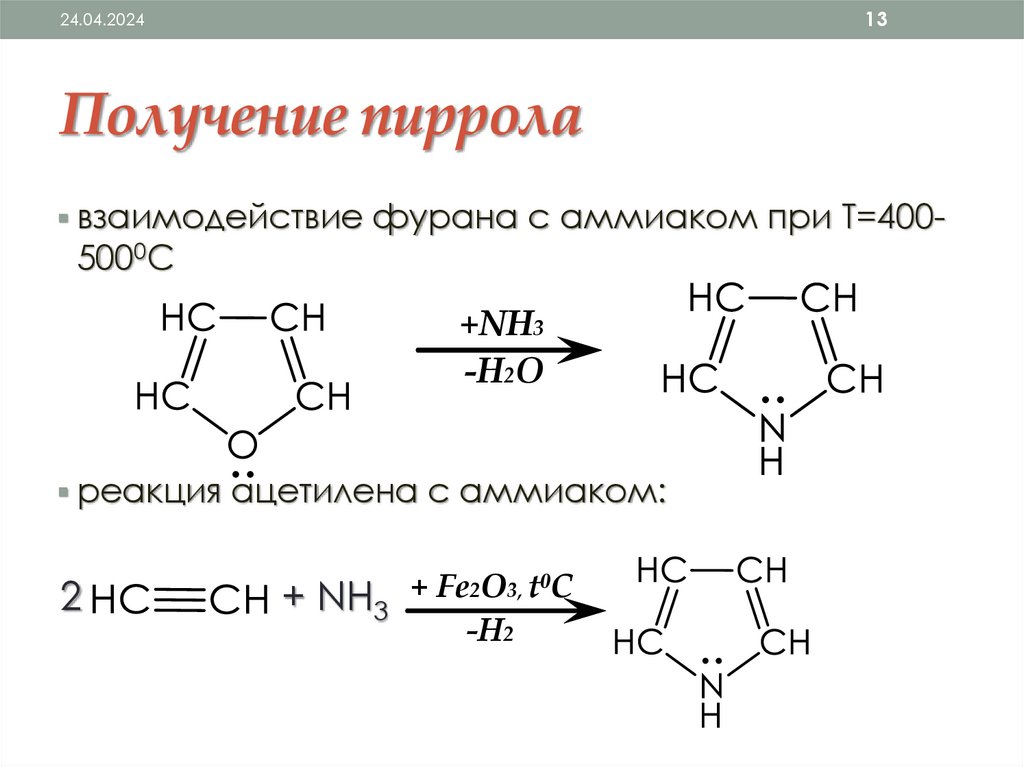
Получение пиррола
взаимодействие фурана с аммиаком при Т=400-
5000С
+NH3
-H2O
реакция ацетилена с аммиаком:
2
+
Fе
2O3, t0C
+ NH3
-H2
14.
1424.04.2024
Получение пиридина
впервые был выделен англ. химиком Т.Андерсоном в
1849г из продукта сухой перегонки костей (костный
деготь);
в 1877г англ. химик У. Рамзай предложил
лабораторный способ получения пиридина:
2CH≡CH + H-C≡N
С(графит),t0C
C5H5N
☼
15.
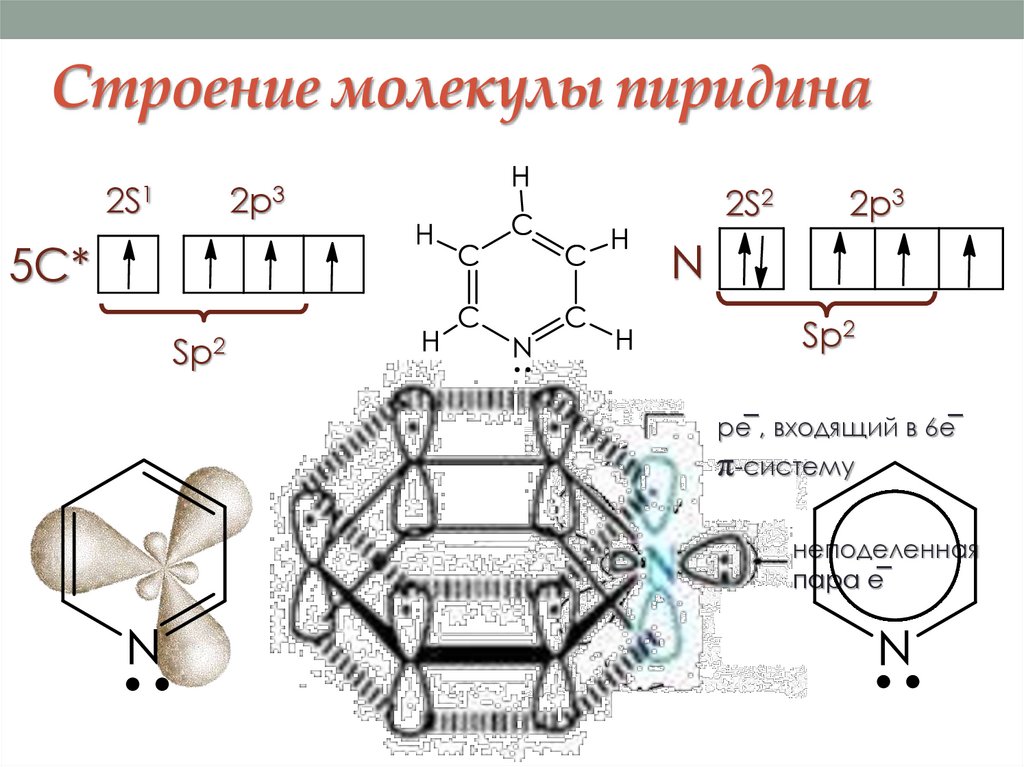
Строение молекулы пиридина2S1
2p3
2S2
2p3
N
5С*
Sp2
Sp2
рe̅ , входящий в 6e̅
π-систему
неподеленная
пара e̅
24.04.2024
15
16.
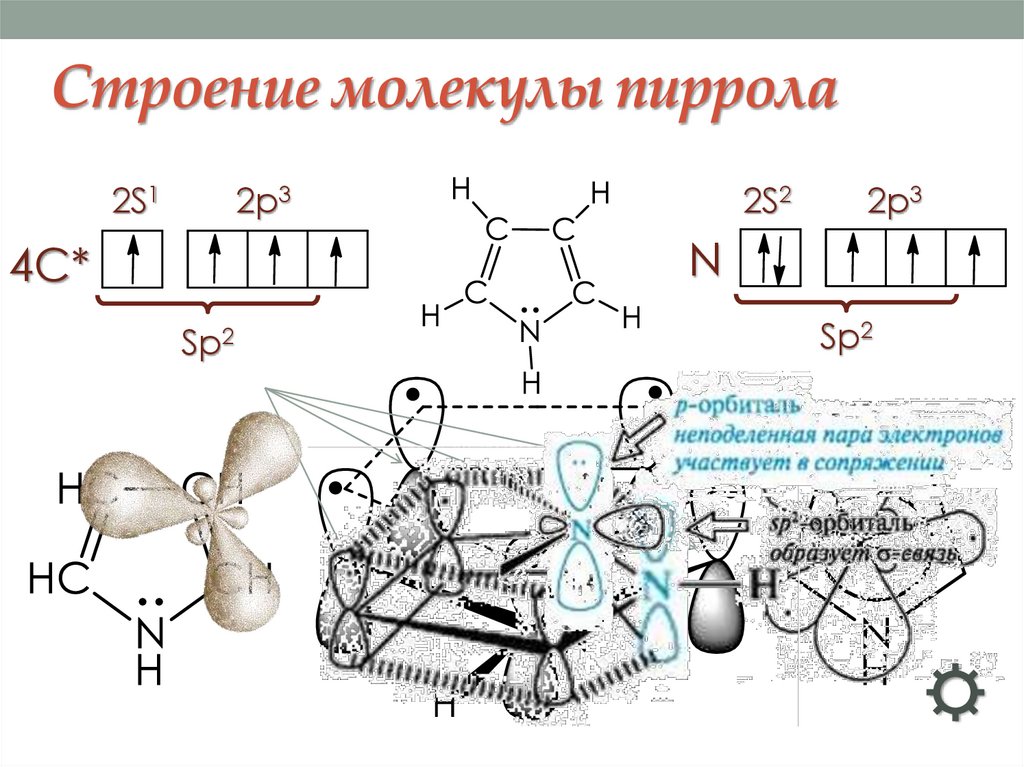
Строение молекулы пиррола2S1
2p3
2S2
N
4С*
Sp2
Sp2
24.04.2024
2p3
16
☼
17.
24.04.202417
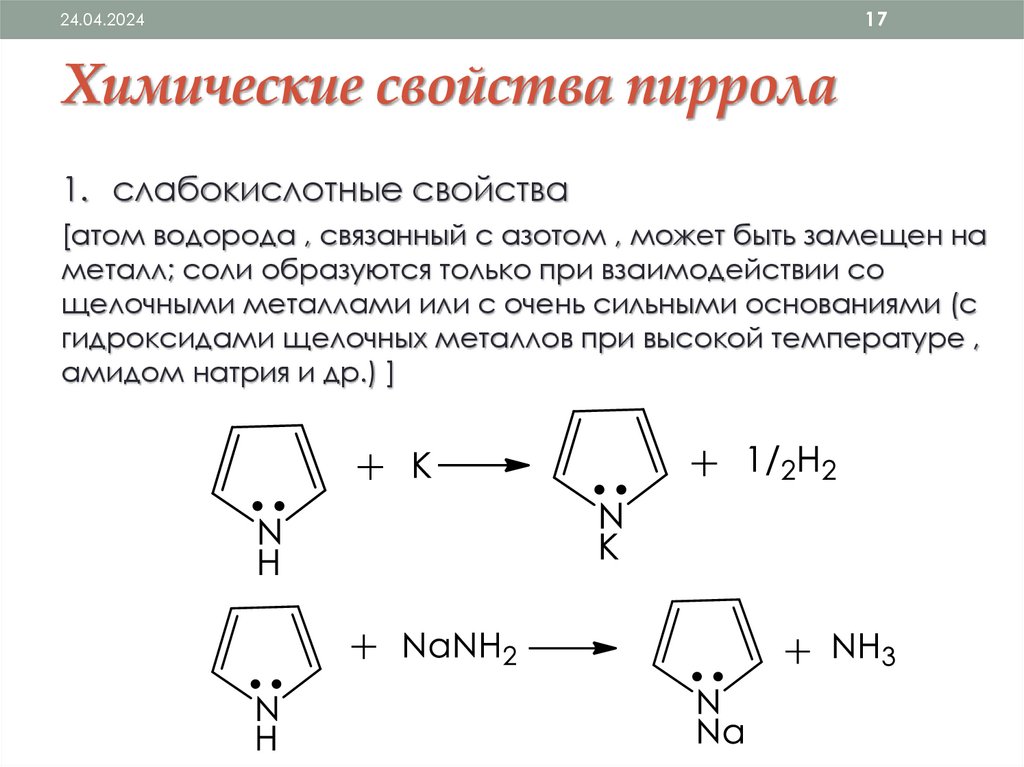
Химические свойства пиррола
1. слабокислотные свойства
[атом водорода , связанный с азотом , может быть замещен на
металл; соли образуются только при взаимодействии со
щелочными металлами или с очень сильными основаниями (с
гидроксидами щелочных металлов при высокой температуре ,
амидом натрия и др.) ]
18.
1824.04.2024
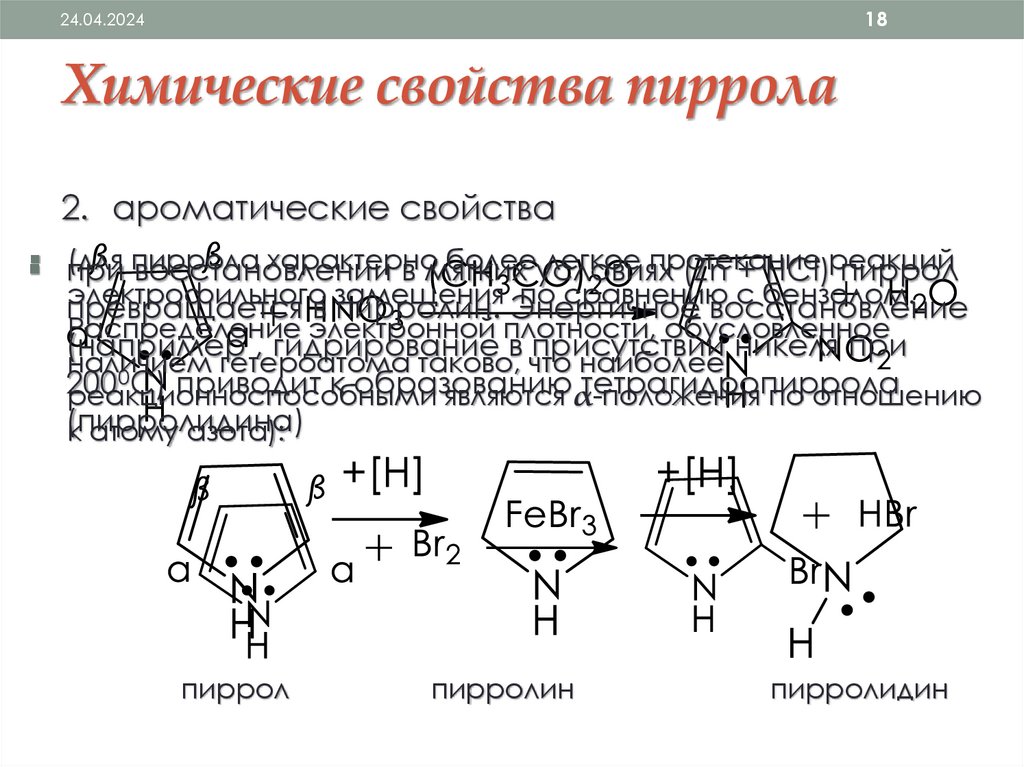
Химические свойства пиррола
2. ароматические свойства
(для пиррола
характерно
болееусловиях
легкое протекание
при
восстановлении
в мягких
(Zn + HCI)реакций
пиррол
электрофильного замещения по сравнению с бензолом.
превращается
в пирролин. Энергичное восстановление
Распределение электронной плотности, обусловленное
(например , гидрирование в присутствии никеля при
наличием
гетероатома таково, что наиболее
0
200
С) приводит к образованию
тетрагидропиррола
реакционноспособными
являются α-положения
по отношению
(пирролидина)
к атому азота):
пиррол
пирролин
пирролидин
19.
24.04.202419
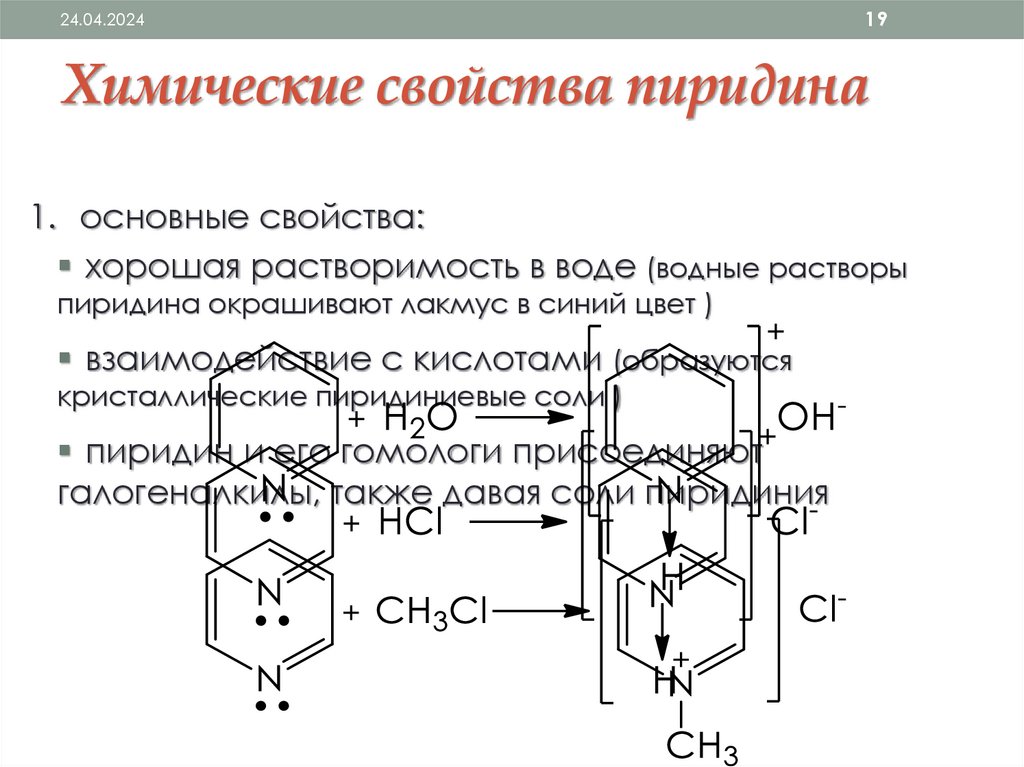
Химические свойства пиридина
1. основные свойства:
хорошая растворимость в воде (водные растворы
пиридина окрашивают лакмус в синий цвет )
взаимодействие с кислотами (образуются
кристаллические пиридиниевые соли )
пиридин и его гомологи присоединяют
галогеналкилы, также давая соли пиридиния
20.
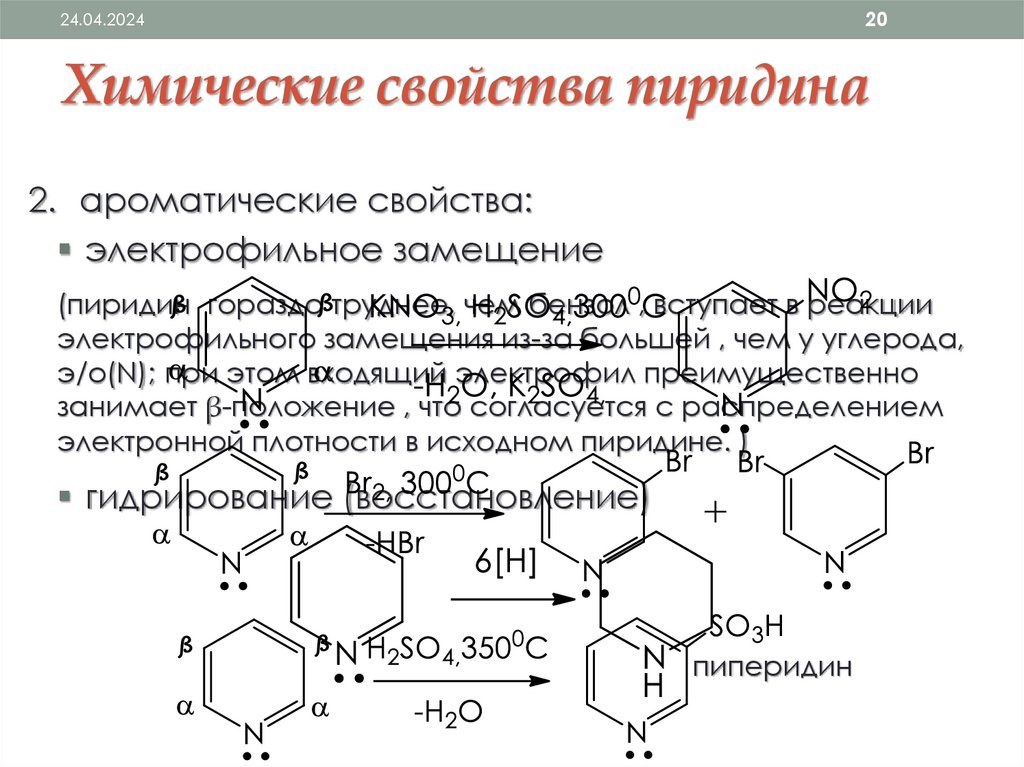
2024.04.2024
Химические свойства пиридина
2. ароматические свойства:
электрофильное замещение
(пиридин гораздо труднее, чем бензол , вступает в реакции
электрофильного замещения из-за большей , чем у углерода,
э/о(N); при этом входящий электрофил преимущественно
занимает β-положение , что согласуется с распределением
электронной плотности в исходном пиридине. )
гидрирование (восстановление)
пиперидин
21.
24.04.2024Домашнее задание
§ 56, 57,
упражнения после параграфов
21
22.
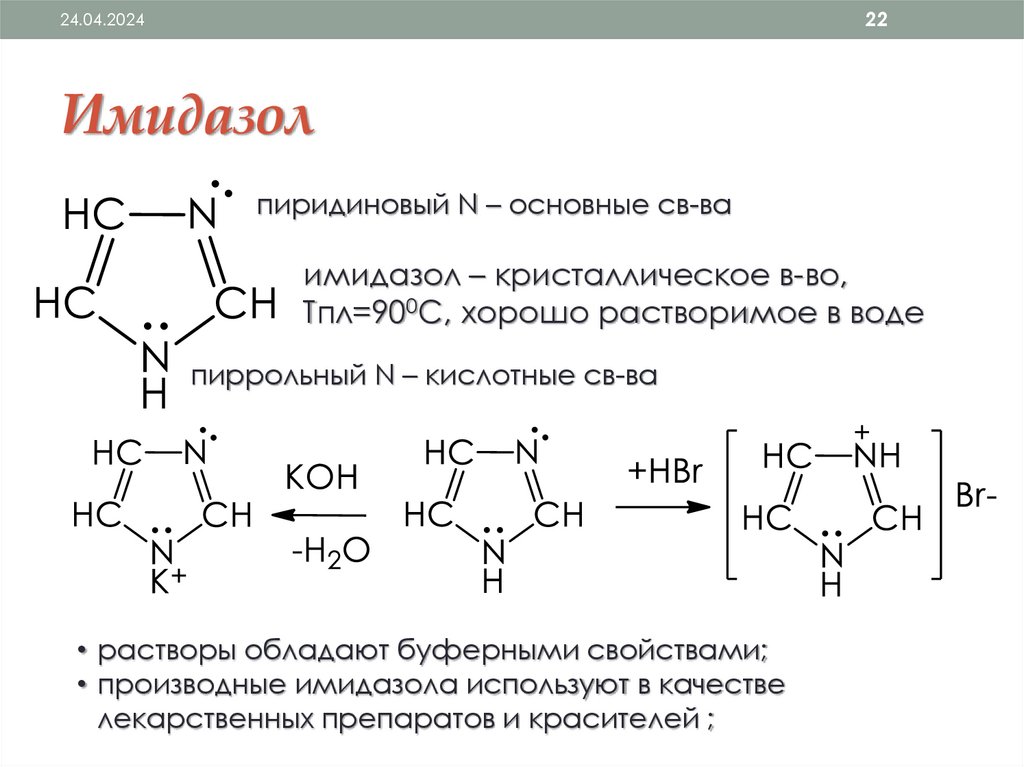
2224.04.2024
Имидазол
пиридиновый N – основные св-ва
имидазол – кристаллическое в-во,
Тпл=900С, хорошо растворимое в воде
пиррольный N – кислотные св-ва
• растворы обладают буферными свойствами;
• производные имидазола используют в качестве
лекарственных препаратов и красителей ;
23.
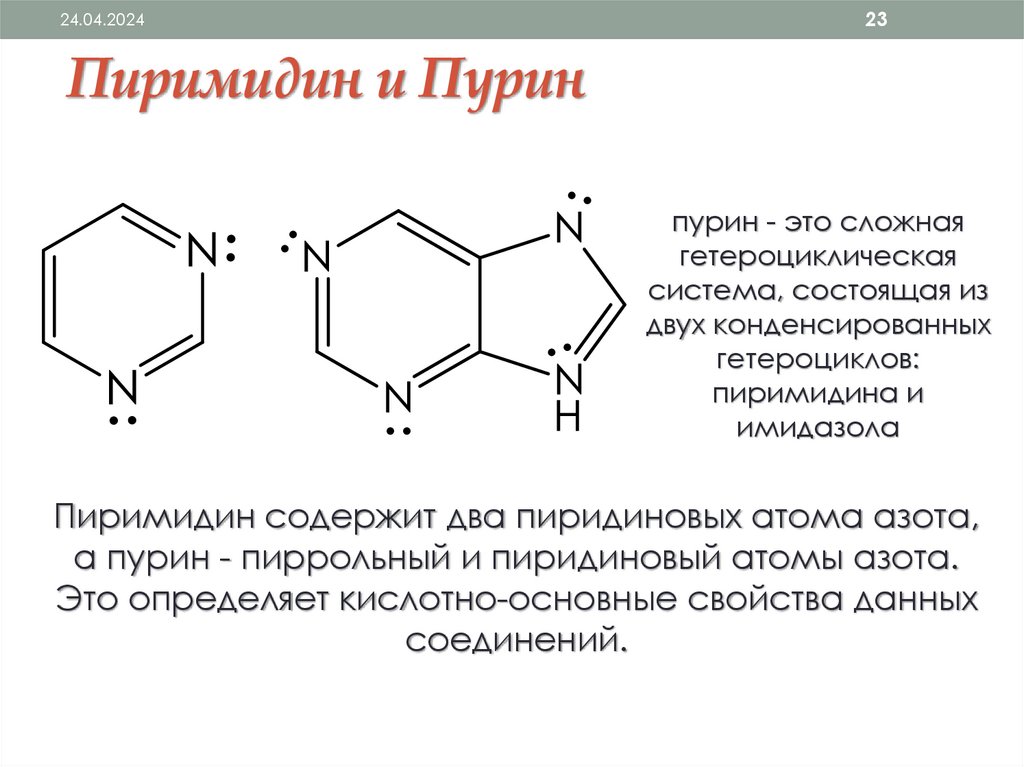
24.04.202423
Пиримидин и Пурин
пурин - это сложная
гетероциклическая
система, состоящая из
двух конденсированных
гетероциклов:
пиримидина и
имидазола
Пиримидин содержит два пиридиновых атома азота,
а пурин - пиррольный и пиридиновый атомы азота.
Это определяет кислотно-основные свойства данных
соединений.
24.
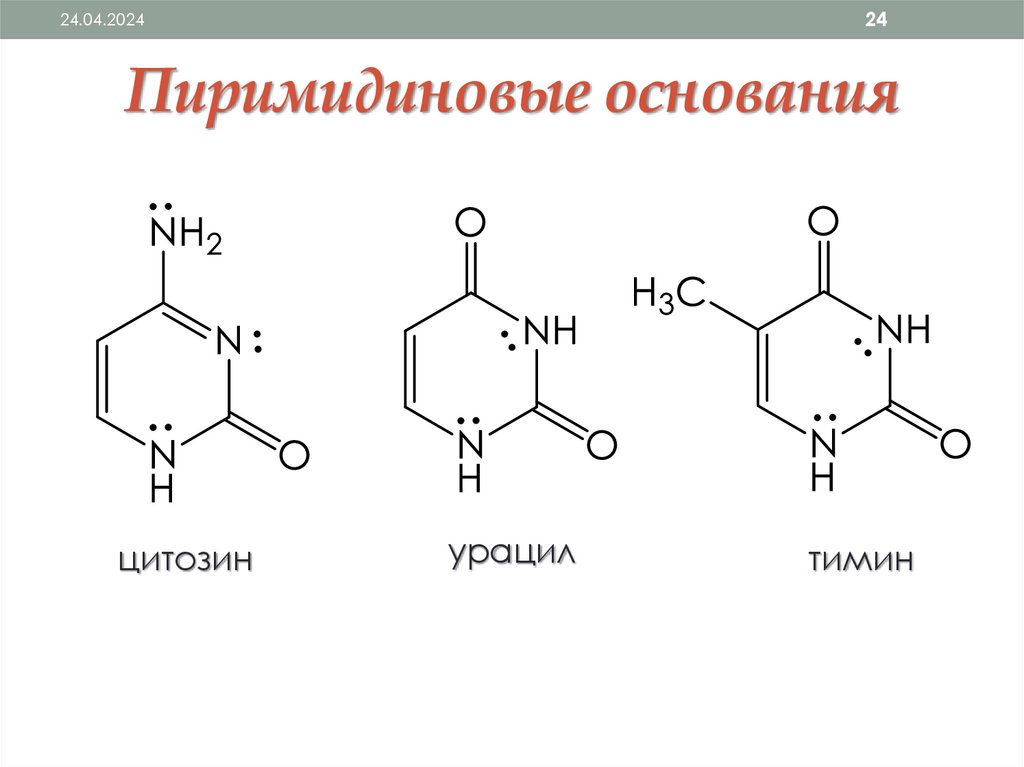
2424.04.2024
Пиримидиновые основания
цитозин
урацил
тимин
25.
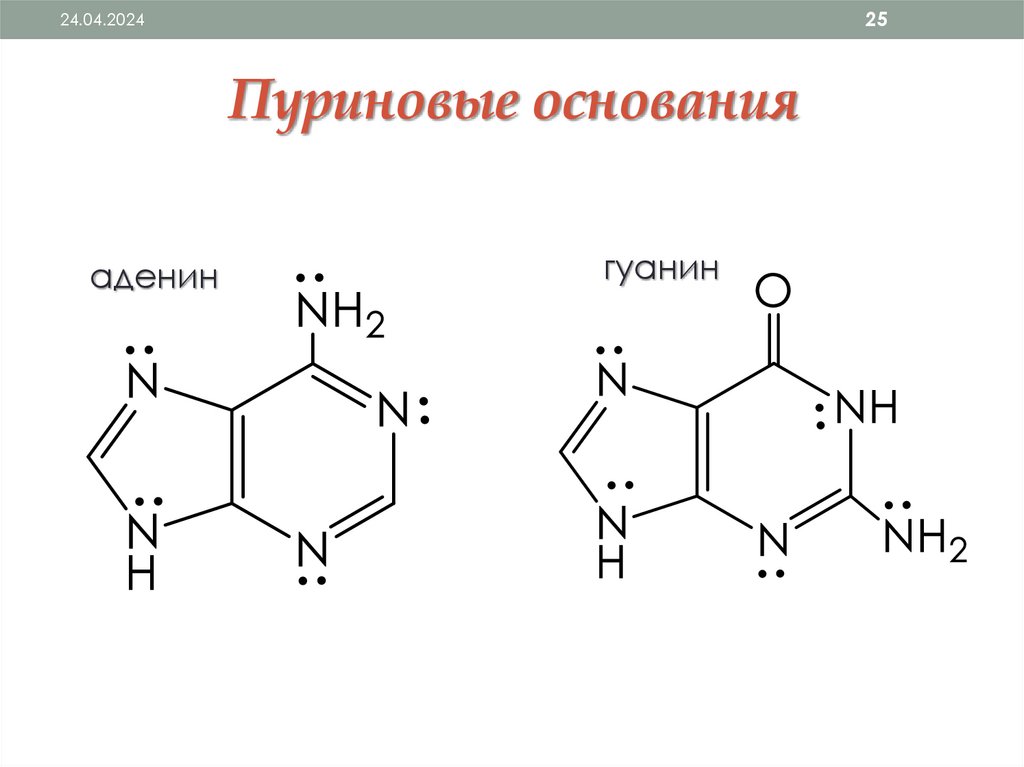
2524.04.2024
Пуриновые основания
аденин
гуанин
26.
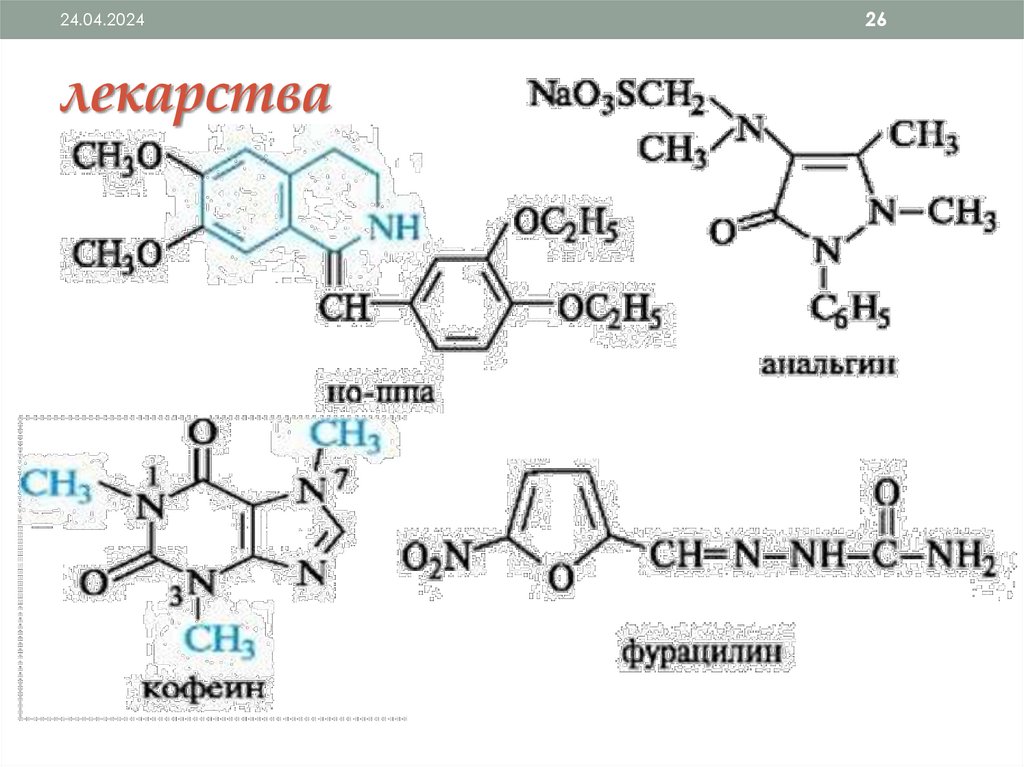
24.04.2024лекарства
26
27.
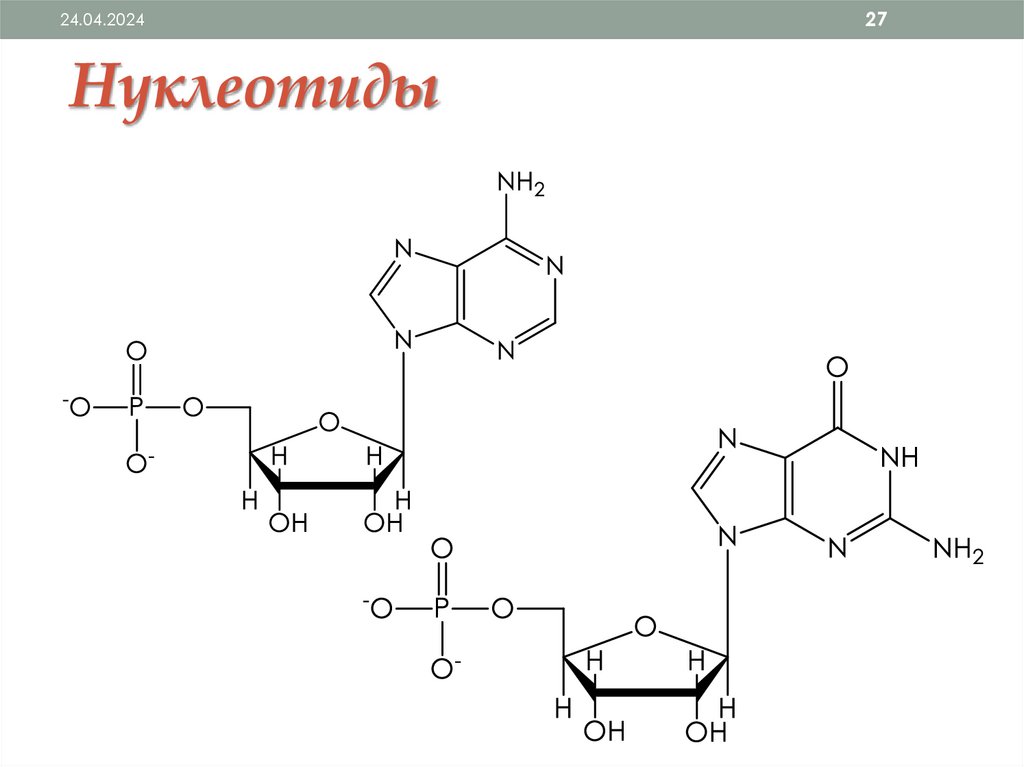
24.04.2024Нуклеотиды
27
28.
24.04.2024Домашнее задание
стр 359
§60
упр. 1-9 стр 367-368
28




 chemistry
chemistry








