Similar presentations:
Элементы квантовой физики
1.
ЭЛЕМЕНТЫКВАНТОВОЙ ФИЗИКИ
2.
Модели атомаПостулаты Бора
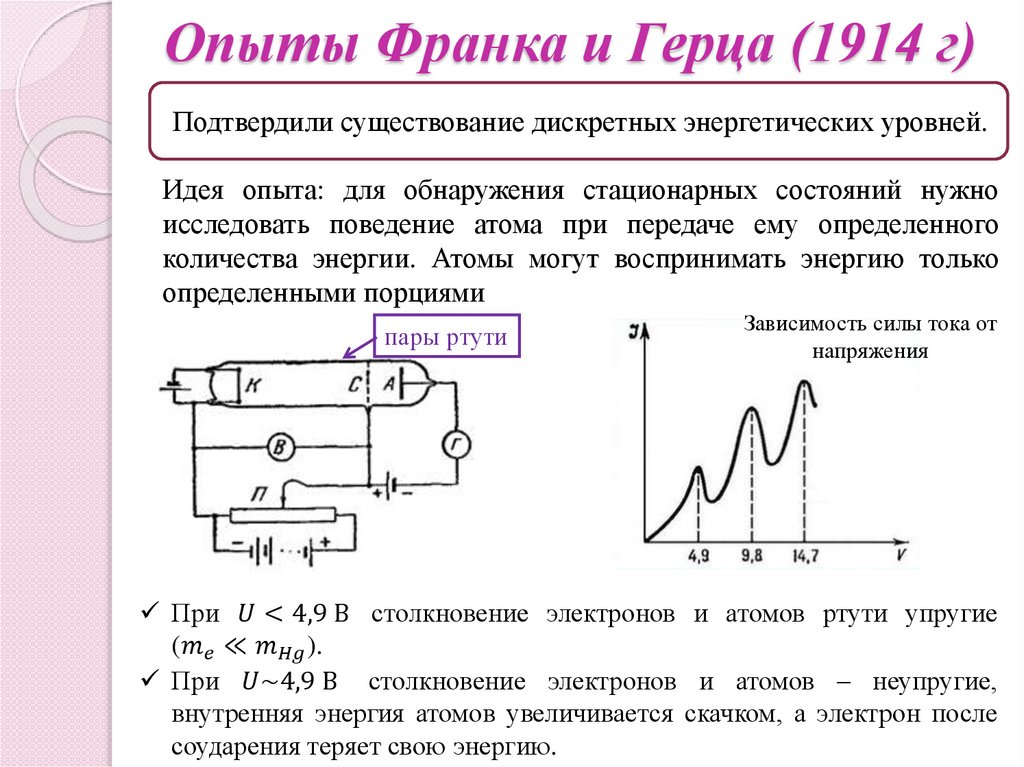
Опыты Франка и Герца
Теория Бора для атома водорода
Спектр атома водорода по Бору
Квантовая модель
Принцип неопределенностей
Гейзенберга
Волновая функция
Уравнение Шредингера
3.
Модели атомаОткрытие сложного строения атома – важнейший этап становления
физики 1859 г. – немецкие физики Бунзен и Кирхгоф разработали
метод спектрального анализа: определение химического состава
вещества по его спектру.
Спектры, которые дают вещества, находящиеся в атомарном
(газообразном) состоянии, являются линейчатыми
Вывод: вещество излучает свет только определенных длин волн!
Свет излучают атомы, которые практически не взаимодействуют
друг с другом.
4.
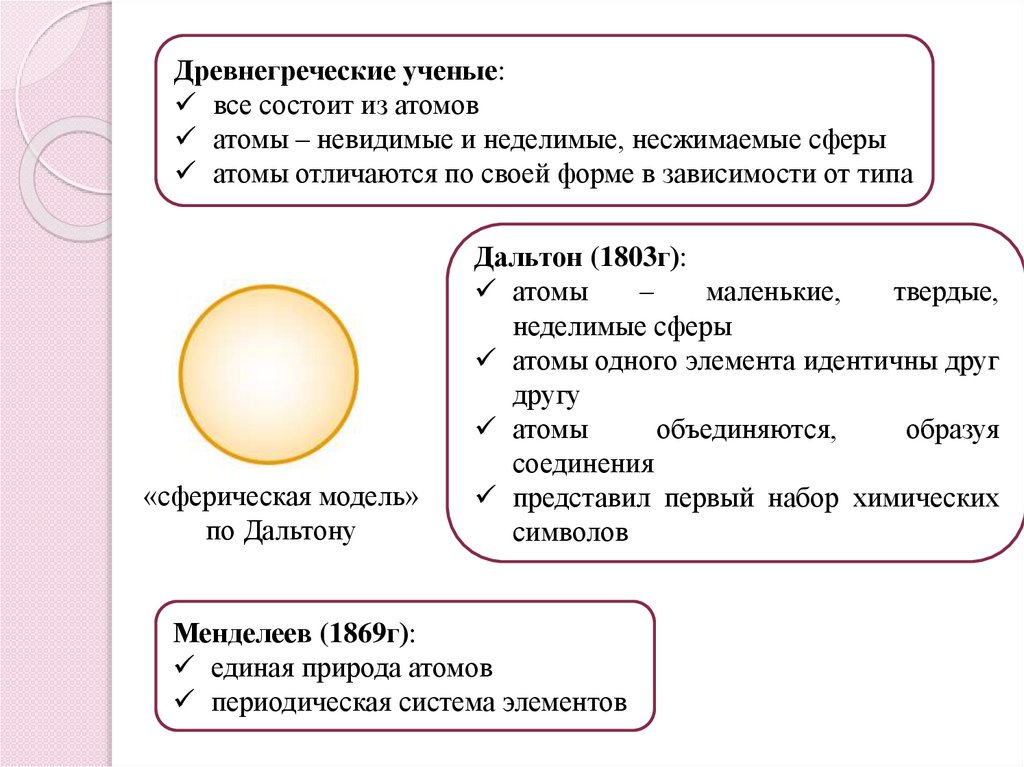
Древнегреческие ученые:все состоит из атомов
атомы – невидимые и неделимые, несжимаемые сферы
атомы отличаются по своей форме в зависимости от типа
«сферическая модель»
по Дальтону
Дальтон (1803г):
атомы
–
маленькие,
твердые,
неделимые сферы
атомы одного элемента идентичны друг
другу
атомы
объединяются,
образуя
соединения
представил первый набор химических
символов
Менделеев (1869г):
единая природа атомов
периодическая система элементов
5.
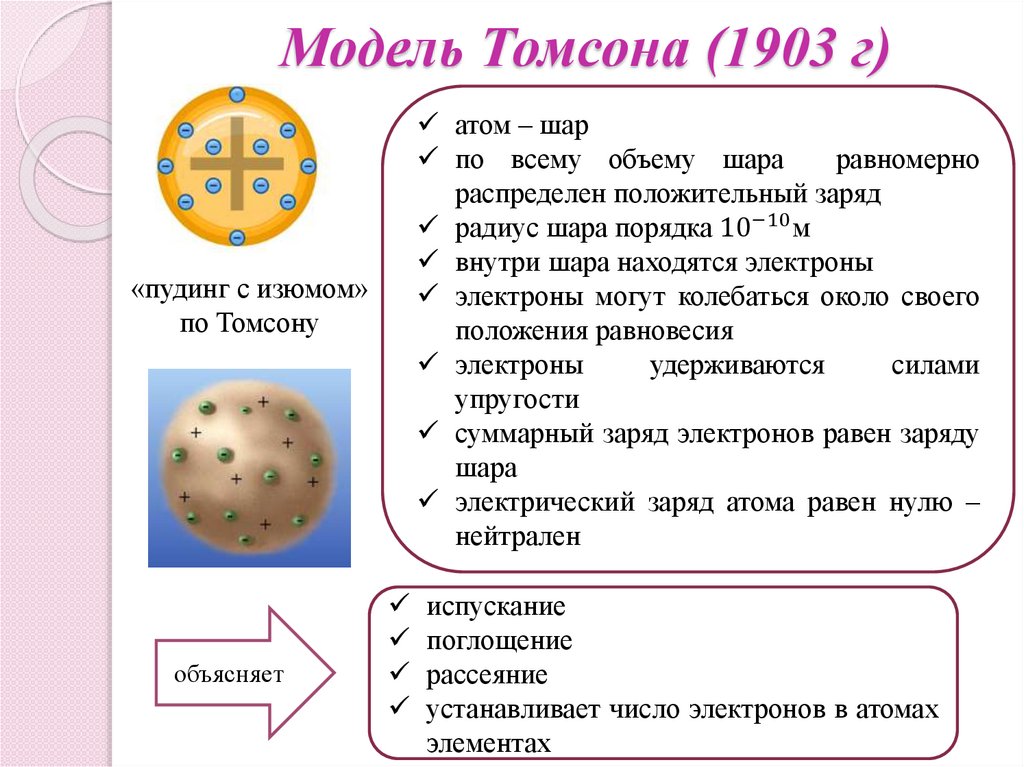
Модель Томсона (1903 г)«пудинг с изюмом»
по Томсону
объясняет
атом – шар
по всему объему шара
равномерно
распределен положительный заряд
радиус шара порядка 10−10 м
внутри шара находятся электроны
электроны могут колебаться около своего
положения равновесия
электроны
удерживаются
силами
упругости
суммарный заряд электронов равен заряду
шара
электрический заряд атома равен нулю –
нейтрален
испускание
поглощение
рассеяние
устанавливает число электронов в атомах
элементах
6.
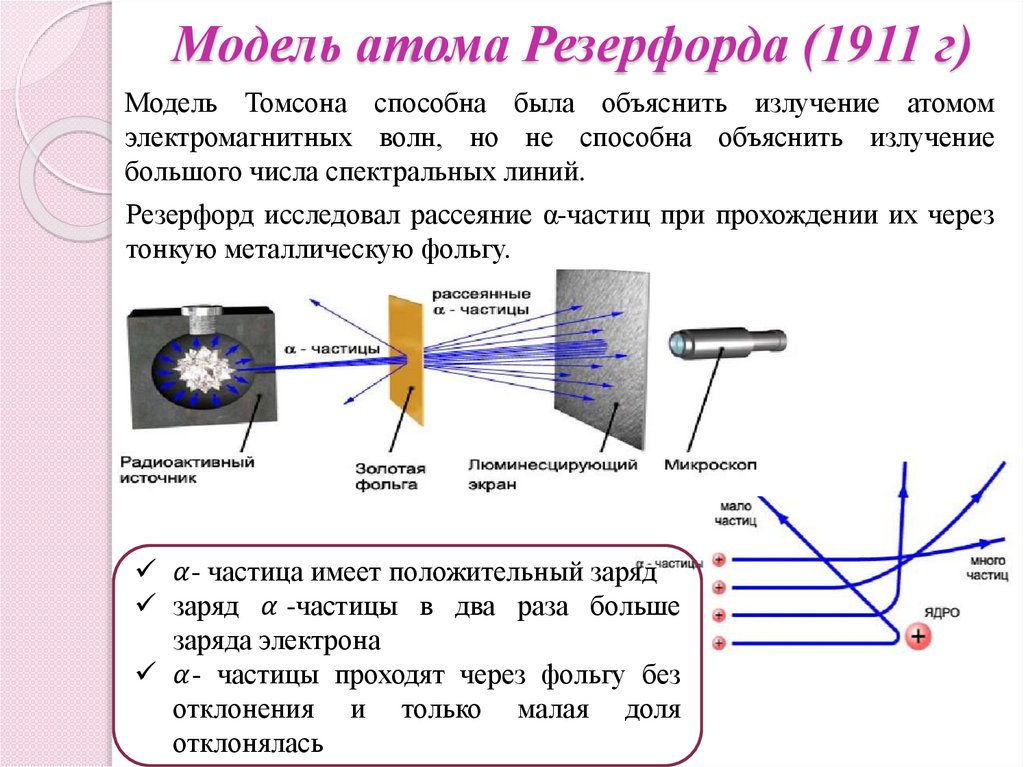
Модель атома Резерфорда (1911 г)Модель Томсона способна была объяснить излучение атомом
электромагнитных волн, но не способна объяснить излучение
большого числа спектральных линий.
Резерфорд исследовал рассеяние α-частиц при прохождении их через
тонкую металлическую фольгу.

















 physics
physics








