Similar presentations:
Основные направления современной науки о полимерах
1.
Основные направления современнойнауки о полимерах
БИОМЕДИЦИНА
авиационаяпромышленость;це
ллюлозно-бу
мажнаяпромышленость;э
ле
ктроника; бытоваятехни
ка
МАТЕРИАЛЫ
ав
томобилестроение; космическаяпромышленость;
те
ки
сльнаяиле
гкаяпромышленость
2.
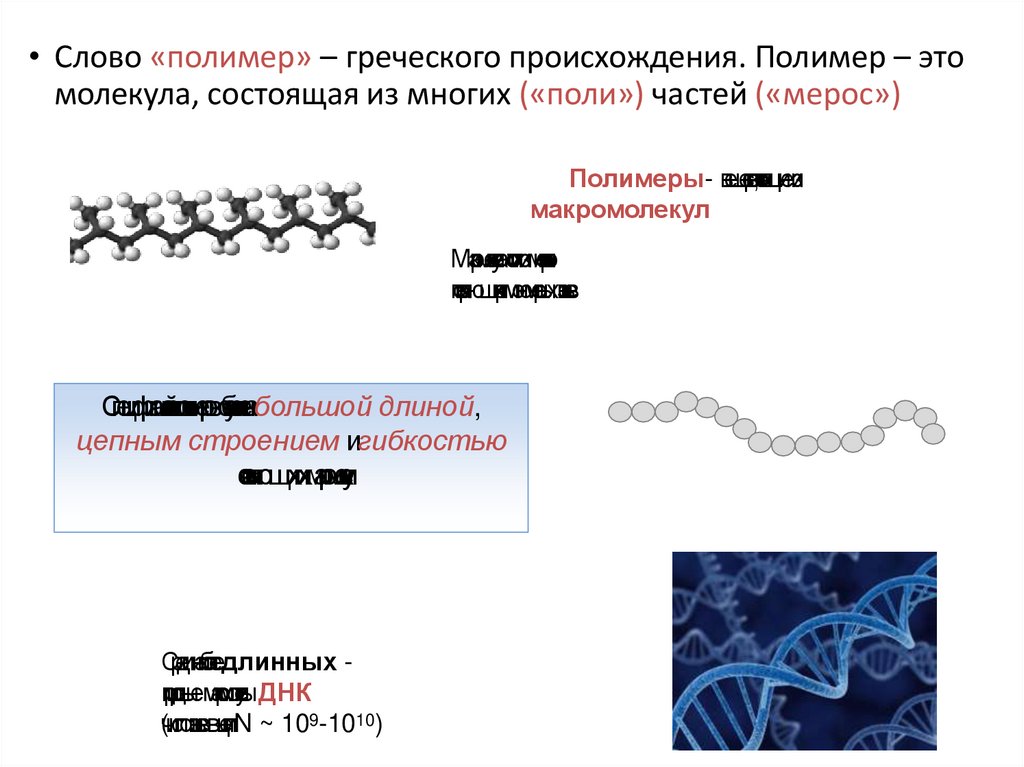
• Слово «полимер» – греческого происхождения. Полимер – этомолекула, состоящая из многих («поли») частей («мерос»)
Полимеры- вещества,со
тящиеиз
макромолекул
Мар
комоле
куласо
тситизмногр
катно
пов
торяющисхямономерныхзв
еньев
Спецификасв
ойсв
тполимеровобу
слов
ленабольшой длиной,
цепным строением игибкостью
состав
ляющихихмакромолеку
л
Срединаиболеедлинных природные-макромоле
кулыДНК
(числозв
еньеввцепиN ~ 109-1010)
3.
Основные направления современнойнауки о полимерах
Регенеративная медицина
Хирургия
искусственные органы
шовный
материал
скаффолды
протезы
3D-биопринтинг
БИОМЕДИЦИНСКИЙ
АСПЕКТ
Офтальмология
контактн
ые линзы
Фармакология
лекарственные
препараты нового
поколения
4.
П Р И М Е Н Е Н И Е ПОЛИМЕРОВ В М Е Д И Ц И Н ЕБиосовместимость— способность материалов выполнять
свои функции и не вызывать существенных негативных реакций в
организме
Основные требования к биоматериалам:
недо
лжнывызыватьместнойвоспалите
льной
реакции;
недо
лжныо
казыватьто
ксическо
гиаллергическогдействиянаорганизм;
недо
лжныпровоцироватьразв
итеинфекци;
должнысо
храняь
тфункциональныесвойствавте
чниепредусмотрено
г срокаэксплуатации.
Биодеградация- процесс разложения материалов при
контакте с микроорганизмами, живыми тканями, клетками и
биологическими жидкостями
5.
Макромолекулы распадаются на олигомеры, которые затемперерабатываются микроорганизмами или ферментами
Н2О, CO2
Коне
чныепродуктыраспада-
Б И ОДЕ Г РАДИРУЕ М Ы Е
(БИОРАЗЛАГАЕМЫЕ) ПОЛИМЕРЫ
Создание материалов с
регулируемым сроком эксплуатации
медицина
имплана
ты, постепеннозамещаемыеживымитканями(ре
гнеративнаямедицина)
шовныйматериалдлях
ируги
защита окружающей среды
носи
те
лилекарственныхпрепаратов
(контрольвысвобождения)
2 сферы жизнедеятельности
человека
6.
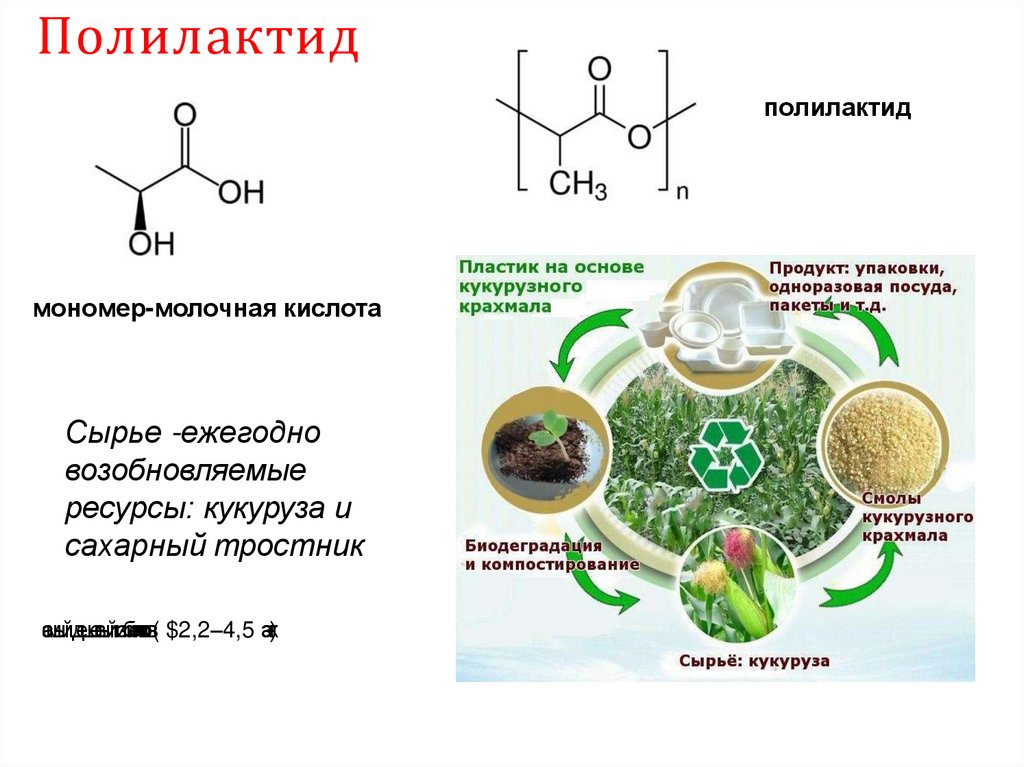
Полилактидполилактид
мономер-молочная кислота
Сырье -ежегодно
возобновляемые
ресурсы: кукуруза и
сахарный тростник
амыйдешевыйизбиопласти
с
ков( $2,2–4,5 закг)
7.
ПолилактидПрименение:
1. Произв
одствоизде
лийскороткимсро
кмслужбы(пищеваяупа
ковка, одноразоваяпосу
да, па
ке
ты,
различнаятара)
2. В медицине: для
производства
хирургических нитей,
штифтов, имплантатов
3. В 3d печати
8.
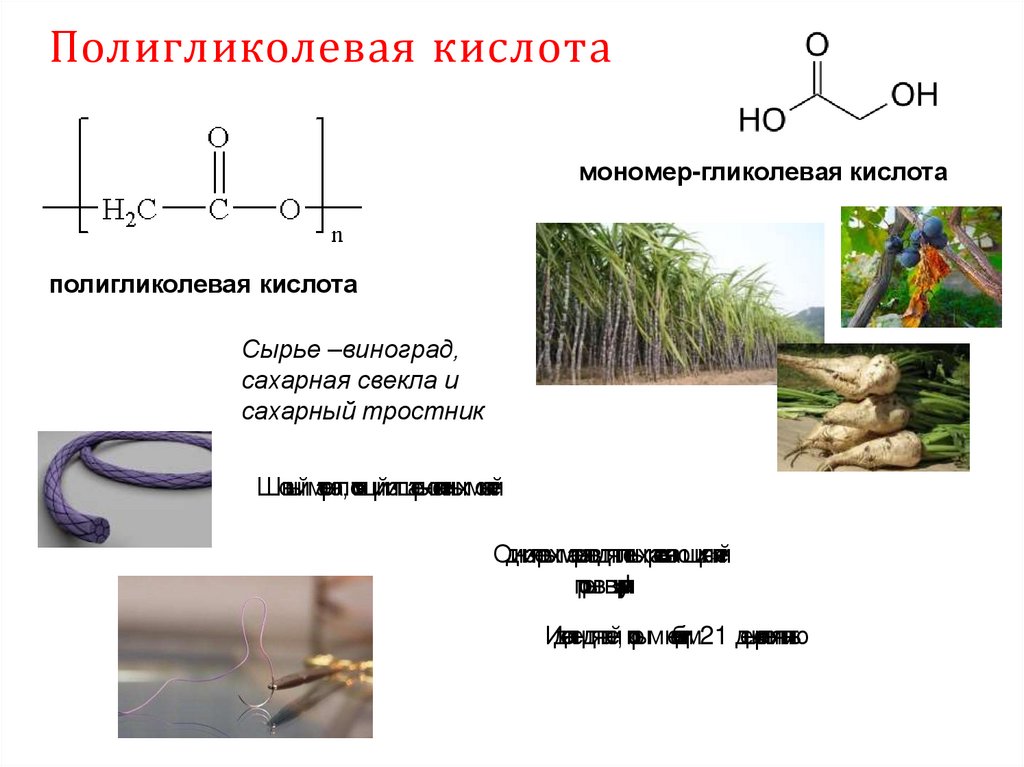
Полигликолевая кислотамономер-гликолевая кислота
полигликолевая кислота
Сырье –виноград,
сахарная свекла и
сахарный тростник
Шовныйматериал,со
тсящийизтщате
льноспле
тнныхмононитей
Одинизпервыхматериаловдляпле
тныхрасасывающихсянитейпрорыввхируги!
Идеалендлятканей,котрымнеобходим21 деньскреплениянитью
9.
ПоликапролактонБиомедицинское применение
Шовныйматериал(про
чныеиэ
ластичныенити), проив
зодитсякомпаниямиSolvay и
Union Carbide
Биоде
гр
адациявте
лече
лове
капроисо
хдитмедленно, о
кло3 ле
т
Протезысоудовмало
гдиаме
тра(внутренийдиаме
тр2 мм, толщинастенки100 мкм)
р
Гафт(основа) длякровеносн
о
г
сосд
уа
Сохранность каркаса обеспечитвается
до того момента, пока на его месте
не сформируется собственный новый
сосуд
СЭМ изображение графта из поликапролактона
10.
ПоликапролактонЭлектроспиннинг - вытягиваниеуль
тра
тонкихволо
книзжидкойсре
ды по
ддействиемэ
ле
кр
тическо
гпо
ля
Воснове-воздейсв
тиевысо
кг э
лектрическогнапряжения(десятки киловольт) нараств
ор
полимера.
У
станов
ка: источниквысокогнапряжения,капилляр(м.б.
вращающимся) и
принимающаяпластины(барабан).
11.
ПоликапролактонПродуктыде
гр
адации:
, Н2О, CO2
капроноваякислота
СЭМ изображение нановолокон,
полученных методом электроспиннинга
Недо
стаки:приутилиа
зциипродуктовгидролиа
звозможнавоспалите
льнаяреакция
Исполь
ютс
зу
другимибиосовместимымиполимерами
12.
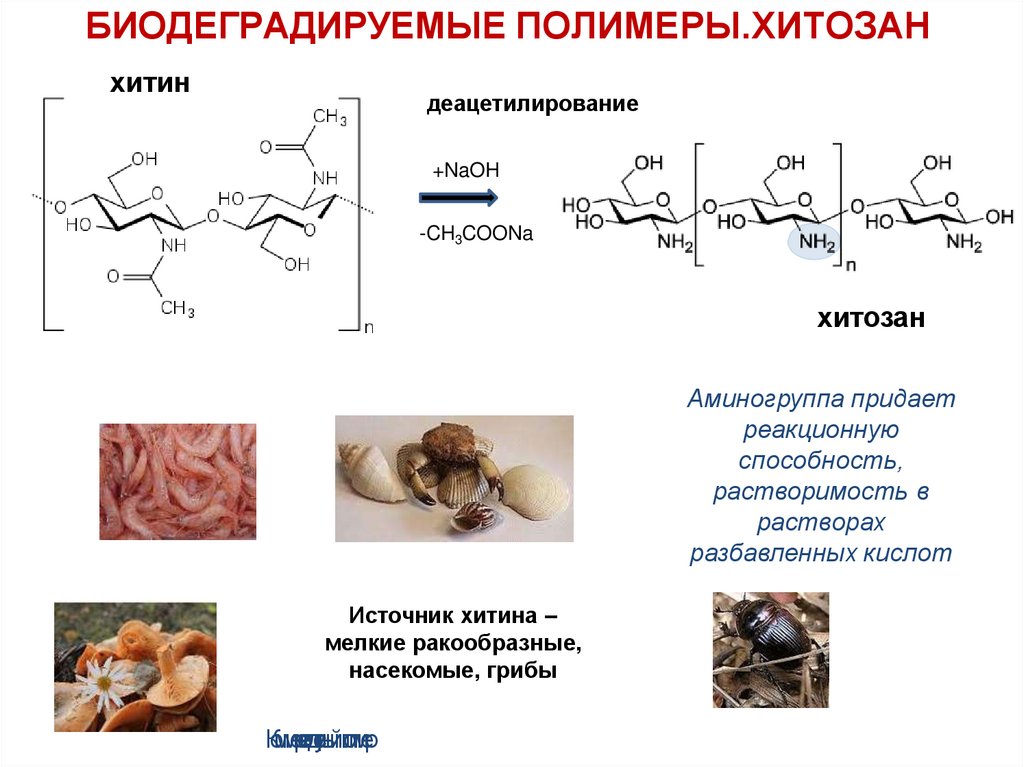
БИОДЕГРАДИРУЕМЫЕ ПОЛИМЕРЫ.ХИТОЗАНхитин
деацетилирование
+NaOH
-CH3COONa
хитозан
Аминогруппа придает
реакционную
способность,
растворимость в
растворах
разбавленных кислот
Источник хитина –
мелкие ракообразные,
насекомые, грибы
Коммерчеи
скдо
ступныйпо
лимер
13.
ХИТОЗАН. ОБЛАСТИ ПРИМЕНЕНИЯразрешендлябиомедицинско
г применения
можетбытьпо
лученвразличныхформах: ввиде
порошка, тонкихпленокгидроге
ля,идр.
прояв
ляе
тантимикробную а
ктивнось
тиантиоксидантные
свойства
кровооса
тнавливающеесре
дств
о, коагулянт
уско
р
я
е
транозаживляющиепроцесызасче
тстимуляцииростакле
то
к
универсальныйсорбент(связывае
тивыводит
изорганизмахоле
тсрин,
токсиныидр.)
14.
РАЗЛИЧНЫЕ ТРЕБОВАНИЯ К ПОЛИМЕРАМБ И О М Е Д И Ц И Н С К О Г О НАЗНАЧЕ НИЯ
Объ
екты, котрыедлите
льноевремя должныбытьустойчивывусловияхфункционированиявко
н
та
кеса
гр
есивнойбиологическойсредой
имплантаысдли
те
льнымисроками пребыванияворганизме
Объекты,распадающиесясконтролируемойскоростью
прис
озданииле
карств
енныхпрепаратов
призамещениисуставов-длите
льноевремясущесв
тованияворганизме;
призамещениико
жи- быстроезамещение
живойтканью
15.
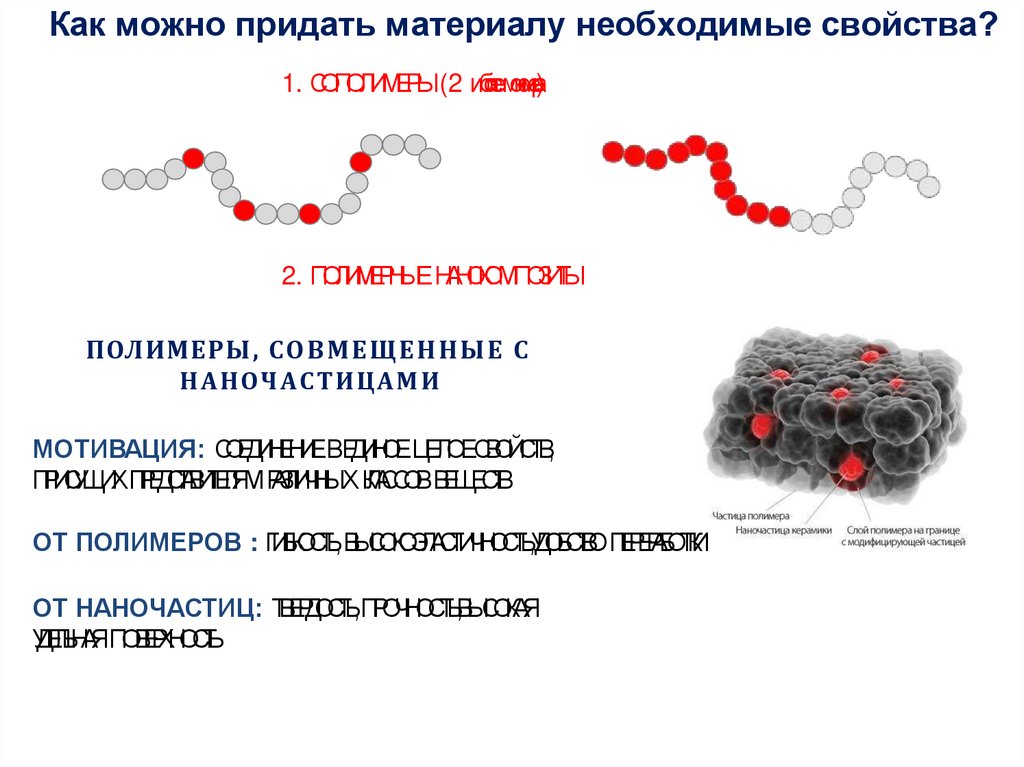
Как можно придать материалу необходимые свойства?1. СОПОЛИМЕРЫ(2 иболеемономера)
2. ПОЛИМЕРНЫЕНАНОКОМПОЗИТЫ
ПОЛИМЕРЫ, С О В М Е Щ Е Н Н Ы Е С
НАНОЧАСТИЦАМИ
МОТИВАЦИЯ: СОЕДИНЕНИЕВЕДИНОЕЦЕЛОЕСВОЙСТВ,
ПРИСУЩИХПРЕДСТАВИТЕЛЯМРАЗЛИЧНЫХ КЛАССОВВЕЩЕСТВ
ОТ ПОЛИМЕРОВ : ГИБКОСТЬ,ВЫСОКОЭЛАСТИЧНОСТЬ,УДОБСТВОПЕРЕРАБОТКИ
ОТ НАНОЧАСТИЦ: ТВЕРДОСТЬ,ПРОЧНОСТЬ,ВЫСОКАЯ
УДЕЛЬНАЯПОВЕРХНОСТЬ
16.
МНОГОФУНКЦИОНАЛЬНЫЕНАНОКОМПОЗИТЫ :
В СОВОКУПНОСТИ:
новые свойства (механические,
теплофизические,
электрические, магнитные,
оптические, барьерные и т.д.)
ГЛАВНОЕ УСЛОВИЕ - полная совместимость основного
материала и добавляемых к нему наночастиц
Свойства композитов могут
изменяться при очень малых
изменениях концентрации
наполнителя
17.
ПОЛИМЕРНЫЕ НАНОКОМПОЗИТЫНАНОКОМПОНЕНТЫ ( ЧАСТИЦЫ, ПЛАСТИНЫ, ВОЛОКНА)
частицы оксидов алюминия или титана, серебра, углеродные,
кремниевые нанотрубки и волокна, др.
Наночастицы серебра (ПЭМ)
Наночастицы золота (СЭМ)
(Na,Ca)0,33(Al,Mg)2(Si4O10)(OH)2·nH2O
18.
П Р И М Е Н Е Н И Е НАНОКОМПОЗИТОВ В М Е Д И Ц И Н ЕИмплантаты, которые могут постепенно заменяться в
организме костной или другой живой тканью.
Поражениеэ
лемено
твсерде
чно-сос
дис
у
тойсистемы
Замещениекостныхисуставныхэлемено
тв
Протезированиесвя
зо
кису
ожилий,мягкихтканей
х
Соединениерасе
ченныхтканей
Повреждениекожногопокрова
Поражениязубов
Пораженияситемыоргановзренияислух
а
Стоматология восстановление зубной
эмали
Шовный материал
19.
БИОРАЗЛАГАЕМЫЕ НАНОКОМПОЗИТЫ ДЛЯРЕКОНСТРУКЦИИ КОСТНЫХ ТКАНЕЙ
Преимущества:
Полимерыотличаютсяги
бкостью, ч
тодае
твозможностьи
го
зтав
ливаь
тимплантаы, полностьюпов
торяющиеформукоси
т.
Полимерпостепенора
злаге
тсясобразованиемновойкостн
ойткани
Продуктыбиодеградаци
выводятсяизо
р
ганизмаестеств
еннымпутем
Необ
ходимось
тхируги
ч
е
ксо
гвмешате
льсв
таотс
е(металличеси
в
у
кеикерамическиепротезынужноменятьилиив
л
зекать)
Вдоль поврежденных
костей устанавливают
направляющие рост и
регенерацию шарниры
из полимерного
нанокомпозита
20.
ПРЕИМУЩЕСТВА3d пе
ча
ь
тпозволяе
тсоздаь
т
индивидуальныйимпланталюбой
формыдляконкре
тн
о
гпациента
Т
омографическийснимок– пе
ча
тькости-постепеннаядер
гадацияпо
лимера- образование
новойкостнойткани
21.
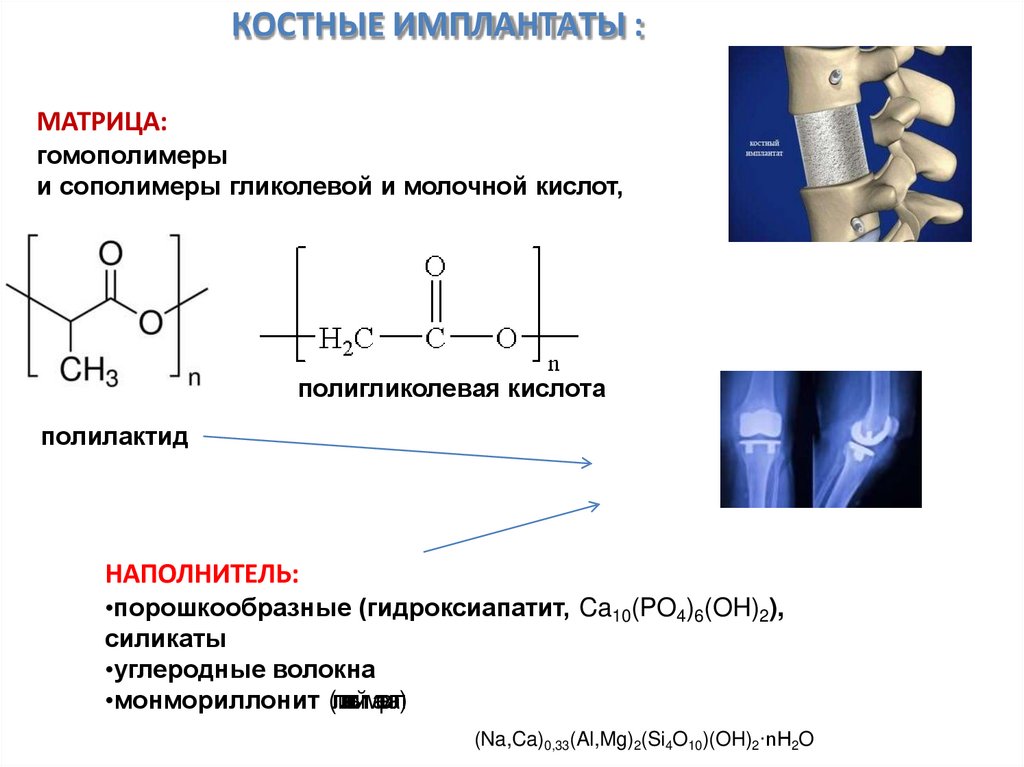
КОСТНЫЕ ИМПЛАНТАТЫ :МАТРИЦА:
гомополимеры
и сополимеры гликолевой и молочной кислот,
полигликолевая кислота
полилактид
НАПОЛНИТЕЛЬ:
•порошкообразные (гидроксиапатит, Ca10(PO4)6(OH)2),
силикаты
•углеродные волокна
•монмориллонит (глинистыйматериал)
(Na,Ca)0,33(Al,Mg)2(Si4O10)(OH)2·nH2O
22.
Наполните
ль- гидроксиапа
тит(минеральнаяосновакостнойткани)
БИОРАЗЛАГАЕМЫЕ НАНОКОМПОЗИТЫ ДЛЯ РЕКОНСТРУКЦИИ
КОСТНЫХ ТКАНЕЙ
Матрица- наосновепо
лила
ктида
Напо
лните
ль- наночастицы
глинисто
гматериаламонтмориллонита
Ca10(PO4)6(OH) 2
Химический Факультет
Томского ГУ
Какиреальнаякосн
таяткань,содержитбольшоеко
личествопор
Гидроксиапатит/монтмориллонитвхо
дитвкостнуютканьи
провоцируе
терост
Клиника Бемонта (Ирландия)
23.
П Р И М Е Н Е Н И Е НАНОКОМПОЗИТОВ В М Е Д И Ц И Н ЕМатрица- природный
разветвленный полисахарид
арабиногалактан
(из древесины
лиственницы)
Водорастворимый
композит:
наночастицы серебра,
стабилизированные
арабиногалактаном
ПРЕИМУЩЕСТВА
универсальныйпрепара
тширочайшегоспектрадействия
то
ксичнось
твсотн
иразниже,чемуантибиотиков
применение в качестве растворимого
биодеградируемого лекарственного средства
24.
П Р И М Е Н Е Н И Е НАНОКОМПОЗИТОВВ МЕДИЦИНЕ
С помощью нанокомпозита,
содержащего магнитные и
флуоресцирующие частицы,
можно быстрее обнаружить
опасные образования в
организме
Во время оперативного
вмешательства флуоресцирующая
составляющая облегчает работу
хирургов
25.
КОМ ПОЗ И Т Ы НА О С Н О В Е Х И ТОЗ А НАРаневыепокрытиянаосновенанокмпозитовхитозанасчастицамиAg
для лечения хронических
воспалений, открытых ран,
экзем
Продолжительность
антибактериального
действия покрытия несколько дней
Частицы серебра - от 10 до 30 нм
уско
р
я
е
транозаживляющиепроцесызасче
тстимуляцииростакле
то
к+ антимикробныйэффе
кт
СЭМизображениенанокмпози
та
хитозан-Ag2O
26.
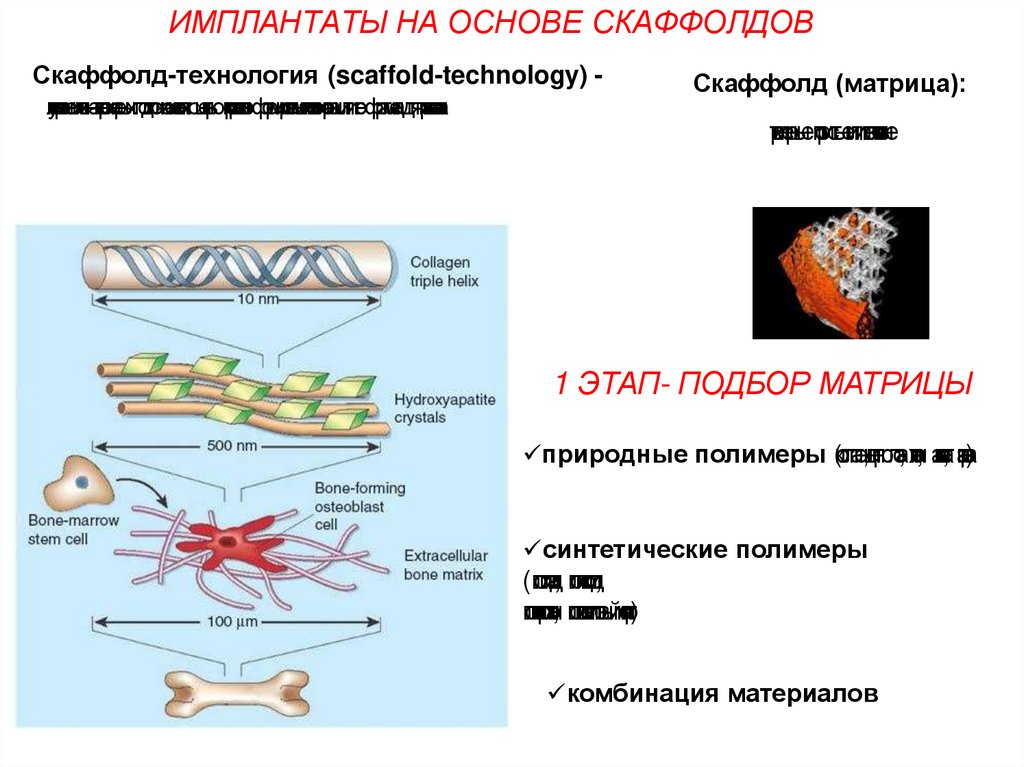
ИМПЛАНТАТЫ НА ОСНОВЕ СКАФФОЛДОВСкаффолд-технология (scaffold-technology) л
куь
тивированиекле
токнатрехмерныхподложках-носите
ляхсцельюпространственогформированияклеточ
н
ого
р
ганаилие
гофрам
гентадлятранспланта
Скаффолд (матрица):
тре
хмерныепористыеиливолокнистые
1 ЭТАП- ПОДБОР МАТРИЦЫ
природные полимеры (коллаген,це
ллюлоза, хитозан, альгинат, а
гроза)
синтетические полимеры
(по
лила
ки
тд, по
ли
гликолид,
по
ликапрола
ктон, поливиниловыйспир
т)
комбинация материалов
27.
Скаффолд (матрица):природные полимеры (биосовместимость)
коллаген: фибриллярныйбе
ло,ксотав
ляющийосновусоединительнойтканиорганим
заиобеспечива-ющийеепрочнось
тиэ
ласи
тчнось
т
недостатки: оченьвысо
каяскорось
т
биодеградации(сшивают), плох
иемеханически
е
войства(химическаямодифи
с
кация)
целлюлоза
недостатки: плохаябиодеградацияиз-ао
тсув
и
яучеловекаспецифическихферментовгидролаздляеерасщепления
хитозан
недостатки- низкаямеханическаяпро
чность
Вместе с гидроксиапатитом
–основные компоненты
кости
28.
2 ЭТАП- ПОЛУЧЕНИЕ СКАФФОЛДОВМетоды быстрого прототипирования
формированиетрехмерногобъектапрактическилюбойформыпоцифровоймоде
ли
1. Лазерная
стереолитографияпроцесс
фотополимеризации
Испо
ль
ютжиди
зу
кйфотопо
лимер, с
пособныйза
тв
ердеваь
тпо
двоздейсв
тиемлазерногизлучения.
Скаффолдыформиру
ютпослойно, первыйслойоб
лучено
г фотополимераприкрепленкдвигающейсяплатформе,ко
траяпослекаждогциклаполимеризацииперемещаетсянавысотуо
дногслоядлядальнейшейобработки
2. 3D-печать
29.
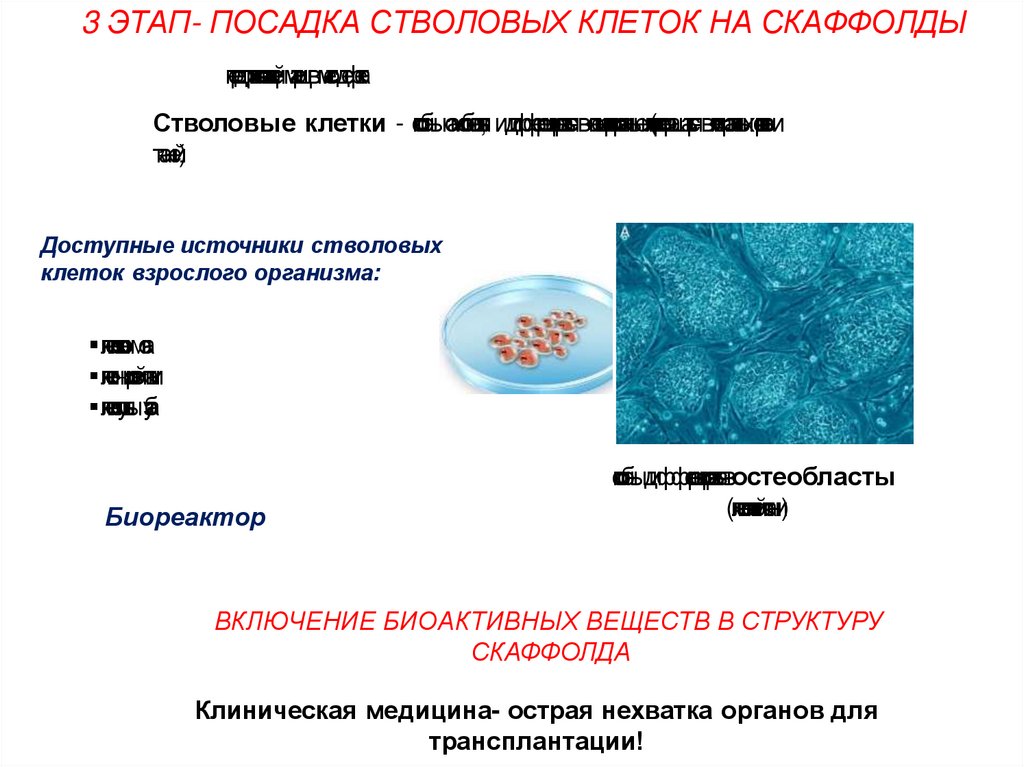
3 ЭТАП- ПОСАДКА СТВОЛОВЫХ КЛЕТОК НА СКАФФОЛДЫпередтрансплантациейматрицвместодефекта
Стволовые клетки - способнысамообновлятьс, идифференцироватьсявспециализированныекле
ки
т(превращатьсявкле
ки
тразличныхорганови
тканей).
Доступные источники стволовых
клеток взрослого организма:
кле
ткико
стнгомозга
кле
ткижировойткани
кле
ткипульпызуб
а
Биореактор
способныдифференцироватьсявостеобласты
(кле
ткикостнойткани)
ВКЛЮЧЕНИЕ БИОАКТИВНЫХ ВЕЩЕСТВ В СТРУКТУРУ
СКАФФОЛДА
Клиническая медицина- острая нехватка органов для
трансплантации!
30.
С И С Т Е М Ы ДЛЯД О С ТА В К И ЛЕКАРСТВ
НА О С Н О В Е
ПОЛИМЕРОВ
31.
НАНОФАРМАКОЛОГИЯОбычный способ применения лекарств – инъекции или
таблетки – резко увеличивает их концентрацию не
только в больном, но и в здоровых органах
нежелательные побочные эффекты
НАНОКОНТЕЙНЕРЫ
Наночастица с полостью, содержащая
различные вещества, доставляющая их
к нужной точке
•для перемещения в
организме медикаментов:
32.
Уменьшение эффективной дозыПонижение токсичности
Направленность действия
Пролонгированность действия
меньшаетс
у
ячис
лоприемовилиинъец
кий;
устраняютсяколебанияконцентрациа
кти
в
н
о
г
вещества
Возможность использовать высокоэффективные препараты,
применение которых ограничивается из-за большого количества
противопоказаний.
Значительное снижение стоимости лечения.
макромолекулярный клубок
способен аккумулировать
низкомолекулярное вещество
или наночастицы
Препаратмедленно
выде
ляе
тсяиз
носите
ля
!
33.
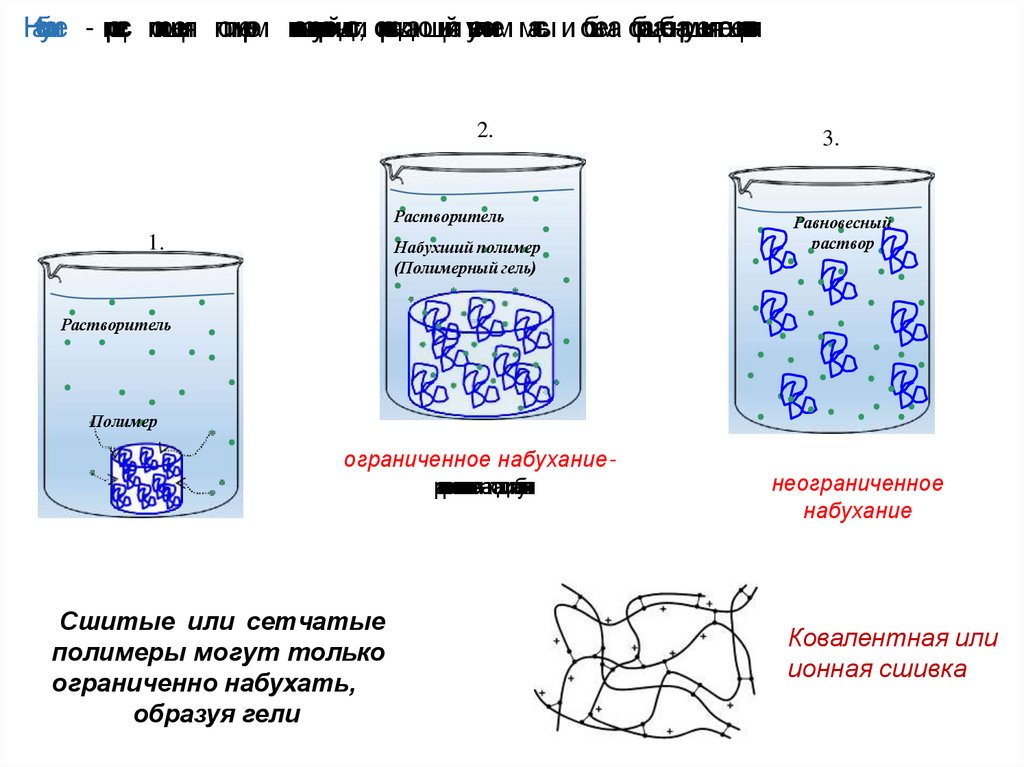
Набухание - процес поглощения полимером низкомолекулярнойжидкости, сопровождающийся увеличением масы и объема образцабезнарушенияео
гцелостн
ости.
2.
Растворитель
1.
Набухший полимер
(Полимерный гель)
3.
Равновесный
раствор
Растворитель
Полимер
ограниченное набуханиерастворениеостанавливае
тсянас
тадиинабухания
Сшитые или сетчатые
полимеры могут только
ограниченно набухать,
образуя гели
неограниченное
набухание
Ковалентная или
ионная сшивка
34.
Наногели на основе сшитого хитозанаПримеры сшивающих агентов:
Глутаровый
альдегид
Сшивка с помощью
эпихлоргидрина
Эпихлоргидрин
Трудно очистить полностью от
сшивающего агента
Дженипин
(растительного
происхождения)
250-300нм
Ионная сшивка (сульфатами)
Можноповлиятьнаразмерчастицгеля,изменивстепеньполимеризации
35.
Полимерные наногели для доставки лекарствПолимернаяматрица
Лекарств
о
Нан
о
ге
ль(~сотн
инм)
Для заполнения достаточно
поместить гель в раствор
лекарственного вещества
Удаление растворителяполучение лекарственной
формы
Высвобождение лекарства
диффузия
разложение
матрицы
энергия
36.
Заполнение полимерных наногелейлекарственными веществами
лекарство
Электростатические взаимодействия
по
лимер
связаное
лекарство
вободноелекарство
с
расщепляемая
св
язь
вода,ферменты
полимер
Ковалентное связывание
37.
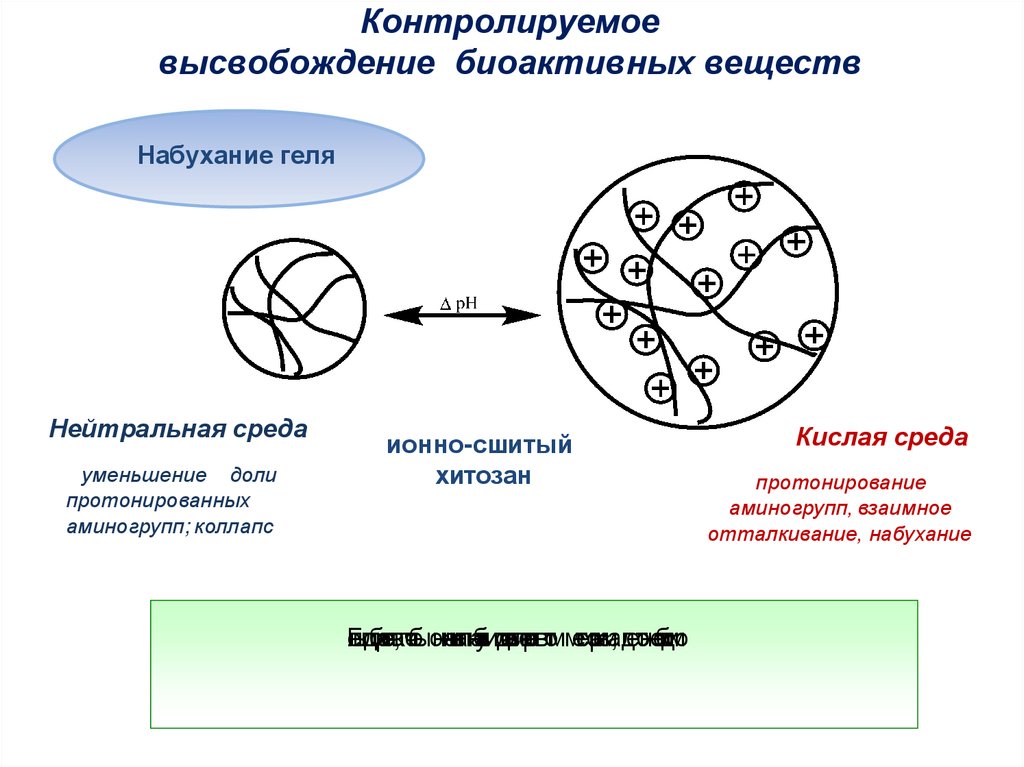
Контролируемоевысвобождение биоактивных веществ
Набухание геля
Нейтральная среда
уменьшение доли
протонированных
аминогрупп; коллапс
ионно-сшитый
хитозан
е
Г
льпо
дбирае
тсята,кч
тобыонначиналнабухатьиотдаватьле
карв
ствтомместеор
а
ганизма, гдеэ
тонеобходимо
Кислая среда
протонирование
аминогрупп, взаимное
отталкивание, набухание
38.
Мицеллы блоксополимеровгидрофильная
«корона»
Мицеллообразование
гидрофильный (водорастворимый)
блок
> ККМ
< ККМ
гидрофобный
блок
В разбавленном водном растворе формируют
мицеллы
Мицелла состоит из нескольких макромолекул
гидрофобноеядро
39.
Мицеллы блоксополимеровГидрофобные лекарства могут быть растворены в ядрах, в
то время как «корона» будет гарантировать
растворимость наноконтейнера в водной фазе.
Corona
Если «корона» состоит из блока, который не вызывает
иммунной реакции (ПЭГ), то содержимое мицеллы будет
невидимым для иммунной системы.
ПЭГ (полиэтиленгликоль)
[-CH2-CH2-O-]n
цисплатин
Для направленной доставки
можно присоединить к
поверхности рН чувствительные элементы
40.
ДендримерыФорма близка к сферической
трехмерные
разветвленные
макромолекулы
регулярного
строения
Размер
1-15 нм
ПЭМ
I
I – ядро, G – генерацииилипокленияве
тлений;A, B, C – дендроны, z –
терминальные(коне
чные) функц
иональные
ппы;* – у
у
гр
злыве
тв
лений
Дендример,
состоящий из трех
крон (дендронов),
растущих из одного
корня
монодисперсность; возможность надежного
контроля над размерами, формой и
функциональностью в процессе синтеза
АСМ
41.
Потенциально в медицине носители для направленнойдоставки лекарств.
Дендримерыприменение в
медицине
В медицинской диагностике,
как контрастные вещества
в МРТ
Вкачествмар
керовиспо
ль
зуютфлюоресцентныеметкии
радиоактивныеизотпы3H, 14C, 88Y, 111Ви125I
Ковалентное и
нековалентное связывание
Преимущества- медленное и
постепенное высвобождение ЛП
Недостатки- образование пор
в бислое липидов, токсический
эффект
модификация поверхностных активных
групп, биосовместимые материалы
42.
ПОЛИМЕРЫНОСИТЕЛИКОНТЕЙНЕРОВ
43.
ВЕЗИКУЛЫ, построенные из фосфолипидов -ЛИПОСОМЫМОЛЕКУЛА ФОСФОЛИПИДА
Криогенная просвечивающая
микроскопия
сходство с природными мембранами
клеток по составу
биодеградируемость и биосовместимость,
не подвергаются атаке со стороны
иммунной системы
легкость получения; возможность
изменения состава и размера
для доставки фармакологически активных
веществ: противоопухолевых и
противомикробных препаратов,
ферментов, вакцин и др.
44.
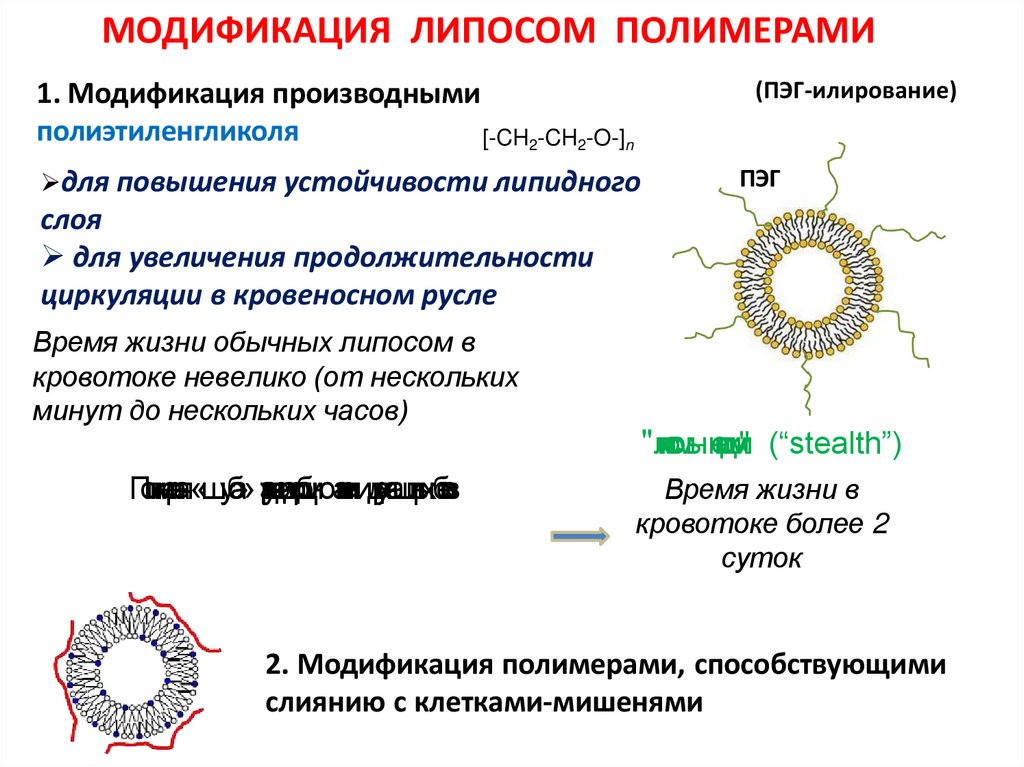
МОДИФИКАЦИЯ ЛИПОСОМ ПОЛИМЕРАМИ1. Модификация производными
полиэтиленгликоля
[-CH2-CH2-O-]n
(ПЭГ-илирование)
для повышения устойчивости липидного
ПЭГ
слоя
для увеличения продолжительности
циркуляции в кровеносном русле
Время жизни обычных липосом в
кровотоке невелико (от нескольких
минут до нескольких часов)
Полимерная«шуба» за
тр
удняе
тадсорбциюантие
лидри
угхзащитныхбе
лков
"липосомы-невидимки" (“stealth”)
Время жизни в
кровотоке более 2
суток
2. Модификация полимерами, способствующими
слиянию с клетками-мишенями
45.
ЛИПОСОМАЛЬНЫЕ ПРЕПАРАТЫдля противоопухолевой, противовирусной и
противомикробной терапии
46.
ЛИПОСОМАЛЬНЫЕ ПРЕПАРАТЫноваялекарств
еннаяформаДо
ксил(Doxil®)
O
пэгилированная
липосомальная форма
доксорубицина
O
OH
C-CH 2 OH
OH
CH 3 O
O
CH3
HO
OH
O ДОКСОРУБИЦИН (Dox),
O
ПРОТИВООПУХОЛЕВЫЙ ПРЕПАРАТ
NH2
меньшаято
ксичностьпрепарат
воздейсв
туенаткани, непораженныеопухолью)
повышениеэ
ффе
ктивностиле
чниярядараков
Преимущесв
та:
(нета
ка
ктивно
47.
Актуальная задача:концентрирование липосом на носителе
повышение эффективности захвата
липосом клетками
усиление терапевтического
эффекта липосомальных препаратов
создание мультифункциональных
лекарственных композиций с учетом
особенностей лечения конкретного
пациента
Муль
тилипосомальныеконср
тукци
Cryo-TEM
Подход: электростатическая
адсорбция липосом на поверхности
носителя
Большоечислолипосом
сконцентрированов
малень
комоб
ъеме
48.
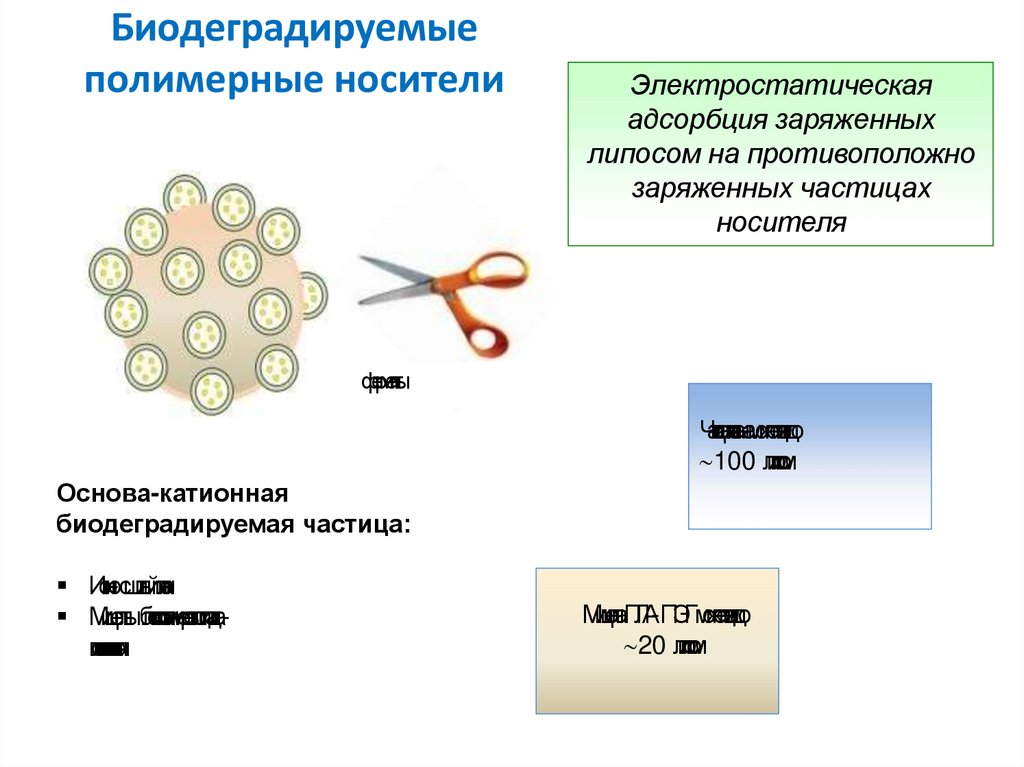
Биодеградируемыеполимерные носители
Электростатическая
адсорбция заряженных
липосом на противоположно
заряженных частицах
носителя
ферменты
Частицах
итозанаможетсв
яза
тьдо
100 липосом
Основа-катионная
биодеградируемая частица:
Ионо-сшитыйхитозан
Мицеллыблок-сополимеровпо
лила
ктидаполиэтиленгликоля
Мице
ллаПЛА-ПЭГможетсв
яза
тьдо
20 липосом
49.
Взаимодействие комплексов с клетками.До
ксрубицин(До
кс)
Лазерная конфокальная микроскопия
Кле
ткиMCF-7/R.
Комплексывзаимодейс
уютскле
тв
ткамисвысвобождениемДо
ксизлипосом
(a) Флуоресцентное изображение,
(b) изображение, полученное в
дифференциальном
интерференционном контрасте.
50.
Стимул-чувстительныесистемыдляадреснойдоставкинаосновеполимеровилипосомТЕРМОЧУВСТВИТЕЛЬНЫЕ КОНСТРУКЦИИ
Коллапс геля = разрушение липосом
51.
рH-ЧУВСТВИТЕЛЬНЫЕ КОНСТРУКЦИИН+
Н+
52.
ПОЛИМЕРЫ В Б И О М Е Д И Ц И Н ЕРЕГЕНЕРАТИВНАЯ МЕДИЦИНА
СКАФФОЛД-ТЕХНОЛОГИИ
3D-ПЕЧАТЬ
НАНОФАРМАКОЛОГИЯ
СИСТЕМЫ ДЛЯ ДОСТАВКИ ЛЕКАРСТВ
ХИРУРГИЯ
ПОЛИМЕРНЫЕ НАНОКОМПОЗИТЫ








































 medicine
medicine








